MC4R基因敲除对雌性小鼠代谢和肝脏脂肪性病变的影响
2019-08-15陈小琳
陈小琳 陈 晨
MC4R是中枢调节能量稳态的关键受体之一。中枢MC4R与弓状核(ACR)内起降低食欲作用的阿片促黑素细胞皮质素原(POMC)神经元合成、分泌的α-黑素细胞刺激激素(α-MSH)相结合,起着降低食欲和促进能量代谢的作用[1~3]。大量研究表明,Mc4r基因敲除雄性小鼠表现为多食、肥胖和高胰岛素血症[4,5]。肥胖和高胰岛素血症与女性生殖功能密切相关[6~8]。本研究旨在观察Mc4r基因敲除对雌性小鼠食欲、体重、血糖、胰岛素水平、糖耐量、胰岛素敏感度、肝脏脂肪性病变的影响,为研究Mc4r基因敲除对雌性小鼠生殖功能影响提供研究基础。
材料与方法
1.实验动物:Mc4r-/-雌性小鼠由Mc4r+/-小鼠交配产生,并进行基因鉴定。所有实验均在澳大利亚昆士兰大学生物医学科学院陈晨教授实验室完成。6周龄小鼠两只一笼饲养,12h光暗周期(光照6:30时~18:30时),室温22±2℃,小鼠自由取水、进食。
2.实验观察:每天测定小鼠进食量和体重。分别在8、12、16、20、26周龄测定空腹、餐后血糖,在8、12、16、20周龄测定空腹、餐后胰岛素水平。
3.腹腔葡萄糖耐量实验(glucose tolerance tests,GTT)[9]:20周龄,两组小鼠分别行GTT。小鼠空腹12h,腹腔注射葡萄糖(2g/kg体重),分别测定注射前及注射后15、30、60、90min末梢血糖。
4.腹腔胰岛素耐量实验(insulin tolerance tests,ITT)[9]:20周龄,两组小鼠分别行ITT。小鼠空腹6h,腹腔注射胰岛素(0.5U/kg体重),分别测定注射前及注射后15、30、45min末梢血糖。
5.肝脏脂肪变性的观察:取新鲜肝组织OCT包埋,冷冻切片(厚12μm),分别快速HE染色和油红染色,Aperio ScanScope XT病理扫描系统扫描成像。
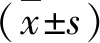
结 果
1.Mc4r基因敲除对C57/BL6雌性小鼠摄食和体长的影响:MC4RKO雌性小鼠每日摄食量大于WTLM雌性小鼠,差异有统计学意义(P=0.000),见图1。16和28周龄MC4RKO雌性小鼠身长长于WTLM雌性小鼠(图2),差异有统计学意义(P=0.000)。
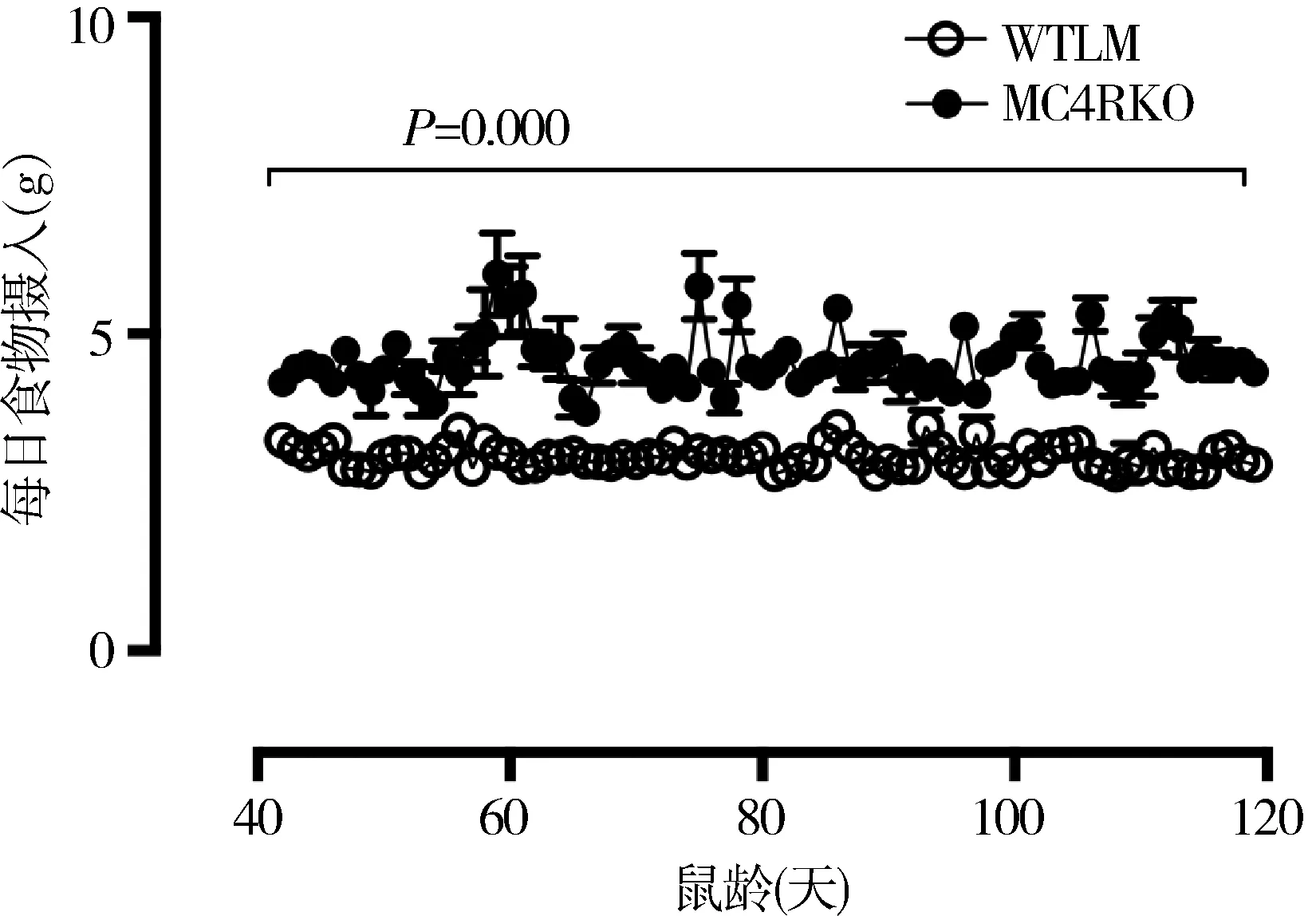
图1 小鼠每日摄食量(g)
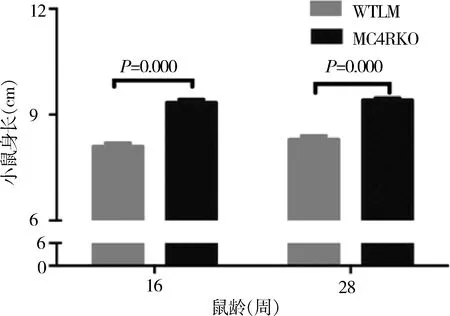
图2 小鼠身长(cm)
2.Mc4r基因敲除对C57/BL6雌性小鼠体重和内脏脂肪的影响:MC4RKO雌性小鼠和WTLM雌性小鼠从8周龄开始体重之间比较,差异有统计学意义(P=0.000,图3A)。16、28周龄MC4RKO雌性小鼠皮下脂肪(图3B)、腹腔脂肪(图3C)、腹股沟脂肪(图3D)、卵巢脂肪(图3E)、肾周脂肪(图3F)均重于同龄WTLM雌性小鼠,差异有统计学意义(P=0.000)。28周龄MC4RKO雌性小鼠和WTLM雌性小鼠皮下脂肪、腹腔脂肪、腹股沟脂肪、卵巢脂肪、肾周脂肪亦均重于16周MC4RKO雌性小鼠和WTLM雌性小鼠,两组间比较差异有统计学意义(P值分别为0.000、<0.01、<0.05)。
3.Mc4r基因敲除对C57/BL6雌性小鼠血糖和胰岛素水平的影响:8周龄,MC4RKO雌性小鼠和WT LM雌性小鼠两组之间空腹、餐后血糖和胰岛素水平比较,差异无统计学意义(P>0.05)。12、16、20周龄MC4RKO雌性小鼠空腹(图4A)、餐后血糖(图4B)和空腹(图4C)、餐后(图4D)胰岛素水平均高于WTLM雌性小鼠(P值分别为0.000、0.000,<0.01、<0.05)。26周龄,MC4RKO雌性小鼠空腹血糖高于WTLM雌性小鼠野,而餐后血糖两组间差异无统计学意义(P>0.05)。
4.Mc4r基因敲除对C57/BL6雌性小鼠葡萄糖耐量和胰岛素敏感度的影响:20周龄MC4RKO雌性小鼠显示葡萄糖耐量异常(图5A),葡萄糖曲线下面积(图5B)大于WTLM雌性小鼠(P值分别为0.000、<0.05)。同时,与20周龄WTLM雌性小鼠比较,MC4RKO雌性小鼠显示胰岛素敏感度降低(图5C、D,P值分别为<0.01、<0.05)。
5.Mc4r基因敲除对C57/BL6雌性小鼠肝脏重量的影响:16周龄和28周龄MC4RKO雌性小鼠肝脏重量均重于16周龄和28周龄WTLM雌性小鼠,两组间比较差异有统计学意义(P=0.000),详见图6。
6.Mc4r基因敲除对C57/BL6雌性小鼠肝组织学和肝细胞脂肪性病变的影响:16周龄(图7B)、28周龄(图7D)MC4RKO雌性小鼠肝脏大体观体积较16周龄(图7A)、28周龄(图7C)WTLM雌性小鼠肝脏体积明显增大,且28周龄(图7D)MC4RKO雌性小鼠肝脏质地较硬,色泽变黄。HE染色光镜下观察,16周龄(图7E)和28周龄(图7G)WTLM雌性小鼠肝脏组织结构完整、清晰,肝小叶正常,肝细胞呈多形、排列成肝索,呈放射状分布。16周龄(图7F)MC4RKO雌性小鼠肝脏HE染色光镜下发现肝细胞体积增大,肝索排列稍紊乱,胞质中有脂滴空泡;28周龄(图7H)MC4RKO雌性小鼠肝细胞体积变小,肝索排列紊乱,肝小叶结构不清晰,胞质中有大量脂滴空泡。油红染色光镜下观察,16周龄(图7I)、28周龄(图7K)WTLM雌性小鼠肝细胞未见红色脂滴,16周龄(图7J)MC4RKO雌性小鼠肝细胞可见大量细小红色脂滴,28周龄(图7L)MC4RKO雌性小鼠肝细胞可见大量较大红色脂滴。
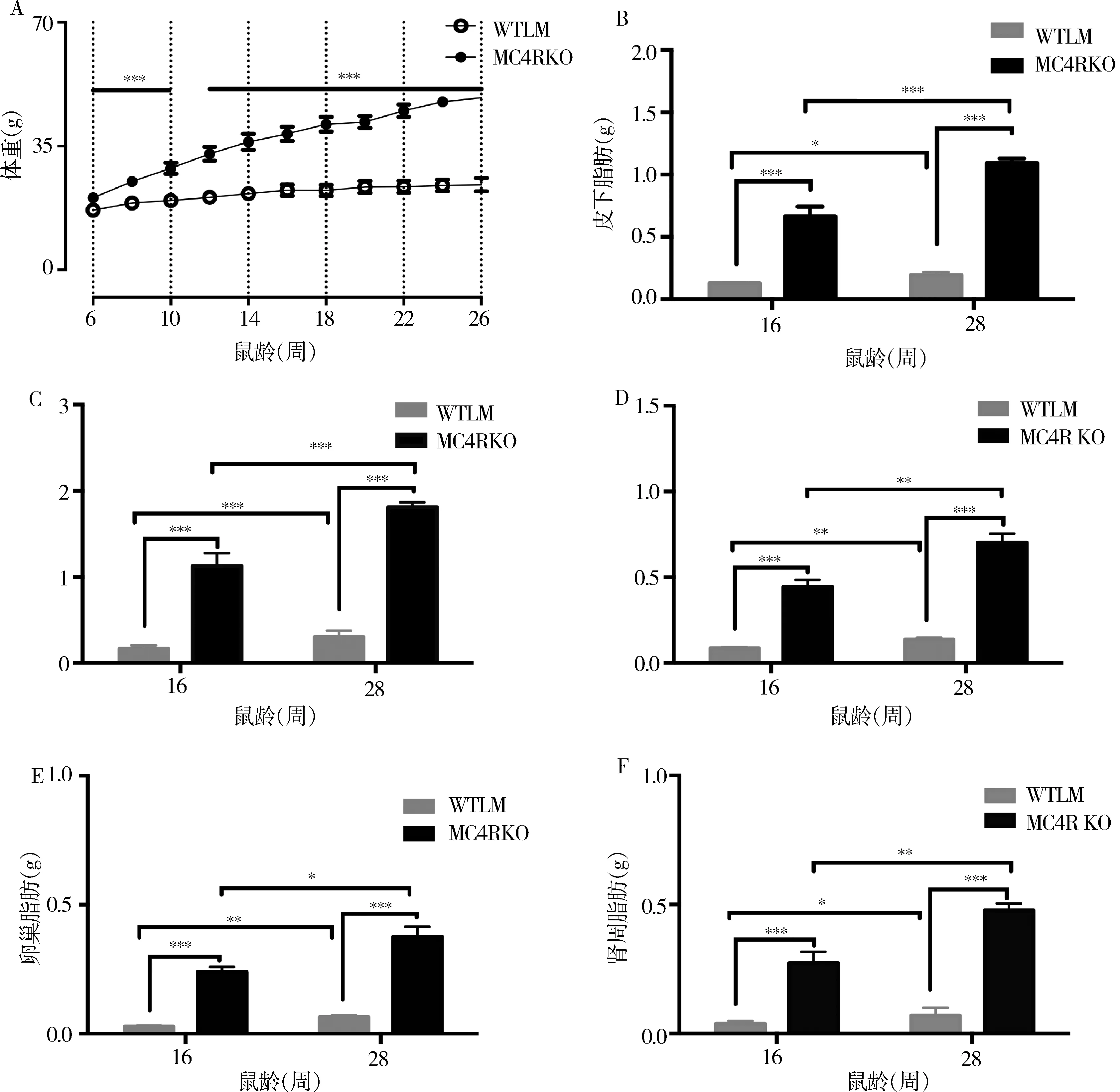
图3 小鼠体重和内脏脂肪含量
A.体重;B.皮下脂肪;C.腹腔脂肪;D.腹股沟脂肪;E.卵巢脂肪;F.肾周脂肪;*P<0.05,**P<0.01,***P=0.000
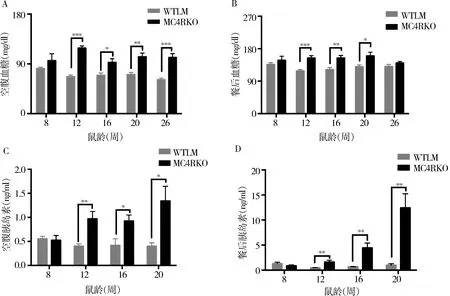
图4 小鼠血糖和胰岛素水平
A.空腹血糖;B.餐后血糖;C.空腹胰岛素;D.餐后胰岛素;*P<0.05,**P<0.01,***P=0.000
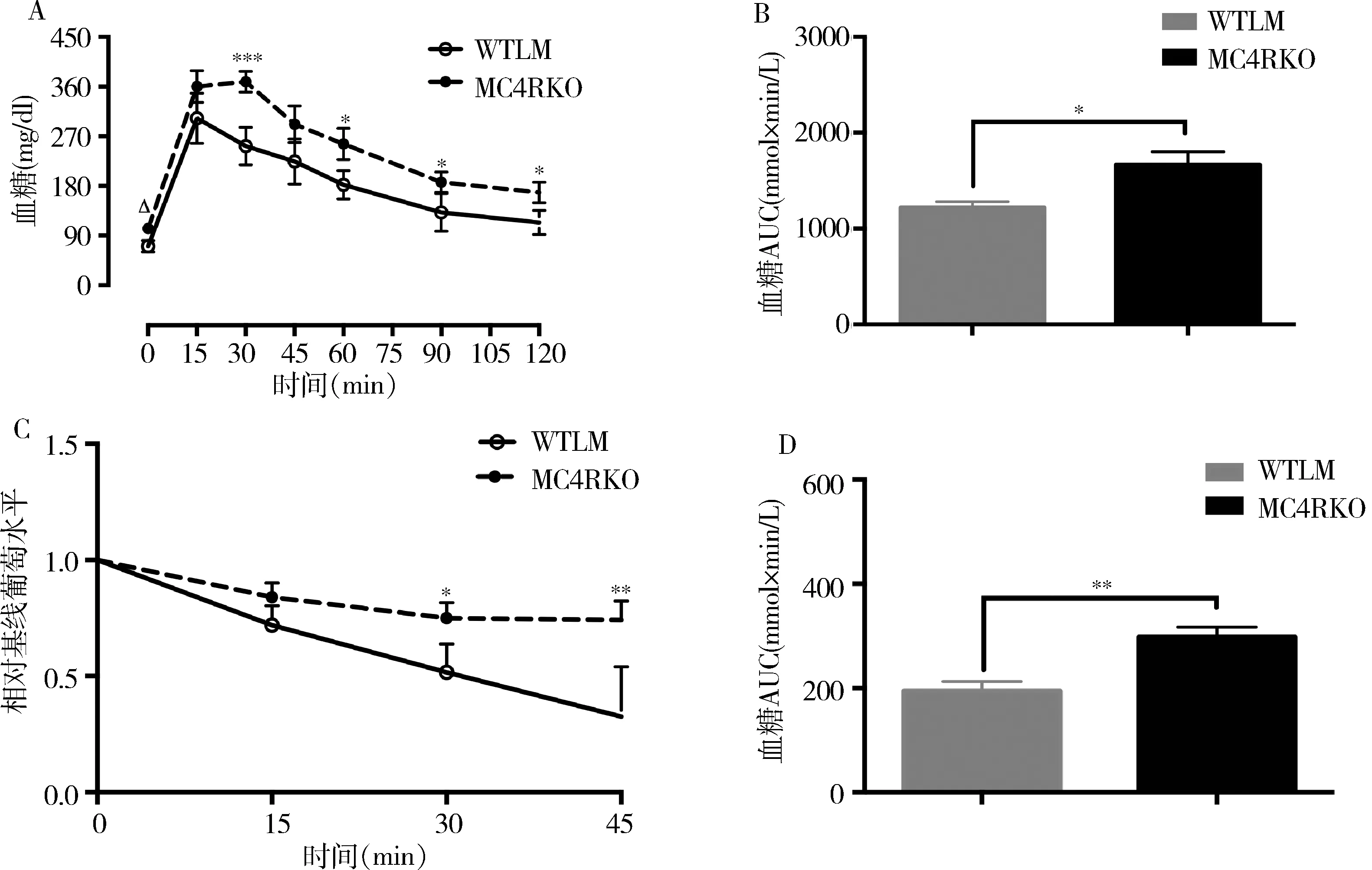
图5 葡萄糖耐量和胰岛素耐量
A.腹腔葡萄糖耐量试验;B.葡糖糖曲线下面积;C.腹腔胰岛素耐量试验;D.相对葡萄糖曲线下面积;*P<0.05,**P<0.01,***P=0.000
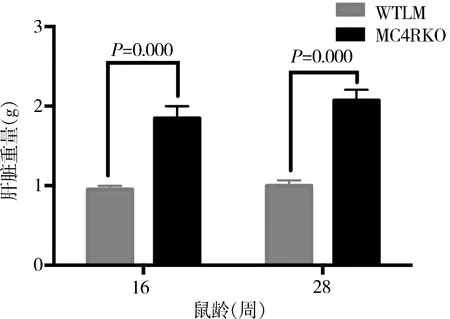
图6 小鼠肝脏重量
讨 论
肥胖引起女性生殖内分泌紊乱是导致育龄女性不孕的主要原因。确切发病机制尚未阐明。到目前为止,还没有一个广泛公认的动物模型用于研究其发病机制、病程发展、临床治疗和预防。下丘脑是中枢调控能量代谢和生殖的关键部位。MC4R属于G蛋白耦联受体超家族(GPCRs)成员之一, 分布在大脑皮质、下丘脑、垂体、性腺,具有雌雄间差异[10,11]。黑皮质素4受体(MC4R)是下丘脑控制食欲和促进能量代谢的关键分子[12~14]。已有研究证实,Mc4r基因敲除的雄性小鼠表现为多食、肥胖和高胰岛素血症。本研究以MC4RKO雌性小鼠为研究对象,观察MC4R基因敲除对雌性小鼠能量代谢和肝脏的影响。
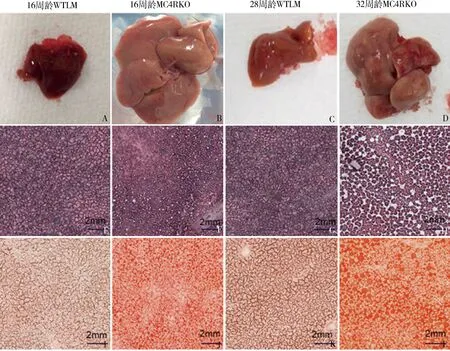
图7 小鼠肝脏组织学
A~D.大体标本;E~H.HE染色(×200);I~L.油红染色(×200)
本研究结果显示,MC4RKO雌性小鼠表现为多食、体长增加、肥胖,尤其是内脏脂肪增加。MC4RKO雌性小鼠在12周龄出现血糖、胰岛素水平显著升高。26周龄基因敲除小鼠和野生型小鼠两组间餐后血糖比较,差异无统计学意义。推测分析可能与基因敲除小鼠此时已表现为严重肝脏脂肪性病变有关。20周龄MC4RKO雌性小鼠已显示糖耐量异常和严重胰岛素抵抗。MC4RKO雌性小鼠在16周龄时已出现肝脏肿大和脂肪性病变,28周龄时肝脏已显示出重度脂肪肝和肝硬化。因而,MC4RKO雌性小鼠可以作为雌性肥胖动物模型进行代谢性疾病的动物实验研究。
肥胖引起女性生殖内分泌紊乱的机制以及肥胖的表型复杂,一种动物模型不能解释所有肥胖表型导致的机体功能异常。由于本实验中MC4RKO雌性小鼠摄入的是普通动物饲料导致肥胖,该模型更适合用于因食欲亢进导致肥胖的动物模型研究。该动物模型是否存在生殖功能异常,何时出现生殖功能紊乱,与生殖相关的激素如何变化,还需要进一步研究。
