独活的质量评价
2019-08-11王计瑞李隆云
王计瑞, 谭 均, 李隆云*, 丁 刚
(1.重庆市中药研究院,重庆市中药良种选育与评价工程技术研究中心,重庆市中药资源学重点实验室,重庆400065;2.中国中医科学院中药资源中心,重庆400065;3.西南大学药学院,重庆400716)
独活为伞形科植物重齿毛当归Angelica pubescens Maxim.f.biserrata Shan et Yuan 的干燥根,其性微温,味辛、苦,具有祛风除湿、通痹的作用[1]。它主要为栽培品,在重庆、湖北、陕西等地广泛种植[2]。
现代药理研究表明,独活中二氢欧山芹醇具有抗炎、修复紫外损伤的角质细胞等作用[3-5];异欧前胡素具有镇痛作用,能显著减少醋酸所致小鼠的扭体次数[6-7];挥发油具有抗炎、镇痛作用[8],均与独活通痹止痛的药理作用密切相关;此外也有研究报道醇提物具有抗肿瘤、抗血管生成作用[9-10]。2015 年版《中国药典》 主要从性状、鉴别、检查,以及蛇床子素、二氢欧山芹醇当归酸酯2 种香豆素类成分含有量方面对独活质量进行检验,未涉及浸出物、挥发油及二氢欧山芹醇、 异欧前胡素含有量[1]。
本研究对独活药材、饮片2 种规格进行水分、灰分、浸出物、挥发油、二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯含有量测定,并运用统计学方法进行分析评价,探究其相关性及各样品之间质量差异性,以期为更全面地评价该药材质量提供依据。
1 材料
Agilent 1260 高效液相色谱仪(DAD 检测器,美国安捷伦科技公司);UV2600 紫外分光光度计(日本岛津公司);Milli-Q Integral5 纯水仪(美国密里博公司);BT224S 电子天平[万分之一,赛多利斯科学仪器(北京) 有限公司];CPA225D电子天平[十万分之一,赛多利斯科学仪器(北京) 有限公司];SB-4200DTD 超声波清洗机(宁波新芝生物科技股份有限公司);8-10 马弗炉(沈阳市节能电炉厂);KDM 可调控温电热套(山东鄄城华鲁电热仪器有限公司);XMTB 数显式电热恒温水浴锅(上海跃进医疗器械有限公司);G2X-9240MBE 电热鼓风干燥箱(上海博讯实业有限公司医疗设备厂)。
乙腈(色谱纯,美国Tedia 公司);其他试剂均为优级纯或分析纯;水为超纯水。对照品蛇床子素(批号MUST-16012417)、二氢欧山芹醇当归酸酯(批号MUST-16022403)、异欧前胡素 (批号MUSY-16032410) 均购自成都曼斯特生物科技有限公司;二氢欧山芹醇(批号Z08A7S12651) 购自上海源叶生物科技有限公司,含有量>98%。
独活药材采收于重庆、湖北、陕西等地或购自成都荷花池药材市场,饮片购自各地区大药房,共18 批,经重庆市中药研究院李隆云研究员鉴定为伞形科植物重齿毛当归Angelica pubescens Maxim.f.biserrata Shan et Yuan 的干燥根,具体见表1。

表1 样品信息Tab.1 Information of samples
2 方法与结果
2.1 水分、灰分及挥发油检测 按照《中国药典》 第四部相关方法进行检测,结果见表2。

表2 样品常规项检查结果(%)Tab.2 Results of routine tests of samples(%)
结果表明,18 批样品水分含有量在3.00%~11.00%之间,有1 批(YP-8) 略超出 《中国药典》 规定,可能是在销售过程中密封不当所致,其他批次均符合《中国药典》 规定;总灰分含有量在4.30%~7.44%之间,酸不溶性灰分含有量在0.73%~2.55%之间,各批样品均符合 《中国药典》 要求。另外,挥发油含有量在0.30%~0.35%之间,药材与饮片差异不大。
2.2 浸出物检测
2.2.1 浸提方法优化 按照《中国药典》 第四部(通则2201) 方法,分别用冷浸法和热浸法制备乙醇浸出物,并测定2 种方法所得浸出物中总香豆素提取率[11-12]和浸膏得率,结果见表3。
结果表明,采用热浸法的浸膏得率和总香豆素提取率均高于冷浸法,故选择其作为独活浸出物的制备方法。
表3 不同浸出方法对样品的影响n=3)Tab.3 Effects of different leaching methods on samples,n=3)

表3 不同浸出方法对样品的影响n=3)Tab.3 Effects of different leaching methods on samples,n=3)
方法 浸膏得率/% 总香豆素提取率/%冷浸法 11.18±0.43 2.32±0.04热浸法 23.14±0.96 2.74±0.04
2.2.2 浸提溶剂优化 按照《中国药典》 第四部(通则2201) 热浸法, 以无水乙醇、80%乙醇、60%乙醇、50%乙醇、40%乙醇、20%乙醇、纯水作为浸提溶剂,测定各组浸出物中总香豆素提取率和浸膏得率,结果见表4。
表4 不同浸出溶剂对样品的影响,n=3)Tab.4 Effects of different leaching solvents on samples,n=3)

表4 不同浸出溶剂对样品的影响,n=3)Tab.4 Effects of different leaching solvents on samples,n=3)
注:同一指标不同小写字母表示有显著差异(P<0.05)
提取溶剂 浸膏得率/% 总香豆素提取率/%1 8 6 5 4 2 0 0 0 0 0 0 0纯%%%%%%乙乙乙乙乙水乙醇醇醇醇醇醇 2 4 4 4 4 5 5 3 2 7 8 9 0 2.......1 7 4 2 2 8 5 4 7 5 4 5 7 8±±±±±±±0 0 0 0 0 2 0.......9 6 4 2 1 9 3 6 9 5 5 9 0 2 edcbaaa bb c c 2 3 4 4 3 2 1.......7 4 8 0 8 3 2 1 7 1 0 7 0 3±±±±±±±0 0 0 0 0 0 0.......0 0 2 1 0 0 0 9 7 0 3 6 5 4 dcabbef
结果表明,随着浸出溶剂中水比例的增加,浸膏得率增加,其中以40%~60%乙醇为溶剂所得的浸膏量无显著性差异(P>0.05);总香豆素提取率则是先升后降,60%乙醇显著优于其他组 (P <0.05)。最终,选择60%乙醇作为热浸法的浸出溶剂。
2.2.3 浸出物测定 采用热浸法,以60%乙醇作为浸提溶剂,检测18 批样品浸出物含有量,结果见表2。 由表可知,60%乙醇浸出物含有量在40.67%~51.69%之间,整体上饮片高于药材。
2.3 香豆素类成分含有量测定
2.3.1 色谱条件 SWELL ChromplusTMC18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)-水(B),梯度洗脱 (0 ~6 min,45%A;6 ~7 min,45% ~49%A;7 ~35 min,49%A;35 ~38 min,49%~ 45%A;38 ~40 min,45%A); 体积流量1.0 mL/min;检测波长325 nm;柱温25 ℃;进样量10 μL。色谱图见图1。

图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
2.3.2 对照品溶液制备 精密称取二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯适量,加甲醇制成相应溶液,分别量取适量,甲醇定容,摇匀,即得(质量浓度分别为36.80、568.40、22.60、168.80 μg/mL),再稀释得到梯度溶液。
2.3.3 供试品溶液制备 精密称取干燥药材粉末(过5 号筛) 0.5 g, 置具塞锥形瓶中, 加甲醇20 mL,称定质量,于25 ℃超声(功率400 W、频率40 kHz) 处理20 min,冷却,甲醇补足减失的质量,摇匀,0.45 μm 微孔滤膜过滤,即得。
2.3.4 线性关系考察 在“2.3.1” 项色谱条件下,将对照品溶液进样测定。以各对照品溶液峰面积为纵坐标(Y),质量浓度为横坐标(X) 进行回归,结果见表5。
2.3.5 检测限与定量限 配制不同质量浓度的对照品溶液,在“2.3.1” 项色谱条件下进样,以信噪比为3 ∶1 时考察检测限,10 ∶1 时考察定量限,结果见表5。
2.3.6 精密度试验 取同一对照品溶液, 在“2.3.1” 项色谱条件下连续进样6 次,测得二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯峰面积RSD 分别为0.10%、 0.04%、0.68%、0.06%,表明仪器精密度良好。
2.3.7 重复性试验 取同一药材,按“2.3.3”项下方法平行制备6 份供试品溶液,在“2.3.1”项色谱条件下进样,测得二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯峰面积RSD 分别为1.03%、0.29%、0.44%、0.33%,表明该方法重复性良好。

表5 各成分线性关系及检测限、定量限Tab.5 Linear relationships of various constituents,LOQs and LODs
2.3.8 稳定性试验 取同一供试品溶液, 在“2.3.1” 项色谱条件下于0、2、4、8、12、24 h进样,测得二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯峰面积RSD 分别为1.09%、0.71%、0.51%、3.23%,表明供试品溶液在24 h 内稳定性良好。
2.3.9 加样回收率试验 精密称取含有量已知的同一药材9 份,每份0.25 g,精密加入一定量二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯对照品溶液,按“2.3.3” 项下方法制备供试品溶液,在“2.3.1” 项色谱条件下进样,计算回收率,结果见表6。
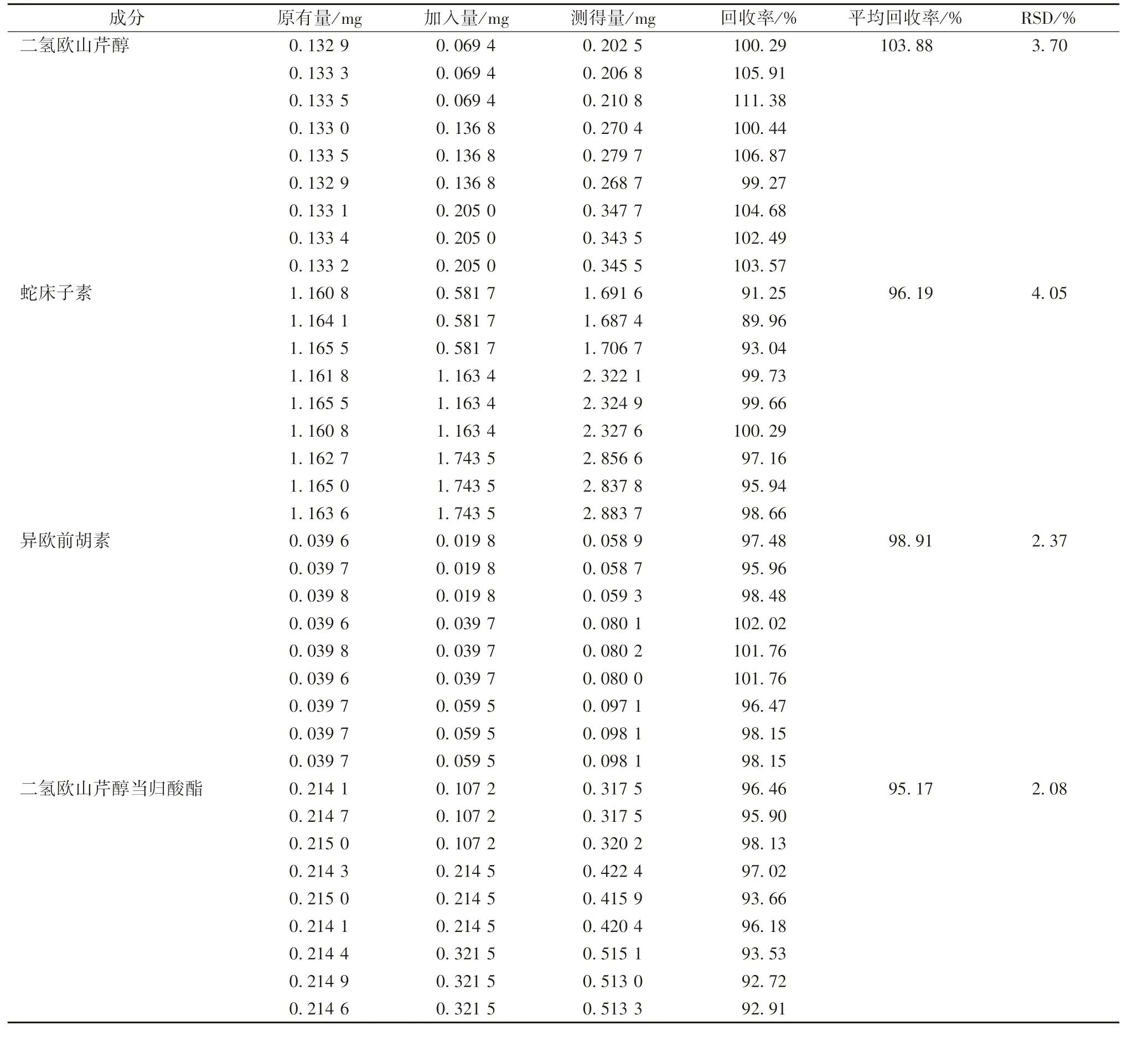
表6 各成分加样回收率试验结果(n=9)Tab.6 Results of recovery tests for various constituents(n=9)
2.3.10 样品含有量测定 按“2.3.3” 项下方法平行制备3 份供试品溶液,在“2.3.1” 项色谱条件下进样,计算含有量,结果见表7。
表7 各成分含有量测定结果,n=3)Tab.7 Results of content determination of various constituentsn=3)

表7 各成分含有量测定结果,n=3)Tab.7 Results of content determination of various constituentsn=3)
注:#表示低于药典规定
编号 二氢欧山芹醇/% 蛇床子素/% 异欧前胡素/% 二当氢归欧酸山酯芹/%醇主合成得分分分排析序综YC-1 0.010 6±0.000 1 0.805 5±0.005 3 0.019 5±0.000 1 0.158 4±0.001 0 13 YC-2 0.066 6±0.000 6 0.785 6±0.003 6 0.027 7±0.000 1 0.290 4±0.001 8 3 YC-3 0.480 5±0.004 9 1.477 6±0.015 8 0.066 1±0.000 5 0.173 6±0.001 9 1 YC-4 0.005 6±0.000 0 0.578 1±0.001 3 0.016 6±0.000 0 0.081 2±0.000 2 18 YC-5 0.024 3±0.000 2 1.799 9±0.014 0 0.032 1±0.000 3 0.224 5±0.001 8 2 YC-6 0.066 7±0.001 2 1.258 6±0.007 7 0.023 5±0.000 1 0.129 7±0.008 7 7 YC-7 0.025 1±0.000 1 1.241 1±0.032 7 0.016 3±0.000 4 0.111 0±0.004 0 15 YC-8 0.024 1±0.000 5 0.714 0±0.008 5 0.032 8±0.000 4 0.216 8±0.002 7 5 YC-9 0.023 0±0.000 7 0.668 9±0.012 2 0.039 6±0.000 9 0.062 4±0.002 0# 12 YP-1 0.037 1±0.000 1 0.565 8±0.004 2 0.030 5±0.000 2 0.077 8±0.001 1# 17 YP-2 0.029 3±0.000 2 0.707 3±0.027 6 0.025 4±0.001 1 0.249 8±0.010 1 6 YP-3 0.048 6±0.002 5 0.814 2±0.025 7 0.024 1±0.000 6 0.145 2±0.002 5 9 YP-4 0.023 8±0.000 2 0.683 7±0.005 8 0.038 7±0.000 4 0.099 2±0.004 8 8 YP-5 0.041 1±0.000 1 0.508 6±0.000 8 0.025 5±0.000 2 0.160 4±0.004 5 10 YP-6 0.044 9±0.000 2 0.654 7±0.001 7 0.022 1±0.000 2 0.318 4±0.001 4 4 YP-7 0.040 0±0.000 9 0.669 4±0.018 2 0.027 7±0.000 8 0.125 8±0.003 0 11 YP-8 0.028 5±0.000 1 0.781 5±0.004 4 0.024 0±0.000 2 0.119 1±0.000 4 14 YP-9 0.014 4±0.000 3 0.667 6±0.007 6 0.030 3±0.000 3 0.086 6±0.000 4 16药典规定 - 0.50 - 0.08 -
结果表明,18 批样品中蛇床子素含有量为0.508 6%~1.799 9%,均符合《中国药典》 标准;二氢欧山芹醇当归酸酯含有量为0.062 4%~0.318 4%,药材、饮片各有1 批低于《中国药典》标准,均为市场购买所得;二氢欧山芹醇含有量为0.005 6% ~0.480 5%, 异欧前胡素含有量为0.016 3%~0.066 1%。
2.4 化学计量学方法分析
2.4.1 相关性分析 影响中药材质量的各指标并不只是孤立的个体,它们之间往往具有一定的相关性,浸出物、挥发油和香豆素类成分含有量是评价独活质量的重要指标。本研究运用SPSS 20.0 软件,对影响独活质量的6 个指标(60%乙醇浸出物、挥发油、二氢欧山芹醇、蛇床子素、异欧前胡素和二氢欧山芹醇当归酸酯含有量) 进行相关性分析,结果见表8,可知15 对指标组合中仅有3对具有显著(P<0.05) 或极显著(P<0.01) 相关性,其中挥发油分别与二氢欧山芹醇、异欧前胡素呈现显著、极显著正相关性,二氢欧山芹醇与异欧前胡素呈现极显著正相关性。

表8 相关性分析结果Tab.8 Results of correlation analysis
2.4.2 聚类分析 运用SPSS 20.0 软件,以余弦距离作为度量标准,以6 个指标为变量,对18 批样品进行系统聚类分析,共被分为2 大类,结果见图2,可知饮片样品和半数原药材样品归为Ⅰ类,有4 批原药材样品被归为第Ⅱ类。由此表明,饮片样品之间质量较均一,原药材样品质量差异性较大,表明通过饮片加工过程可使独活质量趋于均一。

图2 18 批样品聚类树状图Fig.2 Dendrogram of eighteen batches of samples
2.4.3 主成分分析 以独活中二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯含有量作为变量,特征值和累计贡献率作为判定依据,运用SPSS 20.0 软件对不同产地独活进行主成分分析。根据降维结果,共挑选出3 个主成分PC1、PC2、PC3,特征值分别为2.102、1.046、0.680。各成分方差贡献值分别为52.553%、26.159%、16.991%,累积贡献值达到95.702%,代表性强,可以用来评价独活的质量,结果见表9,表明PC1和PC3 主要反映的是二氢欧山芹醇、异欧前胡素、蛇床子素含有量信息,PC2 主要反映的是二氢欧山芹醇当归酸酯含有量信息。
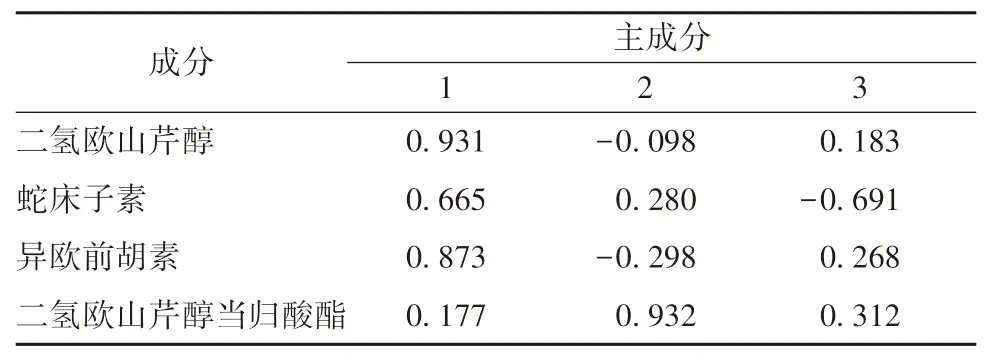
表9 各成分因子载荷矩阵Tab.9 Factor load matrices of various constituents
根据各因子载荷矩阵及特征值计算得分系数,进一步得到PC1、PC2、PC3 及综合得分(Y) 方程式为PC1 =0.642BX1+0.459BX2+0.602BX3-0.122BX4、PC2 =-0.096BX1+0.274BX2-0.291BX3+0.911BX4、PC3 =0.222BX1-0.838BX2+0.325BX3+0.378BX4,其中BX1、BX2、BX3、BX4分别为二氢欧山芹醇、蛇床子素、异欧前胡素、二氢欧山芹醇当归酸酯的标准化值;Y=0.549PC1+0.273PC2+0.178PC3。
利用上式计算各批独活质量综合得分并按结果进行排序,见表7,得分越高,表明独活质量越好,排名越靠前。主成分散点图见图3,可知有4批原药材(YC-3、YC-5、YC-6、YC-7) 因3 个主成分均与其他样品有较大差异而分布较为离散;其他样品之间PC1 和PC3 差异不大,但因PC2 不同而呈现纵向延伸分布。结合表9 可知,各饮片之间二氢欧山芹醇、蛇床子素、异欧前胡素含有量差异不大,但二氢欧山芹醇当归酸酯含有量却存在一定差异,故沿PC2 轴方向分布;药材之间4 种成分含有量均有较大差异,故呈离散分布,表明未经筛选、加工的原药材质量不如饮片稳定,整体上分类结果与聚类分析一致。

图3 各成分主成分分析散点图Fig.3 Scatter diagram of principal component analysis of various constituents
3 讨论
《中国药典》 中未规定独活的浸出物限度,但其又是反映中药材质量的重要指标[13-14],代表的是多种模糊性成分的量。本研究优化并确定了独活浸出物的浸提方式和浸提溶剂,其60%乙醇浸出物含有量可达40%以上。
本研究建立了HPLC 法同时测定独活中4 种成分的含有量,较《中国药典》 多增加2 种成分,而且该方法简单、稳定,易于购买相应的对照品。相关性分析结果表明,增加的2 种成分与挥发油之间具有显著相关性,这与三者均具有较好的抗炎、镇痛等药理作用相一致。因此,二氢欧山芹醇、异欧前胡素、挥发油含有量也应作为评价独活质量的主要指标。
浸出物和4 种成分含有量检测结果表明,与药材比较,饮片质量更优、更稳定,2 种规格中挥发油含有量差异不大,表明独活药材加工成饮片后对其挥发性成分影响不明显。饮片在聚类分析和主成分分析时表现出更好的聚集性,表明药材经过筛选和加工处理后质量更趋均一。
原药材质量的不稳定性增加了后续饮片加工和质量控制的难度,因此应保障生产源头的质量。目前,独活以栽培品为主,大多以个体户形式种植,而种植、采收、初加工技术对中药材品质有着重要的影响[15-16]。因此,应当推广独活规范化种植技术,确立合理的采收时间及统一、有效的初加工技术,从而保证该药材质量的稳定。
