TiO2/ACF复合材料吸附耦合光催化去除甲苯的研究
2019-07-31戴业欣李雨薇齐学进赵朝成王永强
戴业欣,李雨薇,齐学进,李 孟,薛 明,刘 芳,赵朝成,王永强
(1.石油石化污染物控制与处理国家重点实验室,北京 102206;2.中国石油大学(华东)化学工程学院,山东 青岛 266580)
石油石化行业作为国民经济的支柱产业,为社会发展提供必要的石油能源和化工产品,但同时带来的环境污染问题也日益突出。石化企业排放的废气组分复杂,其中以挥发性有机物(VOCs)为主要组分,包括多种有毒有害气体,其中污染物主要有苯系物、醛酮类、卤代烃、醇类等,部分成分具有致癌性,严重威胁大气环境及人类健康[1-3]。因此,如何有效去除VOCs已引起国内外学者的广泛关注。
为去除工业排放的VOCs,已经开发的多种物理化学技术主要包括吸附[4]、凝结[5]、焚烧[6]、催化燃烧[7]、光催化等[8]。其中,吸附法是最有效的技术之一,可以去除中低浓度的VOCs。吸附技术的核心为吸附剂的选择,其中,分子筛[9]、金属有机骨架(MOFs)[10-11]、碳材料[12-13]等吸附剂是吸附VOCs的研究热点。与其他吸附剂相比,活性碳纤维(ACF)对小分子物质的吸附速率快,具有较大的吸附容量、表面积、高孔隙率和表面吸附反应性[14]。然而,当吸附剂经过长时间吸附达到饱和状态后,将无法进一步去除污染物质。当外部环境发生变化,如温度升高或压力降低时,吸附质可能会从吸附剂上脱附,造成二次污染[15]。
除吸附方法外,光催化法也是一种环保、高效的去除VOCs的方法。二氧化钛(TiO2)具有优良的催化性能、良好的化学稳定性、温和的操作条件和廉价的可用性。但由于TiO2的电子-空穴复合,导致量子效率低,限制了其实际应用[16]。将碳纳米管(CNTs)和碳量子点与TiO2催化剂耦合[17-18],为充分利用太阳光开辟了新的途径。碳材料具有优异的光诱导电子转移、电子储存和良好的光致发光行为。碳基TiO2复合材料可以阻碍电子-空穴复合并增强其光催化活性[19]。Wu等[20]采用溶胶凝胶法制备碳纳米管/TiO2复合材料不仅增加了复合材料的表面积,还促进了电荷的分离与稳定,减少了电子-空穴复合,提高了催化反应的效率。
本研究中,笔者采用超声辅助溶胶-凝胶浸渍法制备TiO2/ACF薄膜多孔复合材料,并采用多种分析手段对TiO2/ACF复合材料进行了表征。在自行建立的连续反应器中,以甲苯为处理对象,考察了光照、浸渍次数、甲苯初始浓度、气体流量以及光强等因素对TiO2/ACF复合材料去除甲苯的影响。
1 实验部分
1.1 原料及试剂
钛酸四丁酯、无水乙醇、乙酸、氨水、硝酸、二硫化碳、甲苯、聚乙二醇400、二硫化碳、CS2,均为AR试剂,国药集团化学试剂有限公司产品;活性碳纤维(ACF),宿州市九洲龙环保设备制造有限公司产品。
1.2 实验装置及仪器
HJ-6A型六联磁力搅拌器,天津市泰斯勒仪器有限公司产品;RS80/750/11型管式加热炉;THZ-88型超声波清洗机,金坛市医疗仪器厂产品;DHG-9240A型电热恒温鼓风干燥箱,杭州蓝天化验仪器厂产品;PHS-3C型雷磁pH计,上海精密科学仪器有限公司产品;AL204型分析天平,梅特勒·托利多仪器有限公司产品;活性炭采样管,北京市劳动保护科学研究所产品。
TiO2/ACF复合材料光降解耦合吸附去除甲苯实验装置如图1所示。该装置主要由4部分组成:气体发生装置、光催化反应器、气样检测系统及尾气吸收装置。气体发生装置采用空气泵将空气通入盛有甲苯的试剂瓶中,通过鼓泡的方式制备甲苯气体,然后通过质量流量计调节甲苯气体、空气以及含有水蒸气空气的流量,在缓冲瓶中混合,制备出具有一定甲苯浓度和一定湿度的甲苯混合气体,然后通入光催化反应器中。光催化反应器外壳为圆柱形的不锈钢,内部装有3个紫外灯,TiO2/ACF复合材料置于透明的石英管内,是光催化降解甲苯的场所。在光催化反应器前后设有气体取样口,甲苯浓度通过气相色谱仪检测得到。装置的尾部用盛有聚乙二醇400的吸收瓶吸收处理尾气。

图1 甲苯光降解耦合吸附去除甲苯实验装置Fig.1 Experimental setup of coupling adsorption with photocatalysis for the removal of toluene(a)Appearance;(b)Internal structure diagram
1.3 活性炭纤维(ACF)活化
为了将ACF孔隙中的杂质去除,在使用前需对其进行活化处理,具体活化处理步骤如下:
①将ACF裁剪成10 cm×10 cm×2 mm的方块;②配置氨水与水体积比为1∶1的氨水溶液,将ACF置于氨水溶液中浸泡30 min,用去离子水清洗3次,将ACF中的水分尽量压干;③配置硝酸与水体积比为1∶1的硝酸水溶液,将经②处理后的ACF置于硝酸溶液浸泡30 min,用去离子水清洗3次,用镊子将ACF中的水分尽量压干;④配置乙醇与水体积比为1∶1的乙醇水溶液,将经③处理后的ACF置于乙醇溶液中浸泡30 min,超声清洗3次,再用去离子水清洗3次;⑤放入烘箱中 105 ℃ 烘干,备用。
1.4 制备TiO2/ACF复合材料
取34 mL无水乙醇与17 mL乙酸混合,将 10 mL 钛酸四丁酯加入无水乙醇和乙酸的混合液中,磁力搅拌器搅拌30 min,制得溶液A;将 10 mL 无水乙醇、30 mL去离子水及2 mL乙酸混合,用磁力搅拌器搅拌30 min,制得溶液B;磁力搅拌速率控制在800 r/min左右,将B溶液逐滴滴入A溶液中。滴加完毕,搅拌2 h,在25 ℃下陈化24 h;将活化好的ACF裁剪成2 cm×2 cm×2 mm的小方块,放入上述陈化后的溶胶中,超声5 min,再浸渍30 min;取出浸渍后的复合材料放入烘箱中105 ℃烘干2 h,待其慢慢冷却至室温,此为浸渍1次。将烘干的浸渍后ACF放入管式炉中,在氮气的保护下,以5 ℃/min升温速率升到450 ℃焙烧2 h,制得TiO2/ACF复合材料。按上述方法,将ACF放入陈化后的溶胶中分别浸渍1、3、5次,通过改变浸渍次数,可获得不同TiO2负载量的 TiO2/ACF 复合材料,分别记为TiO2/ACF-1、TiO2/ACF-3、TiO2/ACF-5。
1.5 TiO2/ACF复合材料的表征
采用日立S4800型场发射扫描电子显微镜(SEM)观察复合材料的尺寸、形貌;采用荷兰帕纳科公司AXIOS-Petro X射线荧光光谱仪检测样品的晶体结构;采用美国Thermo Nicolet公司NEXUS傅里叶变换红外光谱仪对材料的官能团进行表征;采用美国麦克仪器公司ASAP3020比表面分析仪测定材料的比表面积及孔径分布;采用赛默飞世尔X射线光电子能谱仪分析样品表面的元素组成及元素价态;采用北京普析通用仪器公司TU-1901双光束紫外可见分光光度计测定材料的光吸收性能;采用上海棱光技术有限公司F97PRO型荧光分光光度计对样品进行检测,研究材料中光生电子的转移与复合。
1.6 甲苯采集
实验前,检查装置气密性,检查完毕后,装置空运行30 min,待装置运行稳定后开始实验。采样方法:在玻璃注射器及取样口之间连接溶剂解析型活性炭采样管,每次采集100 mL气体。采集完最后一个气样后,在进气口采集空白气样。
1.7 甲苯浓度测定
采集气样的甲苯浓度利用北分瑞利SP-3420A气相色谱仪测定。操作条件为:以氢气为燃烧气,空气为助燃气,氮气为载气,氢火焰离子化检测器(FID)为检测器;进样口温度为150 ℃,吸附柱柱温为120 ℃,检测器温度为200 ℃。利用CS2解析法解析吸附管中的甲苯:将采样管中的活性炭取出,加入1 mL CS2溶液,解析1 h。解析完毕,用微量进样器取2 μL解析液进行检测。
1.8 TiO2负载量测定
取3份相同浸渍次数的TiO2/ACF复合材料(2 cm×2 cm×2 mm)称重,质量记为m1(单位为g),将复合材料放入马弗炉850 ℃焙烧5 h,黑色活性碳纤维被烧完,剩余白色粉末质量记为m2(单位为mg),对相同大小的ACF做空白实验,同样在马弗炉850 ℃焙烧5 h,称量残留灰分记为m3(单位为mg)。不同浸渍次数的TiO2/ACF复合材料上TiO2负载质量分数计算公式见式(1)。
(1)
2 结果与讨论
2.1 TiO2/ACF复合材料的表征
2.1.1 扫描电子显微镜(SEM)分析
图2为ACF及TiO2/ACF系列复合材料SEM照片。由图2(a)和(b)可以观察到大量的ACF无序地交织在一起,每根纤维表面光滑并且拥有沿纵向排列的线性凹槽和脊[21]。从图2(d)、(f)、(h)可以看出,ACF的光滑表面已经被粗糙的TiO2薄膜覆盖,且仍保留有光滑表面,但有轻微薄膜从纤维剥落,意味着TiO2以光滑膜的形式较均匀地负载于ACF上。从图2(g)可以看出,浸渍5次的 TiO2/ACF-5 复合材料在ACF周围出现大颗粒或簇状TiO2块体,堵塞了吸附孔道。
2.1.2 X射线衍射图谱(XRD)分析
TiO2、ACF及TiO2/ACF-3的XRD晶型表征如图3所示。TiO2存在3种晶相,包括金红石、锐钛矿和板钛矿[22]。其中,板钛矿相很少见,也最难制备。与金红石相比,锐钛矿相具有更好的光催化效率[23-24]。通过与PDF卡(JCPDS No.21-1272)进行对比发现,图3中TiO2在2θ为25.3°(101)、37.8°(004)、48°(200)、54°(105)、55°(211)、63°(204)处分别出现6个特征峰均为TiO2锐钛矿相的特征峰,表明在450 ℃煅烧所得的TiO2主要以锐钛矿的形式存在。ACF在2θ为25°、44°处出现的宽峰,表明ACF具有类石墨的晶型结构,是典型的无定形结构[25]。TiO2/ACF-3复合材料在2θ为25.3°(101)、37.8°(004)、48°(200)、54°(105)、55°(211)、63°(204)处分别出现6个TiO2特征峰,而并未出现ACF的无定型特征峰,表明通过溶胶凝胶浸渍的方法获得的TiO2/ACF-3复合材料中的TiO2主要是以锐钛矿的形式负载于ACF上。采用谢乐公式[21]计算晶粒尺寸,得出TiO2纳米颗粒的粒径为36.6 nm,而TiO2/ACF-3中TiO2颗粒的粒径为27.3 nm。由于较小的晶体尺寸有利于光催化反应的进行,因此,这似乎意味着TiO2/ACF-3中的TiO2比单体TiO2具有更高的光催化活性[26]。

图2 ACF及TiO2/ACF系列复合材料的SEM照片Fig.2 SEM images of ACF and TiO2/ACF composites(a),(b)ACF;(c),(d)TiO2/ACF-1;(e),(f)TiO2/ACF-3;(g),(h)TiO2/ACF-5
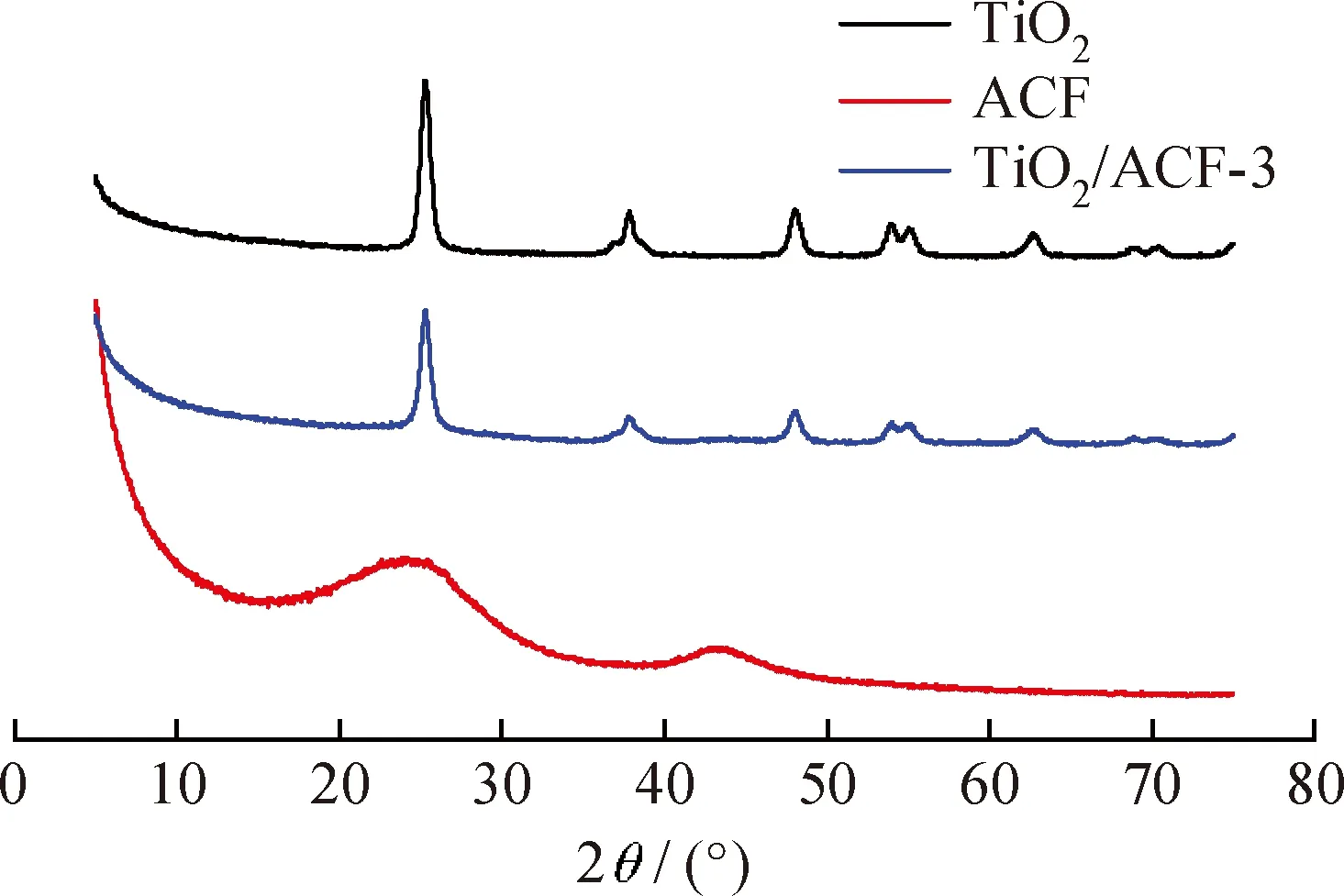
图3 TiO2、ACF及TiO2/ACF-3的XRD谱Fig.3 XRD patterns of TiO2,ACF and TiO2/ACF-3
2.1.3 傅里叶红外光谱(FITR)分析
图4为TiO2、ACF及TiO2/ACF-3复合材料的傅里叶红外光谱图。图4中,在3436 cm-1附近对应的是O—H伸缩振动引起的吸收峰,表明ACF表面及TiO2表面存在大量的O—H。TiO2在 1635 cm-1附近出现的吸收峰为TiO2的O—H弯曲振动吸收峰。一般认为,这是在溶胶凝胶法制备TiO2的过程中产生的[27]。在1084 cm-1附近的峰,是Ti—O伸缩振动引起的吸收峰。在500~700 cm-1处的吸收峰为Ti—O—Ti的骨架振动吸收峰。1084 cm-1处的吸收峰是由Ti—O—C键引起的,说明TiO2/ACF-3中TiO2与ACF结合比较牢固[28]。TiO2/ACF-3复合材料中含有大量的—OH、C—O等含氧官能团。这些官能团的存在将有利于复合材料对甲苯的吸附及光降解。
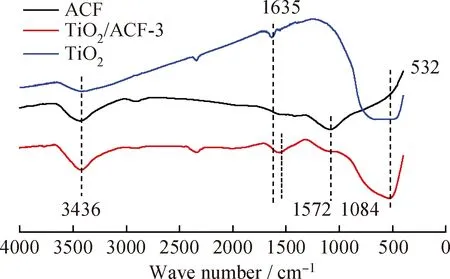
图4 TiO2、ACF及TiO2/ACF-3复合材料的傅里叶红外光谱Fig.4 Infrared spectrum of TiO2,ACF and TiO2/ACF-3
2.1.4 N2吸附-脱附等温线分析
图5为ACF及TiO2/ACF系列复合材料的氮气吸附-脱附等温线。根据BET法及BJH模型计算得到样品中的比表面积、孔体积和孔径分布如表1所示。
由图5可知,4种材料的N2吸附-脱附等温线的形状大致相同。在低于0.1的相对压力下吸附,在0.5~1.0之间存在明显的吸附回滞环,属于IUPAC分类中Ⅳ型等温线,回滞环属于H4型,表明孔结构很不规整,且存在微孔和介孔混合[29]。由表1可知,4种材料的比表面积均比较大,相比于空白活性碳纤维(ACF)的比表面积,TiO2/ACF复合材料的比表面积随浸渍次数的增加而降低,当浸渍次数达到5次时,材料的比表面积降至752.29 m2/g。在浸渍过程中,TiO2负载量随浸渍次数增加而增加,当ACF吸附量达到饱和后,TiO2将发生团聚,形成TiO2块状颗粒堵塞孔道,因此导致比表面积大幅下降。这与SEM表征结果一致。
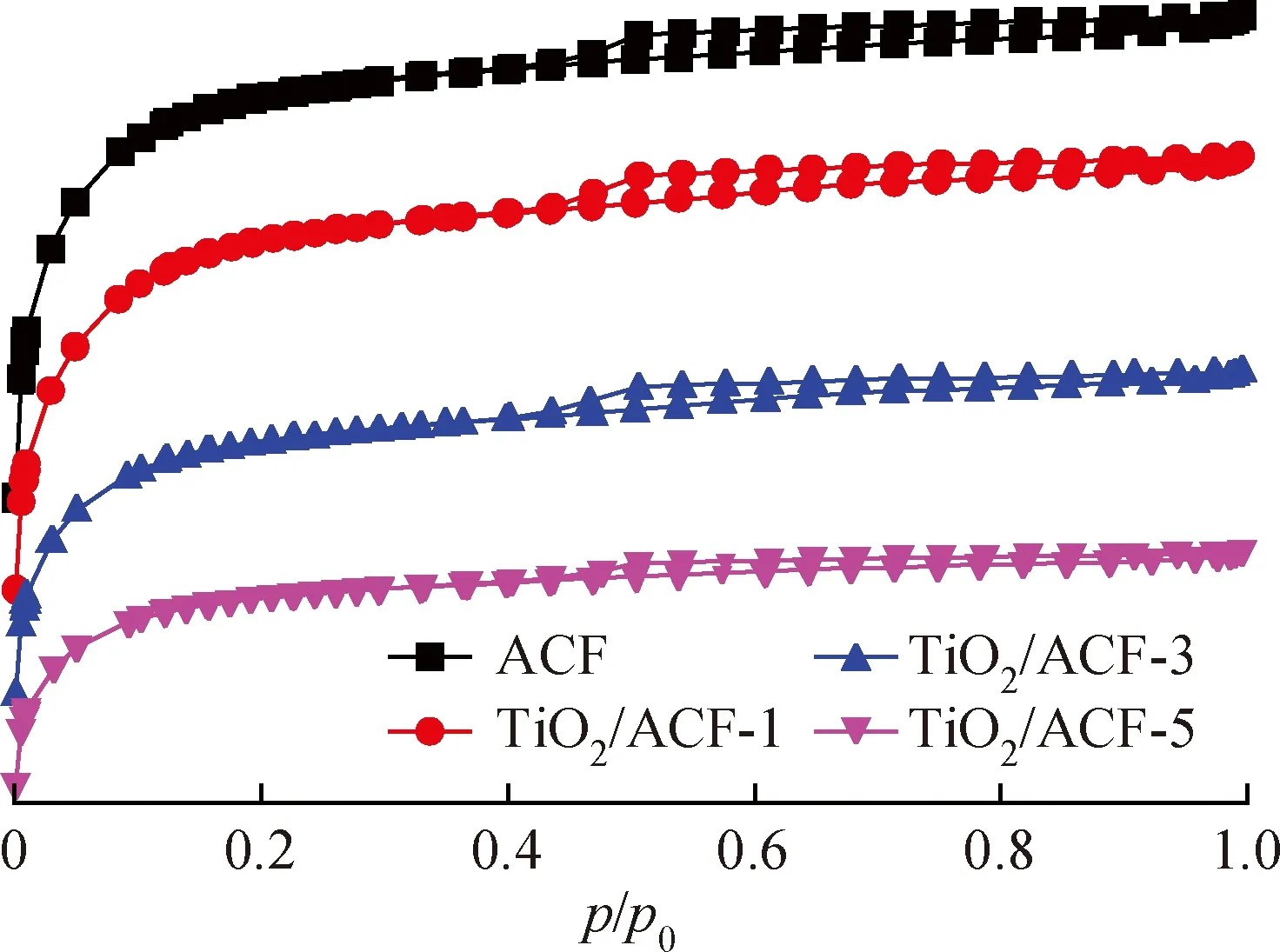
图5 ACF及TiO2/ACF系列复合材料的N2吸附-脱附等温线Fig.5 N2 adsorption-desorption isotherm of ACF and TiO2/ACF composites
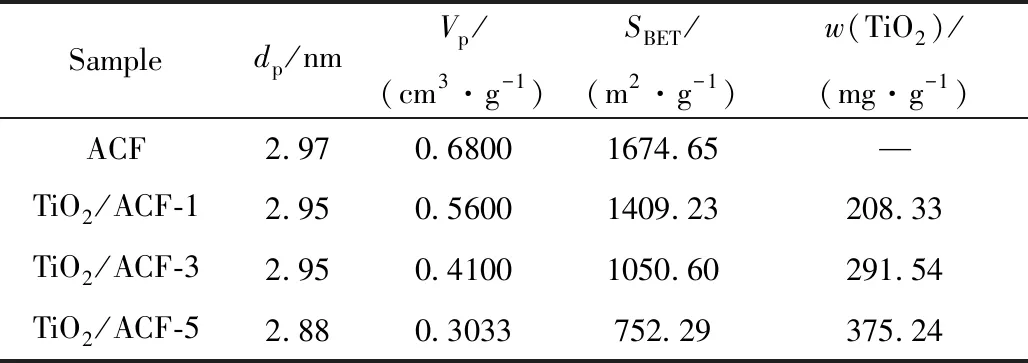
表1 ACF及TiO2/ACF系列复合材料的比表面积、孔径、孔体积Table 1 Specific surface area,pore size,pore volume of ACF and TiO2/ACF composites
2.1.5 X射线光电子能谱(XPS)分析
图6(a)为TiO2/ACF-3复合材料的全谱图,图6(b)~(d)显示了TiO2/ACF-3复合材料中C1s、Ti2p和O1s的高分辨XPS谱图。图6(b)的Ti2p的XPS谱图可拟合为结合能分别为458.9 eV和464.8 eV 的2个峰,分别对应于Ti2p1/2轨道以及Ti2p3/2轨道,这表明TiO2/ACF-3复合材料中的Ti主要是以Ti4+的形式存在[29]。图6(c)中O1s在结合能位于531.05 eV的主峰属于Ti—O—Ti(晶格O)[30];位于532.55 eV的峰归因于TiO2的 Ti—OH 和TiO2/ACF复合材料的Ti—C—O[30],其中O以—OH的形式存在于TiO2/ACF-3复合材料表面。这有利于·OH的生成,进而能够提高TiO2/ACF-3复合材料对甲苯的光降解性能。图6(d)中C1s在结合能为284.6 eV处的峰被认为归属于石墨碳(C—C)[31],结合能为286.4 eV处的峰被认为归属于C—O[32]。
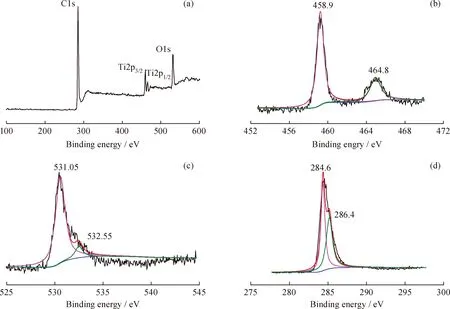
图6 TiO2/ACF-3复合材料的X射线光电子能谱图Fig.6 X-ray photoelectron spectra of TiO2/ACF-3 composites(a)Wide-scan spectrum;(b)Ti2p diffraction pattern;(c)O1s diffraction pattern;(d)Cls diffraction pattern
2.1.6 紫外可见吸收光谱(UV-vis)分析
应用UV-vis DRS进一步研究催化剂的光学性质。图7为TiO2、ACF和TiO2/ACF-3复合材料的UV-vis DRS光谱及对应的(F(r)hν)1/2能谱图。由图7(a)可知:TiO2在波长小于380 nm的紫外光区域具有明显的吸收,而在大于400 nm的非紫外光区域几乎没有吸收,光吸收波长范围窄,对太阳能的利用效率低;ACF及TiO2/ACF-3在可见光区(400~800 nm)表现出强吸收,可能是由于ACF是黑色的。在TiO2/ACF-3复合材料中可以清楚地看到TiO2的特征吸收边缘,且吸收边红移,表明复合材料可以响应较长波长的光线,提高对太阳光的利用效率。
图7(b)中利用(F(r)hν)1/2对hν作图,将直线部分延伸至横坐标,与横坐标的交点即为禁带宽度[32]。由图7(b)可知:TiO2的禁带宽度为3.17 eV;TiO2/ACF-3复合材料的禁带宽度为2.25 eV,禁带宽度相较于TiO2变窄。
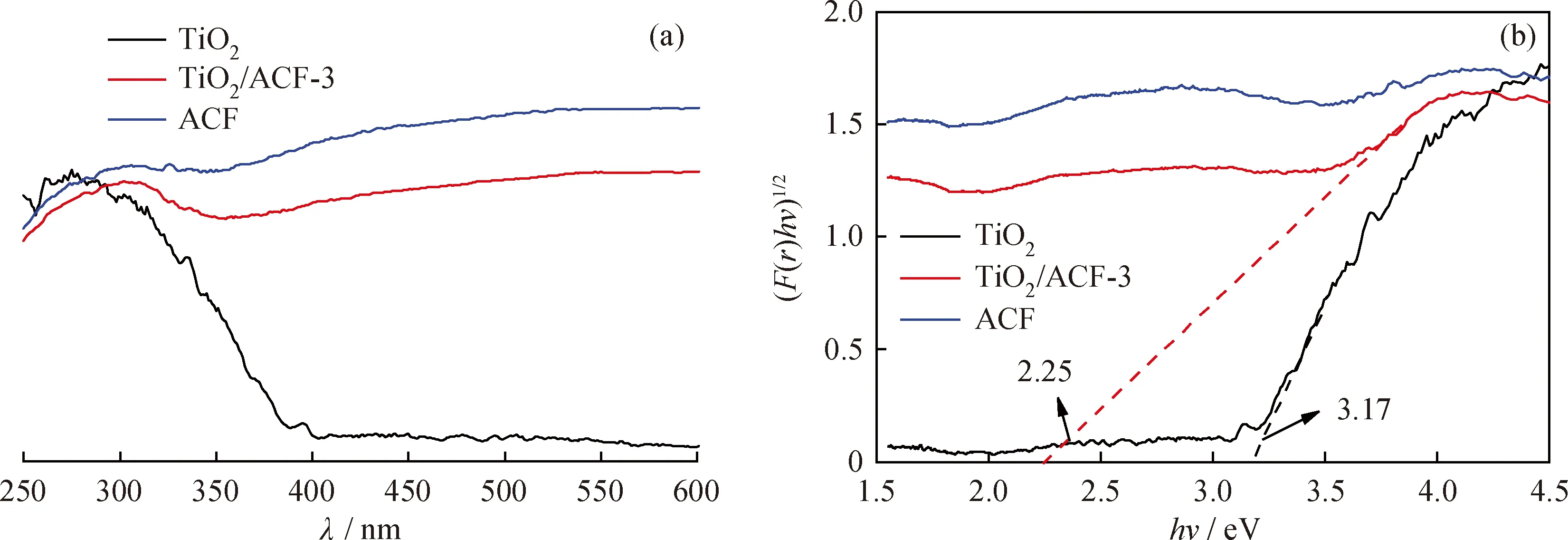
图7 TiO2、ACF和TiO2/ACF-3复合材料的紫外可见吸收光谱及对应的(F(r)hν)1/2能谱图Fig.7 UV-visible absorption spectra and (F(r)hν)1/2 energy spectra of TiO2,ACF and TiO2/ACF-3(a)UV-visible absorption spectra;(b)(F(r)hν)1/2 energy spectra
以[F(r)×hν]n/2/hν作图并做切线可得光催化剂带隙能,光催化剂带隙能可用Kubelka-Muck函数方程计算,见式(2)。
(2)
式(2)中,K为样品吸收系数;S为样品反射系数;r为样品的漫反射率,%;h为普朗克常量,eV·s;ν为光频率(Hz),当样品为直接半导体时n=4,间接半导体时n=1,TiO2为间接半导体。
2.1.7 光致发光光谱分析
图8为TiO2、ACF及TiO2/ACF-3复合材料在305 nm激发波长处荧光光致发光光谱(PL)。由图8看到:TiO2的PL发射光谱在波长414和472 nm处显示出两个主峰;在414 nm处的峰是由声子辅助从边缘到布里渊区中心的间接过渡产生的[33];472 nm处的发射峰是由电荷从Ti3+转移到TiO62-八面体产生的[34]。当TiO2与ACF复合时,TiO2/ACF-3 复合材料的PL信号减弱,由于ACF具有较强的电子转移能力,降低了TiO2的电子与空穴复合,从而提高了光催化反应效率[35]。从图8中还能发现,TiO2具有一个很高且很宽的荧光发射峰,但TiO2/ACF-3复合材料的荧光发射峰较TiO2的荧光发射峰有明显的减弱。荧光发射光谱是电子与空穴的复合产生的,所以电子与空穴的复合数的多少决定了荧光发射峰的强弱[36]。TiO2/ACF-3复合材料中的ACF具有良好的电子转移能力,将TiO2的光生电子与空穴分离,能有效抑制光生电子与空穴的复合,提高TiO2的光催化活性。

图8 TiO2、ACF及TiO2/ACF-3复合材料的光致发光光谱(PL)Fig.8 PL of TiO2,ACF and TiO2/ACF-3
2.2 外界条件对TiO2/ACF复合材料去除甲苯的影响
2.2.1 有无光照的影响
在甲苯初始质量浓度370 mg/m3、甲苯气体流量120 mL/min条件下,光催化反应器中放入浸渍3次的TiO2/ACF-3复合材料,连续通入甲苯气体,以功率24 W的紫外灯作为光源,考察有无光照条件下TiO2/ACF-3复合材料对甲苯的去除率随时间的变化,结果如图9所示。

图9 有无光照条件下TiO2/ACF-3复合材料对甲苯的去除率随反应时间(t)的变化曲线Fig.9 Effects of the light on the toluene removal of TiO2/ACF-3 vs t with or without UV lightC0(Toluene)=370 mg/m3;qν=120 mL/min;T=25 ℃;P(UV light)=24 W
由图9可知:在无光照条件下,TiO2/ACF-3复合材料在40 min左右就达到穿透点,之后随反应时间增加对甲苯的吸附速率开始下降,在 180 min 左右吸附达到饱和;而在光照条件下,TiO2/ACF-3复合材料的穿透时间为80 min,在160 min左右对甲苯的去除率开始趋于稳定,稳定在65%左右。在光照条件下,TiO2/ACF-3复合材料对甲苯的去除率明显比无光照条件下高。这是因为复合材料中的ACF对甲苯的吸附与TiO2对甲苯的光降解作用具有协同作用。TiO2在紫外光下能激发生成电子和空穴,进而生成·OH等具有强氧化性的自由基,自由基能降解吸附在其表面的甲苯,使得ACF对甲苯的吸附能力得以再生。这说明TiO2/ACF-3对甲苯具有持续去除的能力,且去除效果良好。
2.2.2 浸渍次数的影响
在甲苯初始质量浓度370 mg/m3、甲苯气体流量120 mL/min、功率24 W紫外灯作为光源条件下,在反应器中分别放入浸渍次数为1次、3次、5次的TiO2/ACF系列复合材料,连续通入甲苯气体,研究浸渍次数对TiO2/ACF系列复合材料去除甲苯的影响,结果见图10。
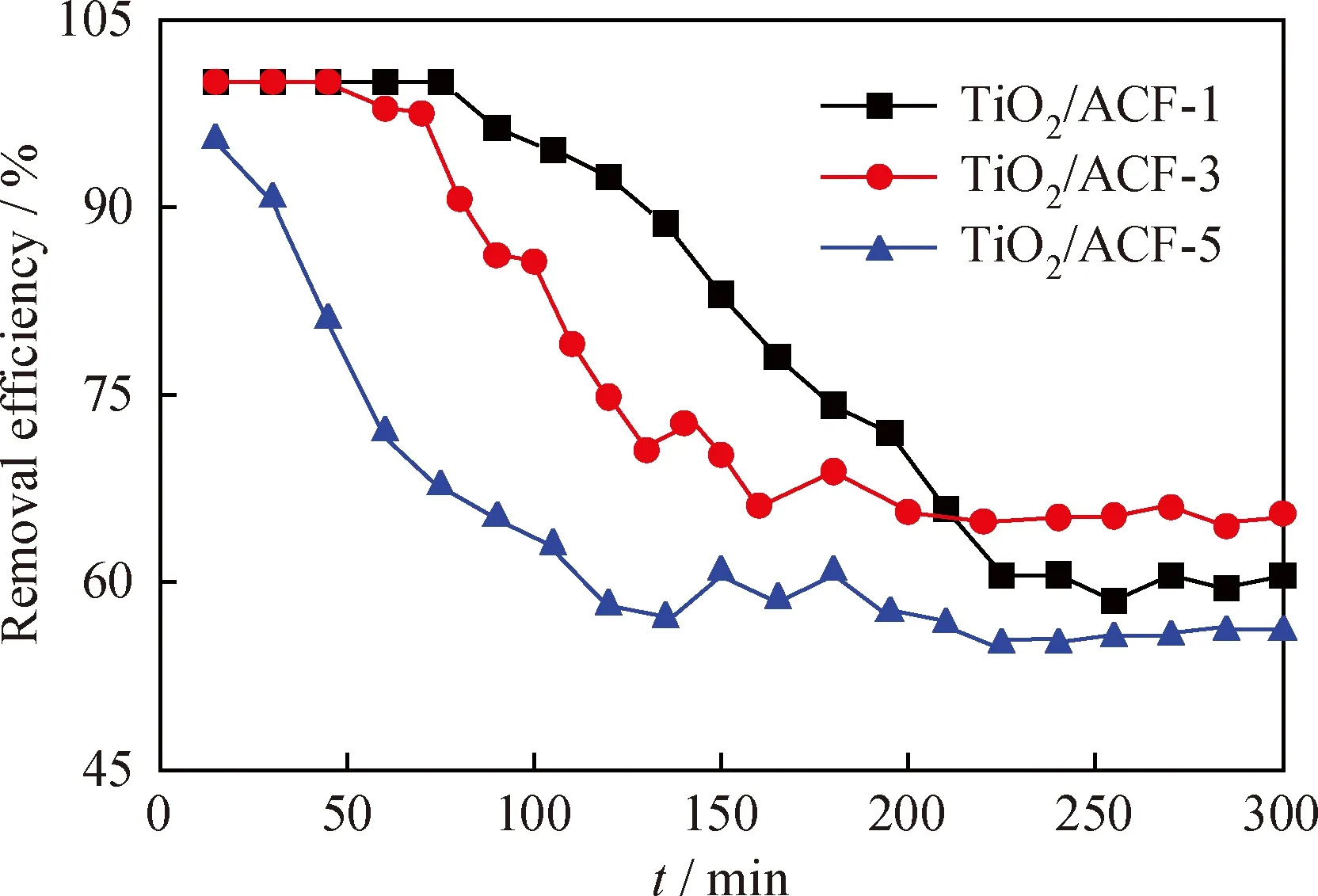
图10 不同浸渍次数条件下TiO2/ACF系列复合材料对甲苯的去除率随反应时间(t)的变化曲线Fig.10 The removal rate of toluene of TiO2/ACF composites vs t with different dipping timesC0(Toluene)=370 mg/m3;qν=120 mL/min;T=25 ℃;P(UV light)=24 W
由图10看到:随着反应时间增加,TiO2/ACF-5复合材料迅速达到穿透点,对甲苯的去除率开始降低;而TiO2/ACF-1复合材料在75 min左右对甲苯的去除率才开始下降,达到穿透点。TiO2/ACF-1、TiO2/ACF-3和TiO2/ACF-5对甲苯的吸附-光降解依次在225 min、160 min、120 min左右达到平衡,对甲苯的去除率趋于稳定,去除率分别为57%、65%、53%。最终达到平衡后,对甲苯的去除率从大到小顺序依次为TiO2/ACF-3、TiO2/ACF-1、TiO2/ACF-5。这是因为随着浸渍次数的增加,ACF上负载的TiO2量越多,复合材料比表面积及平均孔体积均急剧减小,使得复合材料对甲苯的吸附性能急剧降低,TiO2表面的甲苯减少,TiO2光降解甲苯的速率降低。同时这也说明,ACF的吸附性能与TiO2的光催化性能之间存在协同作用。因此,TiO2/ACF复合材料的最佳浸渍次数为3次。
2.2.3 甲苯初始浓度的影响
使用功率24 W的紫外灯作为光源,甲苯气体流量为120 mL/min,光催化反应器中放入TiO2/ACF-3复合材料,连续通入甲苯气体,考察不同初始甲苯质量浓度下TiO2/ACF-3复合材料对甲苯的去除率随时间的变化曲线,如图11所示。
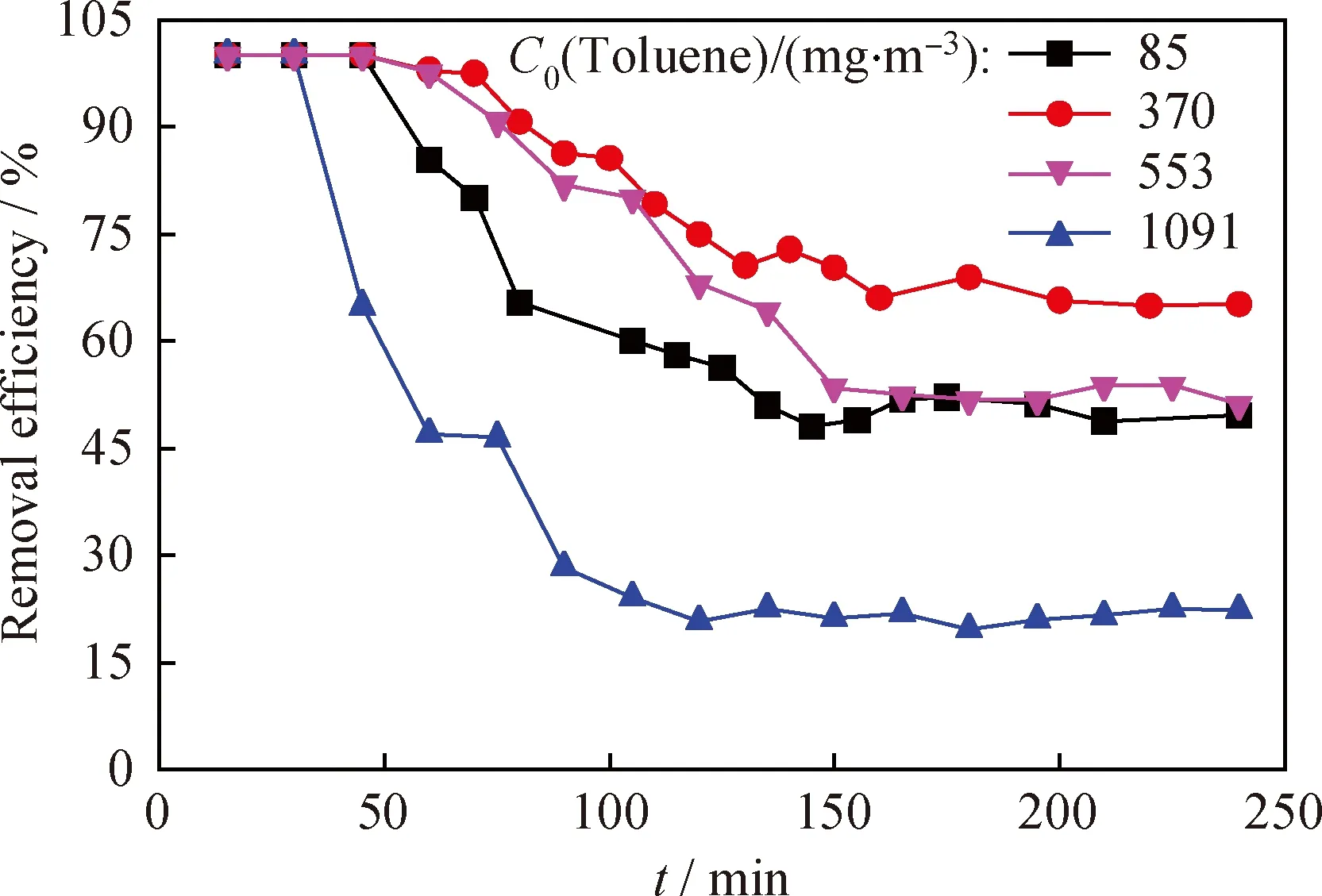
图11 不同甲苯初始质量浓度下TiO2/ACF-3复合材料对甲苯的去除率随反应时间(t)的变化曲线Fig.11 The removal rate of toluene of TiO2/ACF-3 composites vs t with different initial mass concentrations of tolueneqν=120 mL/min;T=25 ℃;P(UV light)=24 W
从图11可以看出,随着甲苯初始浓度的增加,甲苯的吸附-光降解达到平衡后,TiO2/ACF-3复合材料对甲苯的去除率先升高后降低。这是由于TiO2/ACF-3复合材料光降解甲苯的过程可以用Lagmium-Hinsherwood动力学方程进行描述[37]。根据Lagmium-Hinsherwood一级动力学方程,在低浓度下,随着甲苯浓度的增加,TiO2/ACF-3复合材料对甲苯的去除率升高。在甲苯初始质量浓度为370 mg/m3时,对甲苯的去除率最大。甲苯浓度继续增大,光催化反应产生的中间产物也会增加,中间产物会与甲苯分子争夺ACF表面的吸附活性位点及TiO2表面的活性位点,导致ACF的吸附性能及TiO2的光催化降解性能降低,因此TiO2/ACF-3复合材料对甲苯的去除率降低;另一方面,由于甲苯浓度过高,有大量甲苯分子未能与TiO2表面的活性位点接触便被排出了反应器,也会使TiO2/ACF-3对甲苯的去除率降低。因此,当甲苯初始质量浓度为 370 mg/m3时去除率可达最大65%。
2.2.4 甲苯气体流量的影响
使用功率24 W的紫外灯作为光源,在光催化反应器中放入TiO2/ACF-3复合材料,在甲苯的初始质量浓度为370 mg/m3条件下,考察不同甲苯气体流量下TiO2/ACF-3对流动态甲苯的去除率随时间的变化曲线,见图12。
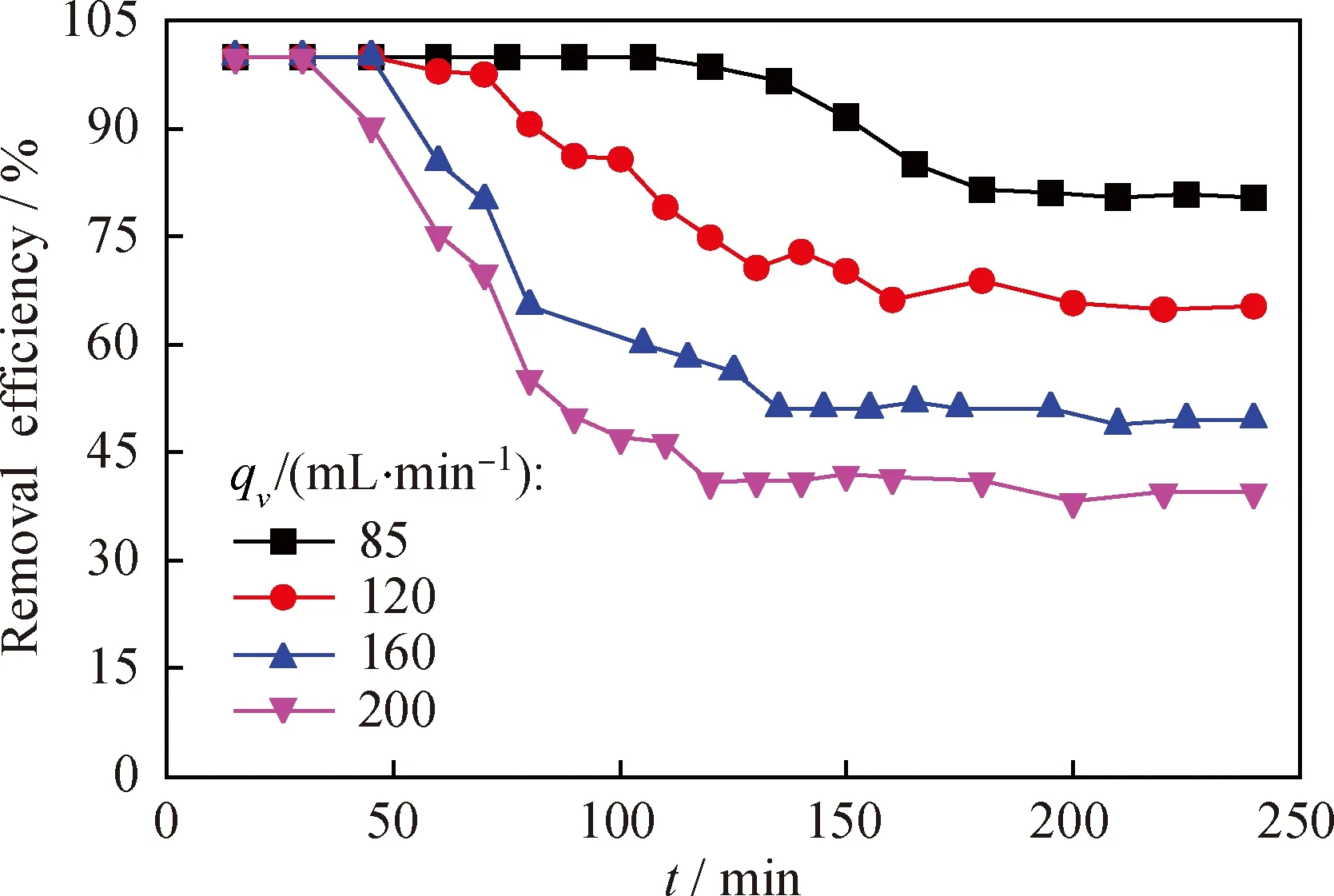
图12 不同甲苯气体流量条件下TiO2/ACF-3复合材料对甲苯的去除率随反应时间(t)的变化曲线Fig.12 The removal rate of toluene of TiO2/ACF-3 composites vs t with different gas flow ratesC0(Toluene)=370 mg/m3;T=25 ℃;P(UV light)=24 W
从图12可以看出,随着甲苯气体流量的增加,TiO2/ACF-3复合材料对甲苯吸附的穿透时间在变短。甲苯气体流量为85 mL/min时,复合材料的穿透时间在120 min左右;当甲苯气体流量为200 mL/min 时,复合材料的穿透时间缩短到 30 min 左右。随着甲苯气体流量的增加,TiO2/ACF-3 复合材料对甲苯的去除效率在减小。气体流量为85 mL/min时,对甲苯的去除率约为80%;当气体流量增加到200 mL/min时,对甲苯的去除率降到40%左右。这是由于气体流量增加,导致甲苯分子在TiO2/ACF-3复合材料表面的停留时间变短,不利于对甲苯分子的吸附;复合材料表面甲苯分子的浓度降低,且甲苯分子的停留时间过短,造成TiO2对甲苯的光催化降解效率降低。虽然通过降低气体的流量可以有效提高TiO2/ACF-3复合材料对甲苯的去除率,但同时对气体的处理量却也在减小。在实际应用中不仅需要考虑到对气体的去除率,也应该考虑到气体的处理量,从而选择合理的气体流速。因此,甲苯气体流量为 85 mL/min 时TiO2/ACF-3复合材料对甲苯的去除率最大,为80%。
2.2.5 光强的影响
在甲苯的初始质量浓度为370 mg/m3、气体流量为120 mL/min条件下,光催化反应器中放入TiO2/ACF-3复合材料,以紫外灯作为光源,调节紫外灯的功率分别为8 W、16 W、24 W,考察不同光强下TiO2/ACF-3复合材料对流动态甲苯的去除率随时间的变化曲线,如图13。
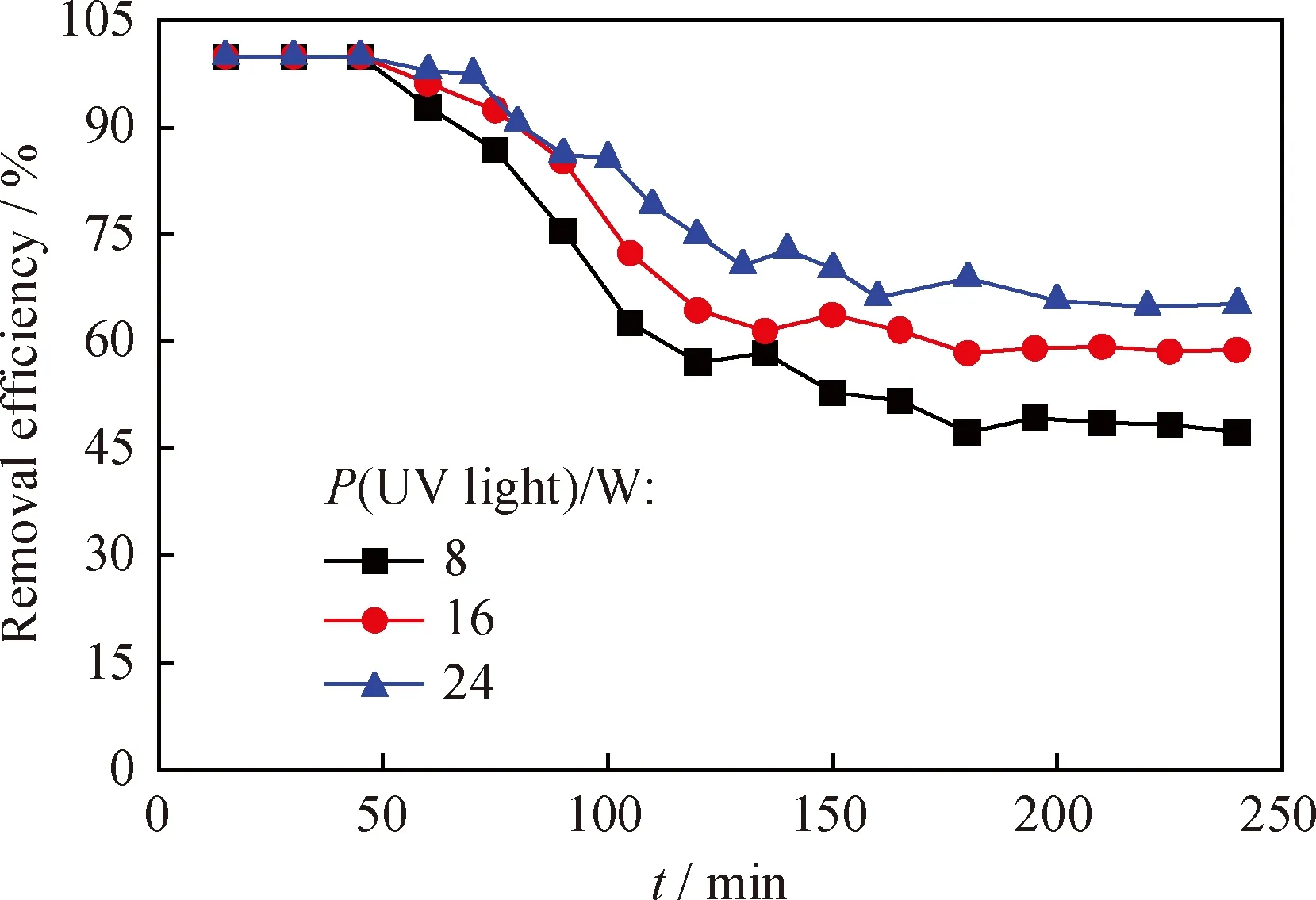
图13 不同光强下TiO2/ACF-3复合材料对流动态甲苯的去除率随时间的变化曲线Fig.13 The removal rate of toluene of TiO2/ACF-3 composites vs t under different light intensitiesC0(Toluene)=370 mg/m3;qν=120 mL/min;T=25 ℃
由图13可知,当紫外灯的功率为8 W、16 W、24 W,TiO2/ACF-3复合材料对甲苯的去除率分别为48%、59%、65%;随着光强的增强,TiO2/ACF-3 复合材料对甲苯的去除率在升高,紫外灯的功率为24 W时,TiO2/ACF-3复合材料对甲苯的去除率最高。一般来说,当光源的波长一定时,光强变大,照射到TiO2表面的光量子数增加,所激发的电子和空穴的数量也会增加,产生更多的具有强氧化性的·OH自由基,因此对甲苯的去除率也会升高[36]。但是,紫外灯的功率由8 W增强到16 W,TiO2/ACF-3复合材料对甲苯的去除率增加了23%;而功率由16 W增强到24 W时,TiO2/ACF-3复合材料对甲苯的去除率却只增加10%。这表明,光强与甲苯的去除率之间并不是成正比的关系。随着光强的增加,TiO2所激发出来的电子和空穴的数量会成正比的增加,但同时电子与空穴复合的速率变大;另一方面,随着紫外灯功率的增加,紫外灯的热效应也会愈加明显,紫外灯的功率增加,会导致光催化反应器内的温度升高,不利于ACF对甲苯的吸附,进而影响对甲苯的去除。
3 TiO2/ACF复合材料对甲苯的吸附耦合光催化去除机理分析
图14为TiO2/ACF复合材料去除甲苯气体示意图。在紫外光照条件下,活性碳纤维富集甲苯,TiO2表面产生负电子e-与强氧化性的空穴h+。由于浓度差和吸附能力两个因素协同作用,吸附态甲苯扩散到TiO2表面。电子与吸附在复合薄膜上的O2反应生成超氧根自由基(·O2-);同时空穴h+与吸附在复合材料上的OH-和H2O发生氧化反应生成氧化性更强的羟基自由基(·OH)。甲苯与上述自由基发生氧化反应生成H2O、CO2以及一些中间产物。其中,H2O和CO2等小分子从复合材料表面脱附,使吸附剂得到原位再生。甲苯光催化反应途径主要为两种,即支链甲基氧化与苯环氧化,其中支链氧化为主要途径[38]。何奕明等[39]采用气相色谱-质谱联用仪(GC-MS)对甲苯降解中间产物进行分析,结果表明其主要中间产物为苯甲醛、苯乙酸、苯、甲酸甲酯、丙烯醛、乙烯等。分析认为:在光照条件下,甲苯可能发生脱氢反应生成苄基自由基,苄基自由基与羟基自由基反应生成苯乙酸,苯乙酸分解生成苯与羟基乙酸,最终氧化为H2O与CO2;苄基自由基可能与羟基自由基发生反应生成苯甲醇,苯甲醇脱羟甲基后与氢自由基反应生成苯与甲醇;苄基自由基可能与O2和e-发生反应生成苯甲醛与羟基,苯甲醛与羟基自由基反应生成苯甲酸,苯甲酸分解生成苯与甲酸,甲酸与甲醇发生酯化反应生成甲酸甲酯,甲酸甲酯最终被氧化为H2O与CO2;苯甲醛的C—C键可能发生断裂生成乙烯和丙烯醛,最终被氧化为H2O与CO2。
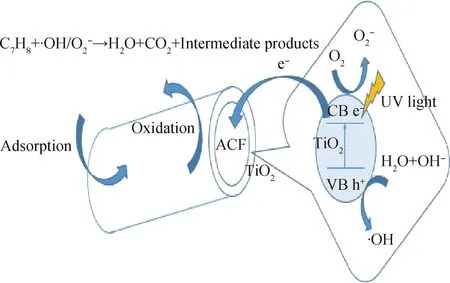
图14 TiO2/ACF复合材料去除甲苯气体示意Fig.14 Schematic diagram of the removal of toluene gas from TiO2/ACF composites
4 结 论
(1)采用超声辅助溶胶凝胶浸渍法制备的 TiO2/ACF 复合材料具有优异的吸附-光催化性能,可用于动态去除甲苯。通过吸附和光催化协同效应,在穿透点之前,对于甲苯的去除率可保持100%。这可能归因于ACF和TiO2之间的相互作用促进了光致电荷的传输和分离,促进了甲苯的光催化,实现了复合材料快速的原位再生。
(2)光照条件下,TiO2/ACF复合材料对甲苯具有良好的去除效果。其中,TiO2/ACF-3复合材料的甲苯去除效果最好。甲苯初始浓度升高,复合材料对甲苯的去除率先升高后降低;气体流量越大,甲苯去除率越低;光强越强,甲苯去除率越高。在穿透点后,当甲苯初始质量浓度为370 mg/m3、甲苯气体流量为85 mL/min、紫外灯功率为24 W时,TiO2/ACF-3 复合材料对甲苯去除率达80%。
