下肢动脉硬化闭塞症减容治疗术中并发症及其处理
2019-07-30李承志林印胜刘玉龙李王海
李承志,林印胜,张 红,刘玉龙,李王海,张 艳
(暨南大学附属第一医院介入与血管外科,广东 广州 510632)
随着血管腔内治疗在下肢动脉硬化闭塞症中的广泛应用,药物涂层球囊等越来越多的新器械应用于临床[1];且有学者[2-3]尝试将减容治疗与药物涂层球囊相结合,以获得更好的长期疗效。但减容治疗的开展也使临床面临一些新问题,特别是发生并发症后如何及时有效处理等。本研究探讨下肢动脉硬化闭塞症减容治疗的并发症及其处理方案。
1 资料与方法
1.1 一般资料 回顾性分析2011年8月—2018年1月于我院接受减容治疗的167例下肢动脉硬化闭塞症患者,男96例,女71例,年龄54~88岁,平均(71.3±12.5)岁;共188条患肢,对同一患者的不同肢体进行减容治疗时至少间隔14天,减容治疗前患者均有不同程度患侧肢体跛行、静息痛、溃疡形成等缺血症状,且经下肢动脉超声、CTA或MRA检查确诊;患肢Rutherford分级:3级15肢,4级59肢,5级77肢,6级37肢。依据减容治疗方式,将患者分为溶栓组(43例46肢接受置管溶栓术)、取栓组(42例49肢接受机械血栓清除术)及旋切组(82例93肢接受定向斑块旋切术)。
1.2 仪器与方法 采用Siemens Artis Zeego DSA机作为减容治疗引导设备。术前根据患者体质量予以肝素化,剂量3 mg/kg体质量,每小时追加半量肝素。
1.2.1 置管溶栓术 对急性期、无出血风险且年龄<80岁患者,通过DSA明确病变位置后,将Unifuse溶栓导管(上海美创医疗器械有限公司)在导丝引导下置入病变段。随后将患者送返病房,以微量泵泵入40万U尿激酶,每日2次。每日复查凝血指标及造影,及时调整导管位置并决定下一步处理(如继续溶栓治疗或拔管结束溶栓治疗)。
1.2.2 机械血栓清除术 对急性期下肢动脉硬化闭塞症患者采用Angiojet取栓导管(Boston Scientific公司),于DSA引导下导丝通过病变段后,沿导丝送入取栓导管,根据出血风险和年龄评估决定是否进行喷药模式(适用于无溶栓禁忌证患者的新鲜血栓),而后对病变段进行反复抽吸。Rotarex取栓导管(Straub公司)适用于急性期及亚急性期下肢动脉硬化闭塞症或慢性期血栓,操作过程同上,但需采用专用导丝通过病变段。
1.2.3 定向斑块旋切术 对钙化相对较轻者选用Silverhawk斑块旋切系统(Medtronic公司),钙化严重者选用Turbohawk斑块旋切系统(Medtronic公司)。确保导丝从动脉真腔通过病变段,而后将斑块旋切系统沿导丝送入病变段,并分四个象限分别对病变段进行反复旋切,速度约1 cm/s;当收集器积满后,将旋切系统取出体外进行清洗,之后再次送入体内,直至旋切满意(DSA示残余狭窄<30%)。
1.3 并发症分析 分析各种减容方式术中并发症的种类、发生率及处理方案。
1.4 评价及随访 术后即刻对患者进行Rutherford分级。术后随访评价血管通畅及症状缓解情况,于术后1、3、6个月对患者随访进行下肢动脉超声检查,术后12、24个月复查CTA,计算患肢血管初期通畅率。
1.5 统计学分析 采用SPSS 13.0统计分析软件。比较3组间术中并发症的发生率,如理论频数>5,或1<1/5及以下理论频数≤5,采用行×列表资料χ2检验;如理论频数<1,或1<1/5及以上理论频数≤5,则采用行×列表资料的Fisher确切概率法。以配对样本Wilcoxon符号秩检验比较术前与术后患肢Rutherford分级的差异。P<0.05为差异有统计学意义。
2 结果
溶栓组以置管溶栓术治疗46条患肢。取栓组中,采用Angiojet取栓导管治疗16肢、Rotarex取栓导管治疗33肢。旋切组中,采用Silverhawk斑块旋切系统治疗21肢、Turbohawk斑块旋切系统治疗72肢。对1例患者的2条患肢因斑块过硬无法充分切除而治疗失败,减容治疗的技术成功率为98.94%(186/188)。
术中并发症见表1、图1~3。血管破裂出血14例,其中6例因出血量>400 ml予以输血治疗;9例(9肢)通过压迫方式止血成功,5例(5肢)压迫无效,予覆膜支架植入后成功止血。5例(5肢)栓子脱落引发栓塞,其中1例(1肢)股深动脉栓塞,经Angiojet取栓导管抽吸后血管复通,2例(2肢)胫前动脉栓塞及2例(2肢)腓动脉栓塞均经置管溶栓后血管复通。2例(2肢)急性血栓形成均位于股浅动脉,考虑为顺行穿刺后股动脉穿刺点压迫止血过紧所致,经置管溶栓后血栓溶解。1例以Rotarex取栓导管清除血栓时,由于血栓头端较硬导致导丝熔断,经抓捕器成功抓捕移除断裂导丝。Fisher确切概率法分析显示,3组间术中并发血管破裂出血发生率差异有统计学意义(P=0.002),而栓子脱落引发栓塞、急性血栓形成及导丝断裂发生率差异均无统计学意义(P=0.891、1.000、0.261)。经对症处理后,术中并发症均得到解决,无手术相关死亡病例。
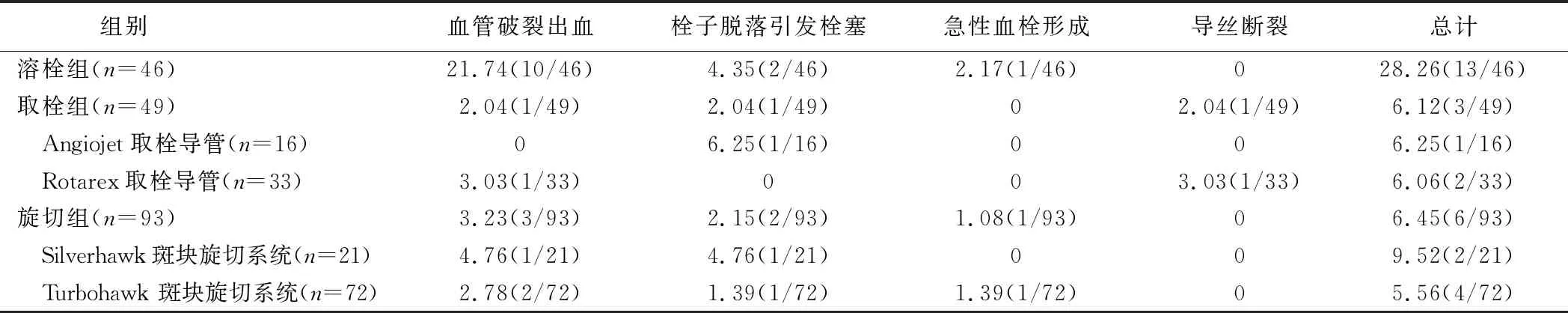
组别血管破裂出血栓子脱落引发栓塞急性血栓形成导丝断裂总计溶栓组(n=46)21.74(10/46)4.35(2/46)2.17(1/46)028.26(13/46)取栓组(n=49)2.04(1/49)2.04(1/49)02.04(1/49)6.12(3/49) Angiojet取栓导管(n=16)06.25(1/16)006.25(1/16) Rotarex取栓导管(n=33)3.03(1/33)003.03(1/33)6.06(2/33)旋切组(n=93)3.23(3/93)2.15(2/93)1.08(1/93)06.45(6/93) Silverhawk斑块旋切系统(n=21)4.76(1/21)4.76(1/21)009.52(2/21) Turbohawk斑块旋切系统(n=72)2.78(2/72)1.39(1/72)1.39(1/72)05.56(4/72)

图3 患者男,81岁,右下肢动脉硬化闭塞,采用Rotarex取栓导管行机械血栓清除术 A.术中DSA示腘动脉远端未显影; B.取栓过程中发生导丝断裂,箭示断裂的导丝头端; C、D.通过抓捕器将导丝断端取出后,继续采用Rotarex取栓导管反复取栓,DSA示右侧胫前、胫后及腓动脉复通
术后随访6~72个月,中位随访时间36个月。术后12、24个月初期通畅率分别为78.19%(147/188)、61.17%(115/188)。术后缺血症状较术前明显好转,患肢Rutherford分级:0级162肢,1级26肢;与术前比较,Rutherford分级差异有统计学意义(Z=2.730,P=0.002)。
3 讨论
为降低下肢动脉硬化闭塞症血管腔内治疗术后再狭窄发生率,减容理念被引入临床,主要包括早期的置管溶栓术及新近的机械取栓术、斑块旋切术及激光血管内成形术等[4]。已有研究[4-6]证实上述减容手术方法效果较为确切,但减容治疗也存在其并发症。本研究探讨减容治疗术中可能遇到的并发症种类及处理策略,以期为临床工作提供参考。
置管溶栓术是针对急性动脉栓塞和血栓形成的经典治疗方法[7],但其并发症尤其是出血的发生率高达30.3%[8]。本组置管溶栓术中患肢血管破裂出血发生率为21.74%(10/46),且其中有6例患者因出血量较多需输血治疗,但经积极用药和术中压迫或覆膜支架植入等处理后均成功止血。术前严格评估适应证和出血风险有助于避免溶栓导致的出血并发症,术中轻柔操作、严格控制溶栓药物剂量并严密监测患者生命体征亦可起到一定预防作用[9]。
采用Angiojet取栓导管行机械血栓清除术是利用液体冲击产生负压的原理将血管内急性期血栓取出体外[10]。本组1例以Angiojet取栓导管取栓患者的1条患肢出现异位栓塞,经及时血栓抽吸后无不良事件发生。在并发症发生率方面,本研究中仅出血率3组间差异有统计学意义,而以Angiojet取栓导管取栓过程中无出血发生,提示其安全性较高,但也可能是与本组样本量过小有关。采用Rotarex取栓导管行机械血栓清除术则是通过取栓导管头端高速旋转的螺旋装置产生负压将血栓吸出体外[6],并发症相对较多,治疗急性或亚急性股腘动脉闭塞时远端栓塞率为6%,穿孔率为1.2%[11]。本研究采用Rotarex取栓导管取栓时,1例1条患肢发生血管破裂出血,另1例1条患肢发生导丝断裂,可能与导管选择及术中操作不当有关。对采用Rotarex取栓导管取栓时,需要严格把握靶血管的直径,6F导管适合治疗直径3~5 mm血管,8F导管适用于直径5~8 mm血管。此外,在机械取栓过程中应经常冲洗导管,避免塞管;一旦发现导丝发热、转动,需立即停止取栓,将导管取出体外清洗。
目前国内常用的定向斑块旋切系统主要为Silverhawk及Turbohawk旋切系统,在顺利通过真腔的前提下,二者均可用于慢性下肢动脉硬化闭塞症的血管腔内减容治疗,且后者更适用于钙化病变[5]。但定向旋切术相关动脉破裂发生率为5.3%,远端栓塞发生率率为3.8%,急性血栓形成发生率为2.0%[12]。本研究旋切组术中血管破裂出血、栓子脱落引发栓塞及急性血栓形成发生率分别为3.23%(3/93)、2.15%(2/93)及1.08%(1/93)。术中血管破裂出血时应立即予球囊封堵及体外压迫处理,如30 min仍无法止血,则需置入覆膜支架止血,对发生在远端的微小栓塞无需特殊处理。
总之,对于减容治疗下肢动脉硬化闭塞症相关并发症应给予足够重视,有效预防是关键;一旦出现并发症,需及时予以处理,以免造成严重后果。
