利用水合物法分离捕集二氧化碳研究进展*
2019-07-18谢文俊徐纯刚李小森
谢文俊,徐纯刚,李小森
(1.中国科学院广州能源研究所,广州 510640;2.中国科学院天然气水合物重点实验室,广州 510640;3.广东省新能源和可再生能源研究开发与应用重点实验室,广州 510640;4.中国科学院广州天然气水合物研究中心,广州 510640;5.中国科学院大学,北京 100049)
0 前 言
CO2是人为制造的最主要的温室气体,根据国际气候变化合作组织的报告,1970~2004年间,CO2的年排放量增加约 80%,排放量由 21 Gt升高至38 Gt。2004年,CO2占人为制造温室气体总量的77%,预计到2100年,大气中CO2含量将达1.03 g/m3,全球平均气温将提高1.9℃[1]。为了减缓全球气候进一步恶化,需要开发利用可替代化石能源的新能源,比如核能、生物质能、太阳能、风能、潮汐能等。这些新能源受到地域条件、自然条件以及能源规模等限制,较难完全替代化石能源以满足社会发展需求。在一定时期甚至较长时期,以化石能源为主的能源结构还将持续,因化石能源的利用而产生的 CO2也将持续。因此,发展高效的分离捕集CO2技术对于实现碳减排十分重要。当前,主要的CO2分离技术包括化学吸收、物理吸附、深冷分离以及膜分离等[2]。这些技术都存在各自不同的缺点,比如环境不友好、能耗高、投资成本高、分离容量低[3],为此,科研工作者仍在努力探索新技术。气体水合物是由水分子和小分子气体分子(如CH4、CO2、N2、H2、SO2、C2H6、C3H8、H2S 等)组成的结晶化合物,水分子通过氢键彼此相连并构成不同结构的空腔,气体分子通过范德华力而稳定存在于空腔。气体水合物受形成压力以及气体分子特性影响主要呈四种结构,立方晶系I型(sI)、立方晶系II型(sII)、六方晶系(sH)以及半笼型(sc)[4]。
自20世纪50年代起,气体水合物及相关技术在能源与环境方面的应用受到越来越广泛的研究,研究结果主要应用于油气管路运输安全、天然气水合物开采、水合物储氢、气体分离及提纯等领域[5-7]。水合物法气体分离原理是水合物在形成过程中气体组分在水合物相和气相中分布有不同选择性。在相同系统,不同气体形成气体水合物的温压条件不同,一定温度下,混合气中水合物形成压力更低的组分因水合物形成驱动力更大会优先形成气体水合物,并在水合物相富集,同时导致对应平衡相在气相中富集。相对于传统的气体分离,水合物法具有工艺简单、投资成本低、较低的材料及能源损耗以及相对环境友好的特点。水合物法CO2分离捕集研究主要集中于水合物形成动力学、热力学、促进剂、分离工艺、分离装备及工艺经济性评估等。本文综合国内外关于水合物相平衡条件、添加剂、微观分析等方面的研究,通过分析和比较进行概括总结,提出发展建议。
1 水合物相平衡条件研究
在水合物形成过程中,判断实验平衡条件通常有两个:(1)水合物颗粒最初形成或最后消失时的温压;(2)压力急剧下降或温度急剧升高趋于稳定时的温压。首先,压力必须高于平衡值,以便有形成水合物的驱动力。其次,系统缓慢加热或缓慢降压使水合物分解[7]。CARSON等[8]验证了判断水合物平衡点的原理。当气体包裹在水合物中时,系统的压力下降,最后一个水合物颗粒的消失通常伴随着压力-温度曲线斜率的下降。通过测量冷却或加热等容线的交点,可以得到水合物形成平衡条件。研究相平衡的主要方法有等温法、等压法和等容法。
对于等温法,系统首先设置压力高于平衡压力以形成水合物,水合物形成后压力逐渐降低,通过观察水合物颗粒的消失可以得到平衡压力。因此,这种方法需要前后带有视窗的仪器[5,9-16]。对于等压法,首先通过注入气体以保持反应釜内压力不变,然后当外部气体注入反应釜内的量显著增加时表明水合物形成,最后缓慢升高温度使水合物分解。在水合物分解过程中,系统压力必须保持恒定,水合物颗粒最后消失的点被认为是该压力下水合物形成的平衡温度。类似于等温法,等压法必须使用带视窗的仪器。
等容法描述了密闭容器内压力随温度和相转变的变化规律。温度首先从气-液(V-L)区开始下降,等容冷却使压力略有下降。在一定温度下,水合物的形成使压力显著降低。随后温度缓慢升高使水合物解离,使压力快速升高。然后找到水合物解离曲线和初始冷却曲线的交点,将该点作为水合物解离的平衡点。等容法是高压下水合物形成的常用方法,不需要肉眼观察。基于等容法,提出了一种等容步进加热法(T-循环法)[17-21]。通过该方法得到的实验结果十分可靠并且可重复。然而,一组测量需要花费超过24 h[18]。HERRI等[22]通过在加热过程中取少量气体和液体样品改善了等容步进加热法,并通过气相色谱、离子色谱和测量折射率分析样品。通过质量守恒,改进的步进加热法可以测定气体和水合物组成。
差式扫描量热法(differential scanning calorimetry,DSC)也用于不同领域二元相(固/固或固/液)。最近,DSC被用于确定水合物平衡条件[23-25],该方法的关键是通过测量纯材料的熔化温度来校准温度,然后在特定温度范围内不同加热速率下测量值与已知熔化温度之间的偏差来计算修正函数。温度校准完成后,DSC软件可以通过校准功能自动校准测量的温度。DSC法需要仔细校准,样品质量和加热速率必须在合理的范围内选择。
2 CO2水合物的添加剂研究
根据国内外研究现状,在纯水中形成CO2水合物需要高压低温,极端的操作条件导致工业应用中的高成本,水合物的形成速率很低。因此,有学者研发了可以改善水合物形成条件和促进水合物形成的添加剂[17,20-21]。添加剂可以分为热力学型和动力学型。热力学添加剂改善平衡条件使水合物在更高温度或更低压力下形成,通常由有机化合物组成,包括四氢呋喃(tetrahydrofuran,THF)、丙烷(C3H8)、环戊烷(cyclopentane,CP)和四丁基铵盐(四丁基溴化铵TBAB、四丁基氯化铵TBACl或四丁基氟化铵TBAF)。动力学添加剂可以加速水合物形成,由表面活性剂组成,包括十二烷基硫酸钠(sodium dodecyl sulfate,SDS)和十二烷基三甲基氯化铵(dodecyltrimethylammonium chloride,DTAC)[26]。
已有研究证实了四氢呋喃溶液可以显著降低给定温度下的水合物形成压力[27-29]。KANG 等[27]、LINGA等[28]和HASHIMOTO等[29]发现THF溶液存在时,CO2-N2和CO2-H2混合物的水合物平衡压力明显低于没有添加剂的压力,并且证明 1.0mol%的THF是从混合物中分离CO2的最佳浓度[27,30],THF可以形成sII型 THF-水合物,和CO2竞争占据大空腔(51264)[30-31]。尽管THF可以改善CO2-N2或CO2-H2形成气体水合物的条件,但并不能显著提高气体消耗量和分离效率[32]。KUMAR 等[33]比较了 CO2-H2和 CO2-H2-C3H8的水合物平衡条件,发现将3.2mol%的 C3H8加入 CO2-H2混合物中,压力可以降低约50%。他们证实了C3H8加入到CO2-H2混合物中降低了水合物相平衡压力而不影响 CO2回收率,通过拉曼光谱发现,CO2-H2混合物形成的sI型水合物和CO2-H2-C3H8(2.6mol% C3H8)混合物形成的sII型水合物中均存在H2[34]。CP也可降低水合物相平衡压力。ZHANG等[35-36]发现,CO2在气相摩尔数为0.320 4时,三元CO2-H2-CP水合物的相平衡压力明显低于三元CO2-H2-THF水合物的相平衡压力,这是由于CO2-H2-CP形成sII型水合物,CP优先占据51264的大空腔,CO2仅能与H2竞争占据512的小空腔,降低了水合物相中CO2相对H2的选择性[36]。在合适的条件下,TBAB在水中形成半笼型水合物,在半笼型水合物系统中,阴离子 Br-与主体水晶格强烈结合,单个 TBA阳离子(TBA+)占据四个空腔,为小气体分子留下了十二面体空腔[4,20,37-39]。ARJMANDI等[20]、OYAMA 等[40]和 DUC 等[41]发现,二元CO2-TBAB水合物的平衡条件明显低于纯CO2水合物的平衡条件。水合物相平衡的压力随着TBAB浓度的增加而降低[42-44]。0.29mol%的 TBAB被认为是从烟道气或整体煤气化联合气(integrated gasification combined cycle,IGCC)中回收CO2的最佳浓度,因为浓度超过0.29mol%的TBAB溶液对回收CO2贡献不大[17,20,45-47]。加入TBAB可降低气体消耗量,这是由于TBA+占据sc型水合物的大空腔。但采用 TBAB作为气体水合物促进剂存在一些争议,TBAB的存在可以提高气体水合物的生成速率和气体消耗量,但对水合物相平衡压力的降低作用不明显。TBAF和TBACl也可以改善水合物平衡条件[46,48-51]。尽管TBAF降低压力的作用优于TBAB,但是由于其价格远高于 TBAB,并没有得到广泛应用。SDS用作动力学添加剂方面,ZHONG等[51]研究了 SDS对气体水合物形成的影响,发现在 SDS溶液或相关表面活性剂溶液存在下,水合物形成速率可以提高多个数量级。TAJIMA等[52]、ROSSI等[53]和TORRE等[54]进一步证实了临界胶束浓度(critical micelle concentration,CMC)的SDS在提高水合物形成速率方面效果最好。
采用热力学或动力学添加剂不能解决水合物法从气体混合物中分离和捕获CO2的所有问题(极端条件、低气体消耗量、低水合物形成速率和低 CO2回收率),因此学者们进一步研究热力学添加剂和动力学添加剂的协同作用。LI等[47]将 DTAC加入到0.29mol%TBAB溶液中,研究水合物法从烟道气中捕获CO2,发现与纯水体系相比,该体系可以显著改善气体水合物的形成条件,提高形成速率和CO2回收率。TORRE等[54]采用THF结合SDS研究通过形成水合物从 CH4-CO2气体混合物中移除CO2,发现添加剂的组合降低了水合物形成压力并且提高了捕获CO2的选择性。LI等[17]发现,CP加入0.29mol%TBAB溶液中可以显著提高水合物法从 IGCC合成气中分离 CO2的气体消耗量,结果可以通过粉晶 X 射线衍射(powder X-ray diffraction,PXRD)进一步被证实[55]。
添加剂在水合物法从气体混合物中分离和捕获CO2的效果尚在研究中。目前,THF和TBAB是最受欢迎的两种热力学添加剂。筛选能显著提高气体吸收的添加剂还需要做大量工作。
3 含CO2水合物微观分析及测量
微观分析及测量方法包括衍射法和光谱法,可以准确地获得水合物(含有 CO2)结构信息(确定水合物结构类型、晶格参数、客体占用率和在腔体内的位置)。含CO2的水合物以液氮(liquid nitrogen,LN)(仅用于光谱分析方法)或原位保护样品的形式进行测量。在原位测量中,在光谱仪中加入一组光纤或微探针,通过含有高纯度二氧化硅的硅窗或蓝宝石窗检测原始形成的水合物。水合物样品首先在干 LN蒸汽中处理并快速转移,然后在预冷阶段进行检测。
3.1 衍射法
衍射方法包括 X射线衍射(X-ray diffraction,XRD)和中子衍射。最早最全面的衍射方法是XRD[56-58]。在一定温度下,通过晶体的XRD数据可以确定水合物结构、晶格常数、含 CO2水合物的组成[59-61]。通过XRD分析,可以确定CO2分子捕集在CO2-THF二元sII型水合物的小的512空腔中[31]。三元体系中,XRD结果显示,在5 MPa和253.15 K条件下,CO2分子同时占据sI型和sII型CO2-H2-C3H8水合物的大笼子[34]。对二元体系,如CO2-H2或CO2-N2,XRD图显示气体水合物是典型的sI型晶体结构[62]。然而,通过分析XRD图得出,水合物结构可能会随着CO2在二元体系中含量的变化而变化。含3mol%~20mol% CO2的CO2-N2气体混合物形成sI型水合物,但含1mol% CO2的CO2-N2气体混合物形成 sII型水合物[63]。CP存在下的0.29mol%TBAB溶液中,CO2占据sII型和sc型水合物空腔。值得注意的是,由于XRD测量的高敏感度,检测样品时必须小心处理以保证其在样品磁盘上的平面。中子衍射研究可以确定客体和主体在水合物晶体中的位置,追踪水合物形成过程中的结构变化,测量水合物晶格中客-主分子相互作用的程度[64-69]。然而,通过中子衍射研究 CO2水合物的报道还很少。HENNING等[66,70]通过中子衍射观察到,随着样品温度缓慢升高,六边形冰完全转化成sI型CO2水合物。
3.2 光谱法
利用光谱法分析测量含CO2水合物,主要包括激光拉曼光谱、傅立叶红外光谱和核磁共振(nuclear magnetic resonance,NMR)波谱。这里主要介绍采用激光拉曼光谱的研究。
拉曼光谱是一种很好的鉴别水合物结构和组成的方法,利用特征拉曼峰可以定性地确定化学键,同时通过定量计算,可获得水合数和相对笼占有率[31,71-77]。对应的分裂峰(分别位于 1 276 cm-1和 1 384 cm-1)是由费米共振效应引起的,对应于CO2分子 C—O 对称拉伸(υ1)和O—C—O弯曲(2υ2)模式。由于测量条件和水合物结构的不同,CO2分子的拉曼位移可能在小范围内变化[31,34,78]。CH4、N2、H2分子的拉曼位移分别位于2 910 cm-1、2 325 cm-1、4 120 cm-1附近,对应的振动模式分别为υ1C—H对称拉伸、υ1N—N对称拉伸和H—H振动(纯分子振动)。因此,通过拉曼光谱很容易从CO2-CH4、CO2-N2和CO2-H2气体混合物中区分CO2。NMR可以用来确定水合物结构和量化相对空腔占有率。目前所研究的水合物法分离CO2的NMR谱集中在1H、129Xe和13C[79-82]。在已有的研究中,1H NMR用于分析乙烷、丙烷和异丁烯水合物[79];129Xe NMR用来鉴别Xe原子在小空腔和大空腔中的比率[80-82];13C NMR应用于研究 CO2,CH4和 C3H8水合物[74,83-85]。SEO等[63,86]基于CO2的13C NMR谱发现,CO2分子占据sI型水合物结构的大空腔,随着CO2在CO2-N2气相中含量的增加,小空腔和大空腔的稳定作用从 N2分子转变到CO2分子。
4 水合物法CO2分离工艺及装备研究
4.1 工艺研究
合适的条件下,气体不断溶解在溶液中并且形成气体水合物,导致系统压力下降。因此,必须不断注入气体以保持系统压力不变。水合物形成是一个放热过程,当形成大量水合物时,引起系统温度的缓慢升高。一旦水合物形成速率下降,由于传热,系统的温度回到设定的温度,根据公式和(n为摩尔数,上标H和G分别表示水合物相和气相,上标feed表示原料气,下标CO2和other分别表示CO2和其他组分)[87],CO2的分离效率随着过程中气体的不断消耗而变化。DUC等[41]在TBAB存在下,对从CO2-N2混合物中分离CO2进行了研究,提出了一个连续的多级分离过程。然而,随着CO2浓度在气体混合物中的下降,水合物法CO2分离变得更困难,并且CO2回收率变得更低,单一的水合物法CO2分离过程不能完全高效地从气体混合物(比如烟道气和燃料气)中分离CO2。因此,学者们提出了多种混合过程,在混合过程中,首先通过水合物法分离 CO2,剩余少量的CO2气体混合物通过化学吸附、低温分离、膜分离等其他方法分离。LINGA等[87]提出了一种水合物法和膜分离法结合的混合工艺,分别从烟道气和燃料气分离 CO2。XU等[88]通过一个两阶段的水合物分离结合化学吸收分离的混合过程,进行了从 IGCC合成气中分离 CO2的实验。SUROVTSEVA等[89]设计了一个结合低温和水合物法从 IGCC烟道气中捕捉CO2的方法。通过以上混合工艺可以得到纯度高于95%的CO2,与传统的CO2分离方法相比,该方法更高效、更经济[32,87-90]。然而,两个问题阻碍了混合过程的中试应用:单位体积水(L)中气体水合物的容量低和单位时间(h)水合物形成速率慢。水合物法 CO2分离过程不使用大的吸收塔或蒸汽-再沸蓄热器,所以两个过程的成本主要在制冷和压缩系统。在设计工艺参数之前,研究人员必须关注一些参数和关键工艺:
水合物的水合数。去除1 mol CO2所需的水分子数量对反应器的除热要求以及制冷系统的大小有很大影响。
浆料浓度。系统中循环的自由水量必须加热和冷却,这也会影响制冷系统的大小。
反应器的温度。系统的性能在很大程度上受到CO2移除或传热过程中温度的影响。
YANG等[91]设计了一个5 kt/d煤供应的车试设备。将混合气和处理过的水计量加入反应器与反应物混合,并使反应物流过尾管(内径为4.8 mm)。在10 MPa和269 K条件下,CO2为0.94 mol/min、H2为 28 mol/min的进料速率下,水合物生成速率为0.271 mol/min,与设计要求一致。在特殊的高压容器中,由于CO2分离效率和气-液-水合物分离受水合物形成路径的影响,即使是小型的中试应用,也还没有成熟的水合物法CO2分离工艺。因此,为了实现工业上水合物法从气体混合物中分离CO2的最终目标,特别是气-液-水合物分离工艺中,在提高CO2分离效率和优化工艺参数方面还有很长的路要走。
4.2 分离装备及相关研究
近年来,研究者根据分离工艺开发了不同的装置,主要集中在水合物形成模式的创新和连续流动反应器的设计上。水合物形成模式通常包括搅拌、鼓泡和喷淋,可以很好地混合气体和水(或溶液)。SZYMCEK等[92]设计了一个中试规模的连续射流水合物反应器(continuous jet hydrate reactor,CJHR)。水合物形成期间,CJHR中安装的多个毛细管使反应物之间相互作用的表面积最大化。此外,新的设计克服了水合物生产的产品限制,减少了未转化的CO2和H2O的量。XU等[45]设计了一个可视鼓泡反应器,并进行了从 CO2-H2混合物中捕捉 CO2的实验。可视鼓泡反应器的体积为40 L(高4 m,底面积为0.01 m2),约为实验室一般反应器的100倍。当气泡通过反应器从底部移动到顶部,整个气泡可以转化为气体水合物。ROSSI[53]等开发了一套捕捉CO2的新装置,通过设计好的喷嘴将水(或溶液)从顶部喷射到反应容器中,将混合气从底部喷射到反应器中,使气液混合更充分。LINGA等[93]设计了一个将搅拌和鼓泡结合在一起增强气体和水接触的新装置。这个新装置和从更小规模的搅拌釜反应器中得到的结果相比,水合物形成速率、气体吸收和从烟道气或燃料气中回收的 CO2明显提高了[28-90]。YANG 等[91,94]开发了一个基于SIMTECHE CO2捕捉过程的流程(图1),形成CO2水合物连续流动反应器,研究了气体载体、流体速度、浆料浓度和温度对水合物形成速率的影响。结果表明,反应器增强了相间混合,降低了传热和传质阻力,最终确保在工业相关工艺条件下全部反应速率接近固有的CO2水合物形成速率。
在特殊压力容器中存在气-固-液分离和低 CO2回收率问题,连续CO2分离过程也尚未成熟。直到目前,还没有一套完整的基于CO2水合物分离和捕捉的设备。因此,进一步开发水合物法的CO2分离和捕捉装置的工艺势在必行。
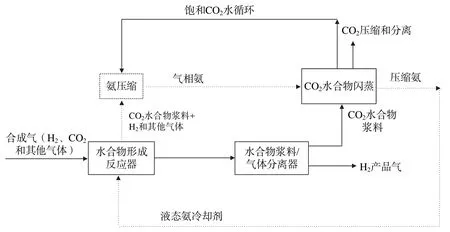
图1 SIMTECHE CO2捕获过程的流程图(用于IGCC)[91]Fig.1 Block flow diagram of the SIMTECHE CO2 capture process (for IGCC applications)[91]
5 成本比较
人类向大气中排放的二氧化碳可以通过不同的方式减少[95],表述如下。

6 总 结
利用水合物法从含CO2的气体混合物中分离和捕捉 CO2被认为是减少人为 CO2排放的一项新技术,受到了广泛研究。本文全面讨论了含CO2水合物形成的平衡条件、水合物形成促进剂、微观分析及测量方法、水合物法CO2分离工艺及装备,并对水合物法CO2分离的成本进行了分析和比较。从不同的体系中获得了含CO2或气体混合物的水合物平衡条件的实验数据,包括纯水体系和含添加剂的溶液体系,为水合物法CO2分离操作条件提供了重要的参考。讨论了热力学和动力学添加剂对水合物相平衡的影响,但这些添加剂不能解决水合物法 CO2分离过程中的所有问题。和单一添加剂相比,THF和SDS、TBAB和CP、THF和C3H8等组合添加剂可以显著改善CO2分离。但仍未能确定哪一种或哪几种添加剂对水合物法CO2分离效果最佳,这可以尝试通过热力学表征从CO2水合物形成机理方面去解决。通过微观分析手段可以确定水合物结构、组成和笼的占有率,但由于取样等条件的限制,很难进行分子水平的测量,因此开发出新设备或新方法使测量更简单是很有必要的。由于平衡条件随着混合气中CO2的下降而变得极端,因此通过水合物法从气体混合物中彻底分离和捕捉 CO2变得非常困难。CO2分离效率和气-液-水合物分离的效果也受特定压力容器中水合物形成方法的影响,即使在小规模的试验应用中,还没有成熟的水合物法CO2分离过程应用到工业中。虽然已经开发了可以促进气体水合物形成的新设备,但是目前的装置还不满足将水合物法 CO2分离这一技术应用到工业中的要求。在提高水合物法CO2分离效率、开发新设备和新工艺方面,还需要更深入的研究。
