细胞实验系统评价制作流程的构建
2019-07-18赵霏赵晋郭忠宋雷张婷姜彦彪邝心颖马彬
赵霏,赵晋,郭忠,宋雷,张婷,姜彦彪,邝心颖,马彬
细胞实验也称为体外实验(in vitro studies/experiments),是指实验对象为各种动物或植物细胞、微生物、细胞器、编码基因、表达蛋白或细胞功能的研究,是基础研究领域中不可或缺的一类实验,其结果对下一步动物实验和临床试验的设计与实施均具有重要的指导意义[1]。
相较于临床试验,细胞实验具有操作技术及方法多样性、同一实验多次实施后结果不一致、细胞来源及种属对实验结果影响大等特点,因此会出现实验方法难以选择、实验可重复性差、实验结果难以整合解释等诸多问题[2]。故有必要开展细胞实验系统评价/Meta-分析(SRs/MAs),以降低将细胞实验所获结果引入动物实验和临床研究的风险,最终提高其结果对后续动物实验和临床研究的指导价值。但相较于系统评价在临床领域中的广泛采纳和应用,其在细胞实验中的应用还很少[3]。此外,由于缺乏细胞实验系统评价检索策略和纳入研究质量评价方法的标准,大部分已经发表的细胞实验SR均存在如检索不完全或无标准的工具进行质量评价等问题[4]。
因此,本文将在循证方法学的基础上介绍细胞实验系统评价的制作流程和步骤,为细胞实验系统评价的开展和实施提供相关参考,以期提高细胞实验系统评价的质量。
1 资料与方法
1.1 纳入/排除标准纳入与细胞实验SRs/MAs的制作流程/方法/步骤、偏倚风险评估工具、检索策略制定方法和报告规范等相关的中英文文献。对纳入研究偏倚风险的准确评估和检索策略的规范制定与报告是影响系统评价结果真实性和科学性的重要影响因素,因而对于某一具体问题的细胞实验SRs/MAs,仅纳入对其纳入研究的偏倚风险进行了评估,和/或提供至少一个数据库检索策略的SRs/MAs研究。排除重复发表文献、会议摘要和综述等。此外,本研究中定义的“细胞实验”是指从始至终在体外或细胞上进行的研究,不应包括前期开展临床干预治疗,随后将临床样本(如血液和脑脊液等)进行后续实验的研究。
1.2 文献检索策略计算机检索PubMed、CNKI和万方数据库,检索时间从建库截至2017年10月。中文检索词包括细胞实验、体外实验、体外研究、临床前实验、原始实验、系统评价、荟萃分析、元分析、Meta分析、报告规范、报告指南、检索策略、方法学等;英文检索词包括preclinical study、cell experiment、cell test、in vitro experiment、in-vitro study、systematic review、Meta-analysis、methodology、protocol、guidance、guideline、reporting guideline、search guide、search strategy、search filter等。其中PubMed的检索策略参见框1。

框1 PubMed数据库的检索策略
1.3 文献筛选由2名评价员(赵霏、张婷)分别筛选文献,意见不统一时通过讨论或由第三名研究人员(马彬)协助解决。
1.4 研究方法对纳入研究进行描述性分析。
2 结果
2.1 文献筛选流程及结果初检共获得相关文献985篇(中文622篇,英文363篇),经逐层筛选,最终纳入16篇研究[5-20],包括中文1篇,英文15篇。文献筛选流程及结果见图1。
2.2 细胞实验系统评价与临床试验系统评价的区别细胞实验渗透于医学研究领域各个方面,其目的在于探讨某一课题或假说的真实性,从而揭示疾病的发生发展及治疗等内在机制,从而为进一步的动物实验和临床试验提供理论基础,同时对动物实验和临床试验的研究设计与具体实施方法提出合理的指导意见。

图1 文献筛选流程及结果
与传统干预性临床试验系统评价一样,细胞实验系统评价本质上仍属于干预性系统评价。但由于原始细胞实验的特殊性,如:①即使不同的研究团队选用同一种细胞株进行实验,但由于细胞来源、培养条件和实验操作技术差异等原因,也较难得出完全一致的实验结果。因此,不同细胞实验间的异质性来源和程度均更加复杂;②细胞实验的结局指标多是采用如PCR、WB实验的手段对结果进行定性描述;③对于细胞实验的质量评价,有些动物实验或临床研究的偏倚风险评估工具并不适用。本研究团队依据目前已发表的细胞实验SR和临床试验SR,总结出二者之间的区别(见表1),供研究者参考。因而,细胞实验SR的制作不可完全仿照临床/动物实验SR的制作流程,应具有其自身特点。
2.3 细胞实验系统评价的制作流程同临床试验/动物实验系统评价类似,细胞实验系统评价的开展和实施也包括8个步骤[21,22]: ①提出并明确研究问题;②制定纳入/排除标准;③证据来源与检索;④文献筛选;⑤纳入研究偏倚风险评估;⑥资料提取;⑦合并单项研究结果,并在可能的情况下进行Meta分析;⑧数据结果呈现及异质性分析。
2.3.1 提出并明确研究问题借鉴临床试验系统评价结构化研究问题的原则[2],一个目的明确的细胞实验系统评价的研究问题同样需要包含以下5个方面的核心要素:①细胞实验的研究对象(participants,P);②具体的干预措施或暴露因素(intervention/exposure,I/E);③进行的对照处理措施(comparisons,C);④结局测量指标(outcomes,O);⑤实验设计类型(studydesign,S)。

表1 细胞实验SR和临床试验SR的区别
例如,预探讨“灰树花多糖诱导肿瘤细胞凋亡的作用”。针对这一选题,按以上原则,对研究问题进行结构化处理:①“P”为肿瘤细胞;②“I”为灰树花多糖处理;③“C”可为灰树花多糖以外的处理方法,包括生理盐水/PBS处理或不处理等,不进行严格限定;④“O”为检测细胞凋亡的结果指标,如TUNEL染色法、流式细胞术检测凋亡率、凋亡相关蛋白表达等凡是能检测细胞凋亡的方法;⑤“S”为细胞实验。
2.3.2 制定纳入/排除标准同动物实验SRs/MAs一样,细胞实验SRs/MAs的纳入和排除标准的制定也应体现结构化问题中所涉及的核心要素[22]。本文以Golbach LA等的研究[12](该研究探讨体外实验中低频辐射(LF MF)暴露对细胞内钙稳态的影响,后文中用GLA代指该研究)为例,具体说明如何制定细胞实验系统评价的纳入/排除标准。
(1)研究对象:为体外培养的细胞或细胞内容物,如正常人体细胞或肿瘤细胞、动物细胞、细胞内某段功能基因或蛋白等,也可以是细胞的某一功能,如分泌、迁移、蛋白表达等。如在GLA的研究中,研究对象为动物或人体细胞,排除原核生物、藻类或真菌细胞。
(2)干预措施/暴露因素:即对细胞进行的各种处理,可为药物、X线照射、特殊染色等,以及具体干预方案。如在GLA的研究中,干预措施为频率为1~300 Hz之间的LF MF暴露,排除静态磁场暴露。同时需要报告暴露的细节,以便可以合理量化曝光参数的不确定性,从而可重复暴露条件。
(3)对照措施:可为空白对照,或阴性对照如生理盐水、PBS等;也可为另一种不同的干预措施。同样,需要阐述其具体干预方案。此外,若为多种干预方案比较,应对实验组和对照组细胞的干预措施均进行详细的规定及描述。如在GLA的研究中,对照措施并未限定,可为空白对照、或其他相关暴露条件。
(4)结局测量指标:需检测的实验结果指标,取决于实验研究的目的,多为某一细胞的特定功能,如细胞因子的分泌水平,凋亡水平或自噬活性等,也可为某一分子的基因或蛋白表达水平。实验结果可为定性指标(如Western blot等指标)或定量指标(如细胞抑制率、凋亡率等指标)。如在GLA的研究中,结局指标为细胞内实际测量到的钙离子浓度,排除应用抑制剂或路径钳夹实验后的钙离子浓度。
(5)实验设计类型:细胞/体外实验,即从始至终在体外或细胞上进行的研究。如在GLA的研究中,纳入体外实验或细胞实验。
2.3.3 证据来源与检索目前,对细胞实验系统评价检索数据库的选择、检索策略的制定和报告、“体外实验”检索过滤器等方面,并无相关的方法研究,也未形成统一规范或共识。已发表的细胞实验系统评价中,在这些方面均有差异[8,12-19]。因此参考动物实验系统评价检索策略制定规范[23],以及目前报告了详细检索策略及来源的细胞实验系统评价[14,16,18,19],同时考虑细胞实验特性,对细胞实验系统评价检索数据库的选择和检索策略的制定等建议如下:
2.3.3.1 数据库选择检索数据库除PubMed/MEDLINE、EMbase和Web of Science外,还需要检索系统评价研究者所在国家和地区的专业数据库。例如对中国的研究者而言,至少需要加入CBM、WanFang Data、CNKI 等中文数据库。此外,根据系统评价课题的具体要求,可选取相关专业数据库如Scopus、Science Direct、CINAHL、LILACS、中医药数据库等。
2.3.3.2 补充检索虽然早在2005年就开始认同并设立临床试验全球注册制度[24],而且已有专门的组织(EQUATOR Network)[25]开展并建立了一系列临床试验和动物实验的报告规范。但目前,对细胞实验而言,尚无相关的实验注册机制和要求,亦未研发和建立其规范的报告标准,细胞实验中阴性结果的报告比临床试验更难估计。因此,重视对未发表研究、阴性结果研究等灰色文献的收集和获取是降低细胞实验系统评价研究发表偏倚的重要手段之一。因此,建议可通过Google或百度检索、Open Grey检索、OpenSIGLE检索,查询会议论文集等多种途径,尽可能获取细胞实验相关会议摘要、实验室数据等灰色文献[23]。
2.3.3.2 检索策略的制定和报告首先,确定检索词的来源和范围。细胞实验系统评价检索词的来源和选择应该仅仅围绕所提出问题包含的核心要素(如上例所示5方面核心要素),其中“P”(细胞或细胞功能)、“I”(干预措施)和“O”(结局指标)相关的检索词为必须检索的检索词。其中对于“O”(结局指标)而言,由于在确定细胞实验系统评价选题时,对结局指标已经明确,如对细胞某项功能改变的影响。因此,“O”相关的检索词也必须进行检索。对于“C”(对照组处理方法)和“S”(体外实验)相关检索词而言,根据该系统评价的范围和要求进一步确定是否需要检索,例如已明确或限定“C”的范围,则其相关检索词也需要检索;反之,不需要。而对于“S”(体外实验),若“P”已明确为某种细胞,如A549肺癌细胞,则不需要检索“S”;若“P”仅限定为某一种疾病,则需要同时检索“S”。
其次,确定检索式,也就是检索词之间的逻辑组配关系(ANDOR NOT)。其基本原理是,同一概念下的检索词之间用OR连接,不同概念下的检索词之间用AND连接。因此,细胞实验系统评价中,检索式应该为“P”AND “C”(根据具体情况选择是否需要)AND “O”(结局指标)AND “S”(根据具体情况选择是否需要)。
对于细胞实验系统评价检索策略的报告而言,目前并无共识,亦无相关方法研究探讨。我们借鉴临床试验系统评价检索策略的报告认为,细胞实验系统评价检索策略报告应包括检索数据库来源、检索时间范围、语种限制、检索词及完整的检索策略等信息。
2.3.3.3 “体外实验”检索过滤器由于目前尚无针对“细胞/体外实验”的检索过滤器。笔者参考国内外文献中对“体外实验”概念及已发表的细胞实验SRs/MAs,制定了如框2所示的“体外实验”的检索过滤器,供今后细胞实验系统评价/Meta分析制作者参考。
2.3.4 文献筛选和资料提取
2.3.4.1 方法细胞实验系统评价文献筛选和资料提取方法与临床试验系统评价并无差异。首先,确定文献筛选和资料提取流程,排除的标准,提取注意事项等。然后,确定筛选和提取的具体方法、筛选和提取人员的准入标准等,以保证筛选和资料提取过程的科学性和标准化。推荐,需要至少两名评价员独立完成并进行交叉核对,其具体方法原则可参见《系统评价指导手册》[21]。

框2 “细胞/体外实验”的检索滤器
2.3.4.2 内容细胞实验系统评价资料提取内容,除一些基本特征外,特别需要注意对细胞实验重要特点方面资料的提取,如研究对象(包括细胞的来源、类型、种属、培育条件等)、干预措施(包括对照设置、细胞处理方式等)和结局指标(检测技术如流式细胞术或ELISA等、测量结果)等方面相关数据的提取。
2.3.5 纳入研究的偏倚风险评估目前,并无针对细胞实验内在偏倚风险评估工具的方法学研究,已发表的细胞实验系统评价中所采用的标准和工具均不同,有些直接将临床试验[5,6,9,20]、或动物实验偏倚风险评估的工具[10,15,18]直接移植过来使用,尚无公认的标准和工具。因此,我们借鉴Cochrane Handbook推荐的随机对照试验偏倚风险工具(Cochrane Risk of Bias,ROB)[26]和SYRCLE动物实验风险评估工具[27],参考已发表细胞实验系统评价采用的偏倚风险评估条目,结合细胞实验的特性,提出了如表2所示的细胞实验偏倚风险评估条目,包含6类偏倚类型共21个条目。其中,偏倚类型与Cochrane ROB一致,每个条目的评估结果最终以“是”(纳入研究中明确报告判断的相关内容)、“否”(未报告与相关判断内容)、“不确定”(信息提供不充分,无法判断)表示,其中“是”代表低风险偏倚,“否”代表高风险偏倚,“不确定”代表不确定风险偏倚。
2.3.6 合并单项研究结果,根据情况进行Meta分析及异质性分析
2.3.6.1 结局指标的转化处理由于细胞实验结果展示的多样性,提取的结局指标如何转化是细胞实验SR的难点之一。例如,对于检测阳性细胞率的实验,如MTT、ELISA、细胞凋亡率等实验结果,可将每一个细胞视为个体,根据实验前细胞数量和阳性细胞数目把实验结果转化成二分类变
量数据;对于某一细胞因子的分泌量等指标,可视其为连续型变量,采用均数±标准差的形式合并数据;对于如WB、PCR等趋势性实验结果,可用Image J等软件将结果提取出数据,进而转换成连续型变量进行合并[12,28]。
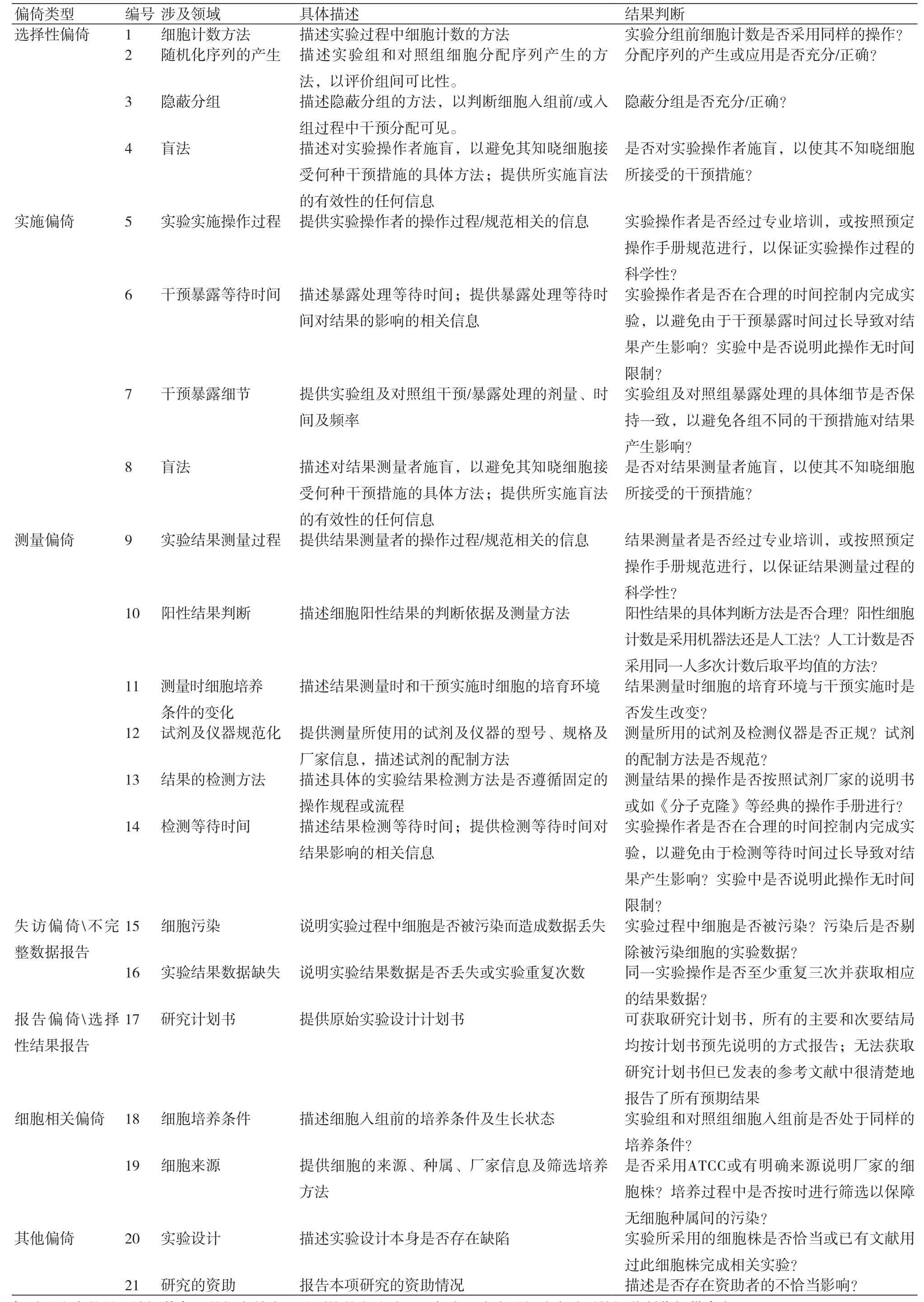
表2 细胞实验内在偏倚风险评估工具
2.3.6.2 异质性分析Meta分析的优势在于可增加检验效能、提高结论准确性、解决不同研究间相互矛盾的结论所引发的争论等[25]。该统计方法同样适用于细胞实验系统评价,但与临床试验系统评价存在一定的差异,如临床试验的研究对象为人群,个体间差异很小,而细胞实验的研究对象为各种各样的细胞,不同来源和种属的细胞在对药物的敏感性以及细胞代谢过程等方面的差异很大。此外,细胞实验在实施中由于技术手法、生长环境不同等造成的细胞生长状态间的差异也不可忽视。纳入研究间异质性是细胞实验系统评价制作中的很大挑战。
细胞实验系统评价中,纳入研究的异质性同样包括研究内和研究间两方面,前者指样本内各观察单位之间可能存在的差异。在细胞实验中为单个细胞,由于生长状态不同可能会有些许差异,但是实验所采用的同批同种细胞间差异十分小,可以忽略不计;后者指由于研究对象来自于不同的总体以及偏倚的控制等诸多方面的差异。由于细胞实验的特殊性,此方面的异质性更明显。如某一中药的抗肿瘤作用,可以在肝癌、胃癌或者乳腺癌细胞上都能观察到,在合并效应量时如果不考虑肿瘤细胞种属的来源问题,直接对多种细胞的抑制作用进行合并,则不可避免会产生异质性。此时,为避免产生异质性,可采用亚组分析的方法,即将同一种属来源细胞株的结局指标进行合并。
此外,细胞实验中干预措施具体实施方法间的差异也可造成某些偏倚的产生,由此而产生的异质性也不可避免。理想的状态是实验中的干预措施应建立在对所有研究对象均无偏倚风险的基础上,包括在干预时间、频率、剂量、实验操作及最短时间控制等方面均一致。但在实验实施过程中,完全消除这方面的差异较难实现,因而可采用亚组分析、Meta回归、敏感性分析等多种方式探讨异质性来源,并在一定程度上降低亚组间异质性。细胞实验系统评价/Meta分析中对于异质性检验的方法与临床研究的系统评价/Meta分析一致。当定量Meta分析不适合时亦可采用其他合成研究的方法,如描述性系统评价的方法。
3 结论
一个经过严谨设计、规范实施步骤的细胞实验系统评价,一方面可避免出现方法学上的缺陷,最小化系统评价研究中的偏倚,有利于证据使用者对其结果的客观评估。另一方面可促进研究人员对相关课题的动物实验和/或临床试验的设计进行更广泛的思考,避免实验设计的缺陷及不必要的实验实施中的浪费。本研究目的在于为构建出细胞实验系统评价规范的流程提供参考。同样的,高质量的细胞实验系统评价的开展与推进,需要不同专业领域中的研究者们未来更多、更深入的研究。
