固体分散体技术的研究进展
2019-07-17陈巧巧王东凯
陈巧巧,董 爽,王东凯
固体分散体技术的研究进展
陈巧巧,董 爽,王东凯*
(沈阳药科大学 药学院,辽宁 沈阳 110016)
固体分散体技术可克服水难溶性药物溶出速度慢和生物利用度低的局限性,利用其制备的药品现已经得到市场化销售。本文作者从固体分散体的优缺点出发,深析固体分散体的科学基础,结合上市产品特点,阐释了两个主要影响因素,即载体材料和制备技术的发展情况,并总结了2000年以来利用固体分散体技术制备的收录在美国橙皮书上的上市药品,旨在让读者对固体分散体的发展前景和科技成果转化有更深刻的理解。
药剂学;固体分散体;综述;载体材料;制备技术;美国橙皮书;上市产品
固体分散体(solid diapersion)是指药物高度分散在适宜的固体载体材料中形成的一种固态物质[1]。固体分散体由药物和载体构成,药物可以在载体材料中以分子、胶体无定形等状态分散存在。狭义上可认为,固体分散体可称为无定形固体分散体。1961年,Sekiguchi等[2]最早提出了固体分散体的概念并加以利用。本文作者以被FDA橙皮书收录的固体分散体上市产品为出发点,紧密结合其特点与相关科研文献,力求架构起科技成果和上市产品之间的桥梁,以期为这方面的研究者在科研成果转化方面提供帮助。
1 固体分散体的优缺点
固体分散体的理论基础必须要首先了解,本节从固体分散体的表象出发,即固体分散体所呈现的优缺点,揭示固体分散体的科学基础。
固体分散体最突出的优点是能够在很大程度上提高水难溶性药物的溶出速度,从而使得药物的生物利用度得到很大的提高。其主要机制如下:a. 药物晶型转变:以无定型或分子分散形式存在于载体中,溶出过程将不需要额外的动力去克服晶格能。张欢等用溶剂法将盐酸普拉格雷溶于聚维酮 K30(Povidone K30,PVP K30)中制成的盐酸普拉格雷固体分散体片,盐酸普拉格雷以非结晶形式存在,药物的溶出速度得到了显著提高[3]。Mishra Jaya等发现广泛作为营养剂的乳清蛋白能够使吲哚美辛(indomethacin)、卡维地洛(carvedilol)和呋塞米(furosemide)的饱和溶解度和溶出速率显著增加[4];b. 润湿性增加:由于药物是被包裹于水溶性载体之中,因此可被溶出介质充分润湿;c. 载体具有一定的增溶作用:利用两亲性的载体,提高药物的溶解速度。 张娟等应用不同亲水性载体材料制备的固体分散体均可提高联苯双酯溶出度,其中以聚乙二醇-聚乙烯己内酰胺-聚醋酸乙烯酯接枝共聚物(Soluplus®)对联苯双酯溶出度的提高最为显著,累积溶出度可达到90%左右[5]。溶解度和固体分散体的形成及性质之间要有所取舍,有研究表明降低药物的溶解度可以影响固体分散体的形成及水吸附性,进而其稳定性得到提高[6]。固体分散体还有其他的一些优点如:可用于油性药物的固化,可以制成速释制剂、缓释制剂或肠溶制剂等;作为一种制剂中间体可制成片剂、胶囊剂、滴丸剂、颗粒剂等。
固体分散体比较难解决的问题是物理稳定性较差,这是因为固体分散体与传统剂型相比,其焓值较高,以及形成的构象所产生的熵值,使得固体分散体整个体系处于高能态,高能态的物质易向较稳定的低能态转化,也就是容易老化(aging)。确定的数值可以用Flory-Huggins理论来解释。
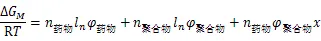
2 固体分散体的载体材料
目前常用的固体分散体载体有水溶性、难溶性和肠溶性三大类,可单独使用也可以联合使用。从上市产品角度出发,结合科研理论成果进行说明。
2.1 水溶性载体材料
水溶性载体可加快药物的溶出速率,提高药物的溶解度,有效提高药物的生物利用度,因而在实际生产中多被应用于速释固体分散体的制备。目前常用的有聚乙二醇(PEG)类、聚乙烯吡咯烷酮(PVP)类、泊洛沙姆、壳聚糖、卡波姆、尿素、枸橼酸、琥珀酸和甘露醇等。结合FDA公布的药用辅料处方推测,1985年批准的Nabilone所用的聚合物载体材料为PVP。张娟等应用不同亲水性载体材料制备的固体分散体均可提高联苯双酯溶出度,聚乙二醇-聚乙烯己内酰胺-聚醋酸乙烯酯接枝共聚物(Soluplus®),制备固体分散体可以显著提高联苯双酯溶出度,载体材料的性质及载药量的高低都会影响固体分散体中药物的溶出度[4]。吴玲以一种非离子型表面活性剂的载体材料泊洛沙姆188为载体,采用熔融法制备固体分散体,其体外溶出度显著提高[10]。
2.2 难溶性载体材料
常用的难溶性载体主要有乙基纤维素(EC)类、含季铵基团的聚丙烯酸树脂类、胆固醇、谷甾醇及二氧化硅等[11]。Sporanox、Prograf、Intelence、Zotress、Onmel等利用HPMC作为载体材料制备的固体分散体已在美国上市。黄兰芷等通过实验证明将EC10cp 作为缓释载体时制备的青蒿琥酯固体分散体可较好地延长药物的释放时间,并增加其生物利用度[11]。近年来,多孔无机材料取得了较大发展,多孔无机材料包括介孔二氧化硅、多孔淀粉、多孔羟基磷灰石、介孔氧化锌和氧化铝等。Maleki等对比了介孔硅泡沫(MSF)和2D-六角二氧化硅纳米结构(SBA-15)两类介孔二氧化硅材料作为载体对提高难溶性药物溶解度的影响,发现两类材料能明显增加药物的释放,并且MSF显示更快的释放速率,证明了介孔二氧化硅材料在提高难溶性药物的生物利用度方面有较大的应用前景[12]。
2.3 肠溶性载体材料
肠溶性载体有羧甲基纤维素(CNEC)、羟丙甲纤维素邻苯二甲酸酯(HPMCP)、聚丙烯酸树脂类(Eudragit L和S)等。赖琼为减少阿司匹林对胃部的刺激和不良反应,选取肠溶性丙烯酸树脂(EL 100-55)为载体,将阿司匹林与载体混合在无水乙醇中,然后将其直接喷洒在空白丸芯上,形成膜衣骨架型的共沉淀物固体分散体[13]。
2.4 联合型载体材料
只应用一种载体具有一定的局限性。近几年来,单一载体开始逐渐向联合载体发展,在制备聚合物固体分散体时,加入一定量的表面活性剂,可使得药物的亲水性和分散性得到显著提高,从而能够使固体分散体的理化性质和药物溶出度得到较有效的提升。联合性载体材料的使用在上市产品中已有出现,Kaletra等利用PVP和VA联合使用提高了lopinavir和ritonavir的溶解度和溶出速度。李妍妍等制备的普罗布考固体分散体,KollidonVA64-RH40载体材料使其溶出度得到了显著提高[14]。Wlodarski等发现聚乙烯醇和共聚维酮可协同性提高伊曲康唑固体分散体的溶出度[15]。
3 固体分散体的制备技术
为更好地架构起科研理论与科技成果转化之间的桥梁,仅介绍已上市产品中所使用的固体分散体制备技术—热熔挤出技术、喷雾干燥技术、共沉淀技术和一种发展较快且已趋于成熟的技术—超临界流体技术。其中喷雾干燥技术、共沉淀技术和超临界流体技术是基于溶剂法制备固体分散体的方法。
3.1 热熔挤出技术
FDA最早批准的固体分散体制剂是1987年用热熔挤出技术制备的Isoptin SR-E。热熔挤出技术是指将多相状态的物料在一定区域融化或软化,在强烈剪切与混合的作用下,不断减小粒径,同时进行彼此间空间位置的对称性交换与渗透,最终使物料呈单相状态高度均匀分散于辅料或载体中的新技术[16]。热熔挤出技术主要用于提高难溶性药物的溶出度及其生物利用度,具有工艺简单、连续化操作、生产效率高和在线监测等优点,已成为国外制备固体分散体的主导技术。由于显示出独特的优势和应用潜力,近年来受到药学工作者的广泛关注。郑昕等采用热熔挤出法,以乙烯基吡咯烷酮及乙烯/乙酸乙烯酯共聚物(PVP-VA)为载体制备了尼莫地平固体分散体[17],提高无定形的尼莫地平的量、增大尼莫地平的比表面积及适当增加载体 PVP-VA 的量都可以提高尼莫地平的溶出速率和溶解度。2016年,FDA最新批准上市的Venetoclax口服固体分散体片,就是采用热熔挤出技术,形成无定形固体分散体,提高了口服吸收生物利用度。
3.2 喷雾干燥技术
喷雾干燥技术是FDA所批准的产品中应用最多的技术。从2000年以前的Sporanox、Prograf到2016年批准的Epclusa共计约11种产品得以上市。喷雾干燥技术为溶剂法中第三步干燥除去溶剂所使用的技术。溶剂法制备固体分散体包括3个步骤:a. 将药物和载体溶解(或混悬)于易挥发性溶剂中;b. 分离大部分溶剂以产生固体分散体;c. 二次干燥至进一步除去残留的溶剂[18]。喷雾干燥技术是制备固体分散体比较温和的技术,由于其可以通过较低加工温度来完成,化学降解反应发生的程度较低,能够提高加工材料的化学稳定性。有一项研究比较了热熔挤出技术和喷雾干燥技术制备albendazole固体分散体的稳定性,使用热熔挤出技术制备的用品中有71.1%到97.4%的药物降解,而使用喷雾干燥技术制备的样品在室温下放置了6个月只有不到1%的降解[19]。喷雾干燥技术在提高溶解度方面有一定的优势,李朋朋等利用聚乙烯吡咯烷酮(PVP K30)为载体制备的布洛芬固体分散体,热熔喷雾干燥法制备的样品比热熔挤出法制备的样品溶解度和溶出速率快[20]。
3.3 共沉淀技术
共沉淀技术是溶剂法第三步中比较经典的除去溶剂的方法,利用的是溶剂-反溶剂原理。Zelboraf 于2011年在美国上市,这一经典的固体分散体技术终于实现了产业化销售。Zelboraf中含有vemurafenib,这是一种水溶性差的药物,利用共沉淀技术在体外实现了过饱和状态,产生固体分散体,提高了溶解度。魏振平等利用共沉淀法(溶剂挥发法),以羟丙基甲基纤维素(HPMC)为载体制备的西沙必利(cisapride)固体分散体,其固体分散体的溶解度和释放速率得到很大提高[21]。
3.4 超临界流体技术
超临界流体技术同样是溶剂法第三步中去除溶剂的方法。其制备的产品虽未有被FDA橙皮书所收录的产品,但其成熟度很高,与上述制备方法相比且有着比较大的优势。超临界流体技术适用于热不稳定和易被氧化的水难溶药物固体分散体的制备。该法操作简便,无需后续处理且制备效率也高。Zordi等以PVP为载体,通过超临界反溶剂法制备了水难溶性药物呋塞米的固体分散体,固体分散体中药物的结晶度降低,并以精细的球形颗粒存在于固体分散体中,物理稳定性得到了很大的提高[22]。Rana M. Obaidat等将Soluplus、PVP、HPMC和多孔壳聚糖等聚合物作为载体,使一种免疫抑制剂生物利用度差且可变的他克莫司(tacrolimus)在24 h内累计释放量达到98.76%[23]。
4 上市产品
利用固体分散体技术制备的药品已经有很多产品在市场上销售,表1梳理了自2000年以来被FDA橙皮书所收录的一些固体分散体药品实例[24-25]。从表1可以看出:剂型常为传统剂型片剂,近年来,胶囊剂也得到了应用,能够预见,更多的剂型能够在将来上市,更多的科技成果得到转化;给药方式均为口服,这是固体分散体制剂作为口服制剂无疑是很成功的,口服方式相比其他给药方式较为方便,病人的顺应性较高;制剂规格跨度范围较广,从零点几个毫克到上百毫克,固体分散体技术已得到很大改进,给药剂量的限制已经基本得到解决,能够实现大剂量载药;从专利持有人的角度看,固体分散体技术的应用呈现百家争鸣的态势,而非一家独享,这更有利于固体分散体技术科技成果的转化,且从侧面表明固体分散体制剂得到了更多人的认可,其发展趋势不容小觑;越来越多的固体分散体技术药品得以上市,且上升速率呈逐渐加快的趋势,而且药品研发的周期长,很多固体分散体制剂可能正处于Ⅰ期、Ⅱ期、Ⅲ期临床阶段,将会有更多的固体分散体药品以更快的速率上市销售;基本为处方药,这可能与固体分散体的不稳定性有关,不稳定性导致了高风险性。Incivek已上市但被迫撤市,FDA公布的原因是严重的皮肤反应,包括药物反应与嗜酸性粒细胞增多和系统症状(DRESS)和史蒂文斯-约翰逊综合症(SJS),其根本原因可能或与化合物的基本性质和制剂的稳定性有关。总之,固体分散体技术在药剂方面的应用得到了国际上的认可,且发展趋势会越来越好。

Table 1 Examples of FDA-approved medicines used solid dispersion technologies
To be continue

Continue table 1
Note: *—The strength of such drug product is being expressed in terms of the equivalent strength of the active moiety
5 结语
固体分散体能够使得水难溶性药物的溶出和药物生物利用度得到很大提高,在提高其稳定性方面也有了比较透彻的机制即从热力学和动力学两个方面,越来越多的固体分散体制剂得以上市,引起了很多科研工作者的兴趣,有着广阔的发展前景。
[1] 崔福德. 药剂学[M]. 北京: 人民卫生出版社, 2011: 347-354.
[2] SEKIGUCHI K, OBI N. Studies on absorption of eutectic mix-ture. I. A comparison of the behavior of eutectic mixture of sulfathiazole and that of ordinary sulfathiazole in man[J]. Chem Pharm Bull, 1961, 9(11): 866-872.
[3] 张欢, 姜伟化, 王环宇. 盐酸普拉格雷固体分散体片的制备及体外溶出度考察[J]. 中国药剂学杂志: 网络版, 2015, 13(3): 87-96.
[4] MISHRA J, BOHR A, RADES T, et al. Whey proteins as stabilizers in amorphous solid dispersions.[J]. European Journal of Pharmaceutical Sciences, 2019, 128: 928-987.
[5] 张娟, 徐丽双, 张妍, 等. 联苯双酯固体分散体处方及体外性质评价[J]. 沈阳药科大学学报, 2017, 34(1): 7-13.
[6] HUANG Siyuan, MAO Chen, WILLIAMS R O. Solubility advantage (and disadvantage) of pharmaceutical amorphous solid dispersions[J]. Journal of Pharmaceutical Sciences, 2016, 105(12): 3549-3561.
[7] MARSAC P J, SHAMBLIN S L, TAYLOR L S. Theoretical and practical approaches for prediction of drug–polymer miscibility and solubility[J]. Pharm Res, 2006, 23(10): 2417-2426.
[8] ANDRONIS V, YOSHIOKA M, ZOGRAFI G. Effects of sorbedwateron the crystallization of indomethacin from the amorphous state[J]. J Pham Sci, 1997, 86(3): 346-351.
[9] OSMAN Y B, LIAVITSKAYA T, VYAZOVKIN S. Polyvinyl pyrrolidone affects thermal stability of drugs in solid dispersions[J]. International Journal of Pharmaceutics, 2018, 6(1/2): 111-120.
[10] 吴玲. 淫羊藿素-泊洛沙姆188固体分散体的制备及溶出度研究[J]. 中国药房, 2015, 26(19): 2702-2704.
[11] 黄兰芷, 赵志强, 衡林森, 等. 青蒿琥酯缓释固体分散体的制备及体外溶出度研究[J]. 中成药, 2010, 32(10): 1702-1704.
[12] MALEKI A, HAMIDI M. Dissolution enhancement of a model poorly water-soluble drug, atorvastatin, with ordered mesoporoussilica: comparison of MSF with SBA-15 as drug carriers[J]. Expert Opin Drug Deliv, 2016, 13(2): 171-181.
[13] 赖琼. 基于固体分散技术的阿司匹林肠溶微丸的制备[J]. 生物技术世界, 2015(6): 161-162.
[14] 李妍妍, 李佳, 杨雁, 等. 聚合物/表面活性剂二元载体的固体分散体提高普罗布考的溶出度[J]. 沈阳药科大学学报, 2017, 34(7): 535-540, 605.
[15] WLODARSKI K, ZHANG F, LIU T, et al. Synergistic effect of polyvinyl alcohol and copovidone in itraconazole amorphous solid dispersions[J]. Pharm Res, 2018, 35(1): 16.
[16] 张赫然, 宋丽明, 王彦竹, 等. 热熔挤出技术制备固体分散体的辅料研究进展[J]. 现代药物与临床, 2014, 29(5): 557-563.
[17] ZHENG X, YANG R, TANG X, et al. Part I: Characterization ofsolid dispersions of nimodipine prepared by hot-melt extrusion[J]. Drug Dev Ind Pharm, 2007, 33: 791−802.
[18] PAUDEL A, WORKU Z A, MEEUS J, et al. Manufacturing of solid dispersions of poorly water soluble drugs by spray drying: formulation and process considerations[J]. Int J Pharm, 2013, 453(1): 253–284.
[19] HENGSAWAS SURASARANG S, KEEN J M, HUANG S, et al. Hot melt extrusion versus spraydrying: hot melt extrusion degrades albendazole[J]. Drug Dev Ind Pharm, 2017, 43(5): 1–15.
[20] 李朋朋, 卢恩先, 周丽莉. 热熔挤出法和喷雾干燥法制备布洛芬固体分散体的比较[J]. 中国药剂学杂志: 网络版, 2015, 13(4): 126-133.
[21] 魏振平, 胡会国, 毛世瑞, 等. 西沙必利HPMC固体分散体的制备及对药物体外释放的促进作用[J]. 中国药剂学杂志: 网络版, 2004, 2(6): 132-136.
[22] DE ZORDI N, MONEGHINI M, KIKIC I, et al. Applications of supercritical fluids to enhance the dissolution behaviors of furosemide by generation of microparticles and solid dispersions[J]. Eur J Pharm Biopharm, 2012, 81(1): 131-141.
[23] OBAIDAT R M, TASHTOUSH B M, AWAD A A. Using supercritical fluid technology (SFT) in preparation of tacrolimus solid dispersions[J]. AAPS Pharm Sci Tech, 2017, 18(2): 481-493.
[24] JERMAIN S V, BROUGH C, WLLIAMS III R O. Amorphous solid dispersions and nanocrystal technologies for poorly water-soluble drug delivery–An update[J]. International Journal of Pharmaceutics, 2018, 535(1/2): 379–392.
[25] FDA Release. Orange Book: Approved Drug Products with Therapeutic Equivalence Evaluations[EB/OL]. (2017-08-23)[2019-02-13]. https://www.fda.gov/drugs/development-approval-process-drugs/drug-approvals-and- databases
Research progress of solid dispersions techniques
CHEN Qiaoqiao, DONG Shuang, WANG Dongkai*
(,,110016,)
Solid dispersions techniques overcome the limitations of poorly-water soluble drugs whose dissolution rate and bioavailability is low, and products prepared have been marketed now. Based on the advantages and disadvantages of solid dispersions, this paper introduces the scientific basis of solid dispersions, and combines the characteristics of listed products to explain the development of two main influencing factors-carrier materials and preparation technology. And it summed up the drugs listed in the American Orange Book since 2000. It is intended to give readers a deeper understanding of the development prospects of solid dispersions and the transformation of scientific and technological achievements.
pharmaceutics; solid dispersion; summary; carrier material; preparation; FDA Orange Book; approval products
2019-03-01
陈巧巧(1994-), 女(汉族), 山东菏泽人, 硕士研究生, E-mail 2640189712@qq.com;
王东凯(1962-), 男(汉族), 辽宁沈阳人, 教授, 博士, 博士生导师, 主要从事药物制剂新剂型及缓控释制剂研究, Tel. 024-43520529, E-mail wangdksy@126.com。
R94
A
(2019)04–0127–08
10.14146/j.cnki.cjp.2019.04.006
(本篇责任编辑:赵桂芝)
