水滑石负载AuCu合金催化水煤气变换反应:催化性能与结构组成
2019-07-10沈显荣夏盛杰
沈显荣 孟 跃 夏盛杰
(1安徽工程大学生物与化学工程学院,芜湖 241000)(2湖州师范学院生命科学学院,湖州 313000)(3浙江工业大学化学工程学院,杭州 310014)
0 引 言
清洁能源的有效利用可以缓解能源短缺和环境污染等问题,而其中氢气是最清洁的二次能源,也是当前应用最广泛的清洁能源[1-3]。水煤气变换反应(WGSR):H2O(g)+CO(g)=CO2(g)+H2(g),在将工业产生的CO废气回收再利用的同时是一个重要的制氢手段,具有治理环境及节约能源的双重优点。因此,开发条件温和、活性优异的WGSR催化剂有着重要的意义[4-6]。但是传统的催化剂,如铁铬系催化剂对反应温度要求较高(大于300℃)且活性较低[7-8];铜锌系催化剂和钴钼系催化剂虽可在150~300℃区间催化WGSR,但整体活性仍不甚理想且催化剂易失活寿命较短[9-10],因而开发新一代低温高效水煤气变换反应催化剂成为研究热点。
而金基双金属合金催化剂因其低温高效催化性能已成为近年来的热门研究对象,以纳米金为基础的双金属合金具有良好的协同效应,能够使催化剂具有优异的选择性和催化活性[11-12]。但是由于纳米粒子易团聚,分散性较差,使得其活性、选择性及稳定性受到了较大的限制[13],而负载可以有效地解决上述缺点[14-16]。Gamboa等发现Au-Co3O4/CeO2比Ce3O4/CeO2的还原性更强,负载金能够提高催化剂在WGSR中的活性[17]。Thuy等比较了不同含量的Au/Pt同时负载在CeO2和TiO2时对WGSR催化活性的影响,发现Au/Pt负载量都为5%(w/w)时,300℃以下CO的转换率接近90%,表明该催化剂对WGSR具有较强的低温催化能力[18]。但是此类催化剂的活性、选择性及化学稳定性还有极大地提升空间与需求[19-20]。因此选择合适的载体,设计和开发一种新型金基二元合金负载的催化剂,在WGSR理论研究和工业制氢方面都具有重要的意义。
课题组先前的研究表明Zn基水滑石(LDHs)具有高化学稳定性、大比表面积及自身良好的催化能力等优点,是理想的催化剂载体[21-23],当前暂无合金负载的水滑石体系用于催化WGSR的报道。因此,我们以ZnAl水滑石为载体,构筑了Au以及AuCu合金负载的水滑石体系 (AuCu/LDHs)用于催化WGSR。通过XRD、HRTEM及STEM等手段表征负载体系的结构,研究不同的nAu∶nCu对负载体系催化WGSR性能的影响并与负载Au的水滑石进行对比。利用化学吸附及TEM表征得出材料中Au的分散程度,并比较了其与催化活性的关系;XPS表征分析了3种体系的活性组分,结合实验的活性数据对Au以及AuCu合金负载的LDHs体系催化WGSR活性差异给出了一定的解释。
1 实验部分
1.1 实验试剂
氢氧化钠、碳酸钠、六水合硝酸锌、九水合硝酸铝和六水合硝酸铜均为分析纯(AR),购自杭州萧山化学试剂公司;四氯金酸三水合物和硼氢化钠为分析纯(AR),购自上海阿拉丁试剂公司。以上试剂使用前均未进行再次纯化。
1.2 负载Au及AuCu合金水滑石的合成
1.2.1 ZnAl水滑石的合成
将6.40 g氢氧化钠和1.06 g碳酸钠溶于60 mL水配成溶液A,17.82 g六水合硝酸锌和7.50 g九水合硝酸铝溶于60 mL水配成溶液B。在室温下,将上述溶液A和B同时缓慢地滴加到250 mL含有60 mL去离子水的三口烧瓶中。滴加过程约为20 min,转速恒定为300 r·min-1,溶液的pH值控制在9.5~10。反应浆液经85℃陈化24 h后,以5 000 r·min-1的速度离心5 min,用去离子水洗涤沉淀,直到沉淀的pH值为7。此后,将样品在65℃干燥24 h,经研磨可得白色粉末状固体记作ZnAl水滑石(ZnAl-LDHs)。
1.2.2 负载Au和AuCu的水滑石合成
将2.0 g ZnAl-LDHs加入250 mL含有120 mL 5 mmol·L-1HAuCl4溶液的单口烧瓶中。将上述溶液经300 r·min-1搅拌10 min, 而后加入2 mL 10%(V/V)的氨水,在室温下持续搅拌18 h。将反应浆液经离心、去离子水洗涤、室温下真空干燥等,可得Au负载的水滑石前驱体。然后,在室温下,将1.0 g上述前驱体分散于100 mL去离子水,加入50 mg NaBH4处理2 h。经离心、去离子水洗涤、干燥后,可得红紫色的Au负载的水滑石样品,记作Au/LDHs。
负载AuCu合金的水滑石材料的合成过程与Au/LDHs类似,主要差别是在第一步时加入一定量的 Cu(NO3)2·6H2O(Au和 Cu的总物质的量与 Au/LDHs中Au的物质的量相一致),其中,不同样品中nAu∶nCu=1∶1、2∶1 和 5∶1, 所得材料分别记作 Au1Cu1/LDHs、Au2Cu1/LDHs和 Au5Cu1/LDHs。
1.3 材料表征
材料的成分与晶体结构分析采用Persee XD-6型X射线粉末衍射仪(Cu Kα辐射,管压为36 kV,管流为20 mA,波长λ为0.154 18 nm,2θ范围为5°~70°,扫描速率为 4°·min-1)分析;通过扫描透射电子显微镜(STEM,Hitachi S-4700加速电压15 kV)和自带的X射线能量色散谱仪(EDS,EDAX SUPRA35)表征所合成材料的表面形貌和元素组成;通过Hitachi HT-7700透射电子显微镜(TEM)(加速电压80 kV)进一步研究材料的形貌;采用Kratos AXISUltra-DLD系统进行X射线光电子能谱(XPS)分析,确定催化剂中各个元素的化学组成及活性组分。样品比表面积的测定是基于Brunauer-Emmett-Teller(BET)的方法,采用Quantachrome Autosorb-1C-VP分析仪。测试条件及步骤:待测样品在烘箱中100℃烘干2 h冷却至室温备用。在已测重量的空样品管中加入烘干的待测样品,在一定温度下真空脱气约2 h,冷却后称重,确定样品的真实重量。脱气程序设定为:室温下10℃·min-1升至250℃,保持1 h后降至室温(25℃)。将脱气后的样品装在分析站上,采用多点BET法测定其比表面积。其中测试条件为:脱附温度为250℃,脱附时间为2 h,测试样品重量为250 mg。
采用一套配有自动催化剂表征系统(AutoChem 2920)及在线质谱分析的石英反应器中进行CO的化学吸附实验。实验过程如下:100 mg的样品分别在150~300℃下还原1 h,随后在高纯氦气气氛下保持1 h,再以 5℃·min-1的速度,将温度降低为20℃。随后,引入连续的CO气流,载气为氦气,流速为50 mL·min-1,直到得到稳定的CO质谱信号。利用公式(1)中金属Au的分散度(D)计算基于CO化学吸附的相关参数。

其中,Fs是化学计量学因子,设定为物质的量之比nCO∶nAu=1∶1;MAu、ms、Vad和 Ws分别是 Au 的摩尔质量(g·mol-1)、样品的质量(g)、CO 化学吸附的体积(mL)、Au的重量百分比 (%);Vm是标准温度和压力下CO的摩尔体积(L·mol-1);Dr是 Au 的还原度(%)。
理论金属Au的分散度(Dt)是基于TEM测定得到的Au的晶粒尺寸和半球模型计算所得:
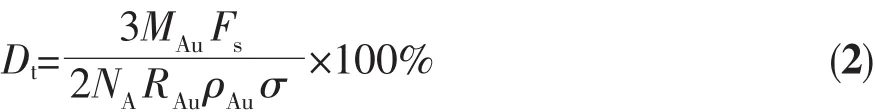
其中,NA是阿佛加德罗常数;σ是原子交叉区域面积(0.064 9 nm2);n表示每克催化剂对CO化学吸附的值(mmol·g-1);RAu是由TEM测定的 Au纳米粒子的平均半径(nm),ρAu是 Au 的金属密度(g·cm-3)。
Au纳米粒子覆盖度(θ)是基于CO化学吸附相关参数及TEM测定所得的Au纳米粒子的晶粒尺寸,采用公式(3)和(4)计算。
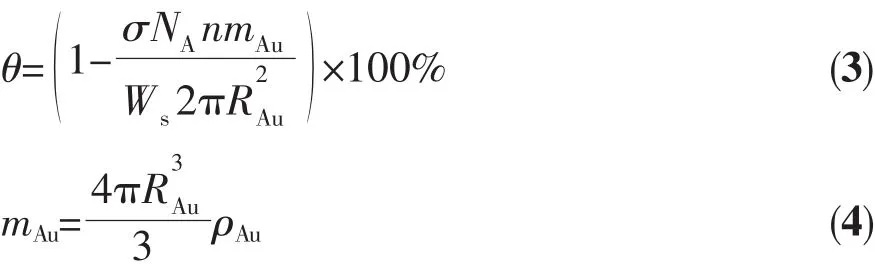
其中,mAu是单个Au纳米粒子的质量(g)。
1.4 WGSR实验
催化剂的活性评价采用小型的固定床反应器,压力为标准大气压。反应器的微石英玻璃管内径为6 mm。反应前,将100 mg催化剂用10%(V/V)H2/Ar混合气以20 mL·min-1的流速在250℃下处理2 h,而后在Ar气氛下冷却到室温。水通过一个高效液体泵通入至250℃的气化室内气化,然后与反应气体混合后进入反应器。反应物的组成主要为3%(V/V)CO以及15%(V/V)H2O/Ar混合气,反应的总流速150 mL·min-1,对应空速为 90 000 mL·gcat-1·h-1。 CO的转化温度范围为150~300℃。反应器进口与出口处气体的浓度由配有TDX-01色谱柱和TCD检测器的气相色谱(GC-2014C)在线检测分析。CO的转化率(XCO)有下列公式(5)进行计算:

负载Au催化剂催化水煤气变换反应在不同温度下的转换频率(TOF)及相应的反应速率(v)的测试,是将催化剂的用量由100 mg降低为5 mg以控制CO的转化率低于20%时测得(假定所有的Au和Cu均具有活性)。TOF及反应速率的测定采用下列公式(6)和(7)计算[24-26]:

其中αCO表示转化的CO的物质的量(mmol),nAu和nCu表示Au和Cu的物质的量(mmol),t为反应时间(s),mcat为催化剂的总质量(g)。
催化剂的表观活化能(Ea)可由Arrhenius公式计算求得(公式(8)):

其中,k为反应速率常数,A为指前因子,R为摩尔气体常数(8.314 J·mol·K-1),T 为热力学温度(K)。
2 结果与讨论
2.1 催化剂的结构表征
图1a是样品的XRD图,其中黑色曲线为ZnAl-LDHs,其具有明显的代表水滑石结构的(003)、(006)、(009)/(012)、(015)、(018)、(110)、(113)和(116)特征衍射峰,与文献报道的ZnAl水滑石结构相一致[27-29]。与ZnAl-LDHs相比,Au/LDHs不仅保留了水滑石的所有特征衍射峰,同时出现了 2θ在 37.9°、44.0°和64.5°分别代表 Au 的(111)、(200)和(220)的衍射峰,表明合成的样品是负载Au的水滑石[30-31]。从AuCu/LDHs的 XRD图可以明显看到表示(111)、(200)、(220)和(311)晶面的特征衍射峰移动到了 38.3°、44.2°、64.7°和 82.2°。 这应该是由于一部分的 Au 原子被尺寸较小的Cu原子取代而形成负载AuCu合金的水滑石所致。

图1 不同样品的XRD图(a)及TEM图(b~d)Fig.1 XRD patterns(a)and TEM images(b~d)of different samples
图 1(b~d)是 ZnAl-LDHs、Au/LDHs 和 Au2Cu1/LDHs的TEM图。ZnAl-LDHs具有明显的片状结构,其粒径尺寸在50~150 nm;负载之后的水滑石样品的片晶上明显出现了代表Au或AuCu合金的黑点,其中Au的分布较为分散,而AuCu合金分布较为密集。图2是Au/LDHs和AuCu/LDHs的HRTEM图,粒径分布图及特定区域的电子衍射SAED图。高分辨率透射电镜中尺度不一的黑点表示负载的Au纳米颗粒,经过相应计算及测量,Au/LDHs中Au(111)面的间距为0.244 nm,其值与文献报道的相一致[32]。AuCu/LDHs的HRTEM图表明,负载的AuCu合金尺度更加均一,其(111)面的晶面间距为0.229 nm,相较于Au/LDHs中Au的(111)面的间距明显减小。这与XRD显示的合金负载体系的2θ向高角度发生偏移(层间距变大)的结果相一致,充分说明合成的样品的是负载AuCu合金的水滑石。
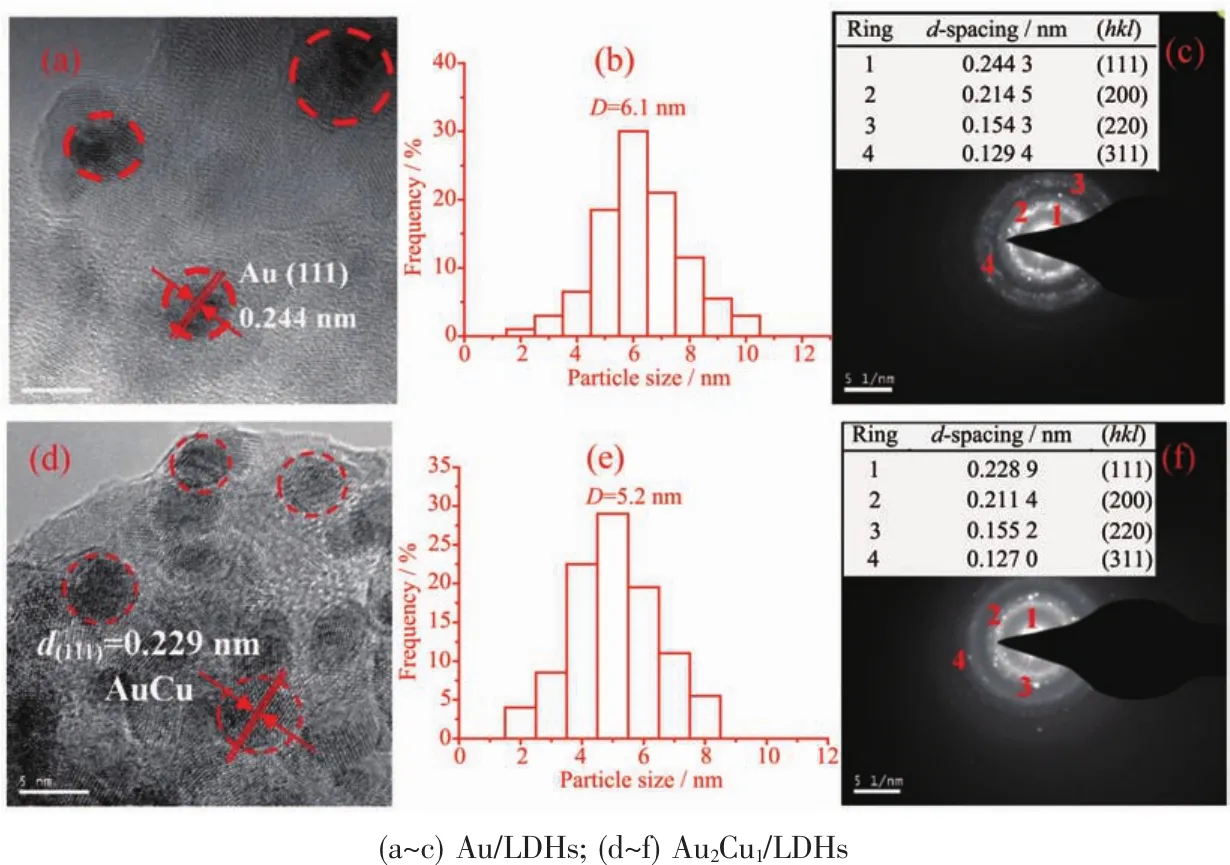
图2 HRTEM图 (a,d),Au或者AuCu合金的平均粒径分布图 (b,e)和电子衍射图SAED(c,f)Fig.2 HRTEM images(a,d),particle size distribution(b,e)and electron diffraction pattern(SAED)(c,f)of samples
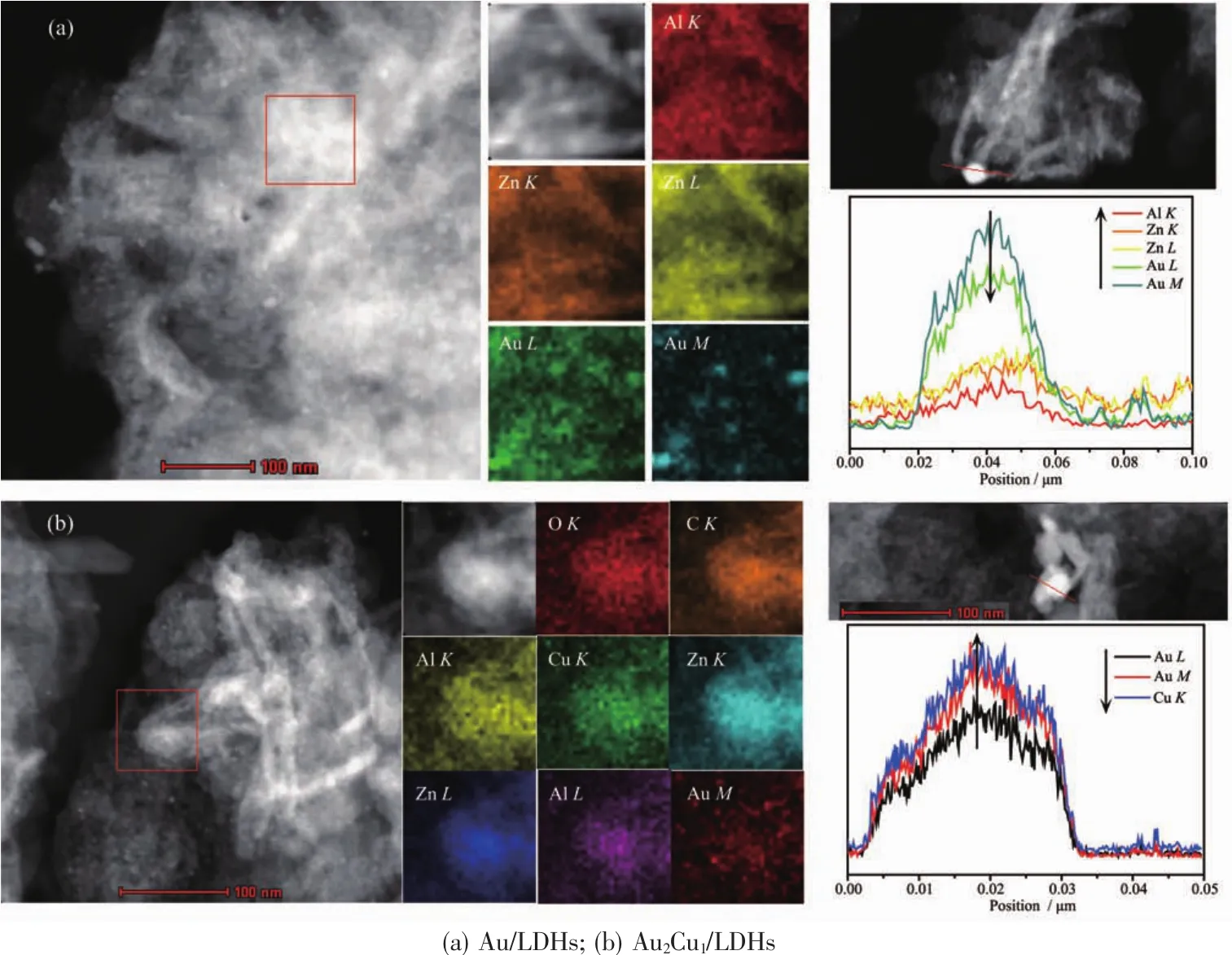
图3 包含主要元素的映射图像及EDS强度谱图的STEM表征Fig.3 STEM images with elemental mapping and EDSintensity spetra
图3 是Au/LDHs和Au2Cu1/LDHs包含主要元素映射图像及EDS强度谱线的STEM表征。元素映射图像表明样品中含有 C、O、Zn、Al、Au 或 Cu 等元素;穿过样品的EDS强度谱线(与元素映射采用不同的选择区域)分析表明,Au/LDHs只含有Au、Zn和Al的相应谱线,而AuCu/LDHs在此基础上又出现了明显的Cu的谱线,进一步证实了合成的样品是负载Au的ZnAl-LDHs以及负载AuCu合金的LDHs。
2.2 催化WGSR的反应活性、稳定性及重复利用性能
图4a是多种样品催化WGSR在150~300℃下CO的转化率曲线。从中可以看出,ZnAl-LDHs的CO转化率非常低,在温度小于200℃时基本没有转化率,当反应温度为300℃时,转化率最高为18.7%。水滑石负载Au后,活性有明显的提高,反应温度为300℃时,Au/LDHs的CO转化率上升为65.9%。负载合金的水滑石体系催化WGSR的活性在单纯负载Au的基础上又有了进一步的较大提升,AuCu/LDHs的CO转化率在300℃时为85.1%~97.5%。并且随着合金中Cu含量的提高呈现先增大后减小的趋势,其中催化活性最高为Au2Cu1/LDHs样品。Mizuno等[33]利用MgAl水滑石负载AuPd合金催化环己醇脱氢反应也得到了类似的结果,他们发现合金负载体系的催化活性随着Au和Pd的比例的提高呈现先增大后减小的趋势,比例过低或过高均会影响合金的结构稳定性进而影响负载体系的催化活性,这与催化体系中活性组分随着AuCu合金组成的改变而变化有关。

图4 不同的催化剂样品催化WGSR的CO转化率随温度变化的曲线(a)以及反应速率随温度变化的拟合曲线(b);反应温度为300℃时CO的转化率随反应时间的变化(c)以及多次重复利用实验结果(d)Fig.4 COconversion rate as a function of temperature(a)and reaction rate as a function of temperature(b)for the WGSR over different catalysts;CO conversion rate as a function of time(c)and reutilization results(d)of WGSR over different catalysts at 300℃
为了进一步分析比较不同催化剂之间的活性位及反应机理之间的差异,控制反应条件使转化率低于20%,在此条件下计算了各个催化剂催化水煤气变换反应的反应速率及转换频率(TOF),结果列于表1。同时,测定了相应的动力学参数并据此计算得出了反应的表观活化能列于图4b。ZnAl-LDHs催化WGSR的反应速率及活化能分别为21.1μmol·gcat-1·s-1和 70.7 kJ·mol-1,而 Au/LDHs的相应数值为 78.6 μmol·gcat-1·s-1和 52.9 kJ·mol-1。对比发现,Au 负载明显地提高了水滑石材料催化WGSR的综合效率。水滑石负载AuCu合金后催化WGSR的反应速率、TOF 值及活化能分别为 153.4~207.1 μmol·gcat-1·s-1、1.32~1.79 s-1、31.1~37.2 kJ·mol-1。 显然,负载 AuCu合金的水滑石体系相比于单纯的负载Au体系具有更高的反应速率、更大的TOF值及更小的活化能,表明引入第二金属Cu形成AuCu合金可以在纯Au负载的基础上进一步提升水滑石材料催化WGSR的效率。
此外,对几种水滑石材料催化WGSR的稳定性及重复利用性能也进行了探讨(图4(c,d))。当反应时间延长到48 h时,水滑石、负载Au水滑石及负载AuCu合金的水滑石(Au2Cu1/LDHs)对CO的转化率从最初的18.7%、65.9%和97.5%分别减小到17.2%、62.1%和93.1%,幅度均较小,说明Au负载后的水滑石材料可以较长时间稳定的用于催化WGSR。将反应过后的催化剂经离心、洗涤、干燥及氢气气氛下还原等操作步骤进行重复利用测试,发现经4次重复利用后的催化剂其CO转化率仍可维持在17.8%,63.2%和96.0%,活性衰减幅度非常小。上述结果说明,Au以及AuCu合金负载的水滑石具有很强的化学稳定性,可长时间且多次重复利用于催化WGSR。

表1 各种样品在300℃催化WGSR的参数Table 1 Catalytic performance of various samples for WGSR at 300℃
2.3 材料的结构组成与催化性能之间的关系探究
对不同催化剂的物理化学性能参数进行了详细的测定及比较,结果列于表2。从BET测定结果可知,负载Au后水滑石的比表面积明显的增大,从71 m2·g-1增大到 86 m2·g-1,而 AuCu/LDHs 材料的比表面积则进一步增大为92~98 m2·g-1。分别由TEM测定和XRD参数计算了负载体系中Au纳米颗粒的平均晶粒尺寸,两者数值较为接近,均遵循Au/DHs<Au1Cu1/LDHs<Au5Cu1/LDHs<Au2Cu1/LDHs的顺序。分别由CO的化学吸附结果及TEM测定得到的Au的晶粒尺寸计算了金属Au的分散程度,结果列于表2,不同材料中Au的分散度与催化WGSR反应的活性数据见图5a。从中可知,虽然TEM计算所得的数值普遍大于由CO化学吸附所测定的数据,但两者的趋势保持一致。AuCu/LDHs比Au/LDHs具有更高的Au分散度及更大的催化活性,并且随着Au和Cu的比例增大,Au的分散度和催化活性均呈现先增大后减小的趋势,说明nAu∶nCu=2∶1时为最佳的催化体系。
为了进一步探究材料的结构组成与催化活性之间的关联,通过XPS表征对不同催化剂体系的活性组分进行了分析比较(图5)。图5b是ZnAl-LDHs和Au/LDHs的XPS谱图,从中可以看出,2个样品均具有明显的C、O、Zn和Al等元素的信号。其中,Au/LDHs的图谱包含有2个明显的代表Au4f轨道的信号峰 Au4f7/2(84.1 eV)和 Au4f5/2(87.8 eV),分别归属于Au和带正电荷的活性种Auδ+[34-35]。图5c为Au2Cu1/LDHs的XPS表征结果。Au2Cu1/LDHs的XPS图谱不仅保留了结合能(BE)在84.1和87.8 eV处的特征峰,且出现了在952.5 eV处代表Cu2p1/2和932.5 eV处代表Cu2p3/2的信号峰,进一步表明合成的样品是AuCu合金负载的水滑石。值得注意的是,比较Au/LDHs和AuCu/LDHs的XPS谱图发现,Au和Auδ+组分的比例发生了较大的变化,负载合金的体系中Auδ+(Au4f5/2)的含量比纯Au负载的体系有明显的增大。为此,根据XPS谱图峰面积积分计算了nAuδ+/ntotalAu的值,结果列于表1。从中可以看出,合金负载后,体系中Auδ+的比例由Au/LDHs的39.7%上升到了57.8%~65.5%。图5d为所有金负载水滑石体系的 nAuδ+/ntotalAu与催化活性之间的关系图。不同的催化体系对CO转化率随着Auδ+含量的提高而明显增大,说明材料体系中Auδ+的含量有利于体系催化WGSR 的活性。对于不同的 nAu∶nCu,Au2Cu1表现出了最大的CO转化率,且具有最高的Auδ+含量,Au5Cu1次之,Au1Cu1最差。
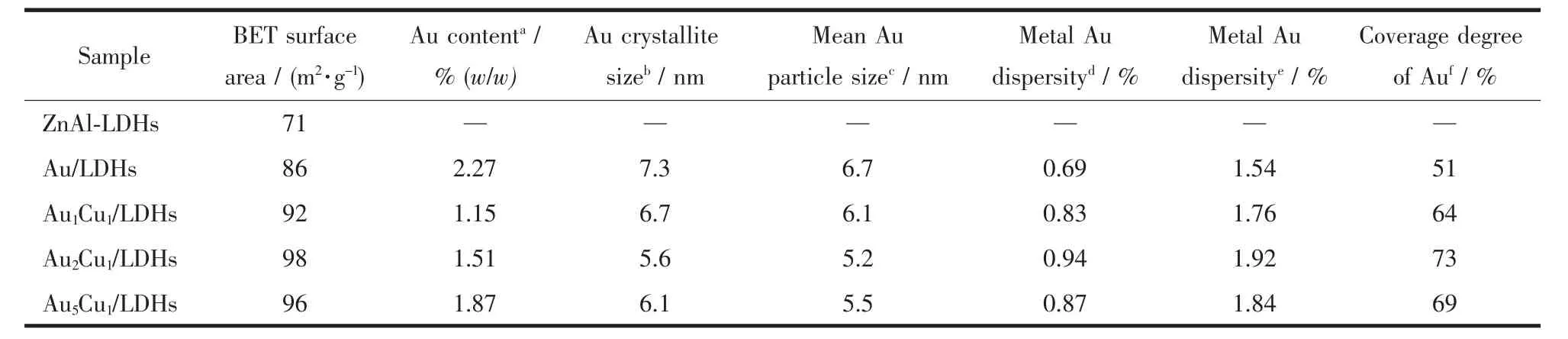
表2 不同催化剂的物理化学性质参数Table 2 Physicochemical properties of different catalysts
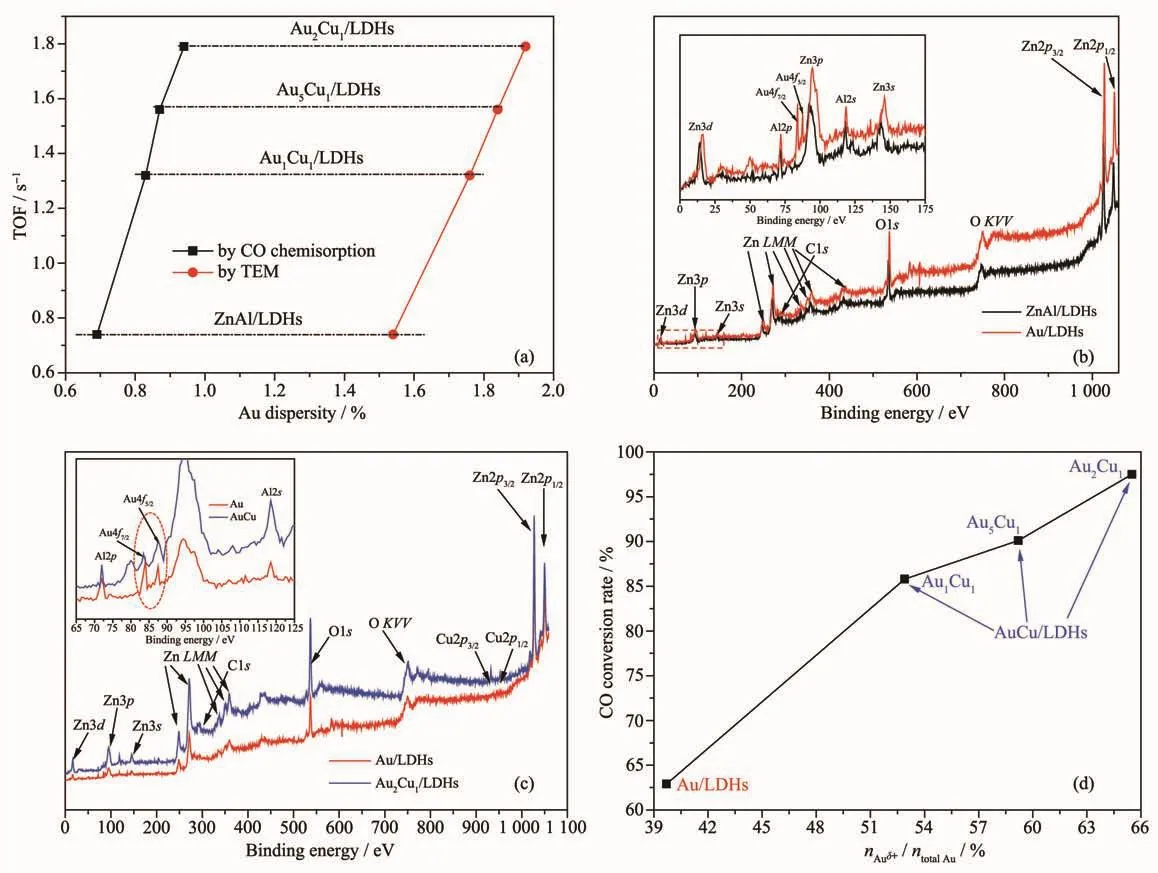
图5 样品中Au的分散程度与活性之间的关系曲线(a);ZnAl-LDHs、Au/LDHs和Au2Cu1/LDHs的XPS图谱;样品的CO转化率与n Auδ+/n total Au的关系(d)Fig.5 Relationship between the Au dispersity and activity(a);XPSspetra of ZnAl-LDHs,Au/LDHs and Au2Cu1/LDHs(b,c);Relationship between CO conversion rate and n Auδ+/n total Au for WGSR of samples(d)
3 结 论
Au的负载可明显地提升ZnAl-LDHs催化WGSR的活性,在300℃反应0.5 h后,ZnAl-LDHs及Au/LDHs催化CO的转化率分别为18.7%和65.9%。而负载AuCu合金的水滑石催化WGSR的CO转化率则进一步提升到了85.2%~97.5%。并且催化活性随着合金中Cu含量的提高呈先增大后减小的趋势,其中活性最高为Au2Cu1/LDHs样品,其催化活性为 207.1 μmol·gcat-1·s-1,TOF 值为 1.79 s-1,活化能为31.1 kJ·mol-1。物化性质分析也表明,负载体系中Au和Cu的比例对催化剂物理化学参数影响较大,其中 nAu∶nCu=2∶1 时,负载体系具有最大的 Au 分散度、最小的晶粒尺寸、最高的表面覆盖度,同时具有最高的催化活性。XPS分析表明,加入第二金属Cu形成合金后增大了Auδ+组分在体系中的含量,并且同样遵循 Au2Cu1>Au5Cu1>Au1Cu1。 不同的 Au 负载体系对CO转化率随着Auδ+含量的提高而明显增大,说明Auδ+含量有利于提高体系催化WGSR的活性。Au以及AuCu合金负载的水滑石具有很强的化学稳定性(活性衰减小于3%),可长时间且多次重复利用于催化WGSR。
