复方甘草酸苷片中甘草酸苷含量测定的方法学验证
2019-06-22阿依居来克卡得尔仇艳丽李欣荣孙媛媛高晓黎
阿依居来克·卡得尔, 仇艳丽, 单 宇, 李欣荣, 唐 城, 孙媛媛, 高晓黎
(1新疆医科大学药学院; 2新疆特丰药业股份有限公司, 乌鲁木齐 830011)
复方甘草酸苷片(Compound Glycyrrhizin Tablets)是由甘草酸苷(Glycyrrhizin,GL)、甘氨酸(glycine,GLY)及DL-蛋氨酸(DL-methionine,MET)组成的复方制剂[1]。其中甘草酸苷又称甘草甜素,是一种临床使用的抗炎抗病毒的三萜类化合物[2-3],在体内被小肠细菌代谢为甘草次酸后吸收进入机体发挥药理作用,具有抗过敏、免疫调节及抑制病毒增殖和对病毒灭活的作用。甘氨酸可调节肾功能,干扰 Na+、K+重吸收,防止由甘草酸引起的轻微伪醛固酮症状。DL-蛋氨酸在体内转化为半胱氨酸,后者可提高肝脏的解毒能力,减少过敏反应。
甘草酸苷在临床上用于治疗各种类型的肝病[4-8],改善肝功能异常及治疗各种皮肤病[9-14]。目前已在临床中广泛应用。本实验建立了高效液相色谱法(中国药典2015年版通则0512)测定复方甘草酸苷片中甘草酸苷含量,并依据《方法验证指导原则》对该方法进行了验证。
1 仪器与试药
1.1 仪器LC-20AD高效液相色谱仪(岛津),LC-2030D 3C高效液相色谱仪(岛津),CPA225D精密天平(北京赛多利斯科学仪器有限公司),BSA224S万分之一电子天平(北京赛多利斯科学仪器有限公司)。
1.2 试药复方甘草酸苷片(新疆特丰药业股份有限公司,批号:20181027,20181123,20181206),甘草酸铵(中国食品药品检定研究院,批号:110731-201619、110731-201720,含量为93.0%和97.7%),乙腈为色谱级,其余冰乙酸、95%乙醇均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件色谱柱:Kromasil 100A C18(4.6 mm×150 mm,5 μm);流动相:2%醋酸-乙腈(65∶35);检测波长:254 nm;柱温:30℃;流速:1.0 mL/min;进样量:20 μL;运行时间:25 min。甘草酸苷峰理论塔板数不低于2 000。
2.2 溶液的制备
2.2.1 对照品溶液 称定甘草酸铵对照品12.5 mg置50 mL量瓶中,加50%的稀乙醇溶解并稀释至刻度,摇匀,即得浓度为0.25 mg/mL的对照品储备液。
2.2.2 供试品溶液 称定供试品粉末0.170 g置100 mL量瓶中,用50%的稀乙醇溶解定容至刻度,即得。
2.2.3 阴性溶液 称定空白辅料90 mg、甘氨酸和蛋氨酸分别25 mg,置100 mL量瓶中,加50%稀乙醇溶解并稀释至刻度,摇匀,即得。
2.3 系统适用性试验取对照品溶液,按“2.2.1”项下方法测定,连续进样6针,结果见表1。理论塔板数按甘草酸苷计算应不低于2 000。结果表明,6针主峰峰面积RSD=0.1%,理论塔板数>2 000,拖尾因子<1.5,表明系统适用性良好,符合规定。

表1 系统适用性试验结果
2.4 专属性试验
2.4.1 溶剂、辅料干扰试验 取溶剂、阴性溶液、对照品溶液和供试品溶液,按“2.1”项下方法测定,记录色谱图,结果见图1。可知,甘草酸苷保留时间为11.3 min,溶剂和辅料对检测无干扰。


A: 溶剂B: 阴性溶液


C:对照品溶液D:供试品溶液
图1 溶剂、辅料干扰专属性HPLC图谱
2.4.2 强制降解试验
2.4.2.1 强酸破坏 称取供试品粉末0.170 g置100 mL量瓶中,加20 mL溶剂溶解,后加入1 moL/L盐酸溶液1 mL,置室温下18 h,加1 moL/L氢氧化钠溶液1 mL中和,加稀乙醇稀释至刻度,作为酸降解溶液,按“2.1”项下方法测定,记录色谱图,结果见图2。

图2 酸降解专属性HPLC图谱
2.4.2.2 强碱降解试验 称取供试品粉末约0.170 g置100 mL量瓶中,加20 mL溶剂溶解,后加入1 moL/L氢氧化钠溶液2 mL,置80℃下4 d,取出放置室温后加1 moL/L盐酸溶液2 mL中和,加稀乙醇稀释至刻度,作为碱降解溶液,按“2.1”项下方法测定,记录色谱图,结果见图3。
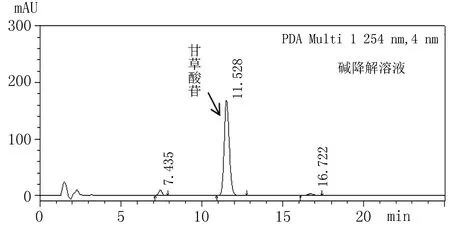
图3 碱降解专属性HPLC图谱
2.4.2.3 氧降解试验 取供试品粉末0.170 g置100 mL量瓶中,加20 mL溶剂溶解,后加入3%H2O2溶液2 mL,置80℃下4 d,取出放置室温后加稀乙醇稀释至刻度,作为氧降解溶液,按“2.1”项下方法测定,结果见图4。

图4 氧降解专属性HPLC图谱
2.4.2.4 高温降解试验 称定供试品粉末0.170 g置称量瓶中,放置80℃高温条件下28 d,取出放置室温后,加稀乙醇稀释转移至100 mL量瓶中,溶解定容至刻度,作为高温降解溶液,按“2.1”项下方法测定,记录色谱图,结果见图5。

图5 高温降解专属性HPLC图谱
2.4.2.5 光照降解试验 称定供试品粉末0.170 g置称量瓶中,放置光照(4 500±500)LUX条件下28 d,取出后,加溶剂稀释转移至100 mL量瓶中,加稀乙醇溶解定容至刻度,作为光照降解溶液,按“2.1”项下方法测定,记录色谱图,结果见图6。

图6 光照降解专属性HPLC图谱
2.4.2.6 专属性试验结论 专属性试验结果表明,溶剂、辅料及强制降解溶液不干扰甘草酸苷测定。该方法专属性良好。
2.5 检测限和定量限试验取“2.2.1”项下对照品溶液进一步稀释,分别量取20 μL进样,得检测限(S/N≥3)和定量限(S/N≥10)。结果表明甘草酸苷的检测限为0.082 μg/mL,定量限浓度为0.413 μg/mL,6针定量限主峰保留时间RSD<2.0%,峰面积RSD<5.0%,见表2。
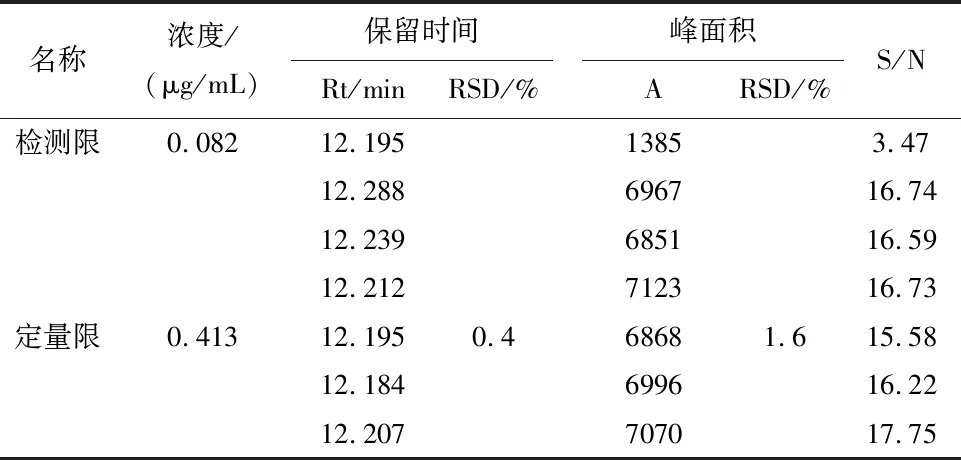
表2 检测限和定量限测定结果
2.6 线性关系考察称取甘草酸铵对照品适量,分别配制成每1 mL分别含206.39、219.28、232.18、239.18、257.98、283.78、309.58 μg的系列对照品溶液,分别依法测定,结果见表3,以甘草酸苷峰面积为纵坐标(Y),浓度为横坐标(X)。甘草酸苷线性方程为Y=16 331.86X+3 053.83,r=0.999 2,表明甘草酸苷在206.39~309.58 μg/mL范围内线性良好。

表3 线性测定结果
2.7 精密度试验取同一批样品按照“2.2.2”项下方法制备6份供试品,按“2.1”项下方法测定重复性。取同一样品,在另一台HPLC仪上由另一操作人员,于不同日期同法测定中间精密度。结果见表4,结果表明重复性6次测定结果RSD≤2.0%,中间精密度12次测定结果RSD≤5.0%,重复性和中间精密度符合要求。

表4 精密度试验结果
2.8 回收率试验取空白辅料90 mg,共9份,按照处方比例加入低、中、高不同量的甘草酸单铵盐原料药分别置装有、甘氨酸和蛋氨酸分别为25 mg的100 mL量瓶中,按“2.2.2”项下制备供试品溶液,按“2.1”项下方法测定,按外标一点法以峰面积计算含量,并计算回收率。结果见表5。结果显示,单一回收率和平均回收率为98.0%~102.0%,RSD为0.6%,表明方法准确度良好。
2.9 溶液稳定性试验取“2.2.2”项下的供试品溶液,分别于0、14、24、48 h进样分析。结果表明供试品溶液室温放置48 h,含量无显著变化,RSD为0.4%,RSD<2.0%,表明供试品溶液室温放置48 h稳定,见表 6。

表5 准确度试验结果

表6 溶液稳定性试验结果
2.10 耐用性试验取“2.2.2”项下的供试品溶液,按“2.1”项下方法测定,于不同流速、柱温及有机相比例(表7)测定甘草酸苷含量。在试验流速、柱温、流动相比例变化下,甘草酸苷含量变化RSD<2.0%,表明该方法耐用性符合要求,结果见表8。

表7 色谱条件变动的参数

表8 耐用性试验结果
2.11 样品含量测定取3批复方甘草酸苷片样品按“2.1”项下方法测定含量,结果表明3批样品含量均符合规定,结果见表9。

表9 样品含量测定结果
3 讨论
复方甘草酸苷片为临床常用药物。本研究按照(中国药典 2010 年版二部附录Ⅴ D)对复方甘草酸苷片中甘草酸苷含量测定并对方法进行考察。为提高本品的质量标准提供依据,控制复方甘草酸苷片的质量。
方法验证对含量测定方法的专属性、系统适用性、线性范围、回收率、重复性、中间精密度、稳定性、耐用性等各方面进行了考察,发现该方法专属性好,准确度高,结果稳定可靠,适用性强,均符合规定。
