大鼠口服艳山姜挥发油后的入血成分分析*
2019-06-10吴林菁王兴兰李婉蓉刘学杨佳佳肖婷张嫩玲周雪姜丰沈祥春陶玲
吴林菁, 王兴兰, 李婉蓉, 刘学, 杨佳佳, 肖婷, 张嫩玲, 周雪, 姜丰, 沈祥春**, 陶玲**
(1.贵州医科大学 药学院 天然药物资源优效利用重点实验室, 贵州 贵阳 550025; 2.贵州医科大学 药学院 药用植物功效与利用国家重点实验室, 贵州 贵阳 550025; 3.贵州医科大学 药学院 贵州省普通高等学校天然药物药理与成药性评价重点实验室, 贵州 贵阳 550025; 4.贵州医科大学 药学院 贵州省特色天然药物资源高效利用工程中心, 贵州 贵阳 550025)
艳山姜Alpiniazerumbet(Pers.)Burtt. et Smith作为为贵州少数民族常用药,具有抗炎、镇痛、抗心血管疾病等作用,收载于《贵州省中药材、民族药材质量标准》(2003版)[1]。基于艳山姜果实挥发油所具备的显著心血管药理学活性,课题组开展了艳山姜生药学[2]、提取工艺及化学成分[3-5]、药理学[6-15]、新剂型[16-17]等方面的研究。艳山姜果实挥发油中主要活性组分α-蒎烯、1,8-桉叶油醇、β-蒎烯、莰烯对血管内皮细胞具有显著的调控保护作用[7],但其活性成分在体内的吸收过程还尚不明确。在研究中药复杂成分的过程中,普遍认为中药发挥药效的活性成分可能是其被吸收入血的成分[18-20]。因此检测口服中药后有哪些成分被吸收入血或经过人体代谢后会有哪些成分发生变化,是深入研究中药药效物质的重要基础[21-23]。本实验采用气相色谱-质谱法(GC-MS),结合血清药物化学实验方法,对大鼠灌胃艳山姜挥发油(EOFAZ)后的血浆样品进行分析检查,考察EOFAZ在大鼠体内的入血成分,为EOFAZ的下一步药代动力学研究提供参考,也为EOFAZ的治疗心血管疾病药效物质基础研究提供依据。
1 材料与方法
1.1 材料
1.1.1实验动物 健康成年雄性 SD 大鼠6只,体质量(250±20) g,清洁级,由贵州医科大学实验动物中心提供,合格证号为SCXK(黔)2018-0001,实验前12 h禁食不禁水。
1.1.2药品与试剂 艳山姜采自贵州省黔西南州贞丰县连环乡巧岩村,经贵州医科大学龙庆德副教授鉴定为姜科山姜属植物艳山姜Alpiniazerumbet( Pets. ) Burtt. et Smith 的干燥成熟果实。乙酸乙酯(分析纯,上海申博化工有限公司,1601101),肝素钠(北京索莱宝科技有限公司,1024E027)。
1.1.3仪器 Agilent 6890 /5975C GC- MS联用仪(美国安捷伦公司),E104 /02型电子天平(梅特勒-托利多仪器上海有限公司),Microfuge 20R型冷冻离心机(美国贝克曼库尔特公司),XW-80A漩涡混合仪(上海驰唐电子有限公司),KQ3200型超声波清洗器(昆山市超声仪器有限公司),UPW-UP-10超纯水处理器(成都天莘宁科技有限公司),GC-MS Solution色谱工作站标准谱库(美国 NIST 质谱检索数据库)。
1.2 方法
1.2.1艳山姜挥发油的提取 参照文献[4]中艳山姜挥发油的提取方法,精密称取艳山姜干燥成熟果实100 g,按照1∶10的比例加入蒸馏水1 000 mL,水蒸气蒸馏提取5 h后收集挥发油,加入适量无水硫酸钠脱水,所得艳山姜挥发油具有较为浓烈的香味,并呈淡黄色透明液体,得率为0.98%。
1.2.2艳山姜挥发油供试品的制备 精密吸取艳山姜挥发油50 μL,置于5 mL的棕色洁净容量瓶中,加适量乙酸乙酯溶解并定容至刻度线,摇匀,超声15 min,12 000 r/min离心 10 min,取上清液即得,备用。
1.2.3血浆样品采集 取SD雄性大鼠6只,给药前自颈静脉插管取血0.5 mL,置含有10 g/L肝素的2 mL EP管中,4 ℃ 3 000 r/min离心10 min,取全部上清液作空白血浆,放置于-80 ℃的冰箱储存备用;大鼠灌胃艳山姜挥发油2.0 mL,1 h后自颈静脉取血0.5 mL,处理方法同空白血浆。
1.2.4血浆样品处理 取大鼠血浆200 μL,置于2 mL EP管中,加入乙酸乙酯800 μL,涡旋5 min,于4 ℃ 12 000 r/min离心10 min,取上清液加入双蒸水200 μL,涡旋5 min,12 000 r/min 4 ℃离心10 min,取上清液3 μL于GC-MS进样检测。
1.2.5气相色谱条件 色谱柱为ZB-5弹性石英毛细管柱,运行时间为62 min;初始温度为45 ℃并保持2 min,以20 ℃/min的速率升温至75 ℃并保持2 min,2 ℃/min升温至100 ℃并保持2 min,4 ℃/min升温至200 ℃并保持1 min,以10 ℃/min升温至310 ℃并保持5 min。载气为高纯He(99.999%),分流比20∶1,载气流量1.0 mL/min,柱前压7.65 psi,溶剂延迟时间4.0 min,汽化室温度250 ℃。
1.2.6质谱条件 电子能量70 eV,接口温度280 ℃,倍增器电压1 659 V,发射电流34.6 μA,离子源温度230 ℃,四极杆温度150 ℃,离子源为EI源,质量范围29~450 amu。
1.2.7结构鉴定 对总离子流图中的各峰,经过质谱计算机数据系统检索,及核对标准质谱图Nist2005、Wiley275,鉴定其检测出的化合物,并利用峰面积归一化法,测定各化学成分的相对质量分数。
2 结果
大鼠灌胃EOFAZ前后,气相-质谱联用仪分析色谱图见图1,从血样中检测出化合物的结果如表1所示。艳山姜挥发油经GC-MS检测并鉴定出51个成分。大鼠灌胃EOFAZ 1 h后的血浆经GC-MS分析,检测出入血成分37个,其中主要活性成分β-蒎烯、α-蒎烯、莰烯、1,8-桉叶油醇在EOFAZ及入血成分中所占百分含量均较高,且β-蒎烯在EOFAZ及给药后血浆中都是相对百分含量最高的成分。

图1 EOFAZ及大鼠EOFAZ灌胃前后血样GC-MS结果 Fig.1 GC-MS chromatogram of EOFAZ and blood samples of rats before and after gavage of EOFAZ in rats
3 讨论
由于EOFAZ极性小,在前期实验中分别考察了氯仿、石油醚、正丁醇、乙酸乙酯作为溶剂,将其用分别配制成同一浓度的样品进行GC检测,根据GC检测结果和溶解现象综合比较,发现乙酸乙酯溶解的样品出峰数目较多、峰面积较大、分离度良好,且EOFAZ溶液呈澄清透明状态。因此,最终确定乙酸乙酯作为EOFAZ的溶剂。同时考察了不同比例的乙酸乙酯溶解EOFAZ,其结果表明乙酸乙酯和EOFAZ的体积比为100∶1是最佳的溶解比例。
为了更多地检测出EOFAZ在大鼠体内的入血成分,在预实验时共考察灌胃EOFAZ后15 min、30 min、45 min、1 h、2 h、3 h、4 h、5 h、7 h、9 h、12 h、24 h共12个取血点,采用Aglient7890B型气相色谱仪分析对比空白血浆和含药血浆的GC色谱图,发现大鼠口服EOFAZ后1 h取血点出峰最多,且峰面积较大,因此最终确定取血时间点为1 h。
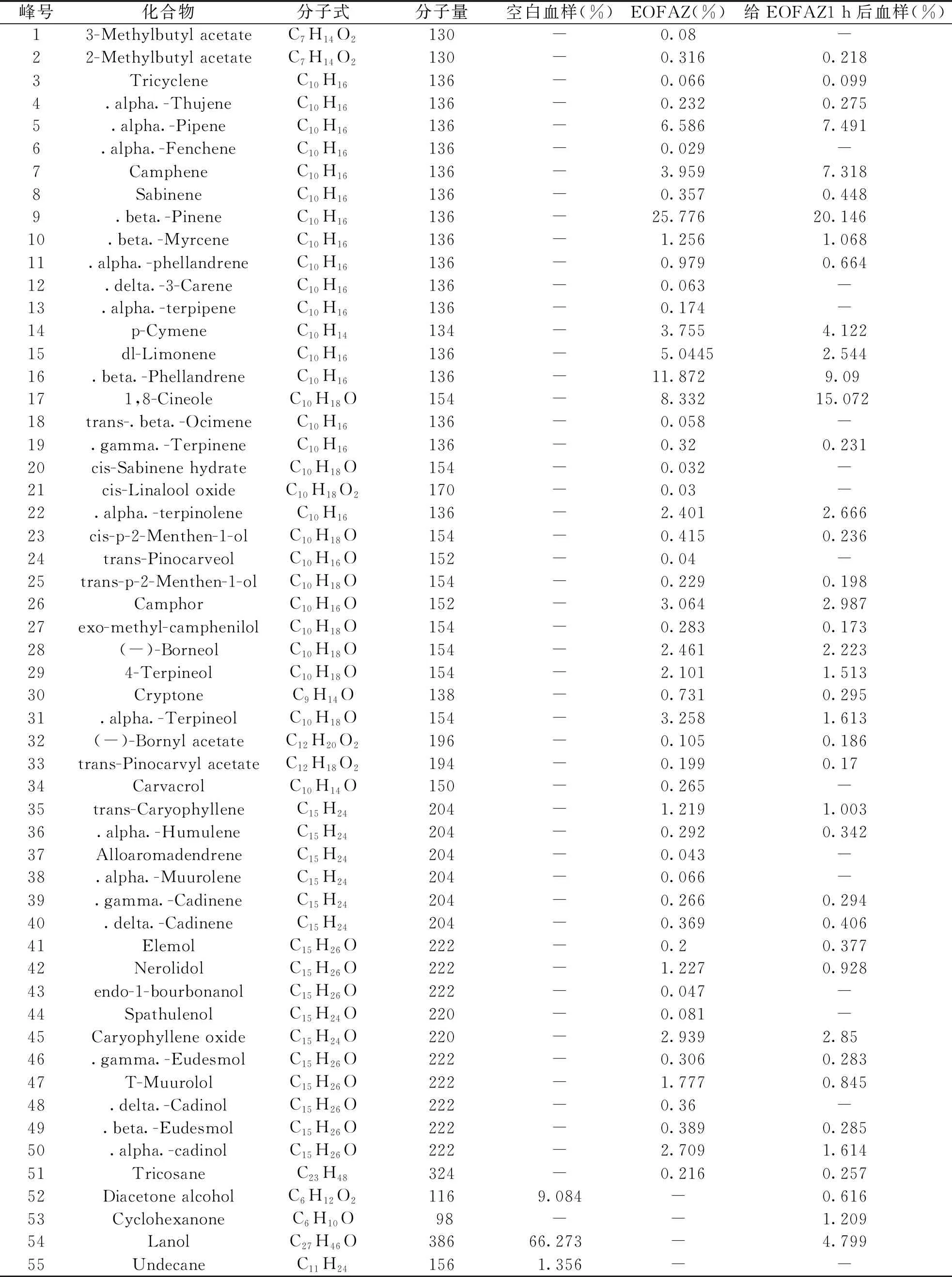
表1 EOFAZ及大鼠EOFAZ给药前后血样化合物成分的GC-MS分析Tab.1 GC-MS analysis of EOFAZ and blood samples of rats before and after administration of EOFAZ
注:“-”表示无该成分
生物样品的预处理是样品分析中极其重要的一个环节,在测定血样时,首先应除去样品中的蛋白质,使结合型的药物释放出来以便测定药物总浓度。沉淀蛋白的方法有盐析法、有机溶剂沉淀法、等电点沉淀法等。由于艳山姜挥发油在常温下极易挥发,应当处理完样品立即进样检测,防止有效成分挥发,有机溶剂可使蛋白质分子内及分子之间的氢键发生变化而使蛋白质迅速凝聚,使与蛋白质结合的成分释放出来,因此本实验选用有机溶剂去除蛋白,同时考虑利用有机溶剂高效萃取血浆中挥发性入血成分,分别考察了正丁醇、甲苯、石油醚、乙酸乙酯、正己烷等有机试剂沉淀蛋白及萃取挥发性入血成分作用,分别取各试剂沉淀蛋白后的上清液,水洗后再取其上清液,采用Aglient7890B型气相色谱仪进样分析,比较各试剂沉淀蛋白后血样的出峰数目、分离度、峰面积等条件后,发现石油醚杂峰太多且分离度差,正丁醇、乙酸乙酯、甲苯、正己烷的出峰数目和出峰时间较为相近,但乙酸乙酯的分离度较高和峰面积较大,最终确定沉淀蛋白及萃取挥发性入血成分的有机溶剂为乙酸乙酯。同时对乙酸乙酯的用量进行考察,结果显示乙酸乙酯与血浆样品的比例为4∶1时,蛋白沉淀较为完全且出峰数目较多、峰分离度较好,经水洗后能有效除去血浆中的水溶性物质,使含药血浆溶液澄清透明,GC-MS检测更加精准无干扰。因此,本实验确定采用乙酸乙酯为蛋白沉淀剂,且乙酸乙酯与血浆样品的比例为4∶1时沉淀蛋白的效果最佳。
本实验通过GC结合MS法确定EOFAZ在大鼠中的入血成分有37种,主要有β-蒎烯、1,8-桉叶油醇、β-水芹烯、α-蒎烯、莰烯、对伞花烃、樟脑、石竹烯氧化物、α-异松油烯、d-柠檬烯、冰片、α-荜澄茄烯、α-松油醇、4-松油醇、β-月桂烯、反式松香芹乙酯等(百分含量分别为20.146%、15.072%、9.09%、7.491%、7.318%、4.122%、2.987%、2.85%、2.666%、2.544%、2.223%、1.614%、1.613%、1.513%、1.068%、1.003%),这37种成分能是EOFAZ药效的物质基础,更多入血成分的鉴定有待进一步研究[13]。本研究阐释了艳山姜活性部位挥发油进入大鼠血液中的成分,为进一步研究艳山姜药材的体内过程和药效物质奠定了基础。[22-23]
