3D快速黑血管壁磁共振成像技术对基底动脉狭窄诊断的价值
2019-06-10汪振佳樊昭阳
汪振佳 樊昭阳 刘 文 于 薇
基底动脉狭窄(basilar artery stenosis,BAS)常导致后循环血供不足,重度狭窄者的卒中发生风险骤增,其所致卒中预后差,患者病死率高达70%[1-3]。因此早期准确诊断、积极干预治疗基底动脉重度狭窄病变有助于减少卒中事件的发生进展,降低患者的致残率、致死率[4]。颅脑磁共振血管成像(MR angiography,MRA),作为常规无创影像技术可以对基底动脉狭窄做出诊断,但无法评估狭窄动脉管壁情况[5]。新近研发T1加权3D变动翻转角快速自旋回波序列(3D T1-sampling perfection with application-optimized contrasts by using different flip angle evolutions,3D T1-SPACE)是一种3D黑血管壁成像技术,具有高空间分辨率、快扫描速度、各向同性、小部分容积效应等特点,能够提供管腔组织结构、管壁厚度、斑块成分等信息,可实现血管壁和血管腔病变的同步评估,对颅颈部血管病变的显示具有独到的优势[6-9]。本研究旨在评估3D T1-SPACE技术对基底动脉狭窄疾病的诊断价值。
资料与方法
1.患者一般临床资料 收集首都医科大学附属北京安贞医院,2016年7月至2018年8月,经头颅血管MRA检查疑似存在基底动脉狭窄并且拟接受数字减影血管造影(digital subtraction angiography,DSA)的患者54例。所有患者在接受DSA检查前3~7 d于医学影像科完成3D T1-SAPCE成像检查。排除标准:①患者存在MRI检查禁忌证;②患者存在DSA检查禁忌证;③患者无法耐受MRI检查。本研究经由北京安贞医院伦理委员会同意,所有患者在检查前均已签署知情同意书。
2.MRI扫描方法 所有患者均在西门子(德国)Verio 3.0T磁共振成像仪接受检查。固定患者头部,微抬下颌,患者佩戴8通道相控阵颈动脉表面线圈(上海辰光)及头颅线圈,保持静止体态并减少吞咽运动,以颈总动脉分叉为扫描中心,坚持覆盖颈总动脉远段至大脑前动脉胼周段区域,矢状位扫描。3D T1-SPACE参数如下:TR 900 ms,TE 14 ms,带宽488 MHz,FOV 204 mm,矩阵284 mm×320 mm,192层,0.625 mm层厚,0 mm层间距,各向同性体素0.625 mm×0.625 mm×0.625 mm。采集时间7min3s。
3.DSA 全麻后,患者在GE 3100(美国)数字剪影血管造影机接受DSA检查。操作术者首先在股动脉选取穿刺点以Seldinger技术逆行穿刺,在双侧椎动脉及双侧颈总动脉依次导入5F或6F鞘管,然后穿入5F猪尾导管实现选择性血管造影。通过高压注射器对患者注入非离子型对比剂(碘帕醇370,博莱科,上海,中国),对比剂注入速率由手术医师依据患者动脉血流流速进行调整,常设置为3~4 mL/s,总注入约每根血管6~7 mL。所有血管都实现标准正位、侧位及斜位成像。
4.图像分析 (1)MR图像质量评分:一名高年资放射科医师对MR图像以4分法进行评分,具体标准如下:4分:血管内、外壁及管腔显示清晰,无伪影;3分:血管内外壁及管腔部分显示清晰,无伪影;2分:血管内外壁及管腔部分显示清晰,有伪影,但不影响诊断;1分:血管内外壁及管腔显示不清晰,存在严重伪影干扰诊断。1分者排除出本次研究[10]。
(2)狭窄程度:以WASID(the warfarin-aspirin symptomatic intracranial disease)方法[11]为标准进行基底动脉狭窄程度测量:基底动脉狭窄率=l-(狭窄段管径/狭窄近端正常段管径)×100%。分别在DSA侧位图像及3D T1-SPACE的矢状位图像进行测量。依据管腔狭窄程度将血管分为正常组(无狭窄)、轻度狭窄组(1%~49%)、重度狭窄组(50%~99%)和闭塞组(100%)。对于存在弥漫性斑块或合并多处狭窄的血管,测量该支血管病变最重处的管腔狭窄率(图1)。3D T1-SPACE和DSA的图像被分别分析。将二者图像统一传送至PACS工作站,3D T1-SPACE图像经MPR重建处理后,由两名放射科医师(放射科医师1和放射科医师2)采取双盲法对3D T1-SPACE图像进行病变分析。DSA图像由一名不知道MR结果的介入医师进行分析。
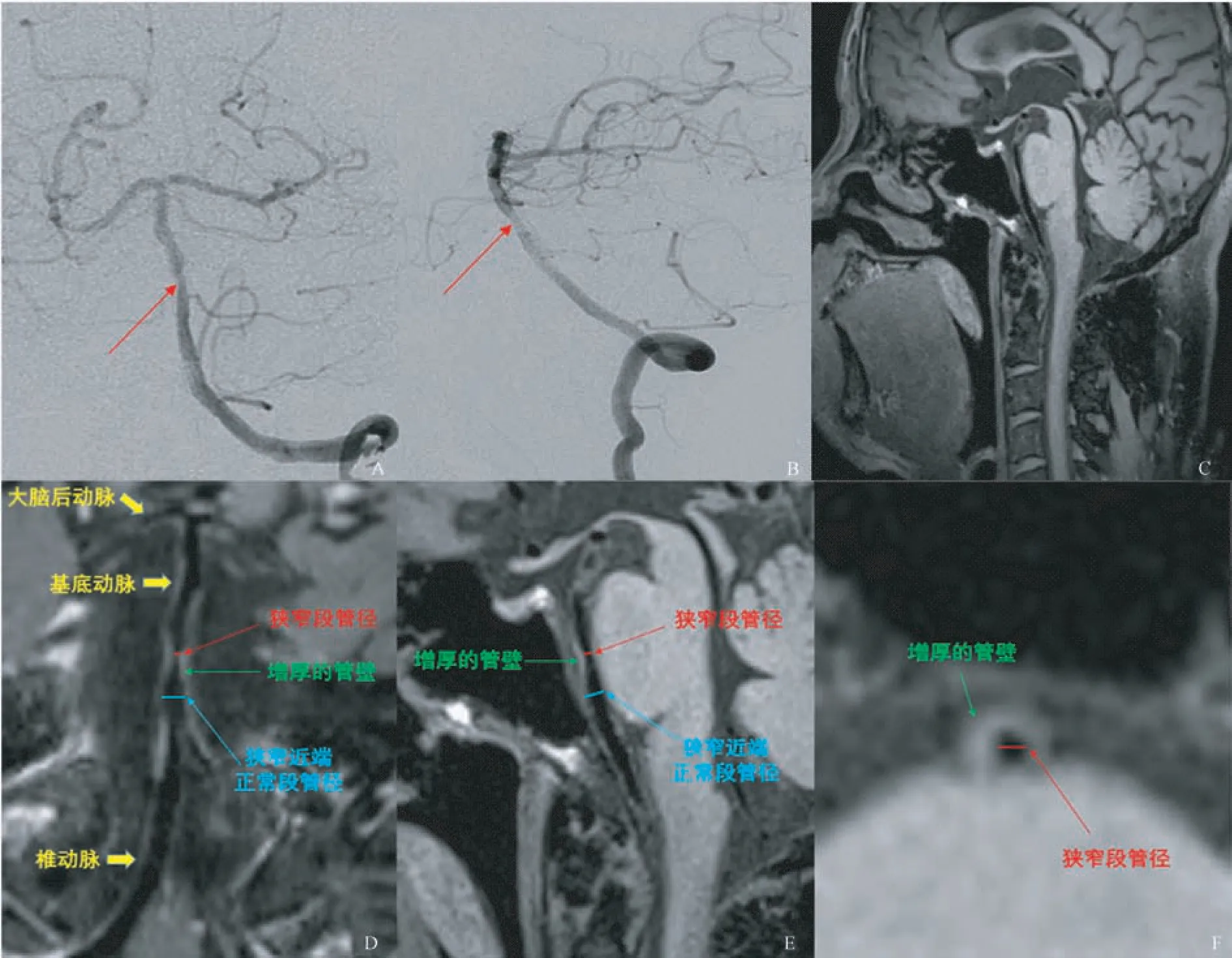
图1 DSA和3D T1-SPACE图像 A~B:分别为基底动脉DSA正、侧位图像,红色箭头所指为病变最窄处。C~F:分别为该患者的3D T1-SPACE原始扫描、冠状位、矢状位、横轴位图像,清晰显示基底动脉全程管壁、管腔病变特征。该患者图像质量评分为4分
3.统计学分析 采用SPSS 16.0软件进行统计学分析。连续变量以均数±标准差表示,计数资料以频数表示。计算Spearman秩相关系数评价二种成像方法间狭窄测量结果的相关性;计算组内相关系数(intraclass correlation coefficient,ICC)评价不同观察者的3D T1-SPACE测量结果间的信度与3D-T1 SPACE测量结果与DSA测量结果的信度;Bland-Altman图用于比较两名放射科医师MR测量结果间的一致性与MR-DSA两种成像方式间测量结果的一致性。以DSA为金标准,计算3D T1-SPACE诊断基底动脉重度狭窄的一致率、灵敏度、特异度、阳性预测值、阴性预测值、阳性似然比与阴性似然比。ICC<0.2,信度差;0.20≤ICC<0.40,信度较差;0.40≤ICC<0.60,信度中等;0.60≤ICC<0.80,信度良好;ICC≥0.80,信度优异[12]。P<0.05为差异有统计学意义。
结果
1.患者基本临床资料 共计有54例患者顺利完成上述两种检查,基本资料见表1。其中2例患者的MR图像被评定为1分。因此余下52例患者纳入本次研究,图像质量评分为(3.14±0.57)分。
2.图像分析 (1)MR-MR图像分析 两名放射科医师(1、2)测得的3D T1-SPACE图像基底动脉狭窄率分别为(37.80±16.29)%和(38.32±16.58)%,二者比较,差异无统计学意义(P=0.376)。Bland-Altman图提示94.2%的点在95%一致性界限之内,两名医师的所测量的狭窄率结果相比,差值的绝对值最大为7.6%,差值平均值为0.5%,认为二者测量结果具有高度一致性(图2)。两名放射科医师测得狭窄处管腔内径、狭窄近端正常管腔内径以及狭窄率间的信度高(表2)。
表1 患者基本临床资料[,n(%)]

表1 患者基本临床资料[,n(%)]
项目 数值年龄/岁 58.7±9.1男性 41(75.9)高血压 39(72.2)高血脂 31(57.4)糖尿病 29(53.7)冠心病 36(66.7)吸烟 38(70.4)
表2 观察者间52例MR图像测量结果()
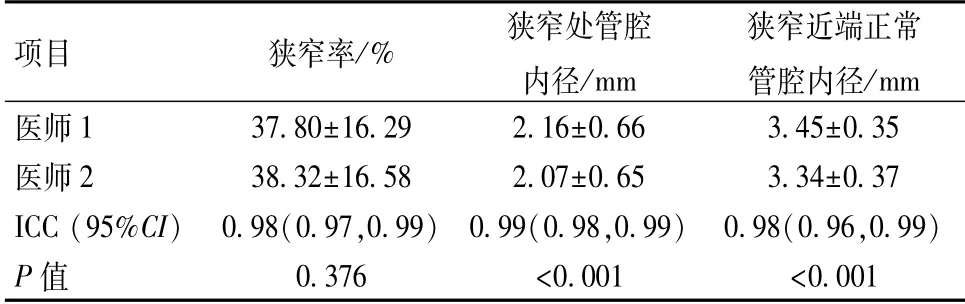
表2 观察者间52例MR图像测量结果()
项目 狭窄率/% 狭窄处管腔内径/mm狭窄近端正常管腔内径/mm医师1 37.80±16.29 2.16±0.66 3.45±0.35医师2 38.32±16.58 2.07±0.65 3.34±0.37 ICC(95%CI) 0.98(0.97,0.99)0.99(0.98,0.99) 0.98(0.96,0.99)P值 0.376 <0.001 <0.001

图2 观察者间MR测量狭窄率一致性的Bland-Altman图
(2)MR-DSA图像对比分析 由于Bland-Altman图提示两名放射科医师的MR诊断结果一致性高,经医师1、2共同评定后,选取放射科医师1的诊断结果为最终结果与DSA测量结果进行最终分析。在3D T1-SPACE图像中测得的基底动脉狭窄率为(37.80±16.29)%,稍大于DSA上测得的狭窄率(37.06±16.17)%,但二者比较,差异无统计学意义(P=0.11)。两种成像方法的测量结果具有强相关性(r=0.979,P<0.001)(图3)。两种成像方法结果的观察者间信度高(ICC=0.99,95%CI:0.98~0.99,P<0.001)。Bland-Altman图(图4)提示3D T1-SPACE测得的基底动脉狭窄率略大于DSA的狭窄率,狭窄率差值均数为0.11,94.2%的点分布于一致性区间范围之内,两种成像方法对于狭窄测量具有高一致性。DSA共发现24根血管存在重度狭窄,3D T1-SPACE图像中发现22根重度狭窄的基底动脉。以DSA为金标准,3D T1-SPACE诊断基底动脉重度狭窄的一致率、灵敏度、特异度、阳性似然比、阴性似然比、阳性预测值和阴性预测值见表4。

图3 MR和DSA基底动脉狭窄率直线相关图
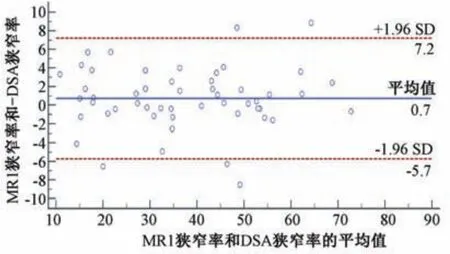
图4 MR和DSA基底动脉狭窄率一致性的Bland-Altman图
表3 52例MR与DSA测量结果比较()
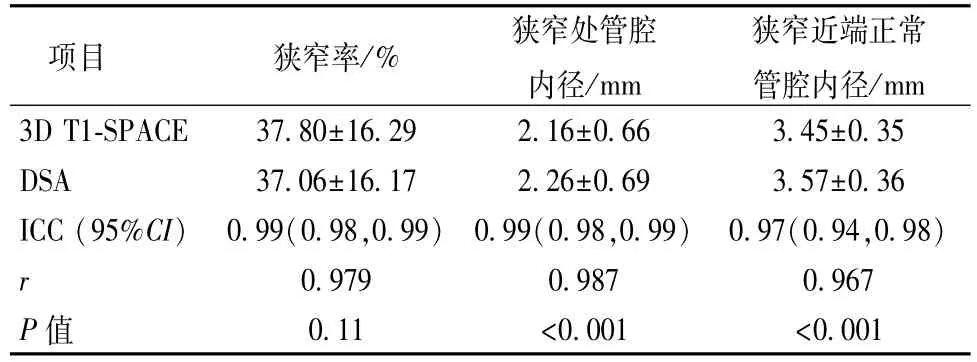
表3 52例MR与DSA测量结果比较()
项目 狭窄率/% 狭窄处管腔内径/mm狭窄近端正常管腔内径/mm 3D T1-SPACE 37.80±16.29 2.16±0.66 3.45±0.35 DSA 37.06±16.17 2.26±0.69 3.57±0.36 ICC(95%CI) 0.99(0.98,0.99)0.99(0.98,0.99) 0.97(0.94,0.98)r 0.979 0.987 0.967 P值 0.11 <0.001 <0.001

表4 3D T1-SPACE诊断基底动脉重度狭窄与DSA的对比结果
讨论
本研究首次评估了3D T1-SPACE技术对基底动脉狭窄病变的诊断价值。对比3D T1-SPACE与DSA测量结果,3D T1-SPACE对基底动脉重度狭窄病变的诊断具有高一致率(92.3%)、灵敏度(87.5%)及特异度(96.4%)。Bland-Altman图认为二种成像方法分别测得的基底动脉狭窄率具有高一致性。提示3D T1-SPACE成像可以实现基底动脉狭窄病变的准确、无创、定性和定量的综合分析。
DSA被认为是诊断颅颈动脉血管狭窄的金标准[13-14],但是该项检查存在有创、过敏、电离辐射暴露、价格昂贵、一过性神经功能障碍等诸多不足[15-16],不适用血管狭窄患者的常规筛查和对比剂过敏患者。三维时间飞跃法磁共振血管成像(3D time of flight MRA,3D TOF MRA)是一种无创快速磁共振血管成像技术,目前已被广泛应用于颅颈部血管狭窄疾病的诊断[17-19]。石光等[20]使用3D TOF MRA和DSA对基底动脉狭窄病变进行联合评估,其结果表明3D TOF MRA对基底动脉狭窄的诊断具有较高的灵敏度(94.3%)和特异度(85.7%)。两种成像方式对于狭窄率的检测结果具有良好的相关性(r=0.985)。既往研究认为[21-23],3D TOF MRA对血管狭窄常存在过度诊断,可能的原因有:基底动脉等颅颈部血管管径纤细,MRA空间分辨率低,对于重度狭窄的病变细节难以清晰显示;扫描技师触发信号不当导致靶血管内对比剂充盈欠佳或对比剂过度充盈致使静脉血流逆灌注、目标血管信噪比低,与本底对比度差,从而无法实现病变处形态学信息的准确测量。并且,MRA无法进行管壁成像,对于斑块成分等详细信息无法正确评价。
本研究使用3D T1-SPACE技术采用非选择脉冲和变角度回聚脉冲进行联合黑血管壁成像,通过并行采集和K空间重排扩大图像自由度,从而大幅度提升扫描速度及图像质量[6-7]。此外,3D T1-SPACE图像层厚仅为0.625 mm,0mm层间距进行扫描,图像层面内分辨率达0.625 mm×0.625 mm,实现各向同性分辨率,明显减轻图像部分容积效应,从而更为精细地展示病变特征。此外,3D T1-SPACE技术对管壁病变清晰显示,弥补了MRA无法评价管壁病变的不足,实现对管腔、管壁病变的全面评估,对患者卒中发生风险作出正确预测,指导临床实施正确治疗方案。本研究认为3D T1-SPACE比DSA测得的基底动脉狭窄率略高,但二者相比并无统计学差异。并且Bland-Altman图显示,二种成像方式间狭窄测量差值均数小,仅为0.11。94.23%(49/52)的点分布于95%一致性区间之内,提示两种成像方式测量结果具有高一致性。值得注意的是,3D T1-SPACE作为3D成像序列可实现任意方向的图像重建,便于多角度观察病灶特征,较传统2D黑血管壁检查节约了扫描时间、提高了实际成像效率、改善患者检查舒适度[24-25],并且该序列成像范围广,可覆盖颈总动脉远端至大脑前动脉胼周段水平间全部颅颈段血管[26],有助于整体评价患者病变程度,制定个性化诊治策略。
本研究不足之处主要包括以下两点:第一,入组研究样本量较少且仅为单中心数据;第二,3D T1-SPACE技术可获得基底动脉管壁的高分辨影像,但因缺乏相应病理对照,本研究未对管壁斑块成分行进一步分析,后续有关斑块成分与临床症状的相关性研究将逐步开展。
综上所述,3D T1-SPACE技术对基底动脉病变诊断的准确性强、价值高,是一种安全可靠的无创影像学评价方法,可作为诊断基底动脉狭窄的常规筛查工具。
