甲醇转化制丙烯反应机理
2019-05-21贺振富
贺振富
(国家能源集团公司, 北京 100011)
目前,煤基甲醇反应制丙烯(MTP)技术在我国已经实现了工业化[1-3],具有良好经济效益,走在世界前沿,但反应机理研究一直滞后。甲醇制烯烃(MTO)反应机理较复杂,在30多年里,研究提出了20多种不同的反应机理,归纳起来可以分为串联型机理和并联型机理两大类。
串联型机理认为乙烯是首先生成的产物,但在SAPO-34上发生的MTO反应初期通常是丙烯含量高于乙烯[4]。并联型机理中,Dahl和Koboe[5-6]提出烃池机理认为,在催化剂上首先形成大相对分子质量的烃类物质并吸附在催化剂孔道内,一方面这些物质作为活性中心不断与甲醇反应引入甲基基团,另一方面这些活性中心不断进行脱烷基化反应,生成乙烯和丙烯等低碳烯烃分子。目前,“烃池”机理已经得到了普遍认可[7-8],烃池机理提到了B酸中心在MTO反应过程中的作用。严志敏[9]认为,在反应过程中B酸中心直接参与了中间物种生成,但没有对反应物与B酸中心相互作用及生产的中间物种作出进一步说明。
碳烯离子机理[10]指出,在沸石催化剂酸、碱中心的协调作用下,甲醇经α-消除反应脱水得到碳烯[CH2],碳烯含有1个电中性的二价碳原子,在这个C原子上有2个未成键的e-,然后通过碳烯聚合或者碳烯插入甲醇或二甲醚分子中即可形成烯烃,但没有进一步研究甲醇分子与分子筛B酸中心相互作用。Li等[11]在MTO反应过程中观察到了中间体七甲基苯基碳正离子(heptaMB+)及其去质子化产物(HMMC),验证了该中间体在甲醇转化中的重要作用和以此碳正离子作为中间体的烯烃生成途径。Wu等[12-13]研究了甲醇在SAPO-34上转化反应中二甲醚(DME)/甲醇与表面甲氧基物种(SMS)之间的关系,认为初始C-C键是由表面C1反应物、DME/甲醇和SMS直接反应形成,一旦形成初始烯烃,它们将转化为大分子的烃,烯烃生成的反应路径是表面甲氧基/三甲基氧离子协助DME/甲醇活化转化的协同反应机理。上述研究未能真实反映出催化剂与反应物之间相互作用。
笔者利用杂化轨道理论和含Si、Al元素固体酸催化剂酸中心研究方面的认识,研究甲醇分子与催化剂B酸中心相互作用,揭示甲醇制烯烃反应机理本质。深入研究甲醇催化转化制丙烯反应机理,对于甲醇催化转化制丙烯催化材料设计,提高催化反应转化率及选择性具有重要意义。
1 6配位B酸中心H3AlO6的形成
SAPO-34或ZSM-5分子筛是含Si、Al元素固体酸催化剂,其催化活性来源于其酸性,而酸性取决于Al原子的O原子配位数,2、3配位的Al原子形成L酸中心,4、5或6配位的Al原子形成B酸中心[14-15]。根据前面文献分析,下面就以6配位B酸中心为例,研究甲醇在B酸中心作用下反应生成烯烃的机理。
6配位B酸中心H3AlO6是由1个Al原子、6个 O原子和3个H原子组成,其结构式为H3AlO6。按照杂化轨道理论分析,Al原子外层有6个 sp3d2杂化轨道,其中3个轨道上都有1个未成键e-,剩余3个轨道为空轨道;H原子的s轨道有1个e-;O原子外层有4个sp3杂化轨道,其中2个轨道上各有1个未成键e-,另外2个轨道各有1对成键e-对,详细结构见图1(a)和图1(b)。


图1 6配位B酸中心形成与失活Fig.1 6-Coordinate B-acid center formation and inactivation(a) Hydrogen atom and aluminum atom outer orbit; (b)Oxygen sp3 hybrid orbit; (c) H3AlO6;
2 反应机理分析
甲醇反应生成丙烯的反应方程式如下:
3CH3OH→C3H6+3H2O
(1)
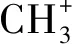
2.1 甲基碳正离子的生成
图2为H+离子攻击甲醇分子中C-O键生成甲基碳正离子的电子轨道变化示意图。图2(a)中,C原子4个未成键sp3杂化轨道分别与3个H原子s轨道和O原子1个未成键sp3杂化轨道重叠形成3个C-H键、1个C-O键,O原子的另1个未成键sp3杂化轨道和第4个H原子s轨道重叠形成1个 O-H键,则1个C原子、1个O原子和4个H原子形成甲醇分子,如图2(b)所示。图2(b)中,甲醇分子C-O键受到6配位B酸中心释放的H+攻击并相互作用,形成C、O和H三原子外层电子轨道重叠且共用1对e-结构,如图2(c)。


图2 H+离子攻击甲醇分子中C-O键生成甲基碳正离子Fig.2 H+ attack C-O bond in methanol molecule to form methyl carbocation(a) Atoms outer layer orbit; (b) CH3OH; (c) CH3-HOH; (d) (e) H2O
2.2 中间体H-form的生成
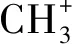
目前,通过实验方法还不能捕获中间体H-form C↑↓〇H2,中间体H-form C↑↓〇H2不同于碳烯[CH2],碳烯[CH2]含有1个电中性的二价C原子,在这个C原子上有2个未成键的e-,而中间体H-form C↑↓〇H2结构中C原子外层有1个空轨道和1对孤对e-,C↑↓〇H2是构成烯烃和二甲醚基本结构单元。

图与失活6配位B酸中心作用生成H-form C↑↓〇H2Fig.3 Methyl carbocation interacts with the inactive 6-coordinate B-acid center to generate H-form C↑↓〇H2(a) (b) (c) CH3-AlO6(CH3)2; (d) CH2-H3AlO6(CH2)2; (e) H3AlO6; (f) H-form C↑↓〇H2
2.3 中间体H-form C↑↓〇H2生成丙烯
图4中有3个C↑↓〇H2结构C原子,第1个C原子上的孤对e-占据第2个C原子上空轨道,第2个C原子上的孤对e-占据第1个C原子上空轨道,这2个C原子共用2对e-结构形成了C=C键结构;当第3个C原子外层空轨道和第1个C原子外层C、H原子重叠轨道再次重叠,且第1个C原子上H+转移到相邻的第3个C原子外层孤对e-所在轨道上,则第1个C原子与第3个C原子共用1对e-,形成了C-C键,那么3个C↑↓〇H2结构C原子形成C=C-C结构,即生成丙烯CH2=CH-CH3。
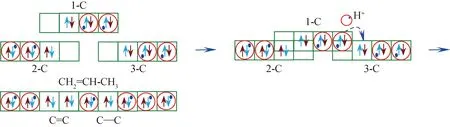
图4 中间体H-form C↑↓〇H2生成丙烯Fig.4 Intermediate product H-form C↑↓〇H2 generates propylene
2.4 反应机理分析
由上述分析可知,甲醇在6配位B酸中心H3AlO6作用下反应过程如下:
(2)
(3)
(4)
反应方程式(2)、(3)和(4)相加得到反应方程式(1)。因此可知,甲醇分子在6配位B酸中心H3AlO6作用下生成丙烯的反应过程可分为3步:
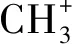
(3)3个H-form有3个C↑↓〇H2结构的C原子,通过构成C=C键、C-C键和H+转移过程,形成了C=C-C结构,即生成丙烯。
3 结 论

(2)甲醇制丙烯反应的催化剂只要存在B酸中心、能够提供H+就可满足要求,催化剂B酸中心的配位结构对反应无影响。
