急性脑梗死患者全身炎性反应综合征的发生率相关危险因素及对患者预后的影响
2019-05-20蒋玉侠
蒋玉侠
商丘市中心医院神经内科,河南 商丘 476000
急性脑梗死(acute cerebral infarction,ACI)是临床常见脑血管疾病,起病突然,且具有较高发病率、致残率及病死率,是目前威胁人们身心健康的重要疾病之一。全身炎性反应综合征(systemic inflamma-tory response syndrome,SIRS)是近年研究的一项热点,机体内抗炎-促炎自稳失衡所引起的、持续不受控且伴免疫防御功能下降的炎症反应为其基本病理变化[1-6]。ACI患者易并发多脏器功能障碍综合征,进一步对其生命安全造成威胁,而临床研究发现,SIRS是多脏器功能障碍综合征的初始阶段,故早期预防、发现SIRS,及时给予有效干预,对降低多脏器功能障碍综合征发生率,改善ACI预后至关重要[7-13]。本研究选取商丘市中心医院收治的224例ACI患者,探讨ACI患者SIRS的发生率、相关危险因素及对患者预后的影响。
1 资料与方法
1.1一般资料抽取2013-01—2016-10商丘市中心医院收治的224例ACI患者,男131例,女93例,年龄49~87(67.58±17.54)岁;其中53例发生SIRS,设为观察组,将171例未发生SIRS的ACI患者设为对照组。SIRS诊断要点[14]:体温<36 ℃或>38 ℃;二氧化碳分压<32 mmHg或呼吸>20次/min;心率>90次/min;未成熟粒细胞>10%或白细胞计数<4×109个/L或>4×109个/L,具备上述2项及以上指标可确诊为SIRS。
1.2纳入及排除标准(1)纳入标准:均符合《各类脑血管疾病诊断要点》中ACI相关诊断标准[15];对本研究知情同意。(2)排除标准:合并严重免疫系统、血液系统疾病;发病24 h内病死;短暂性脑缺血发作。
1.3研究方法(1)记录2组患者性别、年龄、并发症(高血压、糖尿病)发生情况;(2)均抽取静脉血3 mL,3 000 r/min离心20 min,取上层血清送检,以氧化酶法检测TC,酶法检测TG及LDL-C,直接法检测HDL-C,采用酶联免疫吸附法检测CRP;采用血糖分析仪检测FBG水平;(3)以采用美国国立卫生研究院卒中量表(NIHSS)[16]对2组入院时神经功能缺损程度进行评估,分值越高则神经功能缺损越严重;(4)随访3个月,以改良Rankin量表(mRS)[17]对2组预后进行评估,完全没有症状(0分);轻微症状,未见明显残疾(1分);轻度残疾(2分);中度残疾(3分);重度残疾(4分);植物生存(5分);死亡(6分)。统计2组病死率。

2 结果
2.1SIRS危险因素单因素分析观察组年龄、入院时NIHSS评分、FBG、CRP水平均高于对照组,差异有统计学意义(P<0.05),2组性别、并发症、TC、TG、LDL-C、HDL-C水平差异无统计学意义(P>0.05)。见表1。
2.2SIRS危险因素Logistic多因素回归分析Logistic检验可知,入院时NIHSS评分、FBG、CRP水平均为ACI发生SIRS的高危因素(P<0.05)。见表2。
2.32组预后比较随访3个月后,观察组mRS评分高于对照组,且病死率30.19%(16/53)高于对照组8.77%(15/171),差异有统计学意义(P<0.05)。见表3。

表1 SIRS危险因素单因素分析
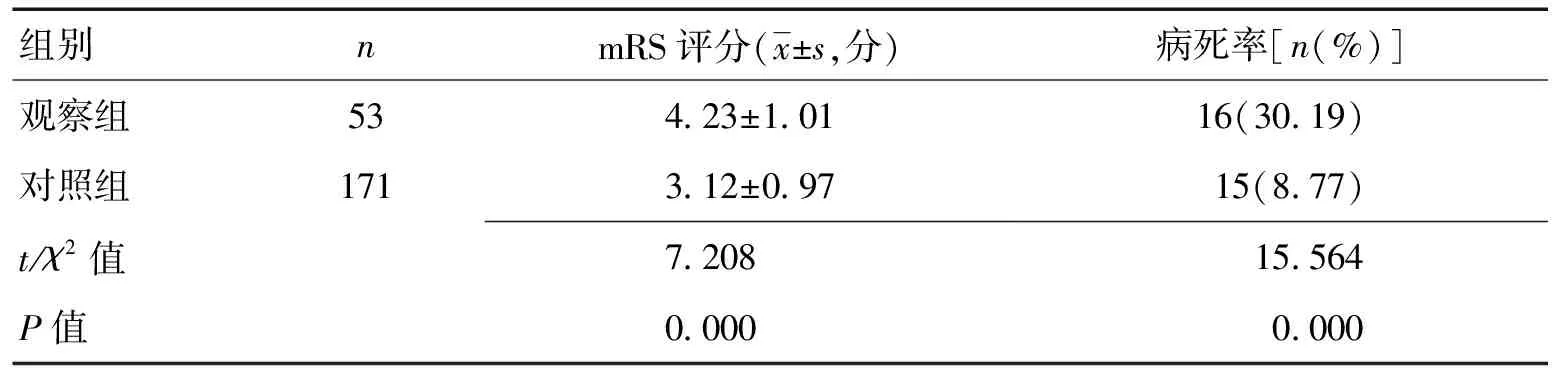
表3 2组预后情况比较
3 讨论
ACI是临床常见脑卒中类型,可占全部脑卒中60%~80%,随近年我国老龄人口增多、生活方式及饮食习惯改变,ACI发病率仍呈不断上升趋势,且发病年龄日渐年轻化,严重威胁着中老年群体身心健康[18-25]。SIRS是机体受到感染或非感染因素打击造成炎性细胞激活而产生的失控性全身炎性反应,也是ACI患者并发多脏器功能障碍综合征的初始阶段[26-33]。
本研究中,SIRS发生率达23.66%,提示SIRS具有较高发生率。大量炎性介质释放可对机体造成二次打击,进一步威胁ACI患者生命安全,故SIRS防治成为改善ACI预后的重要措施[34-39]。目前,已有学者开展对SIRS发生相关危险因素的研究,并取得初步成果[40-48]。本研究结果显示,观察组年龄、入院时NIHSS评分、FBG、CRP水平均高于对照组(P<0.05),且经Logistic多因素回归分析,提示入院时NIHSS评分、FBG、CRP水平为ACI发生SIRS的高危因素(P<0.05),其中年龄属不可干预因素,随患者年龄增加,机体各项生理功能呈退行性变化,衰老所引起的生理改变为不可逆的自然过程[49-56]。入院时NIHSS评分能够对ACI患者病情、神经功能缺损程度进行较好的评估。相关研究发现,NIHSS评分越高,则ACI患者脑梗死面积通常越大,组织水肿越为严重,进而致使周围血管受压,导致血管内皮细胞发生缺血、缺氧性坏死,血管内皮功能受损[57-62]。进而导致大量纤溶酶原抑制剂自动脉血管内皮细胞产生,诱发SIRS,提示入院时NIHSS评分越高则发生SIRS风险越大[63-69]。FBG较高是引发SIRS的又一重要危险因素,数据显示,40%左右患者在发生ACI后出现高血糖,主要原因为发病后交感神经系统被激活,儿茶酚胺过度释放致使血糖应激性升高[70-73]。高血糖状态下造成脑血管源性水肿,脑血流量随之降低,神经细胞葡萄糖无氧酵解增加,致使细胞内乳酸水平显著升高,进一步促使神经细胞损伤增加。此外,血糖应激性升高引起胰岛素分泌及胰岛素抵抗障碍,促进白细胞介素-6、肿瘤坏死细胞因子-α及CRP等炎性细胞因子大量释放,诱发无法控制的炎性反应[71,74-75]。CRP是机体发生急性炎症时而出现的一种非特异性应激蛋白,感染、创伤等均可使其水平显著上升。CRP能够将补体系统激活,诱导单核细胞大量释放多种炎性介质,并对血管内皮细胞造成损伤,进而产生大量纤溶酶原抑制剂,最终导致ACI患者发生SIRS。此外,研究结果还显示,随访3个月后mRS评分及病死率均高于对照组(P<0.05),提示SIRS是影响ACI患者预后的重要原因。早期对患者神经缺损程度进行准确评估,积极采取控制血糖、减轻炎症反应的治疗与干预措施,有利于降低SIRS发生风险,对改善ACI患者预后具有重要意义。
SIRS具有较高发生率,且合并SIRS患者预后较差,其中入院时NIHSS评分、FBG、CRP水平为ACI发生SIRS的高危因素。
