辐射诱导细胞衰老的机制研究进展
2019-05-16尚书英王建林邵宝平
尚书英,王建林,邵宝平
(兰州大学生命科学学院,中国甘肃兰州730000)
人类可能因治疗、诊断、职业和意外事故而暴露在辐射中。辐射会对活细胞和组织造成损伤,这种损伤程度取决于辐射剂量、辐射时间、辐射后的时间间隔以及各个系统对辐射的敏感性等因素。由于辐射被认为是最重要的生物效应,因此该领域的研究主要集中于辐射对DNA的影响[1]。研究表明辐射对人体的损伤主要表现在两方面,一是直接作用:辐射释放的能量直接作用于生物大分子,使DNA受损断裂为单链或双链;二是间接作用:辐射引起原子和分子的电离和激发,导致自由基大量产生,破坏生物大分子,从而活化细胞内的信号分子或激活细胞信号通路,最终导致细胞生物学行为改变[2]。有研究发现辐射会引起大脑的学习和记忆功能受损,其损伤机制可能是突触结构受损[3]。对神经元突触的可塑性研究发现,辐射可引起脑功能和组织结构发生改变,使突触结构受损、神经元变性、神经递质代谢出现紊乱[4]。辐射会致使DNA损伤积累以及DNA修复效率降低,最终出现细胞衰老或凋亡[5]。近年来,有关辐射引起细胞衰老的机制研究少有报道,但有研究发现暴露在电离辐射中容易引起阿尔茨海默病等相关的神经退行性疾病[6]。因此,研究辐射诱导细胞衰老的机制可为相关神经退行性疾病的诊疗提供一定的理论指导。
辐射会导致细胞产生活性氧(reactive oxygen species,ROS),从而对DNA、蛋白质、脂质的结构和功能造成损伤[7],引起代谢和功能的改变,最终导致细胞衰老或凋亡。在生物大分子中,DNA被认为是辐射诱导细胞损伤最关键的分子靶点。辐射致使DNA双链断裂(double-strand breaks,DSBs),DSBs有效地触发一系列细胞反应,即DNA损伤反应,为了确保快速检测和修复DSBs,机体会启动衰老或凋亡程序清除受损的DNA。辐射诱导细胞衰老伴随着一系列特征,其中包括β-半乳糖苷酶(senescence-associated β-galactosidase,SA-β-gal)阳性表达量增加、活性氧含量增加、细胞周期相关蛋白(RB、p53、p21等)和一些表型分泌因子(IL-8、IL-12 等)表达量的增加(图 1)。其涉及的衰老机制复杂,关联许多信号通路。但无论通过哪条通路激活,诱导细胞衰老的信号最终都由p53-p21通路和p16-RB通路执行。此外,最新研究报道,miRNAs也参与细胞衰老的复杂调控。
1 p53-p21信号通路
辐射通过线粒体或细胞膜上的NADPH氧化酶(NADPH oxidases)增加细胞内ROS的水平,进而通过ATM/CHK2-p53-p21通路诱导细胞衰老[8]。DSBs由变性共济失调(ataxia telangiectasia mutated,ATM)识别,其依赖于DNA损伤应答(DNA damage response,DDR)功能来调节体内氧化应激,被认为是细胞衰老的驱动因素[9~10]。DDR包括激活传感器激酶如ATM和ATR,形成DNA损伤位点,如组蛋白变异体H2A.X(γH2A.X)、p53结合蛋白(53BP1)和其他的DNA损伤灶,激活细胞周期检查点如p53蛋白。p53对细胞周期G1监测点的调控主要由p21介导,细胞衰老与细胞周期阻滞密切相关。有研究表明,在p21缺失的人微血管内皮细胞中可以阻止由RAS诱导的细胞衰老[11]。而活化p21可抑制周期蛋白依赖性激酶2(cyclin-dependent protein kinase 2,CDK2)与周期蛋白E(cyclin E)复合物的结合,进一步抑制视网膜母细胞瘤(retinoblastoma,RB)的磷酸化。细胞周期由G1期向S期的转化依赖于RB的超磷酸化,而RB的低磷酸化会抑制性地结合E2F转录因子,最终导致细胞周期阻滞[12~13]。有人在研究辐射诱导内皮细胞衰老时发现,用ATM抑制剂处理细胞,p53和MDM2的表达受到抑制,而且该抑制剂对p21的表达也有一定的抑制作用;当用抗氧化剂处理辐射后的细胞时发现衰老细胞明显减少[14]。该结果表明辐射诱导的细胞衰老主要是由于ROS的产生进一步激活了p53-p21信号通路。
2 p16-RB信号通路
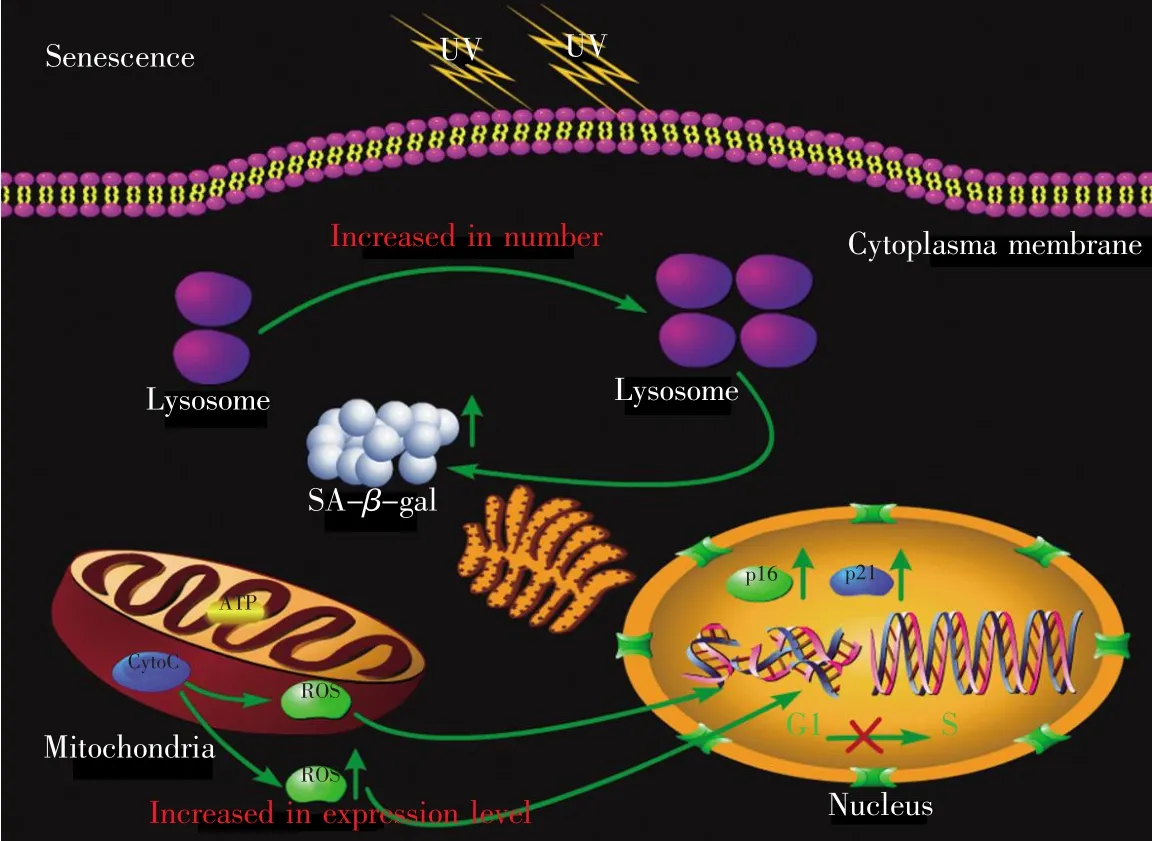
图1 细胞衰老的标记物特征Fig.1 The biomarkers of senescence
辐射会导致细胞内p16表达上升[15],进而调节pRB-E2F通路。目前发现p16基因主要通过两条途径起调控作用:一条是表达p16蛋白,这条途径主要通过抑制细胞增殖进程的p16-cyclinDCDK4/CDK6-RB通路发挥作用;另一条是p16基因的可变读框(alterative reading frame,ARF),其转录为p14ARF蛋白(ARF在鼠细胞中为p19ARF),通过激活p53-p21通路使细胞停滞在G1期和G2期[16]。p16又被称为周期蛋白依赖性激酶抑制因子1,是CDK4和CDK6等周期蛋白依赖性激酶的抑制剂。p16被激活会导致视网膜母细胞瘤的磷酸化(pRB)失活,处于低磷酸化形式的RB与转录因子E2F结合,进而控制细胞的周期进程[17~18]。细胞周期阻滞通过RB家族(pRB、p107和p130)和细胞核中的E2F结合而形成。此外,研究表明p16-RB通路与促分裂原活化的蛋白激酶(mitogen activatedprotein kinase,MAPK)协同诱导活性氧的产生,进而激活蛋白激酶C(protein kinase C,PKC),而后者又可反过来促进ROS的产生,这导致ROS与PKC之间形成正反馈环,进一步使细胞周期阻滞。在MAPK信号通路中,p38对p16的调节是由HMG转录因子HBP1(HMG-box transcription factor 1)介导的[19]。HBP1是一个细胞调控因子,研究表明HBP1作为转录抑制因子参与细胞周期调控和肿瘤抑制[20]。p38信号通路被激活后会引起下游HBP1与其特异性位点结合,使HBP1磷酸化,导致细胞周期G1期停滞[21]。之前的研究发现,不管在体内还是体外,造血干细胞暴露于电离辐射中会衰老,且其中的p38、p16表达水平以及ROS含量都会升高[22]。近期,有关电离辐射诱导神经干细胞衰老的研究发现,细胞每隔3代接受高剂量辐射处理后,其衰老程度加剧,且衰老相关基因(p16、Bim1)也明显增加[23]。在接受全脑放射治疗的患者中,人们发现照射后的原代血管内皮细胞出现了早衰的现象,且获得衰老相关的分泌表型,即促炎因子和趋化因子上调,这些微环境的变化进一步影响神经元的生物学功能[24]。
3 miRNAs参与辐射诱导细胞衰老的调控
miRNAs作为一种调控因子,在细胞衰老以及衰老相关的疾病中起重要作用。外界环境的刺激会改变miRNAs的表达水平,其涉及的机制可能与染色质重塑和DNA甲基化有关。辐射后差异表达的miRNAs可调节细胞内在的辐射敏感性,特别是辐射的遗传反应机制。大鼠辐射两周后血清中 miR-144-5p、miR-144-3p、miR-142-5p 和miR-19a-3p的表达水平明显上调,但这些miRNAs在辐射后的肺中未检测到[25];miR-96-5p和miR-873-3p参与辐射过程中产生DNA双链断裂的靶基因的调控[26]。有研究报道辐射诱导人非小细胞肺癌细胞的早衰与miRNA-34a的表达有关,而且miR-34a对细胞衰老的影响与c-myc的表达水平显著下调有关,沉默c-myc会增加miR-34a的表达,表明在辐射诱导的衰老中miR-34a的功能可能与靶向调控Myc有关[27]。在辐射处理的人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)中,过表达miR-494或miR-99b会增加SA-β-gal的表达,增加G1期阻滞,同时出现组蛋白H2AX的磷酸化以及RB低磷酸化。相反,抑制miR-494或miR-99b会降低SA-β-gal,降低G2期阻滞,激活caspase-3和caspase-7。这些结果表明miR-494或miR-99b会影响辐射引起的细胞衰老[28]。在辐射引起的人成纤维细胞老化中,沉默信息调节因子4(silence information regulator-4,Sirt4)的表达明显增加,而Sirt4表达水平的上调与miRNA-15b水平的降低有关。miR-15b的抑制会使细胞内产生过量的ROS以及衰老相关的分泌表型(senescence-associated secretory phenotype,SASP)[29~30]。
近年来人们相继报道了一些参与辐射诱导衰老的miRNAs。例如:Bae等[31]通过生物信息学分析得出mmu-miR-291a-3p是一种抗衰老因子,用小鼠胚胎干细胞分泌的mmu-miR-291a-3p处理衰老细胞,发现衰老细胞中SA-β-gal的表达降低,细胞的增殖潜力增强,同时p53、p21的mRNAs和蛋白质表达水平降低。此外,有研究表明miRNAs在p53-p21和p16-pRB通路中特异性过表达或下调,对细胞衰老起重要的调控作用[32],相关机制如图2所示。miR-34是肿瘤抑制子和衰老的触发蛋白[33~34],文中以miR-34a为例进行简要说明。在辐射处理的小鼠中,miR-34a参与p53介导的肿瘤抑制作用。miR-34a过表达会激活p53-p21通路,下调E2F的表达,抑制细胞增殖,诱导细胞出现衰老相关表型[35]。而且,miR-34也可以直接抑制Sirt1的表达,进而促进p21的表达,阻滞细胞周期进程,进一步加速细胞衰老[36]。
4 总结与展望
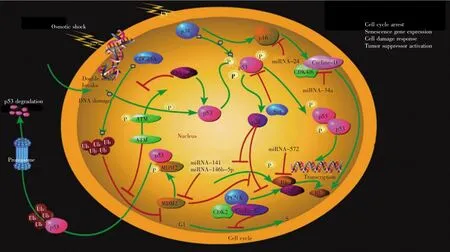
图2 细胞衰老信号通路Fig.2 Cell senescence signaling pathway
辐射导致的细胞衰老主要有3个原因:第一,由于体内氧自由基的大量产生,从而出现脂质过氧化,使DNA受损;第二,衰老的两条信号通过p53-p21和p16-RB被激活,使细胞停滞在G1期或G2期;第三,miRNAs对细胞的衰老也起到一定的调控作用。近年来,以p53-p21和p16-RB这两条信号通路为突破点,寻找有效治疗辐射诱导细胞衰老的靶点被不断报道,但以miRNAs作为治疗靶点预防正常组织的辐射损伤仍有待研究。尽管相关研究取得了很大的突破,但仍有许多问题尚未解决,比如:miR-34a在促进细胞衰老的同时也会直接抑制Sirt1的表达[37~38],因此我们并不能认为miR-34a具有促进衰老的作用,这可能与miRNAs靶向调控多个基因有关。由于miRNAs功能作用的复杂性,目前尚无法判断miRNAs作用的具体靶点,只有探索出miRNAs与靶基因之间的相互作用,不断完善RNA的研究技术,miRNAs的研究成果才能在医疗上得到一定的应用。
