纳微结构Ag2CO3光催化材料的制备及其在光催化的应用
2019-05-10张萌迪陈范云马小帅杨凯余长林
张萌迪, 陈范云, 马小帅, 杨凯, 余长林
(江西理工大学冶金与化学工程学院,江西 赣州341000)
随着工业化和城市化程度加大以及人口急剧增长,清洁水源的需求变得越来越迫切[1-2].由于污染物不断大量排放到自然水循环中,水污染日益严重.因此,废水的再利用和再循环十分必要[3-6].在过去的几十年里,各种不同的废水处理技术不断被开发出来,如化学反应、吸附和微生物代谢等.然而,这些传统的有机废水处理技术通常会带来二次污染或者很难实现有机污染物的高效和深度处理.
光催化是一种通过光触发实现化学反应的高级氧化技术.光催化降解有机污染物可以克服传统化学氧化降解不彻底、易产生中间产物的缺点,具有较强的深度净化能力,被认为是未来水体污染物处理的绿色化学技术[7-26].光催化可以利用太阳光,在固体光催化剂的作用下去除水中的有机污染物和有害细菌.光催化处理水体有机污染物的关键是开发高效、廉价的光催化剂.Ag2CO3半导体的禁带宽度窄、能强烈吸收可见光,在可见光下通常表现出良好的光催化活性,同时具有很强的抗菌性.因此Ag2CO3光催化剂成为近年来光催化的研究热点[27-34].
1 Ag2CO3半导体的结构及光催化特征
Ag2CO3的带隙能约为2.50 eV,计算出Ag2CO3光催化剂所需要的入射光最大的波长为496 nm,因此Ag2CO3可被可见光激发,能很好地利用太阳光中的可见光部分.在可见光照射下,Ag2CO3晶体对多种染料(罗丹明 B(RhB) 、亚甲基蓝(MB)、甲基橙(MO))和苯酚等有机污染物具有高效的降解能力[35].然而,在光催化反应过程中,随着反应时间的延长,Ag2CO3晶体中的Ag+会被自身的光生电子(e-)还原形成金属Ag单质,Ag2CO3表面会被Ag单质所覆盖,发生光腐蚀而迅速失去活性.因此,在Ag2CO3的光催化反应过程中,通常需要牺牲试剂,如Na2CO3和AgNO3等延长它的使用时间.Ag2CO3的易光腐蚀性[36]阻碍了其广泛使用.
Ag2CO3光催化剂的光催化反应过程如图1所示.
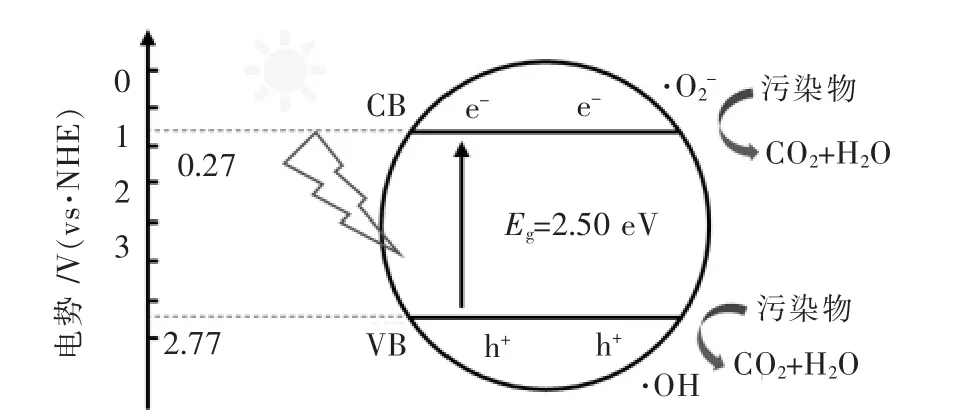
图1 Ag2CO3晶体的能级结构和光催化过程示意Fig.1 Energy band structure and photocatalytic reaction process of Ag2CO3
2 Ag2CO3光催化剂的性能改进
光催化剂的形貌、金属沉积/非金属掺杂、晶体结构、表面性能以及异质结修饰等[37-47]对半导体的光催化性能影响很大.解决Ag2CO3不稳定和易光腐蚀的问题,提高Ag2CO3光催化剂的实际应用性能是其研究重点.各种研究表明,控制Ag2CO3半导体催化剂的形貌、晶体尺寸和比表面积等物理性能可以有效地提高Ag2CO3稳定性和光催化性能;同时贵金属沉积、非金属元素掺杂、半导体复合构建异质结也是提高其光催化活性有效的方法.
2.1 Ag2CO3的形貌和粒径控制
Xu等[48]利用AgNO3和Na2CO3通过沉淀法制备了碳酸银(Ag2CO3)微米棒,形貌如图 2(a)所示.研究表明,在可见光照射下,Ag2CO3微米棒对于亚甲基蓝(MB)和苯酚的降解显示出高度光催化活性.光催化过程中,总有机碳含量 (TOC)下降,表明苯酚被Ag2CO3真正的降解和矿化.通过向悬浮液中加入Na2CO3,Ag2CO3的稳定性得到大幅度提高.此外,Ag2CO3对于抑制大肠杆菌也显示出很强的光催化活性.
Zhou等[49]通过一种简单的超声波化学方法(室温下反应仅 1 h)合成了粒径为 0.5 μm左右的Ag2CO3纳米粒子,如图2(b)所示.他们研究了超声波脉冲模式、超声波时间和pH值对Ag2CO3光降解性能的影响.在可见光照射下(420 nm),通过降解亚甲基蓝(MB)来测试其光催化活性.结果发现,与传统的搅拌方法制备的Ag2CO3相比,超声波法制备的Ag2CO3对MB的降解率大幅度提升.从图2(b)中可以清楚地观察到超声波合成法得到了均匀的小尺寸Ag2CO3纳米颗粒,而传统搅拌形成的Ag2CO3为微米棒.测定样品的比表面积(BET)发现,超声波法制备的样品的比表面积为5.265 m2/g,大于沉淀法制备样品的比表面积 (2.166 m2/g),并且超声法制备的Ag2CO3显示出多孔结构.上述结果表明,在不使用任何表面活性剂或模板的情况下,超声波法能合成粒径更细、尺寸更均匀的Ag2CO3纳米粒子,显示出更高的光催化活性.
Davor等[3]以 AgNO3和 NaHCO3为原料,利用PVP-K40表面活性剂辅助化学沉淀法合成了更细、更长的棒状Ag2CO3晶体,如图 2(c)所示,相比于不加表面活性剂制备的Ag2CO3来说,具有更规则的棒状形貌和更高的光催化活性.Ag2CO3样品的低倍和高倍的FESEM分析表明,PVP-K40存在下所获得的Ag2CO3是由大小非常均匀的六角形多面体状粒子组成的,每一种纳米棒都是由许多纳米晶体颗粒组装而成的,同时具有更大的比表面积.

图2 不同方法制备的Ag2CO3的扫描电镜像Fig.2 SEM images of Ag2CO3obtained using different methods
2.2 贵金属沉积
Yu等[50]采用一种简单的一锅法,大量合成了一种具有高长径比的Ag/Ag2CO3一维非均匀结构.光催化结果表明,在可见光下,它们具有良好的光活性和稳定性.其详细合成过程为:室温下,2 mmol AgNO3和0.4 g PVP溶解于20 mL去离子水,2 mmol尿素加入上述混合溶液,不断搅拌得到均匀溶液.产生的混合物转移到聚四氟乙烯高压反应釜,120°C下加热8 h,自然冷却到室温,离心分离,得到的产品用去离子水和乙醇洗涤,真空干燥.以下是在封闭的高温高压系统中的主要反应:
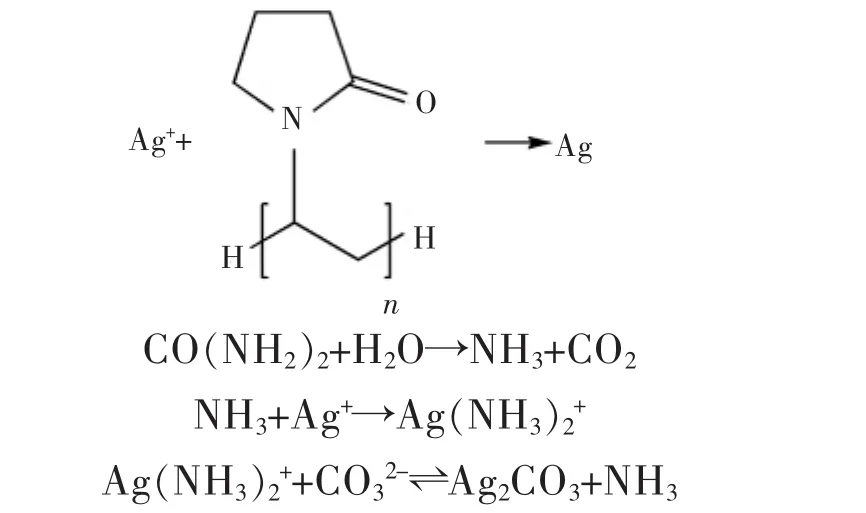
图3(a)是典型样品的扫描电子显微镜照片.很明显,样品的微观结构是均匀的纳米线,没有杂质颗粒或聚集物.许多纳米颗粒被均匀地负载到一维纳米线上,纳米线的直径约为100 nm,长度约5~10 μm.TEM图像如图3(b)所示,表明纳米线是由纳米粒子组成的,具有多孔结构.从图3中可以清楚地观察到在纳米线的表面有许多大小为5~10 nm的微小纳米颗粒,这也是比表面积增大的原因.此外,当Ag2CO3被TEM的电子束照亮时,光腐蚀现象没有发生,这表明该方法制备的Ag/Ag2CO3混合纳米结构比室温下沉淀法制备的Ag2CO3结构更稳定.图3(b)中的插图可以看出,Ag和Ag2CO3的晶格接触非常紧密,表明在合成过程中,Ag和Ag2CO3之间产生了强烈的相互作用.
Dai等[51]通过一种简单的光还原-浸渍法合成了Fe(III)修饰的Ag/Ag2CO3光催化剂.由于Ag纳米颗粒与 Fe(III)纳米团簇的协同作用,Fe(III)修饰的Ag/Ag2CO3光催化剂具有比Ag2CO3和Ag/Ag2CO3更高的可见光光催化活性和稳定性.由银纳米粒子表面的等离子共振效应,催化剂吸收可见光能力增强,催化剂表面的Fe(III)纳米团簇为氧还原反应提供了更多的有效位点,降低了光生电子和空穴的复合速率.
2.3 非金属掺杂
Tian等[52]在Ag2CO3晶体生长过程中,通过加入不同体积的N-CQDs溶液,利用简单的沉淀法制备了一系列N-CQDs/Ag2CO3复合晶体(其中N-CQDs=氮掺杂碳量子点),在可见光下对苯酚进行降解.结果表明,在与微量的N-CQDs耦合后,Ag2CO3的光催化活性和稳定性都得到了极大的提高.碳量子点(CQDS)和氮掺杂碳量子点(N-CQDS)具有良好的水溶性,加入之后影响Ag2CO3的结晶度,导致结晶尺寸显著减小,Ag2CO3晶体的大小和比表面积得到明显增加.此外,N-CQDS具有加快电子转移的能力,所以电荷传递电阻大大降低,光产生电子和空穴的分离效率得到有效提升.N-CQDs在催化剂表面的存在能促进光生成电子的转移,减缓Ag2CO3的光腐蚀速率,从而导致其比裸露的Ag2CO3更稳定.因此,改进形态和电荷转移率的协同效应,使N-CQDs/Ag2CO3具有优异的光催化性能.

图3 Ag/Ag2CO3一维非均匀结构的电子显微镜图像(嵌入图像是Ag纳米颗粒高倍透射电镜图像)Fig.3 Electron microscopy images of a typical Ag/Ag2CO3product
Liu等[53]在DMF(N,N-二甲基甲酰胺)溶剂中通过简单的沉淀法成功制备了纳米 Ag2CO3/CNTs(碳纳米管)复合物.CNTs导电性能好,可以促进光生电子-空穴的有效分离,同时Ag2CO3表面的Ag+不会被还原,Ag2CO3/CNTs复合光催化剂的活性和稳定性得到很大提高.
2.4 与其它半导体形成异质结
2.4.1 AgX (Cl,Br,I)/Ag2CO3
Dong等[54]通过简便有效的离子交换方法合成了AgX/Ag2CO3异质结光催化剂.利用AgX(X=Cl,Br,I)纳米粒子对Ag2CO3进行表面修饰.与Ag2CO3相比,AgX修饰显着地提高了对RhB(罗丹明B),MB(亚甲基蓝)和MO(甲基橙)染料的降解活性.各种分析测试证明了AgX/Ag2CO3异质结构的形成.Ag2CO3和AgX之间的相互作用降低了电荷在其界面上的转移阻力,并拓展了480~640 nm的可见光捕获性能.光电流响应和PL光谱证明AgX/Ag2CO3异质结可以有效地促进光生电子-空穴的分离,并抑制它们的复合.染料敏化效果表明,从RhB(罗丹明B)到异质结的有效电子注入也有利于提高催化剂的光催化能力.
Li等[55]研究出一种非水溶液中通过阴离子交换过程快速制备AgCl/Ag2CO3纳米管的方法,该方法仅在室温下10 min内就可以完成.Ag2CO3纳米棒转化成具有复合结构的纳米管,通过活性测试发现该核壳结构具有良好的光催化活性.
2.4.2 Ag2X(X=O,S)/Ag2CO3
Yu等[56]在Ag2CO3的基础上通过煅烧形成了Ag2O/Ag2CO3异质结光催化剂,该异质结构的光催化性能相对于纯的Ag2CO3和Ag2O来说都得到了极大的提高.Ag2O/Ag2CO3异质结光催化剂通过简单的相转变可以成功地合成,图4说明了Ag2CO3在煅烧相变中Ag2O/Ag2CO3异质结的形成过程.在这个结构中,Ag2CO3颗粒表面覆盖一层Ag2O,形成了具有良好接触界面的Ag2O/Ag2CO3异质结构.在150 W氙灯照射下降解甲基橙,相比于纯Ag2CO3(180 min),Ag2O/Ag2CO3异质结构光催化剂的光催化活性得到极大的提高(4 min).
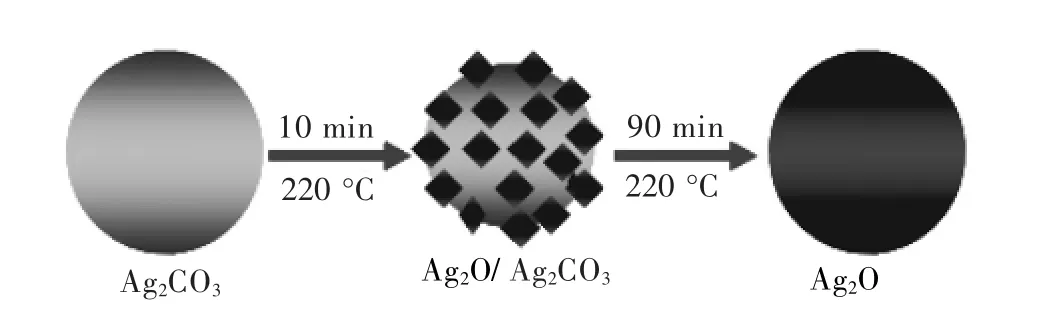
图4 Ag2CO3相变过程Fig.4 Schematic illustration of the phase transformation:Ag2CO3→Ag2O/Ag2CO3→Ag2O
Zhao等[57]介绍了一种简单、绿色、低成本的方法,制备出一种新型Ag2O/Ag2CO3三维中空花状微球(图5).其合成过程为,将Na2CO3水溶液加入AgNO3的乙醇溶液中,利用水溶性的Na2CO3作为模板,制备分层结构的微米球.这些微球是由Ag2O/Ag2CO3纳米粒子组成的,微球的表面形态可以通过调节反应温度来控制,形成有序排列的浅孔和相对光滑的表面.HTEM图像显示Ag2CO3微球被一层薄的Ag2O层包裹,Ag2CO3和Ag2O之间形成了异质结.制备的Ag2O/Ag2CO3微结构显示出了优异的吸附性,稳定性和可见光光催化活性.
田坚等[28]通过共沉淀和连续沉淀法制备了一系列的Ag2S/Ag2CO3复合光催化剂,二者形成了良好的异质结,催化剂稳定性得到提高,对甲基橙和苯酚的光催化降解活性也得到大幅度提升.异质结的形成抑制了光生电子空穴的复合,促进了·OH自由基的生成.Ag2CO3被Ag2S包覆,有力地抑制了Ag2CO3的光腐蚀,从而提高其稳定性.

图5 25°C下制备的Ag2O/Ag2CO3不同倍率的电镜图像Fig.5 Different magnification SEM (a,b) images and TEM (c,d) images of the asobtained Ag2O/Ag2CO3produced at 25°C
2.4.3 Ag的含氧酸盐/Ag2CO3
Fa等[58]利用共沉淀法制备了p-n异质结的Ag3PO4/Ag2CO3复合光催化剂.相比于p型和n型半导体,p-n异质结光催化剂能增强光生电子和空穴的分离,获得的Ag3PO4/Ag2CO3p-n异质结催化剂具有良好的光催化性能.瞬态光电压特性测试和活跃物种捕获实验进一步表明,p-n异质结结构的形成可以极大地增强光生电子-空穴的分离效率,生产更多的自由基活性物种.
Li等[55]研究出一种非水溶液中通过阴离子交换过 程 快 速 制 备 Ag3PO4/Ag2CO3,Ag2C2O4/Ag2CO3和Ag2S/Ag2CO3纳米管的方法,该制备过程仅在室温下10 min内就可以完成.这种酸蚀阴离子交换反应机制可以将Ag2CO3纳米棒转化成的复合结构纳米管(图6).而且产品的最终结构可以通过控制HnX酸和有机溶剂的不同浓度有效地控制不同种类的离子反应的扩散率,得到的纳米管复合材料具有良好的光催化活性.其转换过程如下:

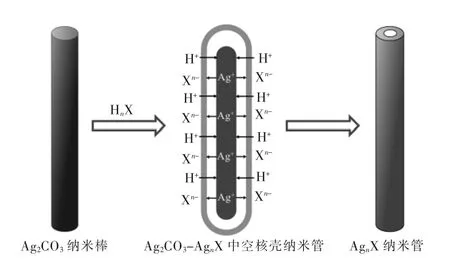
图6 Ag2CO3纳米棒到AgnX纳米管的转换过程示意Fig.6 Schematic illustration of the conversion processes from Ag2CO3nanorods to AgnX nanotubes
2.4.4 Bi盐/Ag2CO3
Fang等[59]通过原位沉淀法制备新型BiOCl/Ag2CO3异质结光催化剂.光催化实验表明,相对于纯BiOCl和Ag2CO3样品,所制备的BiOCl/Ag2CO3光催化剂在可见光照射下降解罗丹明B(RhB)的光催化活性显着提高.显著改善的光催化性能归因于Ag2CO3和BiOCl之间的异质结构,这极大地促进了光诱导电荷转移并抑制了电子和空穴的复合.
Wang等[60]利用水热法和原位沉淀法,成功合成了Ag2CO3/BiOBr复合光催化剂,Ag2CO3/BiOBr复合材料在可见光光照下对有机染料显示出优异的光催化活性.值得注意的是,Ag2CO3/BiOBr复合材料的光催化活性高于纯Ag2CO3和BiOBr样品.较窄的带隙,有利于为Ag2CO3/BiOBr复合材料吸收更大范围的光,同时Ag2CO3和BiOBr之间强烈的耦合作用,促进界面电荷转移,抑制光生电子-空穴的复合,显著增强了光催化活性.
Wang等[61]利用共沉淀的方法,成功地制备了新型的BiOI/Ag2CO3复合光催化剂,并应用于各种污染物的光催化降解,BiOI的加入显著增强了Ag2CO3的光催化活性.此外,BiOI/Ag2CO3复合材料可以减少Ag2CO3的严重光腐蚀,并显示出极好的稳定性和催化回收利用率.
Li等[62]采用一种简单的沉淀法,在室温下合成了Ag2CO3/Bi2O2CO3微米花 (图7).制得的复合材料由许多二维的纳米薄片组成,具有定向的终端排列.对含有罗丹明 B(RhB)、甲基橙(MO)、亚甲基蓝(MB)的有机染料,以及他们的混合物在可见光下进行降解.结果表明,Ag2CO3/Bi2O2CO3的光催化活性比单相Ag2CO3或Bi2O2CO3显著提高.此外,Ag2CO3/Bi2O2CO3光催化剂也显示了良好的光稳定性和可回收性.光生电子-空穴通过Ag2CO3和Bi2O2CO3之间的连接处得到更高效的分离,因此光催化活性得到提高.

图7 典型样品的扫描电镜Fig.7 SEM images of(a) pure Bi2O2CO3,(b)pure Ag2CO3,(c)Ag2CO3/Bi2O2CO3
刘仁月等[63]采用水热法制备了具有片状形貌的BiVO4光催化剂,然后通过简单的沉淀法合成了一系列新型的Ag2CO3/BiVO4复合异质结光催化剂,在可见光照射下考察了其对罗丹明B(RhB)的光催化活性,结果表明,复合光催化剂的光催化活性要明显优于单纯的Ag2CO3和BiVO4.
2.4.5 石墨烯/Ag2CO3
Dai等[64]成功地在 DMF(N,N-二甲基甲酰胺)溶剂中通过一种简单的化学沉淀方法直接合成了纳米级的Ag2CO3/RGO复合材料.通过在可见光照射下的甲基橙(MO)的光催化降解,对样品的光催化活性进行了评价.结果表明,相比于纯纳米级的Ag2CO3,Ag2CO3/RGO纳米复合材料的光催化活性得到显著提升.纳米级的Ag2CO3颗粒沉积在RGO的表面,使得光生电子-空穴的分离效率提高.此外,由于RGO的良好电子传递性能,它的存在可以加速电荷分离、运输和传输,因此Ag2CO3的光催化和结构稳定性得到了极大的提高.
Li等[65]采用液相沉积法合成了一种GO/Ag2CO3光催化剂.GO的存在对Ag2CO3的表面属性和可见光吸收的影响是很显著的.GO/Ag2CO3复合材料显示出了相对较高的比表面积,在很大程度上扩展了可见光的吸收.GO具有良好电子传递性能,有利于Ag2CO3传输光生电子(e-),使其在表面上传输,抑制了电子-空穴的复合,电子可以与吸附O2反应,并转化为·O2-自由基.与此同时,催化剂表面上的基团可以捕获空穴(h+)生成·OH自由基,所以复合材料的光催化活性得到提高.电子(e-)和空穴(h+)分离的增强可以防止Ag+被光生电子还原,因此增强了光催化剂的稳定性.图8阐述了GO/Ag2CO3光催化过程的原理.
2.4.6 g-C3N4/Ag2CO3
图9显示了g-C3N4/Ag2CO3复合材料的制备过程[66].银盐超声分散于g-C3N4中,因为g-C3N4的化学吸收性能,Ag+附着在它的表面,添加 NH3·H2O,在g-C3N4的表面上形成 Ag(NH3)2+,然后,在室温下加入NaHCO3不断搅拌,在g-C3N4的表面上发生了离子交换反应,生成了g-C3N4/Ag2CO3.Ag2CO3粒子沉积在g-C3N4薄片表面,形成了g-C3N4和Ag2CO3之间的异质结结构.
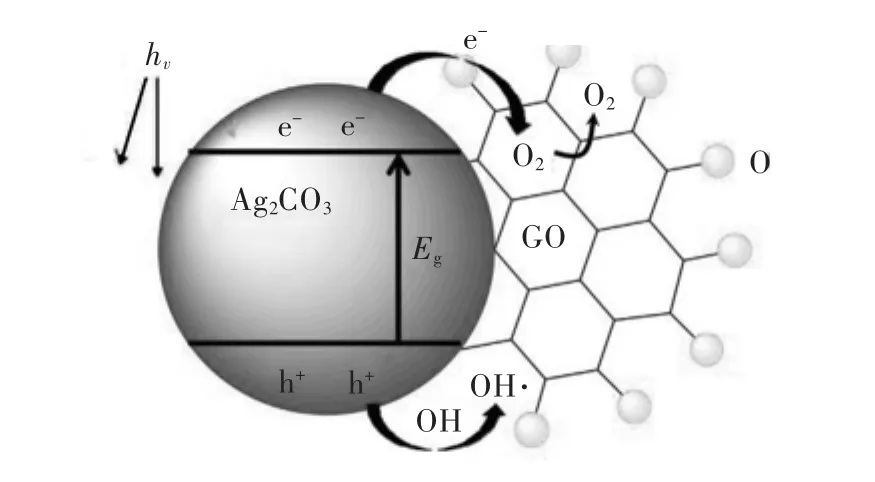
图8 GO/Ag2CO3光催化原理示意Fig.8 The photocatalytic schematic diagram of GO/Ag2CO3samples
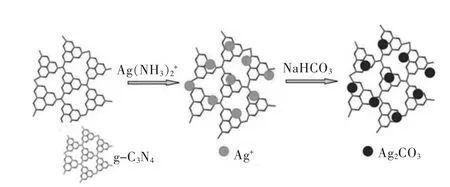
图9 制备g-C3N4/Ag2CO3的原理示意Fig.9 Schematic representation for the synthesis of g-C3N4/Ag2CO3composite
Tonda等[67]通过原位沉淀法合成了一种高效的Ag3N4/g-C3N4异质结纳米材料,Ag3N4纳米颗粒沉积在g-C3N4上.UV-vis漫反射研究表明,合成的Ag3N4/g-C3N4连接在可见光区域表现出更广泛和更强的光吸收.10%Ag2CO3/g-C3N4对罗丹明B的降解速度分别是纯Ag2CO3和g-C3N4的5倍和4倍.Ag3N4/g-C3N4异质结纳米材料光催化活性的增强是由于协同效应,包括可见光吸收的增强,比表面积的增大,电荷转移和分离效率的提高.
2.5 硬模板法
由于多尺度微球结构化剂具有高效的光捕获能力,同时具有比表面积大,不易沉降,良好的物质传输能力和表面的渗透性,因而在液相光催化反应中具有明显的优势.CaMg(CO3)2是一种具有微球结构的半导体,它与Ag2CO3有相同的阴离子结构,但是两者在水溶液中的溶解度相差较大,利用这个特性可以将2个不同的半导体结合在一起,得到一种新型的复合微球.
因此,Tian 等[68]以 CaMg(CO3)2微球为使模板,通过简单的离子交换成功制备了粒径约为10 μm的 CaMg(CO3)2@Ag2CO3核壳结构微球(图 10). 电化学阻抗测试和光电流测试表明,CaMg(CO3)2核的存在可以降低光生载流子的迁移阻力,进而促进光生电子与空穴的分离.另外还表现出更高的催化活性,而且同时具有更好的循环使用性能,制备的成本大幅度降低.

图10 典型样品的扫描电镜Fig.10 SEM images of(a)CaMg(CO3)2and(b)CaMg(CO3)2@Ag2CO3
2.6 PAN/Ag2CO3复合纳米纤维
Panthi等[69]采用一种简单的静电纺丝技术制备了聚丙烯腈(PAN)/Ag2CO3复合纳米纤维(NFs).通过 Ag(NH3)2+与 NaHCO3的离子交换反应制备出 PAN/Ag2CO3NPs胶体溶液,对所得胶体溶液进行静电纺丝,得到PAN-Ag2CO3NFs.在可见光照射下,PAN/Ag2CO3NFs对甲基红(MR)染料溶液的降解显示出高度光催化活性.通过纸扩散敏感性试验(抑制区试验)测试PAN/Ag2CO3NFs的抗菌活性,结果显示,PAN/Ag2CO3NFs对大肠杆菌和金黄色葡萄球菌表现出更强的抗菌活性.PAN具有良好的加工性,显著的疏水性和低密度,使用后易从溶液中分离出来[70].PAN与Ag2CO3通过静电纺丝技术构建出的有机-无机复合结构,保持了纳米颗粒的稳定性,更易于分离回收,可以循环使用,降低成本.
3 结论与展望
Ag2CO3光催化剂是目前研究出的一种新型的高可见光响应的光催化剂,可以作为灭菌剂,也可以有效利用可见光降解各种染料和有机化合物以及还原重金属离子.目前,通过贵金属沉积,非金属掺杂和采用模板的方法改善Ag2CO3性能的研究相对较少,今后可以加深这方面的研究,通过半导体复合的方法改善其性能的研究相对较多,但是还达不到工业催化剂的要求,暂时不能投入到工业生产中使用.
Ag2CO3光催化在未来的发展中可以从以下几点加强研究:
1)积极探索寻找新的半导体材料和改性方法,通过半导体耦合构建异质结结构增加其光吸收性能,提高光生电子空穴的分离效率;
2)研究新的非金属进行共掺杂,探索新的掺杂方式,抑制光生电子-空穴的复合,促进自由基活性物种的产生,从而促进光催化反应的进行;
3)利用简易廉价的模板进行复合,在提升光催化性能的同时降低成本;
4)通过沉积、复合等方法改善Ag2CO3的光腐蚀性和不稳定性,以便回收利用,降低成本.
