食品及食品添加剂中不可溶性硅检测方法的研究
2019-05-09高喜凤刘艳明陈晓媛张喜琦董瑞程月红崔玉花
高喜凤,刘艳明,陈晓媛,张喜琦,董瑞,程月红,崔玉花
(山东省食品药品检验研究院,山东 济南 250101)
硅是人体必需微量元素之一,它能使人体保持柔韧性和弹性,促进骨骼的生长,具有维持动脉壁弹性和保护内壁膜的作用,如果人体的硅摄入量不足,会导致生长迟缓、器官萎缩、骨骼畸形,在膳食中保持一定量的硅元素的摄入,有助于延长机体的衰老,延长寿命。但是如果人体内硅元素含量过高,就会引发高硅症,影响肾脏等器官的正常工作,并且含硅类的食品添加剂如二氧化硅、滑石粉的过量添加将会对人体胃肠道细胞产生一定毒性,长期过量食用有一定的致癌性。因而测定食品及食品添加剂中的硅含量有着重要的意义。硅分为可溶性和不可溶性的,可溶性的硅种类较少、含量低且容易检测,而不可溶硅多以二氧化硅及硅酸镁、硅酸钙等硅酸盐形式存在。二氧化硅、硅酸镁、硅酸钙等由于它们均具有颗粒细微、松散多孔、吸附力强、易吸附导致形成分散的水分、油脂等性质,因此常做为抗结剂用于食品中,用来提高粉状食品的流动性防止其聚集结块或改善干燥粉末在液体里的扩散性能[1-2],我国国家标准GB 2760-2014《食品安全国家标准食品添加剂使用标准》中规定了二氧化硅、滑石粉(其有效成分为硅酸镁)在允许添加的食品中的最大使用限量[3],因而检测其中的不可溶性硅,可以积累数据,为食品监管提供数据支持。由于硅性质的特殊性,使得二氧化硅、硅酸镁、硅酸钙等性质稳定,不与一般的酸反应,因而不可溶性硅的检测成为食品研究的难题。
目前我国针对食品及食品添加剂中不可溶性硅的检测方法非常少,由于不可溶性硅的有效成分主要是二氧化硅,因而最常见的不可溶性硅的研究多为二氧化硅,刘君子[4]、卢华卫等[5]均采用了离子色谱法,由于此方法前处理操作步骤繁琐,检验成本较高,不适用于大批量食品的检测。其他现有的检测方法大多是测定矿石中的二氧化硅,多采用灼烧法、分光光度法、电感耦合等离子体发射光谱法等测定[6-14],但是前两种方法操作繁琐、分析周期长、容易受样品基体的干扰,准确度低,不适用于低含量硅的测定。而电感耦合等离子体发射光谱法分析速度快,时间分布稳定,准确度高,线性范围宽的优点,使其逐渐取代前两种方法,成为二氧化硅的主要检测方法。但是由于食品及食品添加剂与矿石的基体差别很大,基体复杂干扰因素多,因此电感耦合等离子体发射光谱法测定矿石的方法不适用于食品及食品添加剂的测定。
因此寻找一种准确度高、操作简便的测定方式是非常有必要的。基于以上现状本研究开发了一种测定食品及食品添加剂中不可溶性硅的新方法,解决了不可溶性硅难消化处理的难题,为食品监管提供技术支持。
1 材料与方法
1.1 主要仪器和试剂
Optima 8000 电感耦合等离子体发射光谱仪:美国PerkinElmer 公司;Mars 6 微波消解仪:美国CEM 公司;AdvantageA10 超纯水机:美国密理博公司;硝酸、盐酸、氢氟酸、30%的过氧化氢、氢氧化钾(均为优级纯):上海国药集团生产;氢氟酸、氢氧化钾:天津科密欧公司;中国计量科学院的硅标准溶液1 000 μg/mL。
1.2 方法
1.2.1 样品前处理
称取0.5 g 左右样品于聚四氟乙烯消解罐中,加入8 mL 硝酸、1 mL 过氧化氢进行微波消解,设定微波消解程序,见表1,消解完毕后将罐内液体和固体残渣完全转移到定量滤纸上,过滤,水洗。将滤纸及残渣放入聚四氟乙烯消解罐中,加入7 mL 硝酸、5 mL 盐酸、3 mL氢氟酸微波消解,设定微波消解程序见表2,消解完毕后,向溶液中加0.1 g 氢氧化钾反应完毕后将待测溶液转移定容至50 mL 塑料容量瓶中。

表1 微波消解程序1Table 1 Microwave digestion procedure 1

表2 微波消解程序2Table 2 Microwave digestion procedure 2
1.2.2 仪器工作条件
仪器工作参数为功率:1 500 W,等离子体流量:10 L/min,雾化器流量:0.55 L/min,辅助气流量:0.2 L/min,进样延迟:45 s(如选用自动进样模式延迟改为60 s),选取251.611 nm 做为分析谱线进行测试。
1.2.3 标准溶液工作曲线
用5%的硝酸、2%盐酸、1%氢氟酸(体积分数)溶液逐级稀释硅的标准溶液1 000 μg/mL,配制成浓度为0.1、0.2、0.5、1.0、2.0、4.0、10.0 μg/mL 的一系列标准工作溶液。R2=0.999 645,表明在 0.1 μg/mL~10.0 μg/mL范围内呈良好线性关系。标准溶液工作曲线见图1。
2 结果与分析
2.1 消解温度的选择
试验选取了一种食品添加剂滑石粉,考察了从25 ℃到200 ℃的消解温度,对硅回收率的影响如图2所示。

图2 不同消解温度对不可溶性硅测定的影响Fig.2 Effects of different digestion temperatures on the determination of insoluble silicon
从图2中可以看出消解温度较低的情况下,样品消解不完全,回收率低,当消解温度达80 ℃以上时,回收率达到较为理想的要求,但是实际试验过程中需要消解滤纸,消解温度达150 ℃以上,滤纸及过滤后的残渣才能消解彻底完全,溶液呈现无色透明状,但是消解温度过高对微波消解仪及罐体损害较大,且硅可能会有损失,所以最终确定消解温度为150 ℃。
2.2 前处理方式的选择
2.2.1 分步消解体系的选择
2.2.1.1 基底效应试验
本试验各随机选取了挂面、小麦粉、婴幼儿米粉、奶粉、复配食品添加剂各6个分别称取0.5 g 左右于聚四氟乙烯消解罐中,加入8 mL 硝酸、1 mL 过氧化氢按照表1中设定的程序进行微波消解,消解完毕后用超纯水定容至50 mL 塑料容量瓶中待用,电感耦合等离子体发射光谱仪上机测定,发现试样中硅的含量挂面为30.01 mg/kg~43.43 mg/kg,小麦粉为11.65 mg/kg~32.46 mg/kg,婴幼儿米粉为7.418 mg/kg~14.17 mg/kg,奶粉为7.879 mg/kg~20.63 mg/kg,复配添加剂为9.665 mg/kg~51.28 mg/kg。由此可见食品及食品添加剂中含有由此可见食品及食品添加剂中含有可溶性硅元素,因而需要分步前处理去除,进而进行食品及食品添加剂中不可溶性硅的测定。
2.2.1.2 酸体系的选择
在微波消解的高温高压条件下,硝酸、过氧化氢能够氧化分解样品中的有机物,将不可溶性硅与其他可溶性的硅分离开来,硝酸-盐酸-氢氟酸的酸体系中,氢氟酸溶解不可溶性硅,硝酸用于氧化分解滤纸等物质,而盐酸的存在可以加速反应的进行。消解完毕后在消解液中加入氢氧化钾用于中和一部分酸,降低酸度对仪器的损害。
2.2.2 消解方式的选择
由于文献报道的不可溶性硅的前处理方法多为碱融的方法,本研究以不可溶性二氧化硅为例选取0.5 g 含有二氧化硅试样在进行第一步硝酸-过氧化氢体系微波消解前处理除去可溶性硅后分别进行碱融后加酸微波消解和直接加酸微波消解的方式进行前处理比对,碱融的具体操作步骤为过滤后滤渣加入0.1 g 氢氧化钾,镍坩埚 200 ℃熔融 20 min,用 8 mL 硝酸、5 mL 盐酸、3 mL 氢氟酸洗涤转入聚四氟乙烯消解罐中,按照表2的微波消解程序进行微波消解,消解完毕后转移定容至50 mL 塑料容量瓶。发现碱融的回收率为88.4%~95.7%,满足GB/T 27404-2008《实验室质量控制规范食品理化检测》对于加标回收的要求[15],可做为不可溶性硅的检测方法,但由于碱融方法操作较为复杂繁琐,容易损失,不适用于大批量样品的测定,因此本试验选取直接加酸微波消解的方式做为不可溶性硅的测定方法,碱融方法可以做为食品及食品添加剂中不可溶性硅测定的比对方法。
2.2.3 酸使用量的优化
本酸体系中,氢氟酸做为反应物,盐酸、硝酸做为溶剂消化分解样品中的有机物及杂质同时加速反应的进行,根据微波消解罐的容量及尽可能降低酸度对仪器损害的要求,酸的总量控制在15 mL 以内,以称样量0.5 g,样品中不可溶性硅(以硅计)含量在1 000 mg/kg左右为例,本试验考察氢氟酸使用量对硅测定的影响,如图3所示。

图3 氢氟酸的加入量对不可溶性硅测定的影响Fig.3 Effects of the addition of Hydrofluoric acid on the determination of insoluble silicon
从图3中可以看出氢氟酸在2 mL 以上不可溶性硅已经能够完全反应,考虑实际有些样品中不可溶性硅的含量可能更高些,故选取氢氟酸3 mL,此时硝酸与盐酸的量能把滤纸及残渣消化掉。
2.2.4 溶解二氧化硅能力的试验
由于不可溶性硅的有效成分主要为二氧化硅,本试验以二氧化硅为例,考察本文所采用的方法溶解二氧化硅的能力。称取0.5 g 奶粉,添加不同质量的二氧化硅用硝酸-过氧化氢体系微波消解前处理除去可溶性硅后,加入7 mL 硝酸、5 mL 盐酸、3 mL 氢氟酸微波消解,其回收率见图4,可以认为该酸体系能完全溶解二氧化硅质量的上限为60 mg。以称取0.500 0 g 干样品计,可测定干样二氧化硅含量的上限为120 g/kg,以称取2.000 g 湿样品计,可测定二氧化硅的含量上限为30 g/kg。若二氧化硅含量超过测定上限,则需要减少称样量重新消解样品再测定。
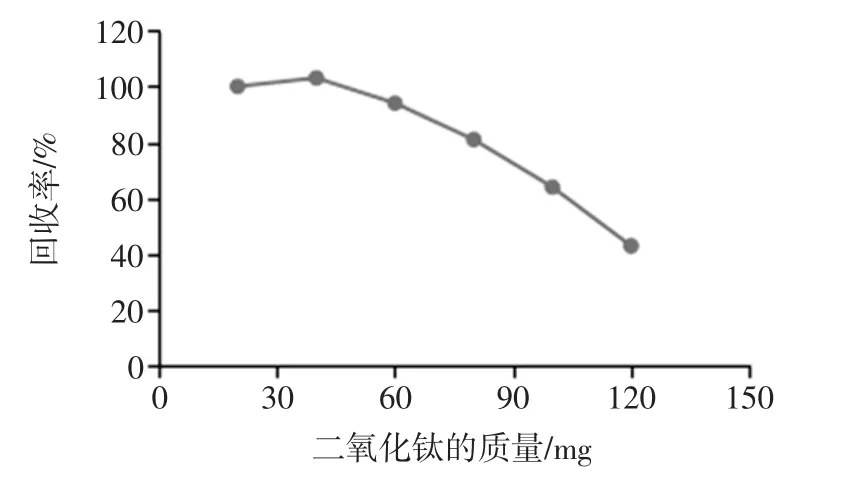
图4 溶解二氧化硅能力的试验Fig.4 Testing on dissolution of silicon dioxide
2.3 分析线的选择
在电感耦合等离子体发射光谱法分析中,分析谱线的选择对于样品分析结果的准确性和精密性有着重要的影响[16-18],本试验选择3 条硅元素较灵敏谱线,其波长分别为 212.412、251.611、288.158 nm,以 4.0 μg/mL的硅标准溶液作为测试液,在仪器最佳条件下,观察各谱线的干扰和背景影响情况,选择其中峰形窄、干扰少、背景值低、信噪比高的谱线251.611 nm 做为分析谱线进行测试。
2.4 方法检出限
在优化试验条件下,对方法的检出限(method detection limit,MDL)进行了测定,即空白样品进行 12 次测量的标准偏差的3 倍所对应的浓度,结果表明以硅元素计的检出限为0.24 mg/kg。
2.5 加标回收及精密度试验
选取两种不同食品试样及滑石粉标准物质进行检测分析及添加不同水平的二氧化硅进行加标回收测定,试验结果见表3和表4。结果表明乳粉的加标回收率为91.0%~102.9%,稻米的加标回收率为93.8%~106.2%,滑石粉的加标回收率为92.7%~105.6%,相对标准差(relative standard deviation,RSD)为 4.76%,相对偏差为-1.89%,均满足GB/T 27404-2008 对于加标回收的要求,由此可见此方法测定二氧化硅的精密度好、准确性高,即本方法测定食品及食品添加剂中不可溶性硅精密度好、准确性高。

表3 不同水平的加标回收测定实验数据Table 3 The experimental data of different spiked recoveries
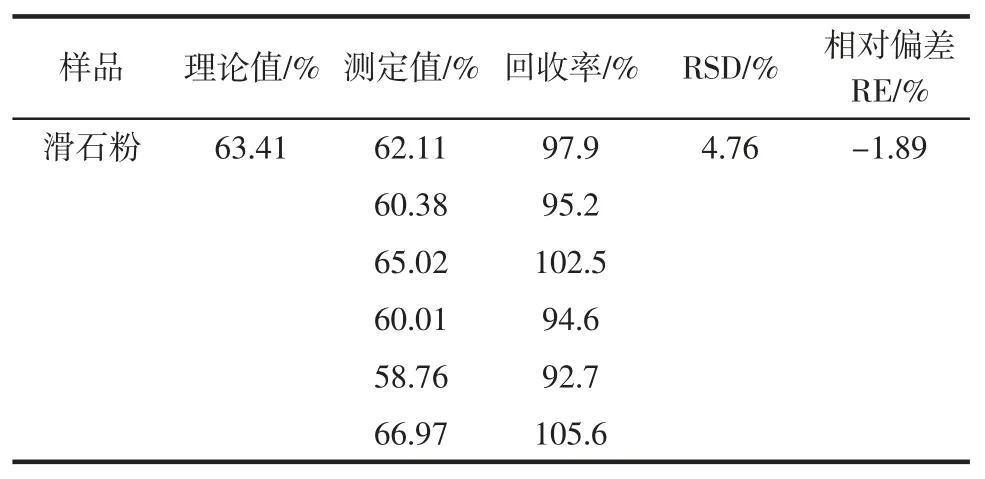
表4 精密度和准确度试验数据Table 4 The experimental data of precision and accuracy
3 结论
通过对不同种类的食品及食品添加剂进行了不可溶性硅检测方法的研究,建立微波消解体系下的电感耦合等离子体发射光谱法检测方法。电感耦合等离子体发射光谱法测定不可溶性硅硅具有分析用时短、准确度高、灵敏度高、检出限低等优点,采用微波消解的方法进行前处理,微波能穿透聚四氟乙烯消解罐对样品进行加热,密闭的消解罐中,压力大、消解速度快、消解效果好,回收率高,不同酸体系消解能够扣除可溶性硅本底的影响,从而使检测数据更加准确可靠,消解后溶液加入氢氧化钾能够中和部分酸,减少大量酸对仪器的损害。此方法适用于食品以及食品添加剂中不可溶性硅的测定,从而为食品及食品添加剂的市场监督与监管提供理论依据与技术支持。
