神经介入术后CYP2C19基因多态性与氯吡格雷治疗药物调整
2019-05-09中国人民解放军总医院药学部临床药学中心北京100853
陈 玥,刘 磊,高 雪,朱 曼,柴 栋(中国人民解放军总医院药学部临床药学中心,北京 100853)
缺血性脑血管病致残、病死及卒中复发率高,给家庭及社会造成极大的经济负担。越来越多的临床研究显示,血管内介入治疗能显著地降低缺血性脑血管病的致残、病死及卒中复发率[1]。抗血小板药物治疗是保证缺血性脑血管病血管内介入治疗安全性和有效性的基石,但目前治疗上由于患者个体化差异大,治疗效果影响因素多,尚无统一用药方案。指南[2]推荐首选阿司匹林或氯吡格雷,专家共识[3]给出了以阿司匹林和氯吡格雷为核心的术前术后用药意见,并指出少部分服用阿司匹林或者氯吡格雷患者的抗血小板功能检查提示存在药物抵抗现象,导致介入术后缺血性不良反应。同时,有研究[4]表明,部分患者对氯吡格雷反应性高,介入术后出血事件时有报道。在神经介入领域,氯吡格雷的安全性评估尚不完善。本文拟探讨在接受神经介入术的缺血性脑血管病患者中氯吡格雷基因多态性与治疗药物调整之间的关系,以便开展面向临床的个体化治疗药物调整。
1 资料与方法
1.1 研究对象
采用回顾式分析方式,收集我院2016 年8 月-2018年7月入院的缺血性脑血管病患者数据。
纳入标准:(1)年龄>18 岁;(2)接受脑血管造影并行经皮神经介入术;(3)术后使用抗血小板药物治疗;(4)进行血栓弹力图检测;(5)进行氯吡格雷CYP2C19基因型检测;(6)所有检测结果在患者住院期间报告。
排除标准:(1)孕妇;(2)本次入院前已使用氯吡格雷;(3)仅进行造影,未手术;(4)数据不全;(5)检测结果在患者出院后报告;(6)肝肾功能异常者(肝功能异常定义为AST、ALT >正常上限3 倍或直接胆红素>正常上限2 倍;肾功能异常定义为肌酐清除率<50 mL·min-1)。
1.2 研究设计
应用PCR-RFLP 法测定氯吡格雷CYP2C19 基因型,应用血栓弹力图测定抗血小板活性,根据血栓弹力图ADP 抑制率结果,研究氯吡格雷相关基因型与血小板聚集率的相关性;收集患者抗血小板药物治疗调整数据,分析治疗药物调整与氯吡格雷相关基因型和血小板聚集率的关系;收集患者住院治疗期间的缺血性或出血性不良事件。定义CYP2C19 *1/*1 为正常代谢型(normal metabolizers,NM);*1/*2,*1/*3为中间代谢型(intermediate metabolizers,IM);*2/*2,*2/*3或*3/*3为慢代谢型(poor metabolizers,PM)[5]。由于中国人群罕见携带*17等位基因的快代谢型及超快代谢型,本次研究中未发现,故未纳入定义。
1.3 药物治疗方案
标准药物治疗方案:术后30 d 内予以阿司匹林(100 mg,qd)+氯吡格雷(75 mg,qd),之后是否继续双联抗血小板方案根据患者病情、支架类型等决定。药物调整方案:通过提取用药记录和时间,将患者在血栓弹力图结果报告后的治疗药物方案分为:阿司匹林(100 mg,qd)+氯吡格雷(75 mg,qd);阿司匹林(100 mg,qd)+氯吡格雷(150 mg,qd);阿司匹林(100 mg,qd)+替格瑞洛(90 mg,bid);阿司匹林(100 mg,qd)+氯吡格雷(150 mg,qd)+西洛他唑(100 mg,bid)。
2 结果
2.1 CYP2C19 基因型的测定结果
本次共收集合格病例60 例,其中正常代谢型30例(50.00%),中间代谢型26例(43.33%),慢代谢型4例(6.67%),详见表1。

表1 CYP2C19 基因型的测定结果Tab 1 Results of CYP2C19 genotype
2.2 血栓弹力图ADP抑制率与CYP2C19 基因型的关系
由于ADP 抑制率与氯吡格雷治疗效果间的关系尚未建立,一般认为< 20%为氯吡格雷不敏感,需要换用其他药物,在20% ~ 50%之间为氯吡格雷反应性低,一般认为未达到治疗效果,需要增加剂量或加用其他药物,或者换药;在50% ~ 75%之间为有氯吡格雷反应性,一般认为达到治疗效果;在75% ~ 95%为有氯吡格雷反应性,抑制效果明显,治疗效果好;> 95%时为氯吡格雷高反应性,可能有出血风险[6]。本次研究的血栓弹力图ADP抑制率与CYP2C19基因型的关系详见表2,其中慢代谢型ADP抑制率均< 50%,视为均未达到治疗效果,正常代谢型与中间代谢型差异不显著。
2.3 治疗药物调整
共有26.67%(16/60)的患者进行了治疗药物调整。治疗药物调整与ADP抑制率的关系见表3,ADP抑制率< 50%的部分患者进行了治疗药物调整,其中抑制率< 20%的患者有50.00%(8/16)进行了调整,4 例换用替格瑞洛,2 例增加氯吡格雷剂量,2 例加用西洛他唑。ADP 抑制率在20% ~ 50%的患者有30.00%(6/20)进行调整,4例增加氯吡格雷剂量,2例更换为替格瑞洛。此外,有1例ADP抑制率在75% ~95%的患者也增加了氯吡格雷剂量,经查阅病历,为临床有缺血性表现后调整药物剂量。治疗药物调整与CYP2C19基因多态性的关系见表4,其中NM组有26.67%(8/30)进行了调整,IM组有26.92%(7/26)进行调整,PM组有1例患者进行调整,构成比为25.00%。
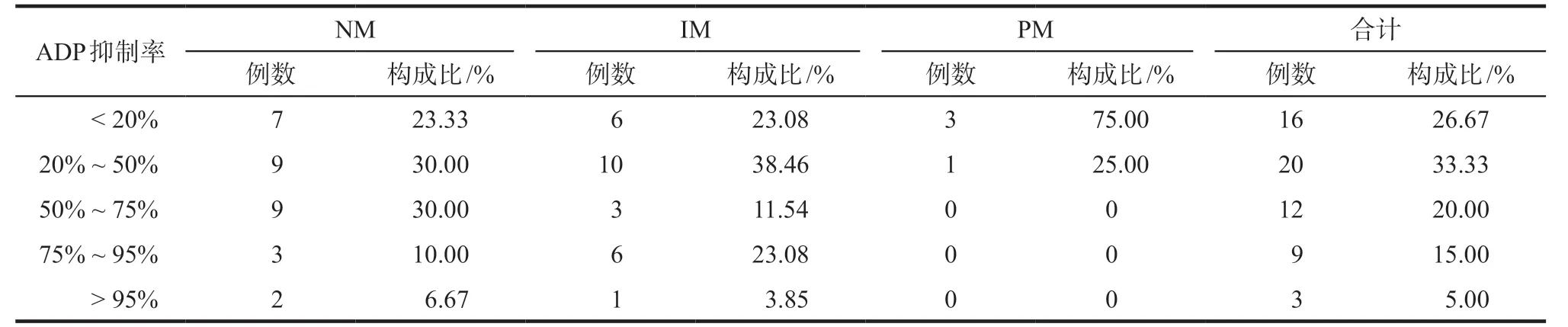
表2 血栓弹力图ADP抑制率与CYP2C19基因型的关系Tab 2 Relationship between ADP inhibition rate and CYP2C19 genotype

表3 治疗药物调整与ADP抑制率的关系Tab 3 Relationship between therapeutic drug adjustment and ADP inhibition rate
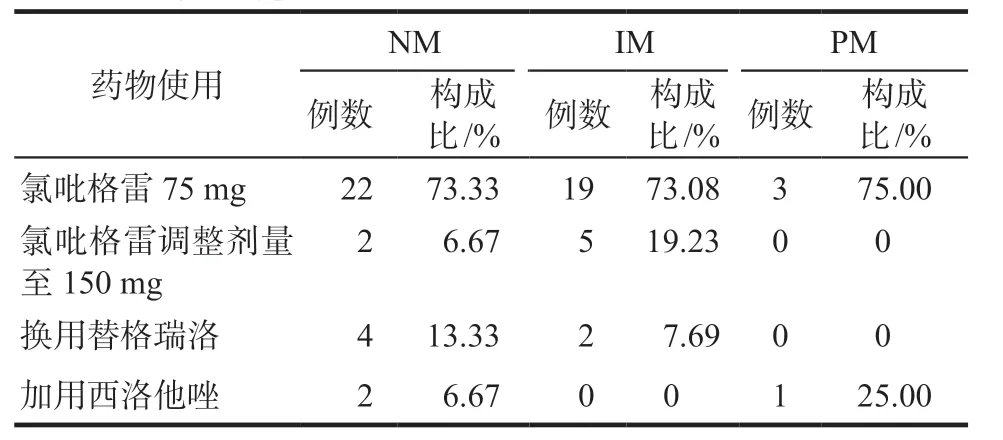
表4 治疗药物调整与CYP2C19基因多态性的关系Tab 4 Relationship between therapeutic drug adjustment and CYP2C19 genotype
2.4 住院期间出血或缺血性不良事件
由于失访率较高,本次研究仅统计了患者住院期间发生的不良事件,共有7例患者出现缺血性不良事件(11.67%),5 例为ADP 抑制率< 50%(71.43%,5/7),表现主要为一过性黑曚、言语不清、头晕头痛等,其中正常代谢型1 例(ADP 抑制率33.40%)、慢代谢型1 例(ADP 抑制率23.10%),中间代谢型5 例(ADP抑制率20% ~ 50% 3例,87.20% 1例,94.80% 1例),中间代谢型3例ADP抑制率在20% ~ 50%的患者之后增加了氯吡格雷剂量(调整剂量至150 mg),正常代谢型和慢代谢型的2例患者均加用了西洛他唑。
3 讨论
3.1 CYP2C19基因多态性与ADP抑制率
文献报道,中国人群中14%为CYP2C19 慢代谢型,41%为中间代谢型,45%为正常代谢型[7]。本研究虽然病例数偏少,慢代谢型人数占比较少,但基本符合上述报道。从血栓弹力图ADP 抑制率判断,慢代谢型均为氯吡格雷不敏感或反应性低,其中75%表现为氯吡格雷不敏感;正常代谢型和中间代谢型差异不显著,但正常代谢型患者可能会有稍高比例出现氯吡格雷高反应性(NM 6.67%,2/30;IM 3.85%,1/26),这种差异可能会随着样本量增大而增加,需要提示临床注意。虽然CYP2C19 基因多态性会对氯吡格雷的治疗效果有一定的影响,进而可能体现在血栓弹力图ADP抑制率上,但导致氯吡格雷抵抗的原因非常多[8],与既往文献报道结果类似[9],本研究也证实CYP2C19基因多态性与血栓弹力图ADP 抑制率并无显著的相关性。
3.2 CYP2C19基因多态性与治疗药物调整
目前尚无针对神经介入患者的氯吡格雷治疗药物调整推荐,可参考的依据是CPIC 指南[10]。本研究表明中间代谢型患者氯吡格雷反应低或不敏感的有61.54%(16/26),进行治疗药物调整构成比为26.92%(7/26),住院期间不良反应发生也以该类患者为主(5/7,71.43%)。在正常代谢型患者中,有53.33%(16/30)对氯吡格雷反应低或不敏感,有26.67%(8/30)进行了治疗药物调整;慢代谢型均为氯吡格雷反应低或不敏感,出现缺血性不良事件的患者进行了治疗药物调整。本研究为回顾性研究,除出现不良事件的患者外,无法确定其他患者治疗药物调整是根据临床症状还是实验室指标。但对于氯吡格雷慢代谢型患者,由于表现为氯吡格雷反应低或不敏感,仍然建议临床换用其他抗血小板药。对于中间代谢型的患者,临床应高度谨慎,并加强药学监护。
3.3 血栓弹力图ADP抑制率与治疗药物调整
尚无权威指南或文献规定氯吡格雷反应性对应的血小板聚集抑制率数值,氯吡格雷高反应性和出血性不良事件的关系已有文献报道[11],但血栓弹力图显示有氯吡格雷反应性和取得临床效果之间,并没有必然的关系[12],共识也尚未推荐通过监测血栓弹力图ADP抑制率指导临床治疗[3]。本研究发现,住院期间发生缺血性不良事件的患者,有71.43%(5/7)属于氯吡格雷不敏感或低反应性。因此,建议临床根据需要对患者进行血栓弹力图监测,如有监测,则应对抑制率偏低的患者给予高度重视,并进行剂量或药物调整。
4 结论
在心血管领域,CYP2C19 基因多态性与氯吡格雷治疗反应的研究已经较多,并对各种风险因素进行了分析[13]。而在神经介入领域,尚无针对氯吡格雷基因多态性的大规模数据分析,已有报道多为小样本量研究,也未能就基因多态性和治疗药物调整进行明确建议[6,14-15]。本文通过严格纳入排除标准,对我院近两年期间进行神经介入治疗的缺血性脑血管病患者CYP2C19 基因多态性进行了分析,汇总了氯吡格雷治疗反应性和治疗药物调整方案,发现CYP2C19 基因多态性与ADP 抑制率并无显著的相关性,但根据现有数据,建议临床应高度关注慢代谢型和中间代谢型患者,慢代谢型患者建议换用其他药物,中间代谢型患者建议进行血栓弹力图监测,对于氯吡格雷不敏感或低反应性患者,应考虑进行治疗药物调整。
