研究铜棒与液氮之间的热传输过程
2019-05-07孙瑞峰苏为宁胡立群
孙瑞峰,苏为宁,胡立群
(南京大学 物理学院,江苏 南京 210093)
1 热交换法的缺陷
研究液氮的汽化过程, 测量液氮的汽化热是大学物理实验中常规实验[1],常采用的实验方案是用换热法测量液氮的汽化热. 实验中用开口的泡沫罐装液氮,空气与液氮热交换,使液氮蒸发,将室温的铜棒(质量为M、温度为T0)投入其中,铜棒放热使液氮剧烈沸腾,测量液氮质量随时间变化曲线,扣除液氮与空气的热交换蒸发的质量,可算出铜棒从初始温度降到液氮温度(77.4 K)时,液氮质量减少Δm,液氮的汽化是等压过程,如果液氮的汽化热是L(待测量),那么铜棒放出的热量为
ΔQ=LΔm,
(1)
这就是第一次换热过程,主要是铜棒与液氮换热. 第二次换热过程:将液氮温度的铜棒放入量热器中,量热器是近似的绝热系统,包括铜质的内筒和搅拌棒(比热容为c1、质量为m1),换热介质为水(比热容为c2、质量为m2),测温计和量热器的初始温度是T1,投入低温的铜棒后,持续不断地搅拌,尽量使内筒里的液体温度均匀,量热器再次达到平衡温度T2,在这个过程中,铜棒吸热ΔQ1,量热器放热ΔQ2,忽略操作过程中铜棒与空气的热交换及系统与测温计的热交换,那么:
ΔQ1≈ΔQ2=c1m1(T1-T2)+c2m2(T1-T2).
(2)
根据能量守恒定律,铜棒在液氮中的放热,有
ΔQ≈ΔQ2+c1M(T0-T2),
(3)
(3)式中的第一项是铜棒从液氮温度(77.4 K)上升到平衡温度T2的过程中与量热器系统之间交换的热量,第二项补偿了铜棒在室温T0与平衡温度T2之间的热能差异. 将测量数据代入(1)~(3)式,可求出液氮的汽化热.
在实验中,铜棒的温度从室温降到液氮温度,温度跨度达到200 ℃以上,金属铜的比热容不能看成常量,上述实验方案克服了这个问题,通过2次换热过程,只要测量室温T0、初始温度T1和平衡温度T2,这些温度之间的差异小于10 ℃,各种介质的比热容都可看成常量,而且物理过程清晰,是一种很好的测量方案. 但从学生实验结果来看,个体差异比较大,分析实验过程发现:在测量过程中,产生误差的因素比较多,比如将液氮温度的铜棒取出放入量热器中,这期间空气与铜棒之间的热交换是不可避免的,而且与学生的操作过程有关;第二,室温T0、初始温度T1和平衡温度T2之间差异不大,所以每种介质的比热容可看成是常量,但由于平衡温度T2不容易测量准确,温度差(T1-T2)和(T0-T2)的相对误差就比较大,直接影响了实验的测量精度.
为此本文提出了改进方案:将不同初温的铜棒(质量为M、温度分别为T01和T02)分2次投入开口的液氮罐中,铜棒、空气与液氮热交换使液氮汽化,测量液氮质量随时间的变化曲线,扣除液氮与空气的热交换蒸发的质量,可算出铜棒从初始温度降到液氮温度(77.4 K)时,液氮质量的减少分别是Δm1和Δm2,比较2次测量结果,也可算出液氮的汽化热L.
2 改进方案实验原理
铜棒从初温降到液氮温度(T00=77.4 K),温度变化跨度约为200 K,其比热容是温度的函数c1(T). 使用同1根铜棒[质量为M、比热容为温度的函数c1(T)],以不同的初温T01和T02,分2次投入液氮中,分别测量液氮的质量随时间的变化曲线,2次铜棒的初始温度T01>T02,那么,2次铜棒的放热Q1与Q2分别为

在实验中,控制T01-T02≈10 K,在[T01,T02]温区,铜棒的比热容可看成常量,那么:

(4)
扣除液氮与空气的热交换,铜棒2次放热使液氮汽化的质量差为Δm1-Δm2,根据2次测量结果的差值,也可算出液氮的汽化热L,即
c1M(T01-T02)=L(Δm1-Δm2).
(5)
在改进实验方案中,最重要的是选择和测量铜棒的初温T01和T02,由于铜是热的良导体,可以将铜棒放在塑料袋中,隔水浸泡10 min,使得铜棒与水达到热平衡,用温度计读出水的温度作为T01(或者T02),然后取出铜棒放入液氮中. 在测定液氮汽化质量时,放入铜棒前后液氮与空气热交换的汽化速度略有不同,忽略这个差别,并且用图像处理法扣除液氮与空气热交换蒸发的质量.
3 实验步骤和结果
实验仪器与用品:电子天平、开口的泡沫罐、秒表、温度计、铜棒、液氮. 称量铜棒的质量记为M=27.8 g. 第一次测量时,铜棒的初温是T01=49.4 ℃,在泡沫罐中加液氮,并将泡沫罐置于电子天平上,记录质量随时间的变化,这时液氮吸收空气热量缓慢蒸发;然后将T01温度的铜棒放入泡沫罐中,液氮剧烈沸腾,液氮表面逐渐趋于平静,紧接着会出现第二次沸腾,然后再一次趋于平静,持续记录直到液氮表面达到平衡后的一段时间. 根据测量数据,得到液氮的质量随时间的变化如图1所示,并通过图像算出铜棒放热导致液氮汽化的质量.
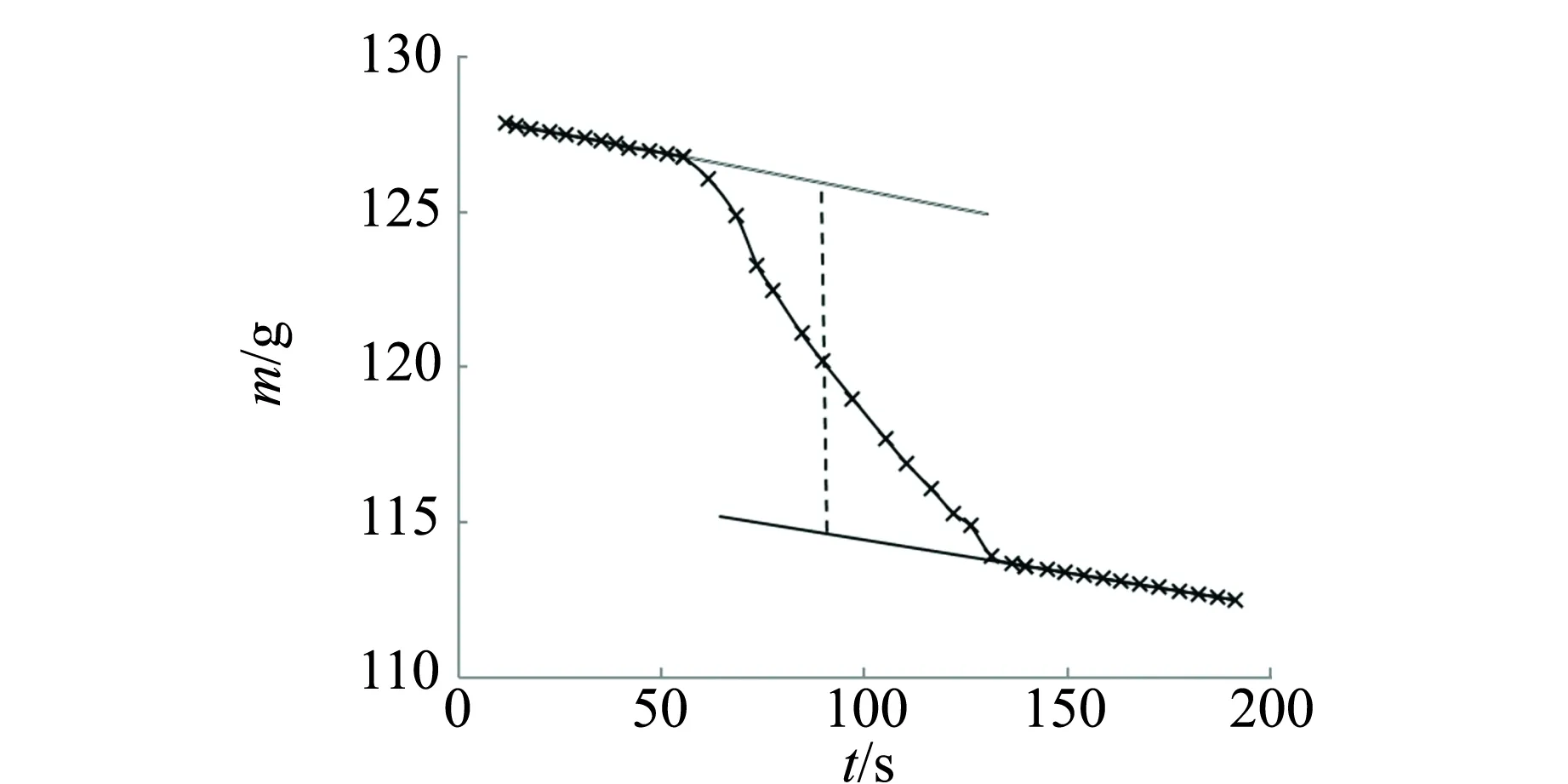
图1 液氮的质量随时间的变化
铜棒放入之前,液氮与空气热交换,液氮的质量随时间的变化是直线,方程是
m=-0.024 7t+128.2,R2=0.998 7.
铜棒达到液氮温度以后,液氮的质量随时间的变化也是直线,方程是
m=-0.021 3t+116.6,R2=0.999 8.
中间的曲线主要是铜棒放热,使液氮快速汽化所致,也包含了空气与液氮热交换导致液氮汽化的质量,其中点位于t=97.46 s处,扣除空气传热使液氮蒸发的质量,计算铜棒放热导致液氮汽化质量的为Δm1=22.24 g.
第二次测量,铜棒的初温是T02=28.1 ℃,液氮的质量随时间的变化关系如图2所示,按照图1的处理方案,可以算出铜棒放热使液氮汽化的质量为Δm2=10.00 g.
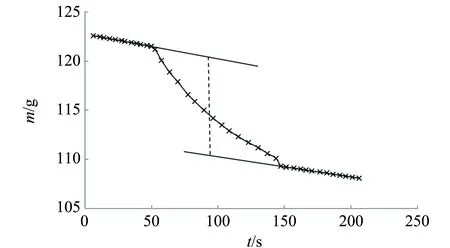
图2 液氮的质量随时间的变化
铜的比热容c1≈0.389 J/(g·K-1),将实验测得的T01,T02,Δm1,Δm2代入(5)式中得到:L=185 l/g.
4 铜棒降温过程的讨论
在改进实验方案中,铜棒的初温与环境温度接近,将初温的铜棒通过空气环境转移进入液氮,铜棒与空气的热交换导致的误差较小. 在实验过程中可以观察到:铜棒刚投入液氮时,液氮沸腾得很厉害,随着时间推移,液氮表面趋于平静,然后还会有一次剧烈的沸腾(称为二次沸腾),再趋于平静,从图1、图2中实验曲线可看到,一开始液氮的质量变化率是比较大的,随着时间的推移,液氮的质量变化率变小,直到二次沸腾后,液氮表面再次趋于平静. 铜棒刚投入液氮时,铜棒与液氮的温度差接近200 ℃,铜棒放热,使液氮快速汽化,这对应于实验中观察到的液氮沸腾;随着时间推移,铜棒的温度降低,铜棒与液氮温度差减小,铜棒放热的速度减小了,液氮汽化的速率也变小了. 事实上,液氮质量减少率(液氮汽化速率)表明了铜棒表面与液氮热交换的速率,而铜棒是块体材料,铜棒内部的温度不能完全同步于液氮质量的变化. 为了探究铜棒与液氮热传导过程中的更多细节,在铜棒上打小孔,加载温度传感器[2-4],实时测量铜棒温度随时间的变化,曲线如图3(a)所示,这次测量铜棒的质量M=27.0 g,铜棒投入液氮后,液氮质量随时间的变化如图3(b)所示,液氮质量变化率随时间的变化如图3(c)所示.

(a)铜棒温度随时间的变化

(b)液氮质量随时间的变化

(c)液氮质量变化率随时间的变化图3 改进后方案的实验数据
因为无法准确截取初始的时间、质量,第一个测量点是不够准确的(实验点仍保留在图中). 可以看到,铜棒刚投入液氮时,液氮的汽化率是最大的,等于0.45 g/s,随着时间推移,液氮的汽化率变小,在93 s至94 s内,液氮的汽化率再次增大,达到0.30 g/s,仅次于最大值,这就是前面描述的二次沸腾.
还注意到,在56~68 s内,液氮的汽化速率等于0.20 g/s,液氮汽化速率在这个值持续了12 s,铜棒温度从-87 ℃降到-125 ℃;同样的,在76~92 s内,液氮的质量变化率等于0.10 g/s,液氮汽化速率在这个值持续了16 s,铜棒温度从-145 ℃降到-173 ℃;在这2个区域内,液氮汽化速率与铜棒、液氮的温差无关. 本文认为,这是因为铜棒表面覆盖了1层氮气膜,铜棒通过氮气膜向液氮传输热量,氮气逃逸的速率趋于常量,每次氮气膜破裂时,铜棒与液氮直接接触,它们之间的热交换模式发生了变化,氮气逃逸的速率也发生变化,当铜棒表面再次形成氮气膜时,氮气逃逸的速率又趋于常量. 图3(c)中液氮质量的变化率为:0.45 g/s →0.35 g/s →0.30 g/s →0.25 g/s →0.20 g/s →0.15 g/s→0.10 g/s,液氮质量的变化率,也即氮气的逃逸速率是台阶式下降的. 铜棒刚投入液氮时,铜棒与液氮之间的温差大,汽化速率大,液氮以这一速率汽化持续的时间短,这对应于实验过程中的液氮剧烈沸腾;随着铜棒与液氮温差变小,汽化速率台阶的持续时间变长,在实验中看到,液氮表面趋于平稳;当铜棒投入液氮的时间到达92 s时,铜棒温度达到-173 ℃,铜棒表面的氮气膜破裂,氮气逃逸,这是在实验中看到的“二次沸腾”,之后铜棒达到液氮温度,液氮表面趋于平静.
换角度来探讨铜棒在液氮中(T0=77 K)的降温过程,根据牛顿冷却定律[5],铜棒单位时间内在空气中散失的热量与(T-T0)n成正比,即:
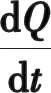
(6)
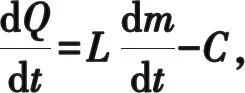
(7)
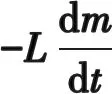
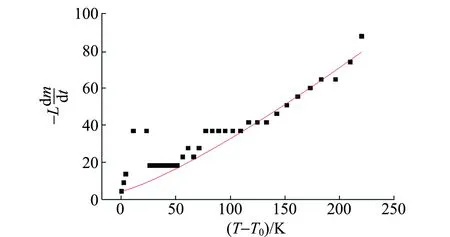
图4 铜棒降温过程放热变化率随时间差的变化
由图4中的拟合曲线可知,在温度差较大(T-T0>100 K)时,拟合曲线与实验数据点符合得较好,而当温度差T-T0降低之后,拟合曲线的值略小于实验测量的放热速率,对照铜棒降温过程的讨论,本文认为这是铜棒与液氮之间的热交换机制的转换导致的结果.
5 结束语
本文在大学物理分组实验——“测量液氮的汽化热”的基础上,提出用差分法测量液氮汽化热的实验方案,根据观察到的实验现象,以及液氮的汽化速率,分析铜棒与液氮之间热交换形式的变化,对照牛顿冷却定律,算出与铜棒表面形状及粗糙度相关的常量K,温差的指数n,对液氮汽化过程和金属铜的降温过程做了详细的研究.
