欧盟和北美抗生素耐药性监测调查现状比较
2019-05-05罗讯徐紫慧张文劲刘畅李祖刚郝海红
罗讯 徐紫慧 张文劲 刘畅 李祖刚 郝海红
(华中农业大学国家兽药残留基准实验室,农业部兽药残留检测重点实验室,华中农业大学国家兽药安全评价实验室,农业部畜禽产品质量安全风险评估实验室,武汉 430070)
近年来,抗生素耐药性问题逐渐发展成为世界上最紧迫的公共卫生问题之一。由于耐药菌的大量产生,曾经很容易治疗的疾病治愈率下降,治疗费用越来越高,对人类健康造成严重威胁。据科学数据统计,细菌耐药性的蔓延已经损害了人类医学研究的进程,如果不采取拯救措施,预计到2050年,每年因此死亡人数将高达上千万[1]。
欧盟和北美作为世界上对抗生素耐药性监测较为权威的两个国家(地区),常作为其他地区制定耐药性监测方案的重要参考,但是针对这两个国家(地区)的耐药监测系统以及耐药发生情况的对比研究仍然较少。因此,在本研究中,作者从抗生素耐药性监测系统、耐药判定标准、耐药流行现状、耐药机制以及耐药管理等多方面对欧盟(包括丹麦)和北美(美国和加拿大)的抗生素耐药性进行比较分析,以期为我国抗菌药物耐药性监测提供相关数据。同时需要注意本文主要侧重于公共卫生及食物和动物源抗生素耐药性,但这并不能掩盖或替代医源性抗生素耐用性的监测。
1 欧盟和北美的抗生素耐药监测系统
欧盟抗菌药耐药性监测网(European Antimicrobial Resistance Surveillance Network,EARSNet)是欧盟政府资助成立的欧洲最大的抗生素耐药监测系统,目的在于为欧洲人类抗菌药耐药性临床表现和流行病学研究提供数据,并分析欧洲抗生素耐药性流行趋势,为政府制定决策提供及时数据[2-3]。欧洲药品管理局(European Medicines Agency,EMA)高度关注抗生素耐药性问题,其下属部门欧盟兽用抗菌药监测(European surveillance of veterinary antimicrobial consumption,ESVAC)[4],主要负责收集兽用抗菌药耐药性数据,该系统每年都会发布一份关于兽用抗菌药全面信息的数据库,以供用户检索。除此之外,欧盟其他成员国也相继实施耐药性监测,其中北欧国家在控制耐药性方面尤为突出,例如丹麦抗菌药耐药性整合监测和研究系统(the Danish integrated antimicrobial resistance monitoring and research programme,DANMAP),该系统成立较早,不可忽视其在欧洲抗生素耐药性监测方面所做出的贡献。
1996年,由美国疾病防控与预防中心(CDC)、美国食品和药品管理局(FDA)、美国农业部(USDA)以及各州和地方卫生部门之间合作成立了国家抗菌药耐药性监测系统(National Antimicrobial Resistance Monitoring System,NARMS),并于2003年在全国范围内普及[5]。其重要任务是从人、肉类零售食品、食源性动物中分离肠道病原菌进行抗微生物药敏实验,耐药流行病学分析等。针对耐药性监测,NARMS各部门之间分工明确,相互协调(表1)。加拿大抗生素耐药性监测综合项目(Canadian integrated program for antimicrobial resistance surveillance,CIPARS)是国家成立的,用于收集、整合、分析和传播抗菌药物趋势以及人类、动物和食源性动物中细菌的耐药性的项目,它每年会发布年报并根据样本的流行病学情况制定基础政策,以控制抗生素的使用和延长抗菌药的效力,并提出遏制耐药菌传播的措施[6]。
因为每个国家的资源、各自监测系统及其负责部门职能和结构均不相同,因此监测系统的组织也各有差异,详细信息见表2。
2 欧盟和北美耐药流行病学比较
欧盟和北美均将监测相关数据发布于网站上,便于数据的交流及研究,关于其药物敏感性实验、耐药现状、耐药机制和耐药监测结果分析等,都可以作为借鉴。
2.1 耐药判定标准
对从人以及家禽、家畜中分离菌株进行定量分析时,欧盟引入野生型临界值也叫流行病学临界值(ECOFFs或者COWT),是根据大量的MIC分布图建立的耐药判定临界值,来区分微生物耐药性。同时亦兼顾临床临界值(COCL)数据进行分析,临床临界值是临床治愈率大于等于90%所对应的MIC值,它将MIC值与临床治疗效应相联系,在一定程度上反映了疗效与耐药判定标准之间的关系。而对于自人体中分离菌株耐药性的定性解释性标准,则通常采用临床临界值将其定性为敏感菌株和不敏感菌株(包含中介和耐药)。欧盟认为当方法以及解释性标准相同时,不同来源的菌株可以直接进行对比分析。

表1 美国NARMS抗生素耐药性监测分工[7-8]Tab.1 Interagency partnership within the NARMS in the United States
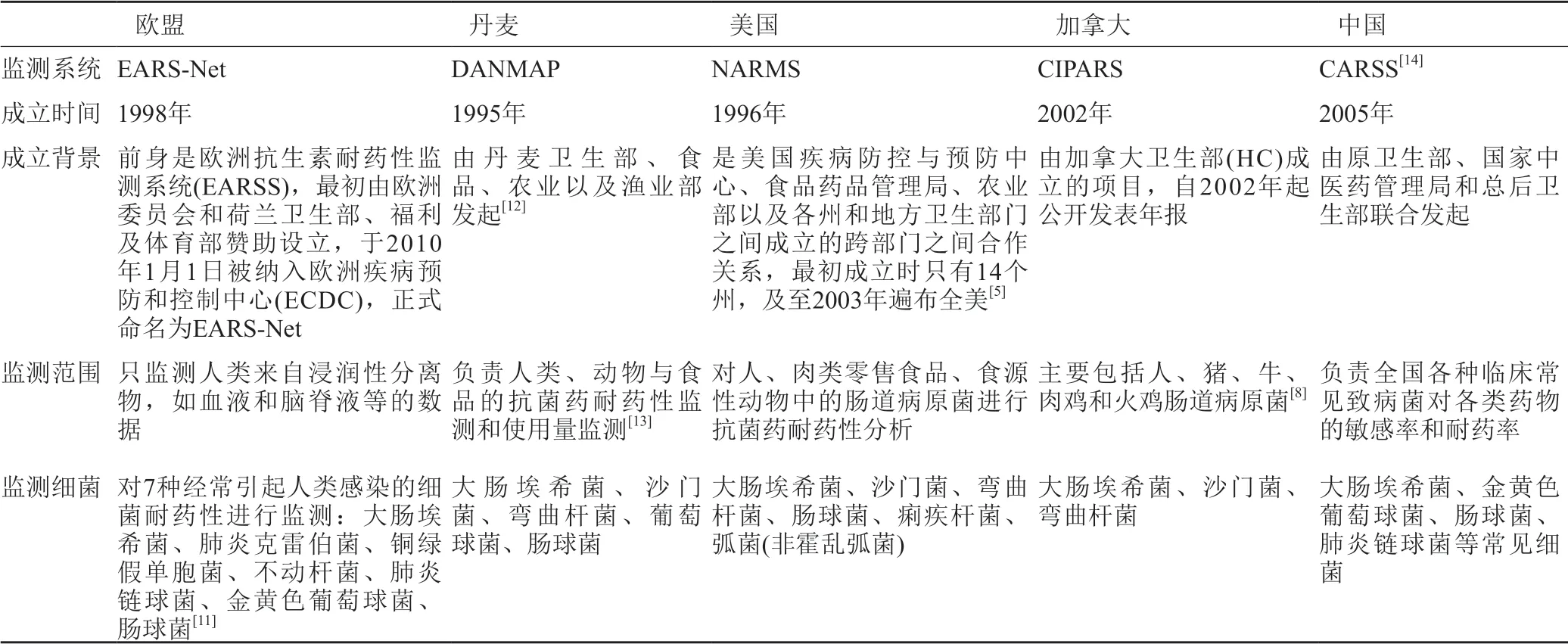
表2 各国家(地区)耐药性监测系统对比Tab.2 Comparison of drug resistance surveillance systems in various countries (regions)
美国亦将野生型临界值广泛应用在耐药性判定中。例如在过去的研究中,美国通常使用对萘啶酸的耐药性来指示对氟喹诺酮类药物的耐药性,而在2013年,美国临床和实验室标准研究研究所CLSI修订了环丙沙星对沙门菌的MIC,研究表明沙门菌对环丙沙星敏感性降低(degrade sensitivity of ciprofloxacin,DSC)(MIC≥0.12µg/mL),目前这一MIC值(COWT)被用于界定沙门菌对氟喹诺酮耐药性的新指标[9],并且使用临界值来判定耐药性比用萘啶酸作为指示更具有临床意义。在2015年年度报告中,美国临床实验室标准化研究协会(CLSI)将沙门菌对环丙沙星敏感性降低和/或哌啶酸耐药作为判定氟喹诺酮类药物耐药的判定标准[10]。
2.2 耐药现状
2.2.1 欧盟耐药性现状
截止到2016年欧盟公布的最新资料中显示,对于人类大肠埃希菌感染,氨苄青霉素(29.5%)、磺胺类药物(34.6%)和四环素(29.2%)已经对其产生极高耐药性,对第三代头孢菌素仍然比较敏感(表3)。细菌对多种药物耐药性攀升导致了药物对疾病治疗失败加剧,据报道,一株分离得到的鼠伤寒沙门菌对9种测试药物中的8种均耐药,仅对美罗培南敏感。从肉鸡、养肥火鸡和它们的肉类食品中分离的沙门菌以及大肠埃希菌,均对氨苄西林、喹诺酮、四环素以及磺胺类药物展现极高耐药性,而对第三代头孢菌素的敏感程度仍然较高。除此之外,沙门菌和大肠埃希菌对黏菌素也保持低耐药水平[16]。在人类,肉鸡以及肉类食品中弯曲杆菌对环丙沙星和四环素的耐药性极高,对红霉素(97.9%)敏感。
2.2.2 美国耐药性现状
NARMS系统中截止2015年关于人类抗菌药耐药现状调查结果见表4[17]。由表可以看出,多重耐药现象十分严重。例如非伤寒沙门菌,对氨苄西林、氯霉素、链霉素、磺胺类药物和四环素均已经耐药。
美国疾病防控中心估计,沙门菌每年可造成120万人患病。大部分患者可以很快得到治愈,但是对于感染都柏林沙门菌的患者,治疗效果并不理想[18]。都柏林沙门菌是沙门菌的一种亚型,通常出现在牛体中,并在人类中传播,引起一种罕见且难以治愈的疾病。美国的都柏林沙门菌病主要通过牛奶制品和牛肉产品得以传播。在过去10年间,超过一半的都柏林沙门菌的病原菌对7种治疗药物耐药,造成了极其严重的临床结果[19]。2015年,在肯塔基州鸡源性沙门菌中首次分离到了对环丙沙星耐药的突变株,这也提示我们氟喹诺酮类药物耐药性的进一步扩大,在过去的几年中,在免疫缺陷宿主或者正常防御宿主中,均有报道指出环丙沙星和其他氟喹诺酮类药物对沙门菌病治疗失败。相比于沙门菌,分离自火鸡的大肠埃希菌耐药现象比较严重(85%的耐药菌分离自火鸡肉,90%分离自火鸡盲肠)。
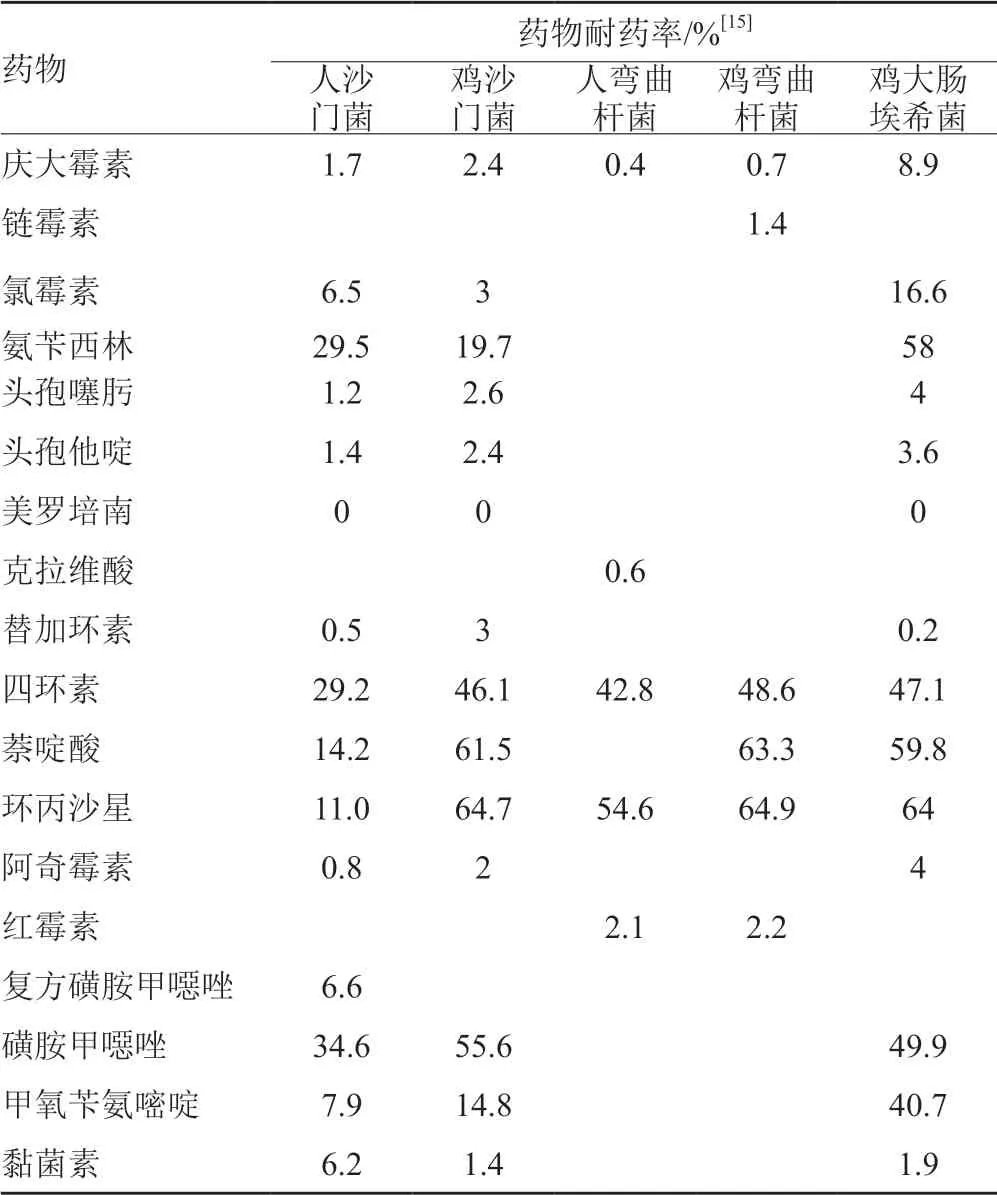
表3 2016年欧盟抗生素耐药发生率统计Tab.3 Statistics on the incidence of antibiotic resistance in EU in 2016
2.2.3 加拿大耐药性现状
目前加拿大可查的最新调查结果是2017年出版的关于2015加拿大抗生素耐药性监测系统报告[20]。报告中显示兽用抗菌药的使用数量是人用抗菌药的1.7倍,而在兽用抗菌药的使用中,用于预防的数量又远远大于治疗疾病和促生长作用。而重要抗菌药使用量的变化也时刻影响着耐药性发生的情况。例如减少使用第三代头孢菌素类药物后发现细菌(包括沙门菌和大肠埃希菌)对头孢曲松钠的耐药性也随之降低。自2011年以来,加拿大地区细菌多重耐药现象迅速攀升,多数沙门菌临床分离株表现出对至少超过5种药的耐药性。而各地区也相继出现了多重耐药大肠埃希菌导致氟喹诺酮类药物治疗失败的案例[21]。 加拿大地区公布的相关耐药情况如表5所示。
2.2.4 丹麦耐药性现状
自1995年以来,DANMAP主要对从肉鸡、猪肉、牛肉以及人类样本病料中分离的鼠伤寒沙门菌、弯曲杆菌以及大肠埃希菌进行监测,直至2014年对沙门菌和弯曲杆菌的药物敏感性实验从未间断过,以期协调欧盟的耐药性监测任务[22]。因为丹麦隶属于欧盟组织,因此其耐药结果也被EMA参考总结,DANMAP2016年公布的耐药情况如下表6所示。
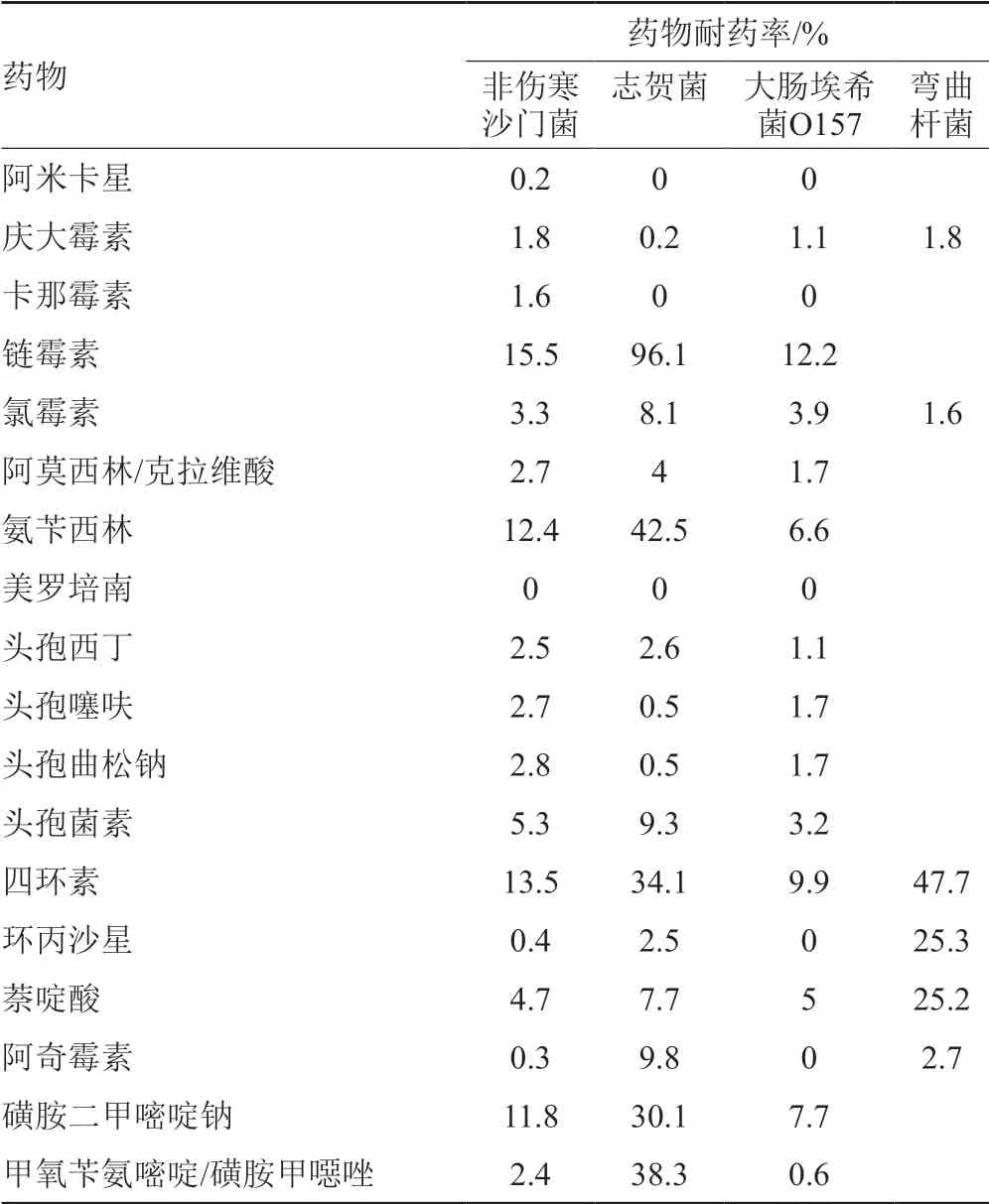
表4 2015年NARMS系统中人用抗生素耐药发生率统计Tab.4 Statistics on the incidence of human antibiotic resistance in NARMS in 2015
2.2.5 中国耐药性现状
以往的调查研究发现,我国每年抗生素的使用量大约为16万吨,其中兽用抗生素高达52%[24]。种种数据表明,抗生素用量的逐年急剧增长,也将成为我国控制抗生素耐药性问题的一大挑战。目前我国抗生素耐药性仍然呈现产生较快,耐药强度增加,耐药谱越来越广等特点,为了解细菌的耐药现状,指导临床用药,以及为耐药决策的制定提供参考数据,我国亦开展了耐药监测计划[25]。国家卫生部于2005年正式成立全国细菌耐药监测网(CARSS),开展抗菌药物敏感实验的判断标准采用2015年CLSI相关标准,监测结果如下表7所示,结果显示大肠埃希菌对第三代头孢菌素、碳青霉烯类药物以及喹诺酮类药物的耐药率相对于2015年分别下降了2.4%、0.4%和0.6%;肺炎链球菌对青霉素和红霉素耐药的全国检出率较上一年分别下降0.3%和上升2.9%;粪肠球菌和屎肠球菌对万古霉素的耐药率分别较2015年下降0.2%和0.9%;而在全国范围内耐甲氧西林金黄色葡萄球菌(MRSA)的全国检出率已达到34.4%,较2015年下降1.4%[26]。在动物源细菌耐药监测方面,日前农业部印发了《2018年动物源细菌耐药性监测计划》,计划规定监测细菌主要包括包括大肠埃希菌、肠球菌(分为屎肠球菌和粪肠球菌)、沙门菌、金黄色葡萄球菌、弯曲杆菌(分为空肠弯曲杆菌和结肠弯曲杆菌)等。沙门菌和金黄色葡萄球菌可根据各地分离情况进行监测。

表5 2015年CIPARS抗生素耐药发生率统计Tab.5 Statistics on the incidence of antibiotic resistance in CIPARS in 2015
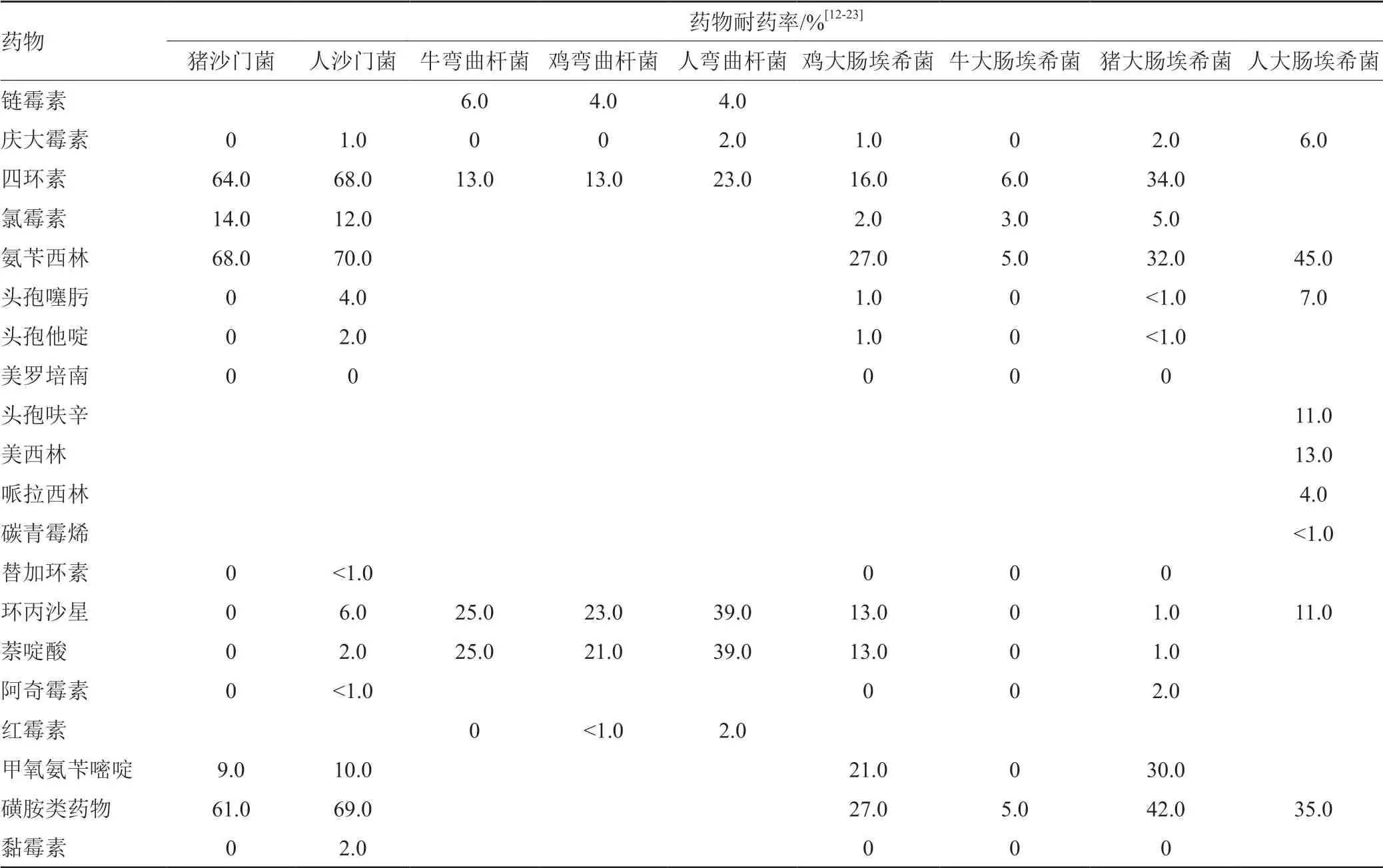
表6 2016年DANMAP抗生素耐药发生率统计Tab.6 Statistics on the incidence of antibiotic resistance in DANMAP in 2016
2.3 耐药机制分析
2014年[18,27],美国首次公布了对于人沙门菌全基因组测序结果,于大多数药物来说,其耐药性是由特定的耐药基因介导的,例如氨苄西林耐药性由blaTEM-1b介导,tetA/B和floR分别介导四环素和氯霉素耐药。传统的头孢类抗生素耐药机制主要由blaCMY-2介导,而近期的研究亦发现了几种携带blaSHV-12、blaSHV-30、blaCTX-M-1、blaCTX-M-55和blaCTX-M-65耐药基因的新超广谱β-内酰胺酶。沙门菌对环丙沙星敏感性降低,则主要是由氟喹诺酮类药物耐药区域(QRDR)突变介导的。大多数环丙沙星耐药菌株都有QRDR突变和质粒介导的耐药基因(PMQR)突变引起。
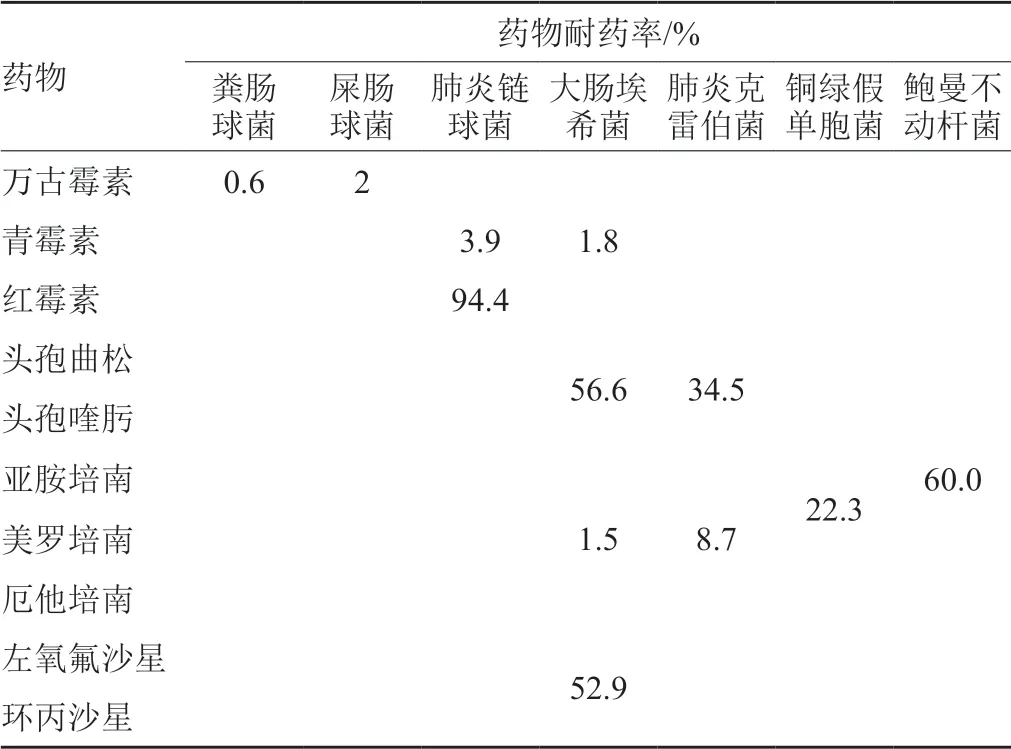
表7 2016年CARSS系统中人用抗生素耐药发生率统计Tab.7 Statistics on the incidence of human antibiotic resistance in CARSS in 2016
在动物源性沙门菌和大肠埃希菌以及人源沙门菌中,因超广谱β-内酰胺酶ESBLs/AmpC β-内酰胺酶产生的耐药菌株比例较低,概率在0~2.7%之间。由产ESBLs/AmpC引起的大肠埃希菌耐药菌株首次在家禽及其肉类食物中评估,结果显示在欧盟各成员国之间具有显著不同。
沙门菌的多重耐药作用模式通常可以描述为(ACSSuT):氯霉素、链霉素、磺胺类药物和四环素多重耐药[28]。2015年,65%的猪沙门菌都对ASSuT耐药[29-30]。另外研究表明,从盲肠中分离得到的肠球菌的多重耐药几率大于从零售肉中分离菌株。多重耐药菌株的比例在欧盟之中高达26.5%,而在美国肯塔基州多重耐药菌株高达76.3%并且超过半数的分离菌株至少对5种类型抗生素耐药。2016年,从欧盟的两个成员国(塞普洛斯和罗马尼亚),检测出了14株含碳青霉烯酶的鸡源大肠埃希菌,在沙门菌血清型中发现极高程度的多重耐药菌。
进一步的细菌分型有助于耐药机制特征研究分析。欧盟将耐甲氧西林金黄色葡萄球菌分为3种表型-社区获得性(community-associated,CA)、卫生保健获得性(health care associated,HA)和家畜获得性(livestock-associated,LA)。例如报道最为广泛的spa基因型归类于LA-MRSA,其中CC38和ST9是欧盟中最普遍存在的类型。目前,西班牙[31]从兔肉中分离出一株单一的spa型t1190耐甲氧西林金黄色葡萄球菌,而以往报道中t1190通常与CC96联合出现,耐甲氧西林金黄色葡萄球菌ST96/CC96仍然没有广泛的报道[32]。利奈唑胺曾是欧盟治疗高耐药MRSA感染的有效抗生素,但是在比利时生猪生产部门分离出两株耐利奈唑胺细菌,尽管在动物体内检测到LA-MRSA中可转移的耐药基因cfr并没有广泛流行,但是仍然有可能对公共卫生造成严重影响。
2.4 对抗耐药性的战略措施
据欧盟的调查结果表明,由多重耐药菌感染而造成每年超过2.5万人死亡,因此造成死亡医疗保健和社会生产力损失高达15亿欧元。而另一方面,仅在美国,每年就有200多万细菌感染病例,而这些细菌至少对一线抗生素已经产生了耐药,美国医疗和保健机构为解决耐药问题所需支出超过200亿美元[33]。针对这些现象,欧盟颁布了新的耐药行动计划,提出共同健康(One health)口号,主张人与动物健康密切关联,疾病可以从动物传播到人类,反之亦然。同时警惕人们注意周围环境的变化也会成为微生物耐药性风险增加的新源头。该计划[34-35]的主要目标建立在3个方面:(1)使欧盟成为耐药性监测的最佳实践区;(2)积极进行耐药性信息数据收集、研究、发展和创新;(3)开展全球议程,使全球耐药信息共享。针对耐药性现象,美国[36]亦提出了4个战略目标:(1)制定更具有代表性的食品动物生产和消费策略,更适用于数据趋势分析;(2)优化数据采集、分析和报告;(3)加强项目合作研究;(4)与国际机构合作,特别是那些致力于减缓耐药细菌传播的国际机构。世界卫生组织(WHO)也一直在关注微生物耐药性问题[37],并于2015年启动了“抗微生物药物耐药性全球行动计划”,该计划分为5项战略目标:(1)提高对抗微生物药物耐药性的认识与理解;(2)加强监测和研究;(3)降低感染发生率;(4)优化抗微生物药物的使用;(5)确保在应对抗生物药物耐药性方面进行可持续投资。
3 展望
针对抗生素耐药问题,世界卫生组织也设立了全球抗生素耐药监测系统(GLASS)[38],该系统2014年发布了首份全球抗生素耐药报告。报告显示世界遭受严重的公共卫生威胁,全球将面临进入“后抗生素时代”的挑战[1],针对当下微生物对多种临床抗生素的耐药性逐渐增强的现状,甚至抗几乎所有临床相关抗生素的“超级细菌”已出现,应当立即开展抗生素耐药防控相关活动,以减缓或规避“无药可救”的情形的到来。目前,欧盟地区和北美地区在应对抗生素耐药性问题方面,都实施了符合本国(本地区)抗生素耐药特点的监控措施。在监测系统,监测细菌种类与范围,耐药判定标准以及数据报道等方面具有差异但同时又相互参考,为国际间的数据交流提供条件。
我国抗生素耐药监测工作进展滞后于北美及欧洲多数发达国家,目前仍然存在监测系统不完善,标准不能统一,监测覆盖面狭窄,数据单薄,信息更新不及时等一系列问题[25],因此我们可以借鉴欧盟与北美一些优秀经验,与国际研究接轨,完善我国耐药监测系统,扩大监测范围,积极进行耐药流行病学动态数据分析。加强药物使用规范,健全药物管理制度。研发治疗疾病新制剂,例如新型抗菌疫苗的研制,新型抗菌肽等活性物质[39]。同时可考虑利用细菌基因组学,比较耐药基因的变化,以获得新的靶标用于特定微生物的抗菌药物的研发[40]。综合运用多种方法和途径,使我国抗生素耐药性监测得到完善与发展。
