慢性阻塞性肺疾病急性加重患者肺栓塞的危险因素及Caprini血栓风险评估量表的预测价值
2019-04-29陈维樊晶艾娇廖俊喆
陈维,樊晶,艾娇,廖俊喆
(1.成都市第三人民医院ICU,四川成都610031;2.成都市第五人民医院急诊科,四川成都611130;3.成都市第五人民医院呼吸内科,四川 成都611130)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是临床常见呼吸科疾病,主要特征为气流受限不完全可逆并呈进行性发展[1]。COPD患者病程中因受到冷空气刺激及环境污染等因素的影响,在治疗过程中极易反复发作,导致慢性阻塞性肺疾病急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)的发生[2]。研究显示,AECOPD患者血液往往处于高凝状态,极易并发肺栓塞。而AECOPD患者一旦并发肺栓塞,死亡风险明显增加[3]。因此,分析影响AECOPD住院患者肺栓塞的危险因素,并根据这些因素采取合理的预防措施,对降低AECOPD患者肺栓塞风险,提升患者治疗有效率至关重要[4]。Caprini血栓风险评估量表是临床评估住院患者发生血栓风险的常用量表,在预测血栓风险方面具有较高的准确性,但是目前鲜见有关将其应用于预测AECOPD患者发生肺栓塞风险的研究[5]。基于此,本研究回顾性分析344例AECOPD患者的各项临床资料,分析AECOPD住院患者肺栓塞的危险因素及Caprini血栓风险评估量表的预测价值,旨在为临床预测及降低AECOPD患者并发肺栓塞的风险提供理论参考。
1 资料与方法
1.1 一般资料
选择我院2011年1月至2018年12月住院部收治的AECOPD合并肺栓塞患者218例作为肺栓塞组,同期入院的AECOPD无肺栓塞患者126例作为对照组。肺栓塞组男138例,女80例;年龄22~78岁,平均年龄(58.61±7.85)岁;病程6个月~12年,平均病程(5.28±0.65)年。对照组男80例,女46例;年龄23~75岁,平均年龄(58.15±7.64)岁;病程7个月~11年,平均病程(5.25±0.62)年。两组患者基础资料比较,差异无统计学意义(P>0.05)。
1.2 纳入、排除标准
纳入标准:①符合急性肺血栓栓塞症诊断标准,即核素肺通气/灌注扫描检查提示肺灌注缺损,与通气不匹配;螺旋CT/电子束CT/MRI证实肺动脉内血栓;肺动脉造影可见肺动脉内血栓;超声心动图发现肺动脉内血栓。②病例资料完整。③有肺栓塞临床症状及体征。
排除标准:①既往有血栓病史,血凝状态异常者;②存在严重肝肾功能不全者;③病历资料不完整者。
1.3 研究方法
根据《急性肺血栓栓塞症诊断治疗中国专家共识(2010)》[6]及《2014版欧洲心脏病学会急性肺血栓栓塞症诊断治疗指南》[7]的相关意见,比较两组患者的各项临床资料,包括糖尿病、恶性肿瘤史、下肢外伤史、6周内手术史、脑血管意外史、长期卧床、肝功能不全、肾功能不全共8项。分析影响AECOPD患者发生肺栓塞的危险因素。
采用《抗栓治疗及预防血栓形成指南》[8]中推荐的Caprini血栓风险评估量表评价两组患者肺栓塞发生风险,其中0~1分为低危,2分为中危,3~4分为高危,≥5分为极高危。
1.4 统计学分析
2 结果
2.1 AECOPD患者肺栓塞的危险因素构成比
肺栓塞组糖尿病、恶性肿瘤史、下肢外伤史、6周内手术史、脑血管意外史、长期卧床等发生率均高于对照组(P<0.05)。两组肝、肾功能不全发生率差异无统计学意义(P>0.05)。见表1。

表1 AECOPD患者肺栓塞危险因素 例(%)
2.2 AECOPD患者肺栓塞危险因素的多因素回归分析
选择有差异的单因素变量为质变量,肺栓塞为因变量,行多元Logistic回归分析。结果表明,糖尿病史、恶性肿瘤史、下肢外伤史、6周内手术史、脑血管意外史、长期卧床均为肺栓塞发生的独立危险因素(P<0.05)。见表2。
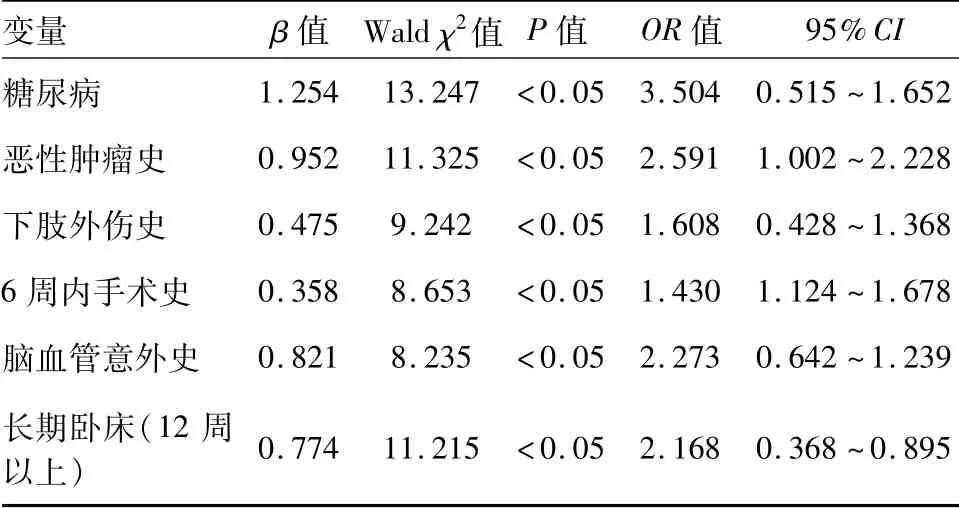
表2 AECOPD患者肺栓塞危险因素的多因素回归分析
2.3 AECOPD患者肺栓塞风险评分及危险度分级比较
肺栓塞组Caprini评分显著高于对照组(P<0.01)。肺栓塞组中,极高危患者比例最高(117例,53.67%),其次为高危患者(53例,24.31%)。高危及以上患者占比达77.98%。对照组中、高危占比为52.37%,其次为低危(28.57%)。两组患者危险度分级构成比间的差异有统计学意义(P<0.05)。见表3。

表3 AECOPD患者肺栓塞风险评分及危险度分级
2.4 AECOPD患者Caprini危险度分级与肺栓塞发病风险的Logistic回归分析
Caprini危险度分级为极高危和高危的AECOPD患者为肺栓塞的高危人群。随Caprini危险度分级的升高,患者肺栓塞的发病风险明显增加(P<0.05)。见表4。

表4 AECOPD患者Caprini危险度分级与肺栓塞发病风险的Logistic回归分析
3 讨论
AECOPD患者多为老年人,肺功能下降,活动受限,部分患者需长期卧床,加之COPD患者机体处于慢性缺氧状态[9],静脉血液瘀滞、静脉系统内皮损伤、血液呈高凝状态[10-11],使AECOPD患者成为肺栓塞及其他血栓事件的高危人群。肺栓塞临床症状隐匿,起病急骤,甚至起病时即为猝死[12]。有报道显示[5,13-14],AECOPD患者继发肺栓塞的发生率较非AECOPD患者高23.6%,这可能与AECOPD患者血液高凝状态、细小动脉原位血栓有关。故针对AECOPD合并肺栓塞危险因素的一级预防显得尤为重要。
本研究通过回顾分析AECOPD合并肺栓塞的临床资料及实验室辅助检查结果,分析肺栓塞发生的危险因素,以指导临床加强对肺栓塞高危人群的重点监测。研究结果显示,糖尿病史、恶性肿瘤史、下肢外伤史、6周内手术史、脑血管意外史、长期卧床为AECOPD患者并发肺栓塞的危险因素。肺栓塞组上述危险因素的构成比显著高于对照组。Logistic回归分析结果也证实,上述6种因素为AECOPD并发肺栓塞的独立危险因素。长期的高血糖状态可诱发凝血机制障碍,使凝血、溶血机制的平衡被破坏,增加脑梗死、心肌梗死的可能性,为肺栓塞的形成提供了可能[15]。恶性肿瘤发生、发展过程中常伴凝血功能异常,肿瘤细胞及肿瘤微环境可促进血小板、凝血因子含量异常升高,造成机体内小血栓形成,从而增加肺栓塞的发生率[16]。短期内手术史(6个月)可增加手术损伤导致血管壁损伤的可能性,术后恢复时间短,血管壁损伤导致的外源性凝血机制并未完全消退,凝血机能亢进,为血栓形成提供了有利条件[17]。下肢外伤史诱发肺栓塞形成机制类似于短期手术史,外伤使凝血功能亢进,造成损伤处静脉血管壁小血栓凝集,诱发聚集性血栓形成[18]。有脑血管意外史的患者脑血管壁有不同程度的血栓形成,血流长期处于低剪切速率与低流率状态,血液黏稠度高,更易形成肺栓塞。长期卧床状态下,下肢静脉回流受阻,累积的凝血因子可激活凝血系统,造成下肢深静脉血栓,从而诱发肺栓塞形成[19]。
本研究还采用Caprini血栓风险评估模型对AECOPD合并肺栓塞及AECOPD不合并肺栓塞患者进行了Caprini评分、Caprini危险等级划分。结果显示,肺栓塞组患者Caprini评分明显高于对照组,AECOPD合并肺栓塞患者Caprini评分模型判定为高危、极高危的比例高达77.98%,明显高于对照组患者中高危、极高危的构成比。进一步对AECOPD合并肺栓塞患者Caprini危险度分级与肺栓塞发病风险行Logistic回归分析,结果显示,Caprini危险度分级升高,肺栓塞发病风险也随之升高,高危、极高危重症患者肺栓塞发病风险均显著高于低危患者。这与国内外关于Caprini风险评估模型的验证结果基本一致[20],说明Caprini血栓风险评估模型在AECOPD合并肺栓塞中同样适用,对肺栓塞的发病风险有良好的预测价值。
综上所述,AECOPD住院患者肺栓塞的危险因素为糖尿病史、恶性肿瘤史、6周内手术史、下肢外伤史、脑血管意外史、长期卧床等。Caprini血栓风险评估量表可用于评估AECOPD肺栓塞病情和预后。
