重组人白细胞介素-11导致急性呼吸衰竭11例
2019-04-27何迎盈陈兆红张友才
何迎盈 陈兆红 赵 雷 张友才
重组人白细胞介素-11(recombinant human interleukin-11, rhIL-11)是肿瘤科常用药物,主要用于化疗后Ⅲ、Ⅳ度血小板减少症(即血小板≤50×109/L)及化疗相关性血小板减少症二级预防治疗[1-3]。rhIL-11因为起效快、半衰期短、安全性高,故广泛用于临床。近年来,随着我科收治的患者数量增加,使用rhIL-11的病例增加,发现部分患者在使用rhIL-11后出现呼吸困难,现对其中11例急性呼吸衰竭进行报道及分析,希望能帮助更多临床医师进一步认识rhIL-11的不良反应及如何治疗。
病例资料
11例患者为2008年12月至2017年12月在德阳市人民医院肿瘤科住院患者,其中男性患者7例(63.64%),女性患者4例(36.36%),60~69岁年龄组6例(54.55%),50~59岁年龄组4例(36.36%),40~49岁年龄组1例(9.09%)。11例患者中,6例肺癌(54.55%),1例肝癌(9.09%),1例鼻咽癌(9.09%),1例结肠癌患者(9.09%),1例乳腺癌(9.09%),1例食管癌(9.09%)。这些患者因接受2~4程化疗出现Ⅲ-Ⅳ度血小板减少,而接受rhIL-11升血小板治疗。给药方法为:50 μg/kg 皮下注射 每天1次。
患者以“气紧、胸闷、乏力”为主诉,伴不同程度的下肢水肿,甚至上肢水肿,为凹陷性水肿,有尿量的明显减少,体质量增加(3.65±1.22)kg,测末梢血氧饱和度(SpO2)下降明显,最低值约(47.25±8.98)%,血压在(101.5±15.8)mmHg。最早症状出现在使用rhIL-11后第3天,最迟在第8天,症状出现的平均时间为使用rhIL-11后第(5.12±1.62)天。
血常规、生化、血气分析、B型尿钠肽(brain natriuretic peptide, BNP)检查,提示血红蛋白由用药前的(105.06±15.81)g/L降至(85.19±12.82)g/L、白蛋白浓度由(35.82±4.60)g/L降至(29.84±4.34)g/L,BNP无明显异常,均值为(36.42±7.23)pg/ml,血气分析血氧浓度均值为(49.52±5.78)mmHg。胸腹部彩超发现7例浆膜腔积液,胸部CT见3例肺水肿,见图1~2。心电图见6例房颤。给予吸氧、利尿、改善通气、化痰、纠正酸碱失衡及电解质紊乱、控制心室率等治疗,肺水肿患者加用甲强龙治疗。经过治疗后,9例无肺水肿的患者1周内明显好转,3例肺水肿患者3周左右好转,无1例死亡患者。
图1 肺水肿及胸腔积液CT表现
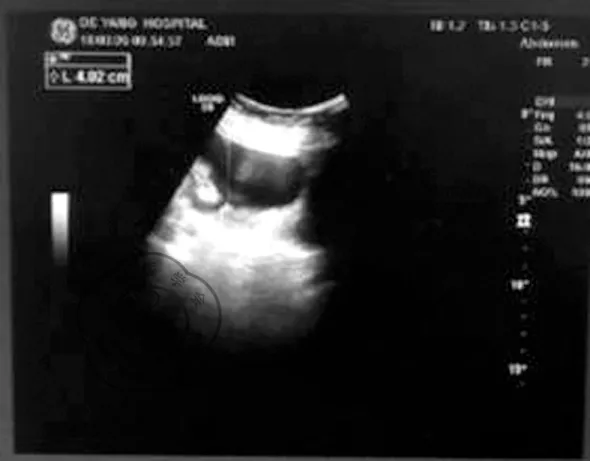
图2 胸腹腔积液彩超
讨 论
血小板降低是化疗后骨髓抑制主要表现之一,不仅增加了出血风险,威胁患者生命,还影响化疗进程。临床中,当患者出现Ⅲ、Ⅳ级血小板减少时,需要立即纠正,其中主要手段是皮下注射rhIL-11或重组人血小板生成素(recombinant human thrombopoietin, rhTPO)[4-5]。
IL-11是由骨髓基质细胞分泌的具有178个氨基酸的活性蛋白,通过直接刺激造血干细胞和巨核祖细胞增殖,促进造血干细胞和巨核细胞的增殖、分化、成熟,促进多阶段的巨核细胞和血小板的生成,进而提高外周血小板的数量[6]。IL-11升血小板作用确切,安全性高,较rhTPO价格明显便宜,故临床使用rhIL-11升血小板治疗更普遍。文献报道rhIL-11的主要不良反应为水肿、乏力、头晕头痛和肌肉、关节疼痛等,在停药后均能迅速消退[7-9]。
本组11例患者以“气紧、胸闷、乏力”为主诉,且伴有水肿、体质量增加、尿量减少的症状,其中有7例浆膜腔积液,3例典型肺水肿,符合毛细血管渗漏综合征(capillary leak syndrome, CLS)的表现。CLS是一种突发的、可逆性毛细血管高渗透性疾病,血浆迅速从血管渗漏到组织间隙而引起一组综合征,其中以水肿、低蛋白血症、低血压、体重增加常见,严重时可发生浆膜腔积液、肺水肿甚至多器官功能衰竭[10]。引起CLS的病因较多,如重症感染、严重创伤、烧伤、药物等,其根本机制为内皮细胞功能失调致微血管内皮通透性增高[11]。
白细胞介素类生物制剂可引 CLS[12]。CLS的诊断主要依靠临床表现和实验室检查,报道最多的病例为婴幼儿。在致病因素存在下,同时出现全身性水肿、血压及中心静脉压均降低、少尿、体质量增加、低蛋白血症、补充小分子晶体物质后水肿更加严重等,则可临床诊断为CLS。临床上分为毛细血管渗漏期和恢复期。渗漏期常持续1~4 d,血管内液体及大分子急剧渗出血管外,致严重低血压、全身水肿、浆膜腔积液、心脑肾等重要器官灌注不足,此时需及时恢复有效血容量;恢复期时毛细血管通透性增高现象逐渐改善,若继续大量补液,常可导致急性肺间质水肿、肺泡萎缩、气体弥散障碍、血氧含量下降、低氧血症,形成恶性循环,甚至导致死亡[13]。
临床上已有结肠癌和肝癌患者使用rhIL-11后出现CLS的文献报道,并提及呼吸困难,但未进行详细描述及分析[14-15]。此外,也有其他研究提及rhIL-11可致呼吸困难,但是否为急性呼吸衰竭未阐述,也未进一步分析rhIL-11导致呼吸困难发生的原因[3,16]。本文的11例患者的血气分析结果符合急性呼吸衰竭的诊断标准,结合他们具有CLS的临床表现,推测,rhIL-11导致的急性呼吸衰竭可能与CLS有关。
本组11例患者中,共有3例发生肺水肿,其中2例患者为肺癌,近期使用过2~3周期吉西他滨联合顺铂化疗,另1例为乳腺癌,近期使用过6程紫杉醇联合曲妥珠单抗靶向治疗。有文献报道,吉西他滨和曲妥珠单抗也可导致CLS。尽管在该3例患者中,不能明确将发生CLS的原因归结为使用rhIL-11,但提醒了我们,在经吉西他滨和曲妥珠单抗治疗后发生血小板减少的患者中,使用rhIL-11需更谨慎,因为有发生较严重的CLS的可能[17-18]。
rhIL-11所致急性呼吸衰竭是否还有其他原因?本文发现这11例患者在无急慢性出血的情况下,均发生了不同程度血红蛋白浓度下降,临床可诊断为中度贫血,其原因除考虑与化疗相关外,还可能与rhIL-11的使用有关[19-21]。血红蛋白的功能之一为携氧,贫血意味着血液携氧能力降低,可进一步加重这些已出现CLS患者的缺氧症状,促进急性呼吸功能衰竭的发生[22-23]。
另外,在11例患者中,有6例发生房颤,均为60~69岁年龄段的患者。IL-11和IL-6是细胞因子IL-6家族中唯一经典成员,IL-6受体和IL-11受体之间可以互换,IL-11和IL-6需结合至受体才能进行信号转导,IL-6受体基因多态性与房颤的发生密切相关,研究显示rhIL-11可诱发房颤,且诱发风险与年龄相关。另外,低氧血症也可诱发房颤发生,房颤又会导致心排出量降低,进一步加重低氧血症,可能促进急性呼吸衰竭的发生[25-27]。
除此以外,全胸部放疗可诱导缺氧性呼吸衰竭,胸腔积液和心脏重塑[28]。本组11例患者中有8例患者接受过胸部放疗(72.73%),放疗总剂量在50-64Gy,这是否为该类患者使用rhIL-11后易发生急性呼吸衰竭的另外一个原因,由于样本量较小,暂无法进一步分析,尚需要收集更多的类似病例进行进一步的临床研究。
综上所述,由rhIL-11诱发的急性呼吸衰竭起病较急,症状无特异性,易和血源性水肿、肺部感染、急性心力衰竭、肺梗塞等相混淆,加上目前这方面报道较少,无标准治疗方案,所以临床对于此类患者的处理需要谨慎。恢复正常循环血容量,保证有效灌注,改善毛细血管通透性及循环功能,维持足够氧供,纠正心律失常,保持水电解质和酸碱平衡是常规处理。但需注意,液体管理是CLS治疗的关键,可能也是该类患者的治疗关键[29-30]。
