柱前衍生结合高效液相色谱-荧光检测法测定人体血浆中脂肪酸
2019-04-25高永平
高永平*
(信阳学院理工学院应用生物化学研究所,河南信阳 464000)

图1 DPPIPE结构式Fig.1 The structure of DPPIPE
医学研究发现,随着社会的发展和人们生活条件的提高,肥胖问题对人们工作和生活的影响凸显。国际糖尿病联盟预计,到2035年全球糖尿病患者将达到5.92亿[1]。研究发现,膳食脂肪酸是造成糖尿病发病的重要因素之一。目前检测脂肪酸的方法多种多样,但或多或少存在不足和缺陷。常用的如重氮甲烷类试剂和溴代香豆素类化合物[2 - 3],不足之处是对水、潮气不稳定,需要在无水环境中进行;溴甲基类化合物和NOEPES磺酸酯对脂肪酸类化合物[4 - 5],缺陷之处是衍生过程需借助催化剂,并且分离前还需要预处理,费时费力。胡娜等[6]采用2-(11-H-苯-a-咔唑)乙基对甲苯磺酸酯对脂肪酸类化合物进行了测定,但存在衍生化过程温度高,样品色谱分离所需时间过长。柱前衍生结合高效液相色谱-荧光检测法,因其优越的选择性和灵敏度,已发展为一种行之有效的检测手段[7 - 8]。
本文采用高灵敏度荧光试剂1-[1-(哌嗪)乙酮]-2-[(4-二甲氨基)苯基]-菲[9,10-d]咪唑(DPPIPE)作为柱前衍生化试剂(结构见图1),对8种混合脂肪进行衍生,衍生物采用高效液相色谱-荧光法测定实现了样品中混合脂肪酸衍生物分离分析,并对人体血浆中微量脂肪酸实现了简单、灵敏、快速、准确的测定。
1 实验部分
1.1 仪器与试剂
高效液相色谱-质谱联用仪(美国,Agilent公司),采用大气压化学电离源(APCI),附Agilent 1100离子阱,配备四元梯度泵、自动进样器、在线真空脱气机和荧光检测器。
DPPIPE(自制),哌嗪(分析纯),N,N′-羰基二咪唑(CDI,分析纯),4-二甲基胺吡啶(DMAP,分析纯),乙腈(ACN,光谱纯),N,N-二甲基甲酰胺(DMF,色谱纯),1-乙基-(3-二甲基氨基丙基)碳二甲胺盐酸盐(EDC,分析纯)。18种脂肪酸标准样品(美国Sigma公司):乙酸(C2);丙酸(C3);正丁酸(C4);戊酸(C5);己酸(C6);庚酸(C7);辛酸(C8);壬酸(C9);癸酸(C10);十一酸(C11);十二酸(C12);8,11,14-十八碳三烯酸(C18∶3);十四酸(C14);9,12-十八碳二烯酸(C18∶2);十六酸(C16);12-十八碳烯酸(C18∶1);十八酸(C18);二十酸(C20)。
血浆样品由信阳中心医院血液检测中心提供。
1.2 实验方法
1.2.1实际样品处理在离心管中依次加入血浆样品100 μL,2 mL磷酸盐缓冲液(pH=6.5),用6 mL氯仿-正己烷(体积比1∶1)分2次萃取,离心,合并上清液,用2 mL乙腈振荡溶解,备用。
1.2.2标准溶液的配制分别定量称取8种脂肪酸标准品,用乙腈配制成2.0×10-2mol·L-1的溶液(长链脂肪酸可加适量DMF助溶)。准确称量27.15 mg DPPIPE,用DMF配制成10 mL 5.0×10-2mol·L-1溶液。低浓度的衍生试剂(5.0×10-3mol·L-1)和脂肪酸(1.0×10-4mol·L-1)的标准液分别用DMF、乙腈稀释而成。
1.2.3标准品的衍生向2 mL安培瓶中,依次加入100 μL EDC,100 μL DMAP,100 μL(5.0×10-3mol·L-1)衍生试剂,50 μL 2.0×10-4mol·L-1的脂肪酸标准品,100 μL乙腈,密封65 ℃恒温水反应1 h,自然冷却后,直接进样分析。衍生反应见图2。

图2 DPPIPE与脂肪酸衍生反应图Fig.2 Scheme showing the derivatization of DPPIPE with fatty acids
1.2.4色谱与质谱条件Hypersil BDS C-8色谱柱(150×4.6 mm i.d.,5 μm;大连依立特公司)。流动相A:50%乙腈水溶液,B:100%乙腈。梯度条件:0~30 min,A由60%到0,B由40%到100%。流动相流速为1.0 mL·min-1,柱温30 ℃,进样量20 μL。最大激发波长:260 nm,最大发射波长:430 nm。正离子模式,干燥气流量:9 L·min-1,干燥气温度:350 ℃,喷雾压力:35 psi,电晕电流:4 000 μA(Pos),毛细管电压:3.5 kV。
2 结果与讨论
2.1 衍生条件的优化
DPPIPE与脂肪酸的衍生化效率,随试剂倍数(衍生试剂量与标准品量的比值)、催化剂/缩合剂、衍生时间、衍生温度的不同存在显著差异。本实验选取C12、C14、C18∶2、C18∶1、C20,考察了试剂倍数(2、4、6、8、10倍)对衍生化效率的影响,结果表明试剂倍数为6时衍生化产率最高,而随着试剂倍数的增大衍生化效率反而降低,可能原因是随着衍生试剂倍数的增大,过多的衍生试剂覆盖了标准品,导致被覆盖的标准品无法充分进行衍生反应。同样对其他影响因素进行了考察,结果表明:EDC和DMAP均取100 μL,衍生时间为1 h,衍生温度为65 ℃时最佳。
2.2 高效液相色谱分离
依照上述优化条件,本文选取C2、C3、C4、C5、C6、C7、C8、C9、C10、C11、C12、C18∶3、C14、C18∶2、C16、C18∶1、C18、C20共计18种脂肪酸标准品进行衍生化。结果发现,C2~C11短链的脂肪酸衍生物色谱峰与衍生试剂峰重叠,因而选取对C12~C20这8种脂肪酸标准品进行衍生化并进行定性定量分析,结果显示:26 min内可实现8种目标脂肪酸混合标准品的基线分离,见图3。
2.3 线性回归方程、检出限和重现性
在相同条件下,对上述8种目标脂肪酸进行分析测定,各脂肪酸衍生物的回归方程、检出限和相关系数,见表1相关数据。按照峰面积(y)、实际进样量(x)进行线性回归。结果显示:各脂肪酸衍生物的线性范围:4.40~13.75 pmol,相关系数范围:0.9986~0.9999,检出限(信噪比S/N=3)为0.290~0.593 pmol;峰面积相对标准偏差(RSD)<0.5749%;保留时间的RSD<3.767%。
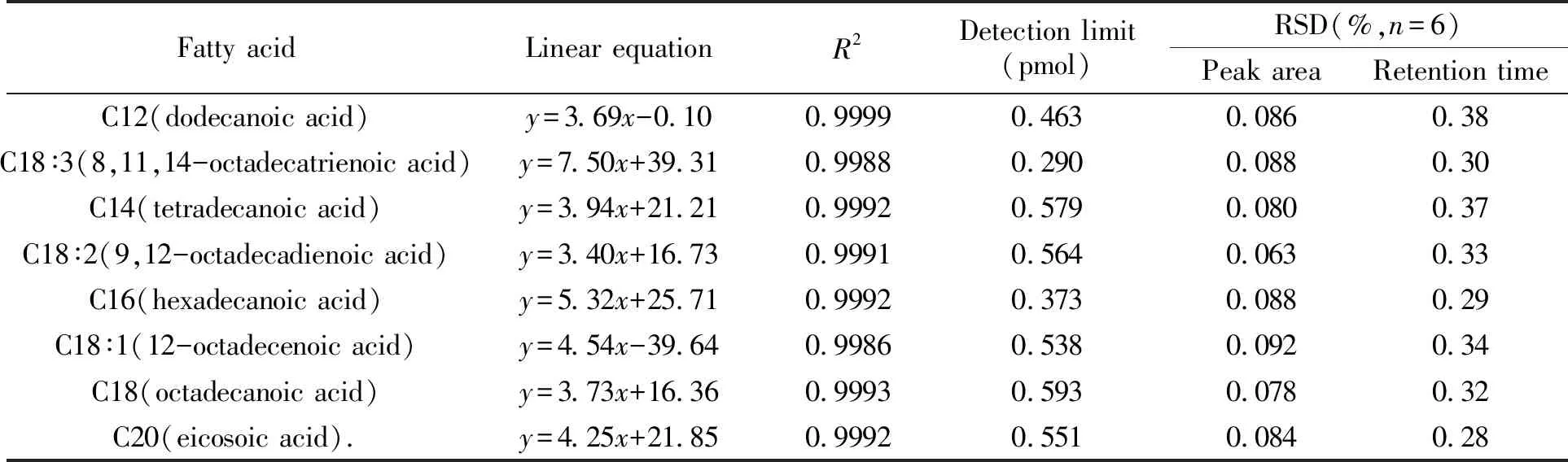
表1 脂肪酸衍生物线性方程、相关系数(R2)、检测限和精密度(RSD)

图3 标准脂肪酸衍生物总离子流(TIC)色谱图Fig.3 TIC chromatograms for standard fatty acid derivatives The number of peaks are the same as Table 1.

图4 血浆样品中脂肪酸衍生物的色谱分离图Fig.4 Chromatogram of fatty acid derivatives from plasma The number of peaks are the same as Table 1.
2.4 回收率和实际样品的测定
血浆样品按照实验方法处理,并按照优化条件衍生,得到各脂肪酸的回收率范围为98.72%~101.9%。在相同的实验条件下,得到人体血浆样品中脂肪酸衍生物的色谱分离图(图4)以及各脂肪酸的测定结果(表2)。

表2 实际样品中脂肪酸的测定结果(n=6)
"-"Not detected.
3 结论
本实验以自制荧光探针DPPIPE作为柱前衍生试剂,采用高效液相色谱-荧光检测技术,通过对衍生以及色谱条件的优化,实现了8种脂肪酸的分离分析,并对人体血浆中脂肪酸的含量进行了测定。本实验对相关疾病发病机理的研究,疾病诊断以及其预防提供有益参考。
