炭基辅料对羊粪好氧堆肥中氮素损失的影响
2019-04-22王海候陶玥玥金梅娟陆长婴施林林周新伟沈明星
王海候,何 胥,陶玥玥,金梅娟,陆长婴,施林林,周新伟,沈明星*
(1.江苏太湖地区农业科学研究所/农业部苏州水稻土生态环境重点野外科学观测试验站,江苏 苏州 215155;2.江苏省安丰生物源农药工程中心有限公司,江苏 太仓 215400)
现代“草-羊-田”农牧循环生产技术模式是江苏苏南经济发达地区生态循环农业发展的一项最新研究成果。针对稻麦秸秆综合利用,构建了“种植废弃物(秸秆)-养殖生产资料(饲料)-畜产品(肉羊)-养殖废弃物(羊粪)-种植生产资料(有机肥)-农产品(稻米)-种植废弃物(秸秆)……”农牧废弃物多级增值利用的循环链,与种养分离传统产业相比,种养结合循环产业净收益增加了45%。在这一技术模式中,养殖废弃物(羊粪)的堆肥化处置是实现“物质链、技术链、价值链”三链融合的重要环节,然而,羊粪有机肥生产过程中,羊粪C/N较低(16~18),而稻麦秸秆等高C/N生物质绝大部分被裹包青贮并用于生产养殖饲料,羊粪堆肥化处置中辅料添加量远小于实际需求量,导致堆肥过程中氮素养分损失较大(>45%),不仅降低了羊粪有机肥的农用价值,而且还造成了养分资源的流失,增加了环境污染风险[1-2]。因此,有效控制并减少羊粪有机肥生产过程中的氮素养分损失是“草-羊-田”农牧循环生产技术模式生态绿色发展的关键环节,影响着该项技术模式的应用前景。
炭基辅料是笔者所在课题组利用树枝等生态林地废弃物,采用生物质炭化设备,通过生物质非充分炭化方法(即生物质表层充分炭化,而内部不完全炭化),研制的一种新型生物质炭,呈粒块状,表层为生物质炭,内部仍然为木质化结构。目前已有许多研究报道了生物质炭应用于堆肥工程中具有较好的固氮作用[3-7],笔者将炭基辅料(粒径6~7 cm)应用于猪粪堆肥过程,堆肥体氮素损失率较对照处理降低了22.8%[8],由于不同类型畜禽粪便具有不同的理化性质[9-11],并且有关羊粪好氧堆肥过程氮素养分损失及控制技术的报道涉及较少[12-13],为此,本文将炭基辅料与羊粪、稻草混合,采用模拟堆肥的方法,研究炭基辅料对羊粪堆肥中温度、氮素形态转化等指标的影响,以期为羊粪堆置过程氮素损失控制及堆肥质量提高提供技术支撑,为炭基辅料在羊粪有机肥生产中的应用提供理论依据。
1 材料与方法
1.1 试验材料
羊粪来源于太仓市城厢镇东林生态羊场,有机碳质量分数为35.6%、全氮质量分数为2.04%、含水率为71.2%。稻草取自太仓市城厢镇东林农场,有机碳质量分数为41.5%、全氮质量分数为0.71%、含水率为16%,用秸秆粉碎机进行3~5 cm切碎处理后备用。炭基辅料由项目组自制,原材料为园林废弃修剪树枝(由常熟市园林住建局提供),选择直径6~7 cm的废弃树枝进行长度6~7 cm切割,然后置于热解炉中(由张家港天源机械厂提供),在无氧条件下经700℃热解处理,热解时间为90 min,之后冷却、备用。炭基辅料如图1所示,粒径6~7 cm,其表层实质为生物质炭,仅在参与堆肥过程的形态规格上区别于常规的粉末状生物质炭。

图1 炭基辅料Figure 1 Carbonaceous amendment
1.2 试验设计与概况
堆肥试验于2016年9—10月,采用静态堆置高温好氧发酵的方法,在太仓东林生态肥料厂进行。试验共2个处理,以羊粪与稻草重量比9∶1混合体为对照(肥料厂常规操作方式),参照项目组前期研究[7],在对照基础上添加重量占比15%炭基辅料为处理,分别用CK、CA表示。CK处理的物料组成为:900 kg羊粪与100 kg稻草充分混匀;CA处理的物料组成为:900 kg羊粪、100 kg稻草及150 kg炭基辅料充分混匀。
混合堆肥体含水率均控制在65%~70%,各处理堆肥物料按等量均分为3份,分别装入3个堆肥反应器内(3次重复),称量每个堆肥反应器内物料质量。堆肥反应器呈立方体箱形,容积为1 m3,采用厚度为2 cm的PVC板,通过塑料焊条拼装而成;反应器底部靠近边角处安装4个活动轮(高度为25 cm);底面均匀分布直径为2 cm的圆形通气孔,通气孔面积总和约为底部面积的1/3;箱壁覆盖海绵(厚度为15 mm)及铝箔胶带,在箱壁正中间布置3个测温孔(直径2 cm),垂直方向等距排列;反应器顶部无盖。当堆体温度超过75℃时或每隔7 d左右翻堆1次,采用人工将箱内物料全部取出,充分混合并称量每堆体物料质量后再次装箱;堆肥结束后,称量堆肥物料的最终质量。
1.3 测定指标与方法
(1)堆温:堆肥过程中,每日10:00或16:00左右,用长度为60 cm的红水温度计,在堆肥反应器上、中、下位置,测定堆肥体内部30 cm左右深处的温度,直至堆肥结束,同时测定气温,并按日期记录温度数据。
(2)堆肥物料各形态氮素含量:堆制后第1、3、7、13、18、27、34 d,每个堆肥反应器内多点取堆肥混合样品2 kg,带回实验室。堆肥样品在实验室内分成3份,一份采用105℃烘干法测定堆肥样品的水分,一份制取新鲜样品的浸提液,一份置于阴凉处进行风干处理。浸提液的制取方法为:称取鲜样40 g放入塑料瓶中,加400 mL去离子水,盖紧瓶盖后置于振荡器内(150 r·min-1),振荡浸提30 min后过滤,收集滤液并做好标记。浸提液测定铵态氮、硝态氮(SKALA流动分析仪)等。风干的堆肥样品进行100目粉碎后,测定凯氏氮(浓硫酸-双氧水消煮、凯氏定氮法),全氮含量为凯氏氮与硝态氮之和、有机氮含量为凯氏氮与铵态氮之差。堆肥样品灰分(马弗炉550℃灼烧法)仅测定了第1 d与第34 d采集的样品。
(3)NH3挥发速率及累积量:NH3挥发收集装置如图2所示,底部为圆环形槽状底座(高8 cm、槽深3 cm、圆环内径18 cm、圆环外径22 cm);中部为开口向下的圆柱形透明有机玻璃箱(直径为20 cm,高度30 cm),玻璃箱内部放置一个250 mL的玻璃烧杯,玻璃箱顶部设有1个通气孔;上部为通气孔与乳胶软管连接,乳胶软管向上延伸至2.5 m高。堆肥开始后,将装有50 mL质量分数为2%硼酸吸收液的玻璃烧杯,放入氨挥发收集装置内,每日观察装置内硼酸的颜色变化,若颜色由红变绿,则需置换硼酸溶液,置换下来的硼酸溶液用保鲜膜盖好,带回实验室立即用稀硫酸(0.05 mol·L-1)溶液进行滴定分析,并记录稀硫酸用量,直至堆肥结束。将1 d内玻璃箱装置收集的氨挥发量乘以31.85(堆肥反应器与氨挥发收集装置的面积比),再与堆肥体质量(每次翻堆时称重)的比值即为单日的氨挥发量。氨挥发累积量[7]:堆肥过程中每日氨挥发量的总和。
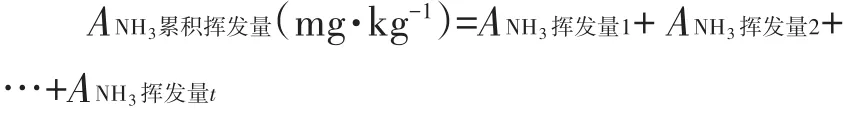
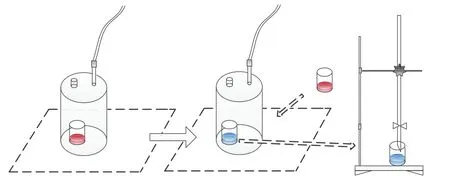
图2 NH3挥发测定示意图Figure 2 Schematic diagrams of measuring ammonia volatilization
(4)N2O排放通量及累积量:采用静态气体采集箱-气相色谱法。N2O气体采集装置如图3所示:底部为方环形槽状底座(高8 cm、槽深3 cm、方环内边长18 cm、方环外边长22 cm);上部是一个开口向下的长方体箱体(长 20 cm、宽20 cm、高30 cm,容积为12 L),采用厚度为1 cm的PVC板,通过塑料焊条拼装而成;在箱体其中一面的2/3高度正中间设置一个取气孔,取气孔用色谱级软胶垫进行密封处理;箱体外表用铝箔胶带进行覆盖处理。分别于堆肥开始后1、3、7、13、18、27、34 d,进行 N2O 气体样品采集与测定。于9:00—11:00,各处理反应器上安装气样采集箱底座,盖上气体采集箱,水密封,于0、5、10、15 min后分别用针筒抽气100 mL,转移至100 mL铝箔气样袋,待分析。每个反应器重复3次。利用气相色谱仪(岛津GC-14B)测定气样中N2O的浓度。N2O排放通量:
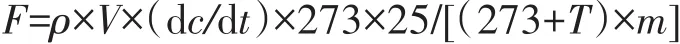
式中,F为N2O气体日均排放量,mg·kg-1·h-1;ρ为被测气体标准状态下的密度,N2O为1.978 kg·m-3;V为取样箱顶部空间的体积,m3;dc/dt为采样箱内被测气体的浓度变化率;T为采样过程中采样箱内的平均温度,℃;25为堆肥反应器与N2O气体采集装置的面积比;m为堆体干基质量,kg。N2O排放累积量:将相邻2次取样时间点的N2O排放通量平均值与该段时间的乘积,得出某一时间段的N2O排放量,再将各时间段N2O排放量依次叠加。
(5)氮素损失率[14]:根据堆制腐熟过程中灰分无损失(绝对量不变),推导氮素损失率的计算公式:
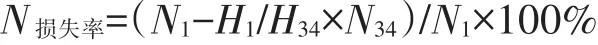
式中,N1为堆肥开始前全氮质量分数(以干基计),%;H1为堆肥1 d时灰分含量分数,%;N34为堆肥为34 d时全氮质量分数,%;H34为堆肥34 d时灰分质量分数,%;
(6)保氮效率:
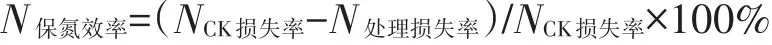
1.4 数据处理与统计分析
数据采用Microsoft Excel 2010整理、SPSS 23.0进行统计分析。
2 结果与分析
2.1 堆肥过程中的温度变化
温度是反映堆肥过程中微生物活动能力、有机物降解速率及是否达到无害化要求的重要过程参数之一[15]。由图4可知,整个堆肥过程中,堆肥温度总体呈先上升后下降的变化趋势,每次翻堆后,堆肥温度有小幅度的上升,但之后均呈现逐渐下降的变化趋势。堆肥后第1~7 d,2个处理的堆肥温度均快速上升,但CA处理的堆肥温度上升速度明显快于CK处理,CA处理的堆肥温度在第2 d达最大值(76.83℃)、CK处理在第7 d达最大值(67.35℃);堆肥第8~34 d,CA处理的堆肥温度总体上大于CK处理,但差异幅度较小。本试验中CA、CK处理的堆肥温度在55℃以上维持了18~20 d,符合高温堆肥无害化和腐熟条件[2]。
2.2 堆肥过程中不同形态氮素含量变化
图5为堆肥过程中各形态氮素含量的动态变化曲线,由图5可知,2个处理的全氮、有机氮含量均呈下降的变化趋势,CA处理的全氮、有机氮含量均高于CK处理。
堆肥过程中CA处理的铵态氮含量小于CK处理(图3),在整个堆肥进程中,CK处理的铵态氮含量先呈现小幅度的上升,在堆肥第2 d达到最大值(2.26 g·kg-1),之后一直表现为下降的变化趋势;CA处理的铵态氮含量呈下降的变化趋势,其中在第7~13 d的变化幅度较大,第13~34 d的变化幅度较为平缓。堆肥过程中CA、CK处理的硝态氮含量在第1~3 d差异较小,CA处理的硝态氮含量在第7~34 d明显低于CK处理,其中CK处理的硝态氮含量在堆肥第3~7 d上升幅度最大。
2.3 堆肥过程中的含氮气体排放
2.3.1 NH3挥发
由图6可知,堆肥过程中2个处理的NH3挥发速率总体上均表现为先上升后下降的变化趋势,且不同处理的堆肥体NH3挥发速率表现不同,整个堆肥过程中CA处理的NH3挥发速率明显低于CK处理。堆肥第1~7 d,2个处理的NH3挥发速率均快速上升,在第6 d达最大排放峰值,不同处理的NH3挥发速率表现为CK>CA;堆肥第8~34 d,堆肥体的NH3挥发速率总体呈下降的变化趋势,但每次翻堆措施对CK处理NH3挥发速率的促进作用明显大于CA处理。
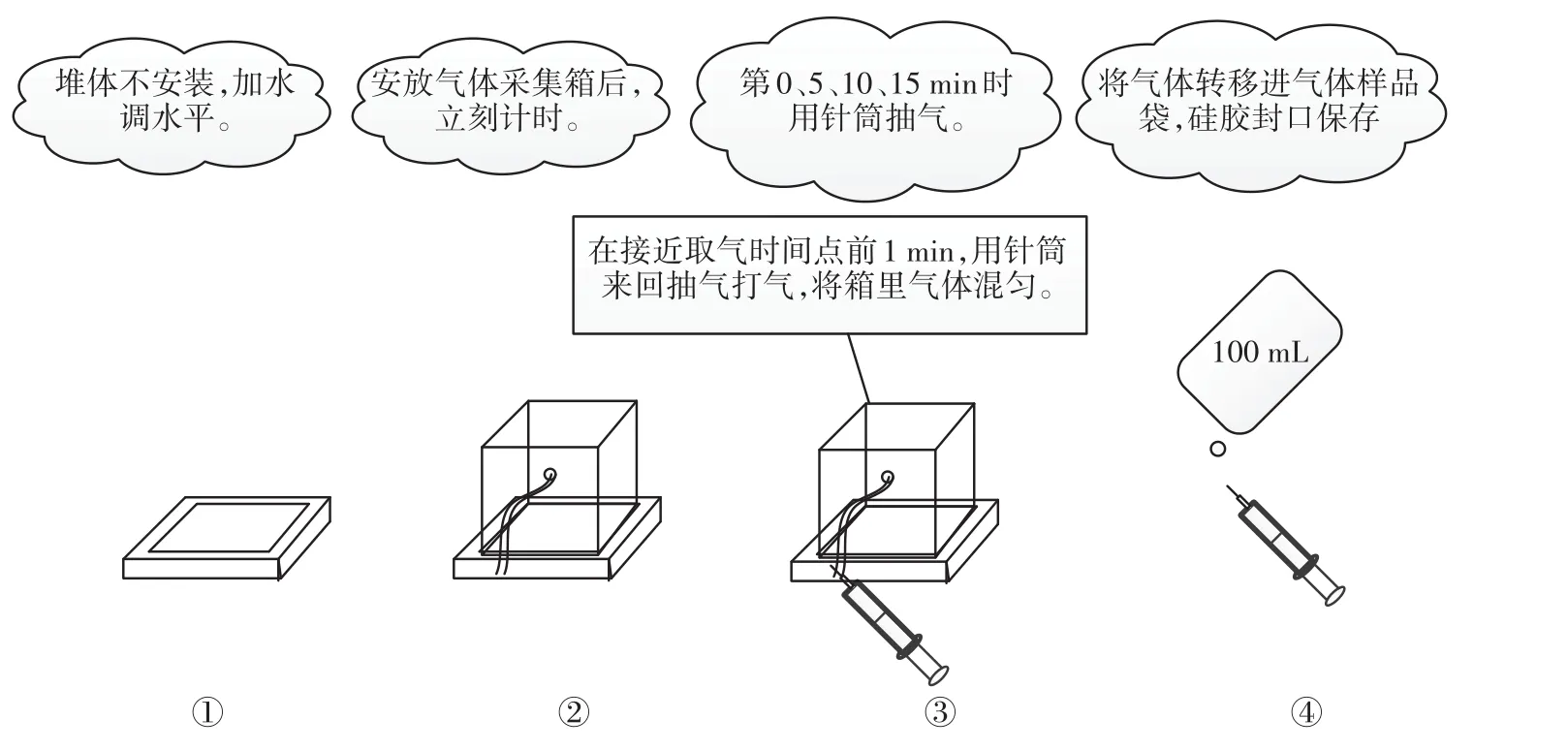
图3 N2O排放测定示意图Figure 3 Schematic diagrams of measuring N2O emissions
从堆肥体NH3累积挥发量来看(图6),堆肥后第1~7 d,所有处理的NH3挥发累积量均快速上升,第7 d时CK处理的堆肥体NH3挥发累积量大于CA处理,但差异不显著(P>0.05);堆肥后第8~14 d,CK处理的堆肥体NH3挥发累积量增长迅速,且显著高于CA处理,第14 d时CK处理的堆肥体NH3挥发累积量显著大于CA处理(P<0.05);堆肥后第15~34 d,CK处理的堆肥体NH3挥发累积量仍然呈快速上升的趋势,而CA处理的堆肥体NH3挥发累积量变化幅度逐渐平缓,且在堆肥后期几乎无增加,堆肥第34 d时,不同处理的堆肥体NH3挥发累积量差异性达显著水平(P<0.05),主要表现为CK处理(368.38 mg·kg-1)>CA处理(175.63 mg·kg-1);整个堆肥过程中CA处理的NH3挥发累积量较CK处理降低了52.32%。
2.3.2 N2O排放
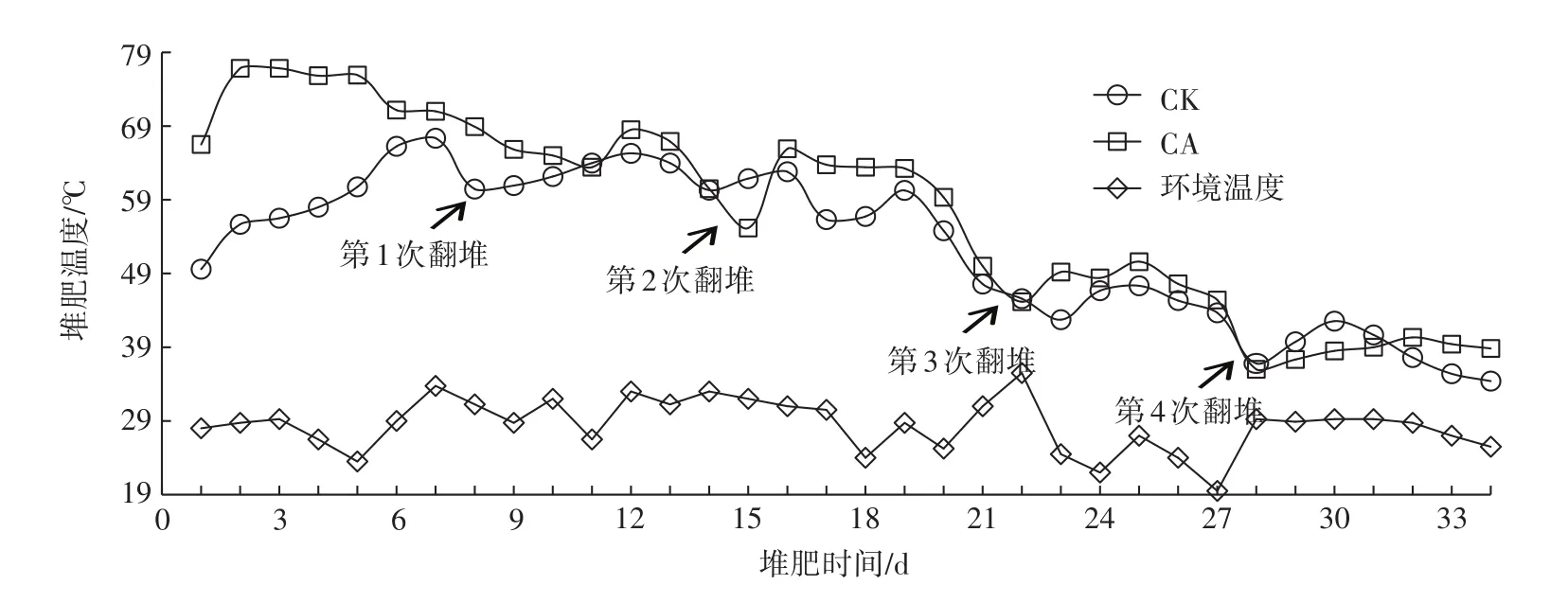
图4 堆肥过程中温度变化Figure 4 Temperature dynamics during composting
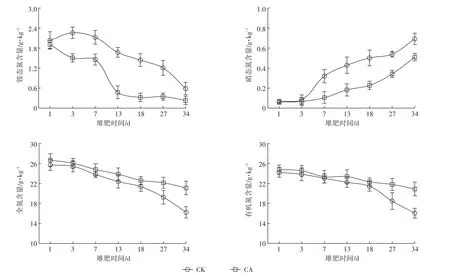
图5 堆肥过程中各形态氮素变化Figure 5 Changes of different nitrogen forms during composting
由图7可知,堆肥进程中,2个处理的堆肥体N2O排放速率均呈先上升后下降的变化趋势,且N2O排放速率在堆肥第18 d时达最大值。堆肥第1~7 d,CA处理的N2O排放速率显著大于CK处理(P<0.05),且上升趋势的变化幅度大于CK处理;堆肥第7~18 d,CK处理的N2O排放速率快速上升,虽然CA处理的N2O排放速率依然大于CK处理,但差异不显著(P>0.05);堆肥第18~34 d,2个处理的堆肥体N2O排放速率快速下降。整个堆肥过程中,CA处理的N2O排放速率均大于CK处理。
根据堆肥体N2O排放累积量分析结果,CA处理的N2O排放累积量大于CK处理,在堆肥第1~3 d差异幅度较小,在堆肥第7~34 d差异幅度逐渐增大。堆肥结束后2个处理的N2O排放累积量分别为:CA处理88.94 mg·kg-1,CK处理50.38 mg·kg-1,CA处理的N2O排放累积量较CK处理增加了76.53%,但无显著差异性(P>0.05)。
2.4 堆肥前后各形态氮素的变化率及保氮效果
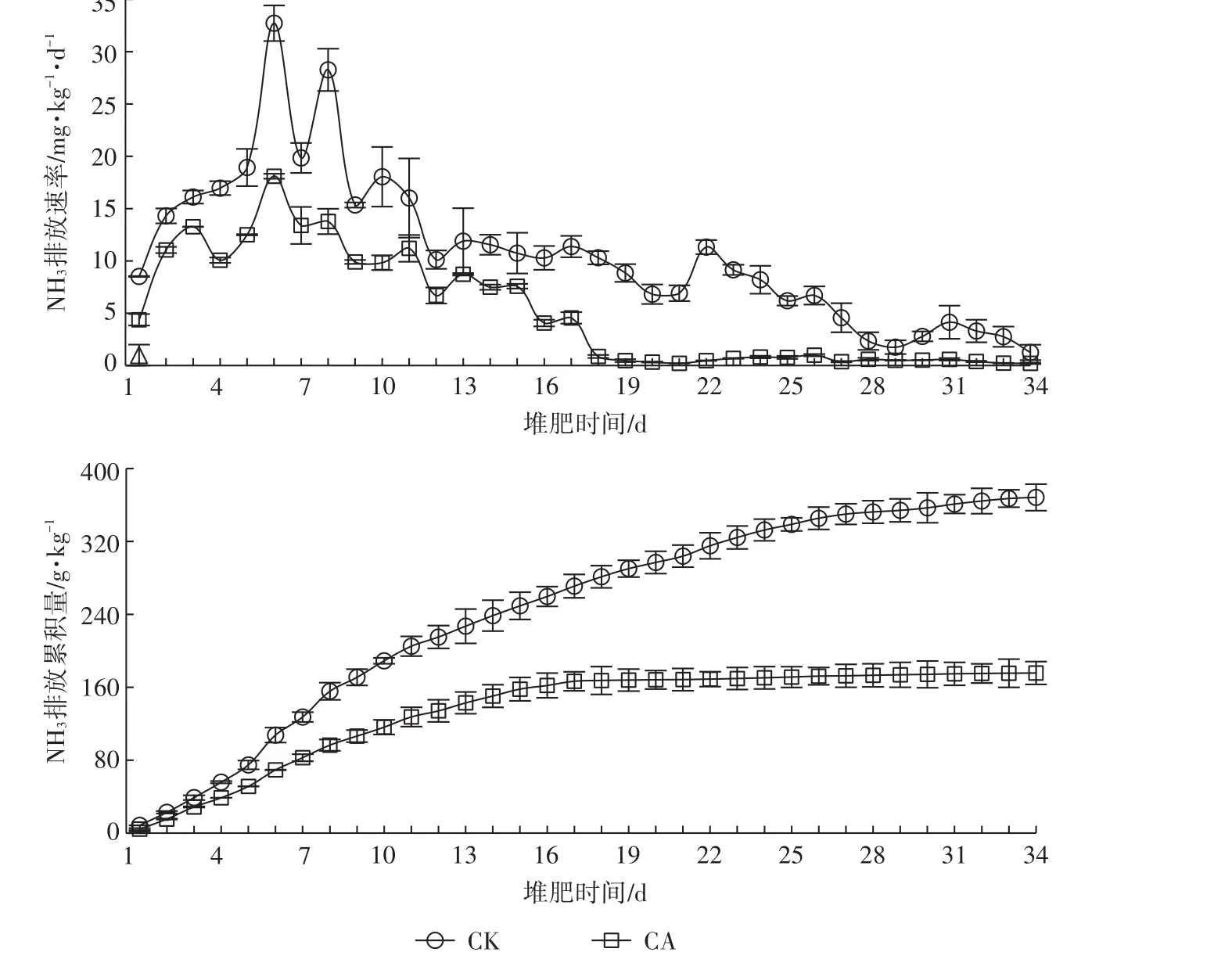
图6 堆肥过程中氨挥发的变化Figure 6 Emission rate of NH3during composting process
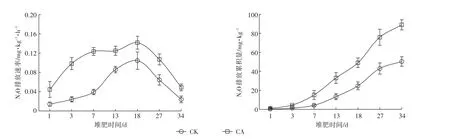
图7 堆肥过程中N2O排放的变化Figure 7 Emission rate and accumulative amount of N2O during composting process

表1 堆肥前后各形态氮素的变化率及保氮效果(%)Table 1 Loss percentage of different nitrogen forms and effect of nitrogen conservation during composting(%)
堆肥前后各形态氮素的变化率如表1所示,由表1可知,堆肥过程中硝态氮的变化率最大、铵态氮其次,但2个处理之间无显著差异性(P>0.05),CA处理的有机氮、全氮含量的变化率显著小于CK处理(P<0.05)。根据有机物料堆制腐熟过程中灰分无损失的原理[20],计算氮素损失率。CK、CA处理的氮素损失率分别为50.49%、32.63%,CA处理的氮素损失率显著小于CK处理(P<0.05)。与CK处理相比,CA处理的保氮效率为35.37%。
3 讨论
3.1 炭基辅料对羊粪堆肥温度的影响
众多研究均表明,生物质炭具有加快堆体升温的作用[8,16-18],如李丽劼等[19]研究发现,在猪粪堆肥中添加适量的竹炭有利于提高堆体温度,加快堆肥腐熟进程;本试验结果表明,与CK处理相比,羊粪堆肥中添加炭基辅料,可以促进堆肥后第1~7 d堆肥温度快速上升,CA处理的堆肥温度在第2 d达最大值(76.83℃)、CK处理在第7 d达最大值(67.35℃),与生物质炭丰富的孔隙结构有关,促进了微生物的扩繁增殖,激发了微生物活性,提高了堆肥前期微生物的代谢与产热能力[20-22];但在堆肥第8~34 d,CA、CK处理堆肥温度差异幅度较小,其原因可能是堆肥物料中羊粪呈颗粒状[12],堆肥体形成了较好的自由空域,提高了堆料中氧气含量,有利于微生物活动[23-24],CK处理的微生物由于缺少激发作用,经历7 d的扩繁增殖才逐渐达到了添加炭基辅料的效果。然而,有关羊粪堆肥过程中温度上升与堆肥体自由空域值的关系、生物质炭添加量与堆肥体微生物代谢与产热能力的关系尚不明确,有待进一步的研究。
3.2 炭基辅料对羊粪堆肥过程氮素转化及损失的影响
氮素在堆肥过程中的转化主要包括有机氮的矿化、硝化和反硝化、NH3吸附和挥发以及有机氮的合成[25]。一方面有机氮经矿化作用转化为无机氮,部分以NH3形式挥发损失,部分与水结合形成在硝化细菌的作用下进一步转化为、N2O,部分经反硝化作用产生N2、N2O等[26];另一方面通过微生物的代谢合成可将部分氮素转化为腐殖质的一部分[27]。本试验结果表明,添加炭基辅料降低了羊粪堆肥体的、含量,且显著减少了NH3挥发累积量,堆肥34 d后CA处理的NH3挥发累积量较CK处理降低了52.32%,与许多已经报道的研究结论相同[2-7],然而,关于添加生物质炭减少堆肥过程氨挥发的原因分析,观点不一:一是认为生物质炭可以直接物理吸附NH+4、NO-3、NH3等氮素物质,并认为物理吸附为主要吸附方式[5-7,28~29],从而减少堆肥过程的氮素损失;二是认为生物质炭表面含有丰富的羧基和酚羟基等酸性官能团,这些酸性官能团通过离子键与堆体中的NH4+结合,并在微生物作用下促使NH+4向其他更复杂的腐殖质态氮素形式转变,从而减少堆肥过程的NH3挥发[30-31],同时,堆肥中来源于NH+4的硝化作用,在硝化底物降低条件下也相应降低[26];笔者认为生物质炭固定氮素过程中物理、化学吸附方式并存,并且不同形态氮素先通过物理吸附迅速固定,而铵态氮向腐殖态氮转化是一个缓慢的过程;但是,有关堆肥过程中生物质炭的保氮作用方式及机理尚不清晰,有待进一步研究。另外,本试验结果表明,羊粪堆肥过程的N2O排放通量呈先上升后下降的变化趋势,在堆肥第18 d达排放峰值,N2O在堆肥前期(0~7 d)的排放累积量很低,之后逐渐快速上升,这主要是因为堆肥的高温期,硝化细菌的生长繁殖受到抑制,之后堆温逐渐下降,硝化作用增强[32-33];但是,添加炭基辅料增加了羊粪堆肥过程N2O排放速率与通量,而付祥峰等[16]认为生物质炭应用于猪粪堆肥过程可以显著降低堆肥体的N2O排放;一般认为,生物质炭可通过改变堆肥体温度、含氧量、pH值、含水率、氮素含量等环境因子,影响氮素循环相关的功能微生物,进而影响堆肥体中硝化与反硝化作用[34];生物质炭具有多孔性和巨大的比表面积,刘宁等[6]认为生物炭能为硝化细菌等微生物群落提供相对适宜的庇护场所,以抵御高温等恶劣的外部环境,利于微生物群落的繁衍和降解活动,促进硝化细菌将NH+4转化成NO-3,通过促进硝化作用来抑制氨挥发;本试验结果表明,粒径为6~7 cm的颗粒状炭基辅料,在堆体内形成孔隙结构,有利于促进堆体含水率的降低(表2),从而有效改善了羊粪堆肥体含氧量等环境因子,与CK相比,CA处理N2O排放增加,可能主要来源于NH+4被物理吸附后的硝化过程。
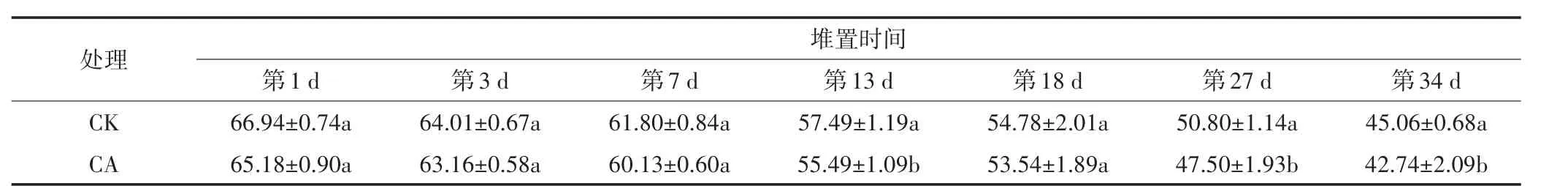
表2 堆肥过程含水率变化(%)Table 2 Change of moisture content during composting process(%)
4 结论
(1)与CK处理相比,添加炭基辅料(CA)明显促进了堆肥后第1~7 d堆肥温度快速上升,但堆肥第8~34 d,两处理间的堆肥温度差异较小。
(2)堆肥34 d后,CK、CA处理的氨挥发累积量分别为368.38、175.63 mg·kg-1,氧化亚氮排放累积量分别为50.38、88.94 mg·kg-1,氮素损失率分别为50.49%、32.63%;羊粪堆肥过程中氨挥发是氮素损失的主要途径,添加炭基辅料显著降低了羊粪堆肥体的氮素损失率(P<0.05),炭基辅料在羊粪有机肥生产中的保氮效率可达35.37%。
