十一烯酸/马来酸酐共聚物的制备与表征
2019-04-17吴美婷张永贺金立维
吴美婷, 张永贺, 金立维*
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业局 林产化学工程重点开放性实验室;江苏省 生物质能源与材料重点实验室, 江苏 南京 210042;2.中国林业科学研究院 林业新技术研究所, 北京 100091)

1 实 验
1.1 材料与仪器
10-十一烯酸(UA)、马来酸酐(MAH)、偶氮二异丁腈(AIBN)、甲苯、四氢呋喃(THF)、石油醚,均为市售分析纯。
Nicolet iS10傅里叶变换红外光谱(FT-IR)仪,美国Thermo Fisher Scientific公司;DRX500核磁共振仪,德国Bruker公司;Viscotek凝胶色谱(GPC)仪,英国Malvern公司;Diamond DSC差示扫描量热(DSC)仪,美国PerkinElmer公司。
1.2 UA/MAH共聚物的制备
将十一烯酸(UA)和马来酸酐(MAH)按一定物质的量比(总物质的量为0.01 mol)加入到带有搅拌桨和温度计的三口烧瓶中,加入一定量甲苯,水浴加热至30 ℃左右使MAH溶解。然后称取一定比例引发剂偶氮二异丁腈(AIBN)溶解在混合溶液中,去掉搅拌,通N210 min,保持反应温度为75 ℃,反应时间为8 h,反应体系中单体总浓度为4 mol/L。反应结束后将聚合物用四氢呋喃溶解、石油醚沉淀后离心分离,真空干燥至恒定质量,得到十一烯酸/马来酸酐共聚物(UMA),反应式如图1所示。

图1 UMA共聚物的合成路线图
1.3 测试与表征
1.3.1共聚物得率(y)的测定 共聚物的得率(y)由下式计算得到[13]:
y=m1/m0×100%
式中:m1—洗涤干燥后所得共聚物的质量,g;m0—聚合之前聚合体系所加单体和引发剂的总质量,g。
1.3.2相对分子质量的测定 使用凝胶色谱(GPC)仪测定干燥后共聚物的相对分子质量,采用聚苯乙烯为标样,色谱纯四氢呋喃为流动相,流速为1 mL/min,柱温为40 ℃,样品质量浓度为4 g/L。
1.3.3FT-IR分析 将分离干燥后的共聚物样品及UA、MAH单体,用傅里叶变换红外光谱仪进行表征,测试方法为衰减全反射法。
1.3.413C NMR分析 称取约10 mg样品,用氘代二甲基亚砜(DMSO-d6)溶解,在核磁共振仪上测定13C NMR谱图。
1.3.5酸酐质量分数的测定 采用苯胺法[14]测定共聚物中酸酐的质量分数,具体操作步骤为:1)称约0.2 g共聚物样品置于100 mL锥形瓶中,加入10 mL吡啶,样品溶解后缓慢加入10 mL水,室温放置4 h。加入2滴酚酞,用0.5 mol/L的NaOH标准溶液滴定到酚酞指示剂的终点。2)称约0.2 g共聚物样品置于100 mL锥形瓶中,加入15 mL吡啶,样品溶解后加入2 mL苯胺,室温反应15 min,加入5 mL水,2滴酚酞,用0.5 mol/L NaOH标准溶液滴定到酚酞指示剂的终点。酸酐质量分数的计算公式如下:
式中:B—共聚物中酸酐的质量分数, %;M—酸酐的摩尔质量,72.02 g/mol;CNaOH—所配NaOH标准溶液的浓度, mol/L;Va—步骤1)中消耗NaOH标准溶液的体积, mL;Vb—步骤2)中消耗NaOH标准溶液的体积, mL;ma—步骤1)中称取共聚物的质量, g;mb—步骤2)中称取共聚物的质量, g。
1.3.6DSC分析 采用差示扫描量热仪测定样品的玻璃化转变温度(Tg)。测试温度为室温至140 ℃,升温速率为20 ℃/min,N2氛围下,Tg由第二次升温曲线测定。
2 结果与讨论
2.1 反应条件对聚合反应的影响
2.1.1单体配比 UA与MAH物质的量之比分别为60∶40、 50∶50、 40∶60和30∶70,AIBN用量0.75%(以单体总的物质的量计,下同),反应温度为75 ℃,反应时间为8 h时,共聚物的相对分子质量见表1。从表1可以看出,随着UA与MAH物质的量之比的减小,共聚物相对分子质量呈减小的趋势。这是因为MAH自身的位阻效应使其自聚能力很弱,它产生的自由基只能引发UA单体进行链增长,UA为烯丙基单体,在自由基聚合过程中会发生链转移,致使聚合度减小,相对分子质量下降。虽然UA用量减小,链转移作用减弱,但是体系中MAH单体浓度增加,使得单位体积内UA浓度减小,随着反应的进行,体系黏度增大,分子链运动受到限制,导致链增长自由基与UA分子碰撞的几率减小,双基终止加快,进而导致聚合度减小,共聚物相对分子质量减小,多分散指数(PDI)也有所减小。

n(UA)∶n(MAH):60∶40;50∶50;40∶60;30∶70图2 单体配比对得率的影响Fig. 2 Effect of monomer ratio on yield
图2为UMA-1~UMA- 4各样品得率随时间的变化曲线,可以看出,随着UA用量(物质的量分数,下同)从60%减小到40%,聚合速率加快,继续减小到30%,聚合速率基本不变,甚至略有减慢。这是由于当UA用量较大时,聚合过程中链增长自由基会向UA单体分子形成链转移,而生成的UA烯丙基自由基的活性较弱,导致链增长的速率较慢,聚合速率下降[15],当UA用量减小时,链增长自由基向单体的链转移作用减弱,聚合效率增加,聚合速率增大。共聚物样品的最终得率见表1,从表中可以看出,UA用量从60%减小到40%,得率逐渐增大,从49.97%增加到61.78%,当UA用量从40%减小到30%,得率又略有降低,为59.32%,这是因为随着体系中UA浓度降低,链增长自由基向UA单体的链转移减弱,且与MAH单体碰撞的几率增大,更易引发MAH单体参与共聚,因此得率会增加,但MAH自聚能力很弱,它所产生的自由基只能引发UA分子进行链增长,当UA用量进一步减小时,体系内MAH浓度过高,会导致部分MAH剩余单体不能参与聚合,因此得率又有所降低。
不同单体配比时,UA/MAH共聚物的酸酐质量分数见表1。随着UA与MAH物质的量之比的减小,共聚物分子链中酸酐质量分数呈先增大后减小的趋势,当UA与MAH 物质的量比为40∶60时,酸酐质量分数最大,为20.05%。结合得率数据可知,UA与MAH的最佳物质的量比为40∶60,在此配比下,UA与MAH可以很好地发生共聚,共聚物分子链上酸酐基团增加,可以更好地进行后续改性。

表1 不同单体配比下共聚物的基本性质
2.1.2引发剂用量 当单体物质的量比为50∶50,反应介质为甲苯,反应温度为75 ℃,反应时间为8 h,AIBN用量分别为0.25%、 0.75%、 1.5%和2.0%时的共聚物样品为UMA-5、UMA-2、UMA- 6、UMA-7,考察样品相对分子质量的变化情况(见表2)。当引发剂用量从0.25%增加到2.0%时,Mn从12 400减小到3 755,这是因为动力学链长与引发剂浓度的平方根成反比,而动力学链长越长,平均聚合度越大,因此引发剂用量增加,平均聚合度减小,共聚物相对分子质量呈下降趋势。由于引发剂浓度较大时,产生的初级自由基增多,链引发、链增长过程具有较好的一致性,因此多分散指数也逐渐减小。
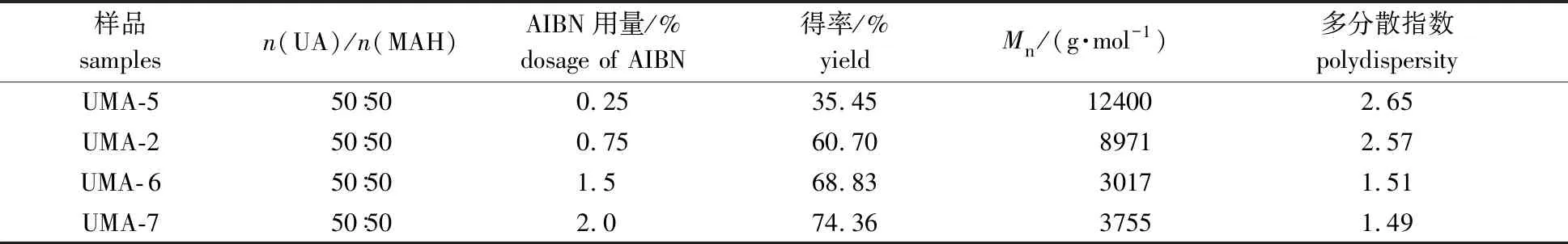
表2 不同引发剂用量下共聚物的得率与相对分子质量
不同引发剂用量下共聚物最终得率见表2,可以看出,随着AIBN用量从0.25%增加到2.0%,得率呈现增大的趋势,从35.45%增加到74.36%。图3为样品得率随时间的变化曲线。如图所示,随着引发剂用量的增加,聚合速率呈增大的趋势,这是因为更多的引发剂会产生更多的活性自由基,从而会产生更多的链增长自由基,虽然链增长自由基易向UA单体链转移形成烯丙基自由基,导致聚合速率减慢,但UA浓度一定时,向UA单体形成链转移的自由基量一定,大部分自由基参与正常的链增长聚合过程,所以引发剂用量的增加,引发链增长的效率增加,聚合速率呈现增大的趋势,因此可以根据所需共聚物的相对分子质量与得率综合选择合适的引发剂用量,本反应体系选择AIBN用量为0.75%。
2.1.3反应温度 图4为不同反应温度下共聚物的得率和相对分子质量,其中UA与MAH物质的量之比为50∶50,引发剂用量为0.75%,反应介质为甲苯,反应时间为8 h。从图4可以看出,反应温度从65 ℃提高到85 ℃,共聚物得率呈增大的趋势,从45.82%增加到68.20%,而相对分子质量呈下降的趋势,从10 300减小到6 224。这是因为温度升高,引发剂分解效率提高,单位时间内产生的初级自由基增多,链引发速率加快,所以聚合速率加快。但温度升高,链转移速率常数增加,且引发剂分解产生的自由基浓度增加,单位时间内产生的单体自由基增多,动力学链长减小,从而导致聚合度减小,Mn下降。

图3引发剂用量对得率的影响
Fig.3Effectofinitiatordosageonyield


图4不同反应温度下共聚物的相对分子质量及得率
Fig.4Molecularweightandyieldofcopolymersatdifferentreactiontemperatures
由上述分析可知,在本研究的反应体系中,当UA与MAH物质的量之比为40∶60、AIBN用量0.75%、反应温度75 ℃时,共聚物得率为61.78%,酸酐质量分数为20.05%,Mn为4 926,提高AIBN用量和反应温度,聚合速率加快,得率升高,但共聚物相对分子质量下降明显,因此可以根据所需共聚物的性质选择合适的反应条件,在该体系中选择的较优的反应温度为75 ℃,AIBN用量为0.75%。
2.2 分析与表征

2.2.213C NMR分析 图6为MAH和UA单体物质的量之比为50∶50,AIBN用量0.75%,反应温度为75 ℃,反应时间为8 h时的共聚物(UMA-2)的13C NMR谱图。

图5FT-IR谱图
Fig.5FT-IRspectra
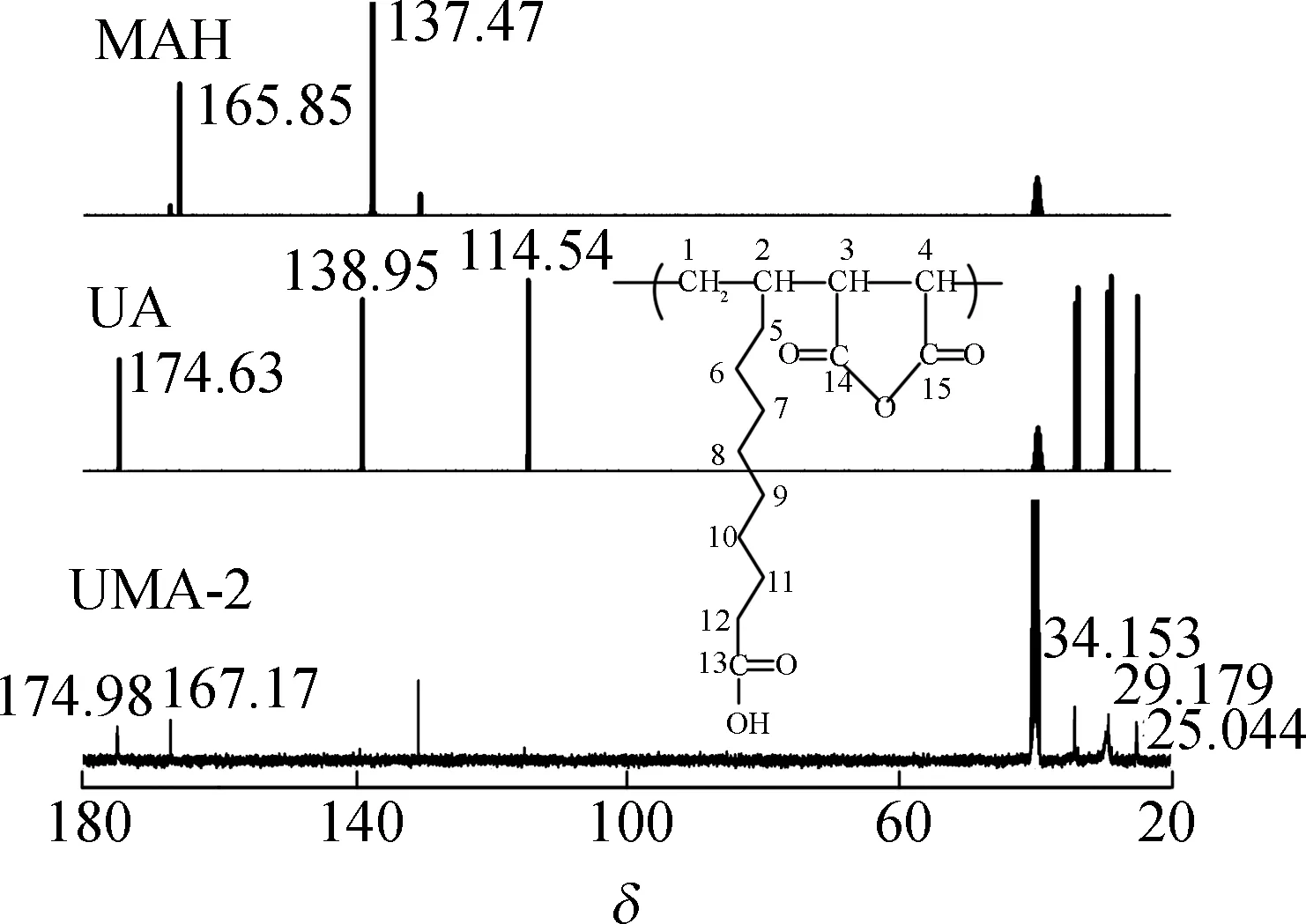
图613CNMR谱图
Fig.613CNMRspectra

图7 不同单体配比时共聚物的DSC曲线Fig. 7 DSC curves of copolymers with different monomer ratios

2.2.3DSC分析 图7为UA与MAH物质的量之比分别为60∶40、 50∶50、 40∶60和30∶70时共聚物的DSC谱图。从图中可以看出,随着单体配比从60∶40减小到40∶60,共聚物的玻璃化转变温度(Tg)从64.38 ℃增加到71.98 ℃,这是因为共聚物分子链上马来酸酐的刚性五元环结构限制了主链的旋转,降低了分子链的柔韧性,因此酸酐质量分数增加,共聚物的Tg呈增大的趋势。当单体配比进一步减小到30∶70时,Tg又略有降低,与酸酐质量分数的测定结果基本一致。
3 结 论
以十一烯酸(UA)和马来酸酐(MAH)为原料,偶氮二异丁腈(AIBN)为引发剂,通过沉淀聚合的方法制备了UA/MAH共聚物,由分析可知,随着UA与MAH物质的量之比的减小,共聚物的相对分子质量及多分散指数呈减小的趋势,得率先增大而后略有减小,酸酐质量分数先增大后略有减小。在该反应体系(反应温度75 ℃、AIBN用量0.75%)中,UA和MAH最佳的物质的量比为40∶60,此时得率最大,为61.78%,酸酐质量分数为20.05%。增加引发剂用量和提高反应温度共聚物得率增加,有利于共聚反应的进行,但相对分子质量降低明显,因此可以根据所需共聚物的性质来选择合适的制备条件。由FT-IR和13C NMR分析表征可知UA和MAH成功发生了共聚反应。DSC曲线表明:随着UA与MAH物质的量之比的减小,Tg先增大后减小,与酸酐质量分数变化基本一致,当n(UA)∶n(MAH)为40∶60时,Tg达到最大值71.98%。
