GCr18Mo轴承钢的镁处理改质效果研究
2019-04-08乔梦然郭曙强郑红妍秦礼彬任忠鸣
乔梦然 郭曙强 郑红妍 秦礼彬 苏 新 任忠鸣
(1.省部共建高品质特殊钢冶金与制备国家重点实验室,上海 200444; 2.上海市钢铁冶金新技术开发应用重点实验室,上海 200444;3.上海大学材料科学与工程学院,上海 200444)
冶炼轴承钢时,常加入金属Al作为脱氧剂,脱氧产物往往是高熔点的硬脆性Al2O3夹杂物,在钢液的搅拌下容易聚集长大形成团簇,不但易造成水口结瘤堵塞,而且在后续加工过程中会成为裂纹源,对轴承的疲劳性能危害极大[1]。目前,对钢中Al2O3夹杂物变质处理最为常用的方法是钙处理,但在实际生产中,钙处理尚存在一些不足,如易生成有害的D类钙铝酸盐夹杂难以去除[2]。近年来,镁处理作为一种新的夹杂物变质技术受到人们的关注。研究表明[3- 4],在炼钢温度下,镁不仅有良好的脱氧与脱硫效果,而且还能极强地控制夹杂物形态与尺寸。对于铝脱氧钢,镁处理在进一步降低钢中氧浓度的同时,还可以将钢中的Al2O3夹杂变质为细小的MgO或MgO·Al2O3尖晶石[5- 7]。
迄今,对于镁处理改质轴承钢中夹杂物机制的研究报道甚少。基于此,本研究以GCr18Mo轴承钢为对象,通过实验室模拟冶炼试验,结合热力学及动力学分析,研究了镁处理对铝镇静轴承钢中夹杂物的控制效果与作用机制,以获得洁净钢的最佳生产技术,为高铁轴承的制造和应用提供试验数据支撑。
1 Al- Mg复合脱氧热力学计算
在Al2O3和MgO的饱和区,其对应活度均为1,反应方程见表4中(a)和(b)。根据化学反应的线性组合原理,可以推导出方程(1)计算MgO·Al2O3的饱和区,方程(2)和(3)分别用来计算MgO/MgO·Al2O3边界和Al2O3/MgO·Al2O3边界,其中MgO·Al2O3的活度分别为0.8和0.47,对应的MgO与Al2O3的活度分别为1[16]。
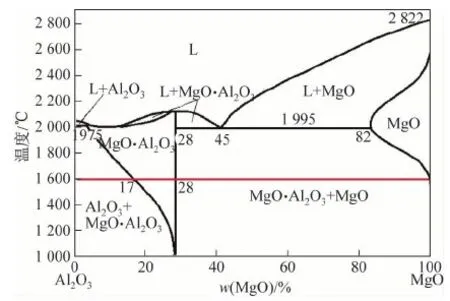
图1 运用FactSage软件计算的MgO- Al2O3二元平衡相图Fig.1 MgO- Al2O3 binary phase diagram calculated by FactSage software

表1 GCr18Mo轴承钢的化学成分 (质量分数)Table 1 Chemical composition of the GCr18Mo bearing steel (mass fraction) %
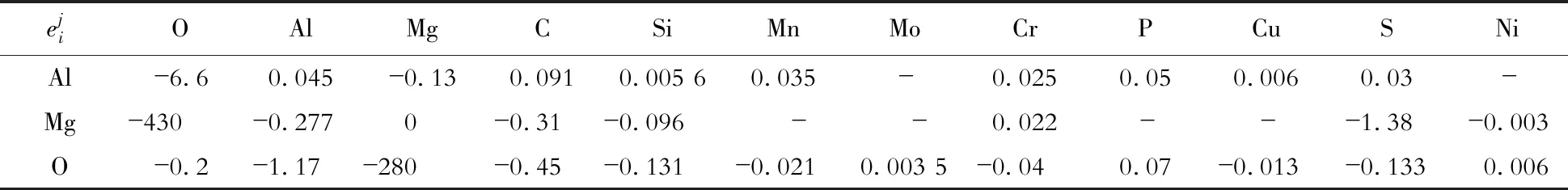
表2 钢液组元的一级相互作用系数 (1 873 K)[8- 15]Table 2 First order interaction coefficients of component in molten steel (1 873 K) [8- 15]

表3 钢液组元的二级相互作用系数(1 873 K)[10]Table 3 Second order interaction coefficients of component in molten steel (1 873 K) [10]
MgO·Al2O3=2[Al]+[Mg]+4[O]
logK1=32.2-103 146/T
(1)
4(MgO)+2[Al]=MgO·Al2O3+3[Mg]
logK2=17.16-49 094/T
(2)
3(MgO·Al2O3)+2[Al]=4Al2O3+3[Mg]
logK3=14.32-53 438/T
(3)

表4 Mg- Al- O系夹杂物形成的化学反应平衡常数[9]Table 4 Chemical reaction equilibrium constants for the formation of Mg- Al- O system inclusions[9]
结合以上计算结果,运用MATLAB绘制得到1 873 K温度下,GCr18Mo钢中Mg- Al- O系的稳定区域相图,如图2所示(虚线为平衡等氧线)。可见,根据钢中铝含量和镁含量的变化,反应产物可以分为Al2O3、MgO·Al2O3和MgO 3个优势区。随着钢中溶解镁与溶解铝含量比值的提高,Al2O3逐渐转变成MgO·Al2O3和MgO。当溶解镁含量在5.9~40 μg/g或1.7 ~13 μg/g的范围内,对应溶解铝的质量分数不超过0.056%或在0.07%~0.32%范围时,可控制钢中氧含量低于3 μg/g,Al- Mg复合脱氧可达到热力学理论上的最佳效果。

图2 GCr18Mo钢中Mg- Al- O系夹杂物的稳定区域图(1 873 K)Fig.2 Stability phase diagram of Mg- Al- O system inclusions in GCr18Mo steel (1 873 K)
2 试验材料与方法
选用脱氧剂为纯Al粒(纯度99.999%,质量分数,%)与Ni- 17.5%Mg合金,试验前需加入Fe2O3增氧,并去除钢中残留Al、Mg等元素。根据图2的计算结果,研究钢液中溶解铝的质量分数分别为0.03%、0.1%和0.3%,不同溶解镁含量落在MgO区、MgO·Al2O3区和Al2O3区,对应的镁铝加入质量比为2.6、2.2和1.8时,对钢中总氧量及脱氧产物的影响。理论计算脱氧剂的加入量如表5所示。

表5 Al- Mg复合脱氧剂加入量计算值Table 5 Calculated values of addition of Al- Mg complex deoxidizer g
采用真空高频感应加热炉冶炼试验钢。将130 g GCr18Mo原始钢与0.7 g Fe2O3粉末置于外套为刚玉坩埚的Al2O3坩埚中,夹层塞入耐火棉以达到更好的保温效果。脱氧剂用铁箔包裹后置于加料器底端,用磁铁从外部固定。采用红外感应测温计定温,误差为±2 K[17]。加热过程通入干燥且去氧的Ar气(99.999%)作为保护气。先升温至1 600 ℃,保温10 min,加入Al粒脱氧15 min,再加入Ni- Mg合金,保温15 min,随炉冷却1 h后空冷至室温。采用线切割在冶炼所得钢样的中心部位横向截取两个8 mm×10 mm×8 mm的试样,用作SEM/EDS分析夹杂物特征。在上、中、下3个位置中心切取3 mm×1 mm×1 mm和3 mm×3 mm×3 mm试样各两组,分别用作ICP发射光谱仪测定酸溶Al、Mg、Ca等元素的含量和氮氧分析测定总氧含量,结果取平均值。
3 试验结果与分析
3.1 钢样成分
经铝脱氧与镁处理后的试验钢的ICP与氮氧分析测试结果如表6所示,并将试验数据标注于图2。其中1号、2号与3号标记线为试验计算纯铝与Ni- Mg合金加入量的理论取值范围,标记点为试验钢对应的平衡Mg- Al含量成分点与钢中总氧量的平均值。
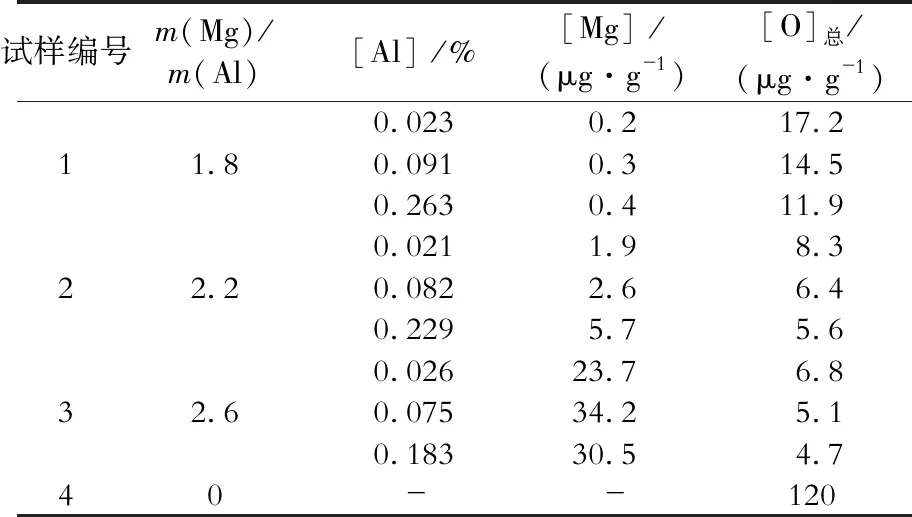
表6 不同镁铝加入质量比的试验钢中酸溶Al、Mg含量及总O含量的平均值Table 6 Average values of Al, Mg content and total O content in the tested steel with different Mg/Al mass ratios
结合图2与试验结果可以看出:Al- Mg复合脱氧时,逐渐增加镁铝加入质量比从1.8→2.2→2.6,试验钢的成分点分布从Al2O3优势区向MgO·Al2O3尖晶石和MgO优势区转移,试验结果与热力学计算相吻合。且钢中总氧含量从原始钢中的120 μg/g降低至4.7~17.2 μg/g,可见,镁铝加入质量比的提高有利于进一步降低试验钢中总氧含量,如图3所示。
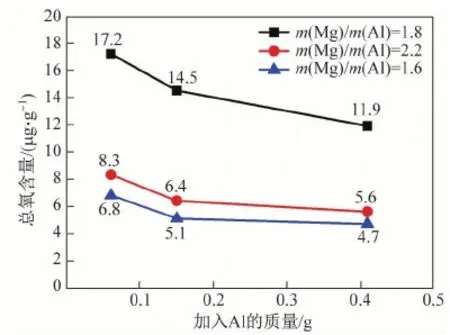
图3 不同镁铝加入质量比的试验钢中总氧量变化Fig.3 Variation of total oxygen content in the tested steel with different Mg/Al mass ratios
3.2 夹杂物形貌与成分分析
为了进一步分析不同镁铝加入质量比对试验钢中夹杂物分布、尺寸、形貌和种类的影响,对钢样进行SEM/EDS分析。将处理后的金相试样在扫描电镜下放大3 000倍,做连续视场分析,每个试样观察并拍摄80个视场。采用Image- J和IPP软件统计夹杂物的尺寸、分布及单位面积的数量,并进行分类,结果如图4所示。可见,相较于原始钢,随着镁铝加入质量比的提高,单位面积内夹杂物的数量明显减少,平均粒径也有所减小。

图4 不同镁铝加入质量比的试验钢中单位面积夹杂物的数量与平均粒径统计结果Fig.4 Statistical results of the number in unit area and size of inclusions in the tested steel with different Mg/Al mass ratios
图5为不同镁铝加入质量比的试验钢的显微组织,可以看出,原始钢(图5(a))中的夹杂物数量较多,平均粒径较大,且集中分布于部分区域。当m(Mg)/m(Al)=1.8时,随着氧活度的显著降低,夹杂物数量明显减少,粒径也减小(图5(b))。当加入m(Mg)/m(Al)达到2.2及以上时(图5(c,d)),夹杂物数量极少,主要为小尺寸的MgO·Al2O3尖晶石与MgO夹杂,洁净度较好。
GCr18Mo原始钢中典型夹杂物的形貌见图6。由于试验钢已进行Al预脱氧处理,且熔炼采用Al2O3坩埚,高温时易被钢液侵蚀,因此,原始钢中主要为B类Al2O3夹杂物,呈球状或带角的不规则形状,相互间吸引力较大,在电磁搅拌的作用下,易聚集长大形成Al2O3团簇(图6(a~c)),尺寸多为5~10 μm。试验钢还含有一定量的S和Mn元素,在凝固时易反应析出长条状硫化物(图6(d)),具有较高的延展性。此外还检测到少量的D类复相夹杂物(图6(e~f)),成分较为复杂,尺寸大于13 μm,对钢的性能危害较大。
镁铝加入质量比为1.8时(图7),钢中夹杂物仍多以Al2O3形式存在, 尺寸主要为2~5 μm,相较于原始钢,夹杂物尺寸有所减小,但由于镁处理的加入量不足,使得Al2O3夹杂没有得到较好的改质。镁铝加入质量比达到2.2时,试验钢的成分点落于图2中的MgO·Al2O3优势区,出现了单颗粒镁铝尖晶石夹杂,呈不规则多边形或外围包裹硫化物的近似球状,粒径大多小于5 μm,见图8。镁铝加入质量比进一步提高至2.6时,试验钢中典型夹杂物多为球状或近似球状的MgO(图9),尺寸更加细小,为1~3 μm。此时钢中几乎没有Al2O3团簇,说明足量的Mg能抑制Al2O3的聚集长大,且能与其发生反应生成尺寸更加细小的Mg- Al- O系夹杂物,实现对Al2O3等有害夹杂物的改质作用。

图5 不同镁铝加入质量比的试验钢的显微组织Fig.5 Microstructues of the tested steel with different Mg/Al mass ratios

图6 GCr18Mo原始钢中典型夹杂物的形貌及成分Fig.6 Morphologies and compositions of typical inclusions in the original GCr18Mo steel
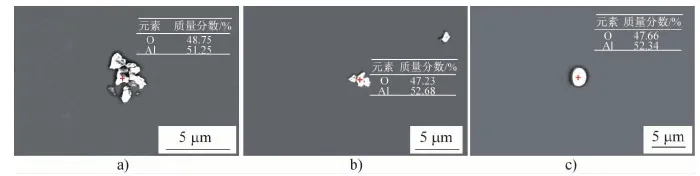
图7 镁铝加入质量比为1.8时试验钢中典型Al2O3夹杂物的形貌与成分Fig.7 Morphologies and compositions of Al2O3 inclusions in the tested steel with Mg/Al mass ratio of 1.8

图8 镁铝加入质量比为2.2时试验钢中典型MgO·Al2O3尖晶石的形貌与成分Fig.8 Morphologies and compositions of MgO·Al2O3 inclusions in the tested steel with Mg/Al mass ratio of 2.2

图9 镁铝加入质量比为2.6时试验钢中典型MgO夹杂物的形貌与成分Fig.9 Morphologies and compositions of MgO inclusions in tested steel with Mg/Al mass ratio of 2.6
研究表明[18],镁系氧化物与钢液的界面能较小,颗粒间的吸引力很小,仅为纯Al2O3颗粒间吸引力的1/10。所以钢中MgO·Al2O3与MgO夹杂以单颗粒形式存在,不会聚集长大,且弥散分布,对基体有强化作用。有研究发现[19],钢中MgO·Al2O3夹杂的尺寸若能控制在5 μm以内,则其对钢的力学性能基本没有负面影响。此外,以尖晶石为凝结核心外包硫化物的夹杂具有一定的延展性,进一步减轻了对轴承钢的危害。
3.3 镁处理改质夹杂物转变模型
冶炼时,先进行铝脱氧,反应产物主要为Al2O3夹杂物。随后进行镁处理,Al2O3夹杂向MgO·Al2O3的转变主要源于钢液中溶解的[Mg]与Al2O3之间的反应,结合上述反应过程,对镁处理改质机制作如下建模:
(1)Ni- Mg合金加入钢液后,被还原产生溶解[Mg]向Al2O3夹杂物- 钢液界面扩散。
(2)溶解[Mg]扩散至中间过渡层- 钢液界面,发生失电子反应:
[Mg]=[Mg2+]+2e-
(4)
(3)Mg2+在中间过渡层聚集,产生浓度梯度,随后穿过中间过渡层向内部扩散。
(4)Mg2+到达Al2O3夹杂界面,二者发生反应(见式(5)),置换出Al3+向外扩散,在中间过渡层得到电子形成[Al] (见式(6) ),随后扩散进入钢液中。
4(Al2O3)+3[Mg2+] = 3(MgO·Al2O3)+2[Al3+]
(5)
[Al3+]+3e-=[Al]
(6)
(5)随着反应的进行,生成的MgO·Al2O3将以Al2O3夹杂为核心,依附于其表层,形成MgO·Al2O3层,从而与Al2O3夹杂中心形成一定的生成物浓度梯度,在扩散与反应充分进行后,形成镁、铝元素分布均匀的MgO·Al2O3夹杂。
将上述Al2O3夹杂改质成MgO·Al2O3夹杂的过程描述为如图10所示的转变模型。Zayan等[20]研究了镁铝尖晶石夹杂物转变的限制性环节,得出[Al]在钢液- 中间过渡层的扩散速度远大于[Mg],因此,[Mg]在夹杂物中的扩散速度直接决定着夹杂物的转变速度。此外,在钢液凝固过程中MnS夹杂可能会在尖晶石表面包裹析出。
4 结论
(1)原始GCr18Mo钢中夹杂物类型主要为B类Al2O3和D类球状氧化物,尺寸较大,尺寸多为5~10 μm。采用Al- Mg复合脱氧,可将原始钢中总氧含量由120 μg/g降低至17.2 μg/g以下, 适当提高镁铝加入质量比有利于进一步降低钢中总氧含量。

图10 Al2O3夹杂向MgO·Al2O3转变模型图Fig.10 Modification model of Al2O3 to MgO·Al2O3 inclusion
(2)在1 873 K,溶解铝的质量分数为0.03%~0.3%时,随着镁铝加入质量比从1.8增至2.2再增至2.6,钢中平衡成分点的位置从Al2O3区向MgO·Al2O3区再向MgO区转变,试验结果与热力学计算分析的优势区相符合。
(3)当加入量m(Mg)/m(Al)=1.8时,钢中典型夹杂物主要为B类Al2O3,尺寸为2~5 μm。当m(Mg)/m(Al)=2.2时,出现不规则MgO·Al2O3尖晶石夹杂物,粒径为1~5 μm。当m(Mg)/m(Al)=2.6时,钢中多为单颗粒球状MgO夹杂物,粒径较小,尺寸为1~3 μm。因此,适当提高镁铝加入质量比,有利于对Al2O3等有害夹杂物的形成起到抑制与改质作用,使其转变为尺寸更细小的MgO·Al2O3尖晶石或MgO夹杂,并弥散分布于钢中。
