基于CoFe2O4载氧体的生物质化学链气化热力学分析及实验研究
2019-04-03,,
, ,
(华中科技大学 煤燃烧国家重点实验室, 湖北 武汉 430074)
与传统化石能源相比,生物质是一种绿色清洁可再生能源,其开发和利用受到了越来越多研究者的关注[1]。生物质化学链气化(Chemical Looping Gasification, CLG)是一种新型的气化技术,其中,载氧体为燃料提供气化反应所需的氧,通过控制燃料和载氧体的质量比,可以制备较高品质的合成气。与传统的生物质气化工艺相比,CLG具有成本低、热值高、焦油含量低等优点[2-4]。载氧体是CLG技术的关键,与整个反应系统的运行紧密相关[5]。
目前,Fe、Co、Cu、Mn等[6-9]金属氧化物,CaSO4[10]以及钙钛矿型载氧体[11]在化学链技术中研究较多。铁基载氧体反应活性较高且成本相对较低[12],但是其载氧能力不够高。针对铁基载氧体的不足,对其进一步改性受到了研究者的关注。CoFe2O4是一种新型的Fe-Co复合金属载氧体,具有钴基和铁基载氧体两者的优点[13]。Wang等[14]利用热重分析仪研究了CoFe2O4在以煤作燃料的化学链燃烧中的反应性能。结果表明,在氧传递速率和反应温度方面,CoFe2O4要优于相应的单一金属氧化物CoO和Fe2O3。在以甲醇或乙醇做还原剂制备高品质合成气中,相比于NiFe2O4,CoFe2O4反应活性更高,且能重新被氧化恢复尖晶石结构[15]。CoFe2O4在化学链燃烧和化学链制备合成气中具有良好的反应性能,为CoFe2O4在CLG中的应用提供了指导。然而,目前基于CoFe2O4载氧体CLG的研究报道相对较少。
本研究通过热力学计算和热重实验开展了基于CoFe2O4载氧体的CLG的研究,同时结合XRD技术对反应前后载氧体的物相组成进行分析,揭示了基于CoFe2O4载氧体的CLG反应特性,对CoFe2O4在CLG中的应用具有重要指导意义。
1 实验部分
1.1 热力学分析
生物质的CLG过程主要分为热解和气化两个复杂反应过程。生物质首先热解析出挥发分,挥发分中的CO、H2、CH4等小分子气体容易被载氧体氧化生成CO2和H2O,然后剩余的焦炭在气化介质作用下生成合成气,同时还伴随有水汽变换以及甲烷、焦油重整等一系列反应[16,17]。主要反应包括:
生物质热解:生物质 → 焦炭 + 焦油 + 气体(H2、CO、CO2、CnHm)
(1)
载氧体参与的反应有:H2、CO、C、CnHm+ MexOy→ H2O + CO2+ MexOy-2
(2)
焦炭气化:C + CO2→ 2CO
ΔH= 167.744 kJ/mol
(3)
C + H2O → H2+ CO
ΔH= 135.548 kJ/mol
(4)
水汽变换反应:CO + H2O → H2+ CO2
ΔH= -32.196 kJ/mol
(5)
甲烷重整反应:CH4+ H2O → 3H2+ CO
ΔH= 225.838 kJ/mol
(6)
焦油重整反应:焦油 → H2+ CO + CnHm
(7)
选用松木屑作为生物质原料,对松木屑进行多次研磨并筛分至200目以下,粒径小于75 μm。其元素分析和工业分析见表1。氮、硫元素及灰分在松木屑中含量很低,可忽略其对气化反应的影响[18],因此,在计算输入物质中只考虑C、H、O这三种元素,生物质化学式可简写为CH1.59O0.7。

表 1 松木屑的元素分析和工业分析
*: by difference
本研究基于吉布斯自由能(Gibbs free energy)最小化原理,利用热力学软件HSC Chemistry 6.0对松木屑与CoFe2O4的反应进行分析。在热力学计算中考虑的物相组分见表2。
碳转化率xC是评价CLG的重要参数,其定义式为:
(8)
nC,s和nC,b分别表示焦炭和生物质中含碳量。

表 2 热力学计算中考虑的物相组分
1.2 热重实验
采用溶胶—凝胶燃烧法制备CoFe2O4载氧体,以工业分析纯Fe(NO3)3·9H2O和Co(NO3)2·6H2O为原料,柠檬酸(C6H8O7·H2O)作为分散剂和燃料,将硝酸盐和柠檬酸按照一定质量比依次溶于去离子水中,将混合溶液放入恒温水浴中搅拌直至呈凝胶状,先将凝胶产物进行干燥然后置于马弗炉中在950 ℃下煅烧6 h。载氧体经过多次磨制并筛分到100目以下,其粒径小于150 μm。
热重实验在热重分析仪(SDT Q600, TA Instruments)上进行。先按不同的质量比(0.8、1.6、2.4和3.2)分别称取较多的载氧体与松木屑,将其在玛瑙研钵中研磨以进行充分混合,每次实验取30-40 mg样品放入坩埚中,通入高纯氮气作为保护气及吹扫气,流量为100 mL/min,热重升温速率为10 K/min,由常温升至1000 ℃。实验结束后通过XRD对载氧体的物相组成进行分析。
2 结果与讨论
2.1 热力学计算
2.1.1载氧体添加量对合成气组分的影响
根据CLG反应机理可知,载氧体的量决定着合成气组分。在模拟反应过程中,压力为常压,松木屑的量为1 kmol,反应温度为1000 ℃,载氧体CoFe2O4的量由0逐步增至1 kmol,研究载氧体添加量对合成气组分的影响,结果见图1。

图 1 载氧体添加量对松木屑气化反应特性的影响
当CoFe2O4的量较少时,合成气主要以CO和H2为主。随着CoFe2O4的量增加,CO的量先上升后下降,而H2的量先是基本保持平稳,然后下降;CO2和H2O的量则逐渐上升。CH4生成量很低,并且随着CoFe2O4量的增加基本不变,这可能是因为甲烷与载氧体的反应以及甲烷重整反应(6)比较容易进行,CH4被消耗[19]。碳转化率xC随着CoFe2O4量的增加先不断增大,当CoFe2O4的量达到0.2 kmol 时接近100%。当CoFe2O4的量为0.075 kmol时,CO的量为0.93 kmol,H2为0.77 kmol,CO和H2总的生成量达到最大值1.7 kmol,碳转化率为92.5%。随着载氧体添加量的增加,能够提供的晶格氧增多,气化反应生成的一部分CO、H2和CH4等小分子气体被氧化生成CO2和H2O。化学链气化主要是为了制备较高品质的合成气,载氧体过多会导致一部分合成气被氧化生成CO2和H2O。因此,在使用CoFe2O4作为载氧体的CLG反应中,当松木屑物质的量为1 kmol时,CoFe2O4的量最优为0.075 kmol,即CoFe2O4与松木屑的质量比为0.72。
2.1.2温度对合成气组分的影响
图2为反应温度对合成气组分的影响,此时松木屑物质的量为1 kmol,CoFe2O4的量为0.075 kmol,反应压力为常压。
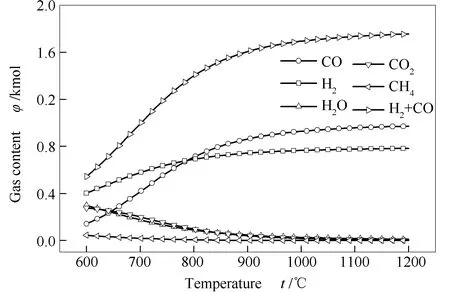
图 2 温度对合成气组分的影响
当温度升高,H2的量逐渐增加,当温度超过800 ℃后增长较为缓慢。CO的量随着温度升高快速增加。当温度达到1000 ℃后,CO和H2的量基本保持平稳不变。H2O和CO2的量随着温度升高不断下降,当温度超过1000 ℃后,H2O和CO2的量都很低。根据勒夏特列原理,升高反应温度可以促进吸热反应正向进行,放热反应逆向进行,从而影响气体产物中各组分的含量[20]。升高温度能够促进剩余焦炭的气化反应(3)、(4)和甲烷重整反应(6)向右进行,CO2、CH4和H2O被消耗,生成CO和H2。升高温度也能促进焦油重整反应(7)向右进行,大分子的焦油在高温下能够发生分解,生成CO和H2。升高温度虽然会促进水汽变换反应(5)逆向进行,但与其他反应相比,促进效果不太显著。提高反应温度也能够使相关氧化还原反应的速率得到提高。当温度达到1000 ℃时,碳转化率为92.5%。反应温度过高不仅会使能耗增加,也可能会造成载氧体的烧结,同时运行中的安全性也会降低。综合考虑,气化温度选择1000 ℃较为合适。
2.1.3水蒸气含量对合成气组分的影响
在固体含碳燃料的转化中,水蒸气可以使合成气的品质得到改善。水蒸气对合成气组分的影响见图3,此时松木屑的量为1 kmol,CoFe2O4的量为0.075 kmol,反应压力为常压,反应温度为1000 ℃,水蒸气的初始量为0,然后逐步增至4 kmol。
当水蒸气的添加量增多,H2和CO2的量增加,CO的量会降低。添加水蒸气能够促进反应(4)和(5)正向进行,H2和CO2的生成量增加。水蒸气也能够促进甲烷的重整反应(6)向右进行,CH4被消耗,反应生成CO和H2。而CO的生成量降低可能是因为水蒸气对反应(5)的促进效果更加显著,一部分CO被消耗,反应生成CO2和H2,因此,CO2的生成量增加。添加水蒸气能够提高合成气中H2和CO的比值,可用来生产甲醇等化工产品,但水蒸气过多会使CO2的量增加,导致合成气热值降低。

图 3 水蒸气对合成气组分的影响
在实际的反应系统中,水蒸气过多不仅需要消耗额外的热量,还会使反应器内温度分布不均匀。此外,水蒸气也会使反应器中混合气的体积流量升高,与载氧体的接触时间缩短,反应不充分。因此,水蒸气的添加量不能过多,应根据实际需要选择某一最佳值。
2.2 热重实验以及载氧体的表征
2.2.1载氧体与生物质不同质量比(O/B)下的反应特性
载氧体的量既决定了合成气的组分,同时也决定载氧体自身被还原的过程。为考察O/B对CLG的影响,利用热重进行了六组对比实验,其中包括生物质热解和载氧体单独的热重实验,另外四组实验中O/B分别为0.8、1.6、2.4和3.2,实验结果见图4。图4中的TG曲线表明,CoFe2O4在从室温升高到1000 ℃的过程中失重很小,在温度达到1000 ℃时最终残留质量为99.82%,说明其在高温下未发生氧解耦释放出氧。当不添加载氧体时,松木屑在100 ℃之前有一个较小的失重峰,这是松木屑中所含水分受热蒸发引起,此过程失重较小;另外在360 ℃左右有一个明显的失重峰,对应于生物质热解过程,该阶段失重较大,主要是由松木屑中挥发分的析出引起。当温度达到500 ℃时,热解过程基本完成。随着温度继续升高,当O/B为0.8时,混合物在760 ℃左右存在一个较为明显的失重峰。当O/B为1.6、2.4和3.2时,混合物除了在760 ℃左右存在一个较为明显的失重峰外,分别在897、932和941 ℃左右也存在一个失重峰。这表明,松木屑热解后剩余焦炭与载氧体在高温下仍会发生反应,CoFe2O4可以提供晶格氧,有效促进气化反应的进行。当O/B从1.6增大到3.2时,高温气化反应阶段两个失重峰对应的最大失重速率降低,同时对应的反应温度也更高;一方面是因为在整个失重过程中,松木屑的失重占主导地位,O/B越大,失重现象越不明显,最大失重速率也越小;另一方面与松木屑热解后剩余焦炭与载氧体之间的传热、传质有关[21],随着O/B增大,载氧体吸热量也会增加,出现热滞现象,生物质和载氧体的反应速率会降低,对应的反应温度也趋向于更高。

图 4 载氧体与生物质不同质量比气化反应的TG和DTG曲线
2.2.2载氧体性能表征
利用XRD对反应前后的载氧体的物相组分进行分析,结果见图5。

图 5 载氧体的XRD谱图
新制备的载氧体仅含有主晶相CoFe2O4,且峰型尖锐,具有较好的晶相结构。结合热重实验和图5可知,当O/B为0.8时,CoFe2O4可提供其全部晶格氧,直接被一步还原生成钴铁合金,在高温气化反应阶段只对应一个失重过程,且反应温度相对较低。Scheffe等[22]研究也发现,在化学链制氢中CoxFe3-xO4能够被合成气还原为钴铁合金。当O/B为1.6、2.4和3.2时,在高温气化反应阶段,CoFe2O4分两步被还原,对应两个失重过程,其最终被还原的程度降低,还原产物中出现Fe3O4。作者前期基于密度泛函理论研究了CO在CoFe2O4表面的吸附和氧化机理[23],结果表明,钴原子相关的吸附位均强于铁原子相关的吸附位,CO在CoFe2O4表面钴原子和铁原子上吸附和氧化的能量势垒均低于Fe2O3表面,钴原子可以提高铁原子的CO吸附性能。在Fe2O3作载氧体的CLG中,最大失重速率对应的温度接近1000 ℃,高于CoFe2O4作载氧体时的温度[24]。综合以上研究和本研究热重实验可认为,钴和铁具有协同作用,钴能够提高铁的活性,促进铁进一步被还原。因此,当O/B分别为1.6、2.4和3.2时,由于载氧体的量较多,钴优先于铁先被还原,在钴的协同作用下,一部分铁也被还原,生成钴铁合金,对应第一个失重峰;随后在更高的温度条件下,剩余铁氧化物被进一步还原生成Fe3O4,对应第二个失重峰。CoFe2O4被逐级还原过程与NiO修饰的铁矿石作载氧体被还原过程类似,其在高温气化反应阶段也分两步被还原,对应两个失重峰[25]。与NiO修饰的铁矿石相比,CoFe2O4反应所需温度较低,能有效避免载氧体的烧结。
在实际反应系统中,受实验条件和动力学因素的影响,载氧体的量应稍大于理论计算值。热重实验结果表明,当CoFe2O4与松木屑的质量比(O/B)为0.8时,在高温气化反应阶段,反应速率较快,可被一步直接还原为钴铁合金,且反应所需温度相对较低。热力学计算也表明,此时合成气中CO和H2仍具有较高的浓度。综合考虑以上因素,CoFe2O4与松木屑的质量比最优为0.8。
3 结 论
本研究应用热力学分析、热重实验和XRD表征,对基于CoFe2O4载氧体的生物质化学链气化反应特性进行了研究。CoFe2O4能够提供晶格氧,使碳转化率得到提高。反应温度上升,合成气中H2和CO的量增加,CO2的量降低。当水蒸气的添加量增多,H2和CO2的量增加,CO的量会降低。添加水蒸气能够使合成气中H2和CO的比值得到提高,合成气的品质上升。热重实验结果表明,钴优先于铁被还原,钴与铁存在协同作用,钴能够促进铁的进一步还原。随着载氧体量的增多,其被还原的程度会降低,CoFe2O4与松木屑的质量比最优为0.8。CoFe2O4具有较好的反应性能,在生物质化学链气化中有较好的应用前景。
