肺癌患者血浆外泌体蛋白质组分析
2019-04-02钟荣斌李捷易绍琼王帅吴晓洁靳海荣王领会王启伟郗永义朱力林艳丽王友亮
钟荣斌,李捷,易绍琼,王帅,吴晓洁,靳海荣,王领会,王启伟,郗永义,朱力,林艳丽,王友亮
1.军事医学研究院 生物工程研究所,北京100071;
2.解放军总医院第一医学中心 胸外科,北京100853
肺癌是全球发病率和死亡率最高的恶性肿瘤,空气污染加重和女性吸烟人数的增多,导致肺癌的发病率仍呈上升趋势。虽然近年来在肺癌诊断、手术及药物治疗方面取得了极大的进步,但肺癌患者的五年存活率仅为10%~15%[1],主要原因是肺癌早期症状轻微,确诊时往往已发展至中晚期,治疗效果并不理想。但早期肺癌患者经过手术切除治疗后的五年存活率可达83%,因此早期诊断对治疗肺癌至关重要。
目前肺癌的诊断方法主要包括组织活检、支气管内镜技术和影像学方法,然而这些具有侵入性的检查方法在肺癌早期诊断方面收效甚微。液体活检这一非侵入式的检查方法在肿瘤早期诊断方面展现出巨大的潜力,而外泌体是液体活检中的一个重要检测对象。所有活细胞均能通过分泌胞外囊泡来进行细胞间的信息传递[2]。外泌体是三大胞外囊泡中的一种,它是由细胞中内出芽形成的多囊泡内体与细胞膜融合后向细胞外分泌的具有脂质双层膜的微小囊泡,直径为40~100 nm[3]。外泌体中包含的脂质、核酸和蛋白质分子是其能在细胞间进行信息交流和物质交换的基础[4],肿瘤相关的外泌体可通过传递这些信号分子来改变细胞微环境,从而介导癌细胞的增殖[5]、转移[6]以及免疫耐受[7]。癌细胞旺盛的生命活动使得其外泌体的分泌量通常高于正常细胞,外泌体所包含的蛋白质也往往与肿瘤的大小以及分期呈正相关性[8]。研究发现,在肿瘤发生早期,影像学方法还没有发现肿瘤实体的时候,血液中已经存在来源于肿瘤细胞的外泌体[9]。此时检测外泌体内的信号分子,可以在一定程度上反映肿瘤细胞的基因信息和增殖状况,因此外泌体是实现肿瘤早期诊断的一个非常理想的研究对象。分泌至细胞外微环境的外泌体即可进入血液,随后通过血液循环扩散至多种其他体液中,如脑脊液、尿液、胆汁、唾液、腹腔积液及支气管洗脱液[2]等。这些体液样本在临床上非常容易收集且可重复取样,这使得外泌体在肿瘤早期体外筛查方面拥有良好的应用前景。此外,外泌体的脂质双层膜结构可以防止存在于其中的信号分子被体液中的相关酶类降解,从而提高了外泌体内容物的稳定性,使外泌体内容物分子与游离在体液中的其他生物活性分子相比更具有成为一些疾病分子标记物的潜能。
蛋白质作为生命功能的承担者具有一定的组织特异性,差异表达的蛋白质不仅是区分不同来源外泌体的关键所在,也是研究外泌体起源的的重要方法[10]。近年来,飞速发展的具有高通量、高灵敏度优点的蛋白质组学技术为深入研究外泌体蛋白质提供了一个更广阔的平台,在全面诠释外泌体蛋白质的组成和功能方面发挥了重要作用。本实验探究能否利用蛋白质组学技术从肺癌患者与肺部良性结节病人血浆外泌体中发现差异表达的蛋白质,并评估超速离心法与质谱联用技术平台筛选用于肺癌早期诊断的分子标志物的可行性。
1 材料与方法
1.1 样品来源及采集
本实验室与解放军总医院第一医学中心胸外科合作,选取2017-06-15至2018-01-31入解放军总医院第一医学中心胸外科接受治疗的肺癌患者与肺部良性研究对象,获得所有病人入院接受治疗前的知情同意后,采集术前血液样品。同时收集了病人详细的临床资料,包括性别、年龄、是否吸烟、吸烟量、吸烟年限、是否传染性病毒感染和有无既往癌症病史等信息。
采集病人术前静脉血10 mL置于EDTA作为抗凝剂的血液收集管中,采血后2 h内分离血浆,室温400 r/min离心15 min,收集上层血浆-80℃保存。剔除有传染性病毒感染和既往癌症病史的病人血液样品后,共收集肺腺癌血浆样品59例、肺鳞癌血浆样品28例、肺部良性结节病人血浆8例。随机选取肺腺癌病人血浆15例、肺鳞癌病人血浆10例作为实验组,肺部良性结节病人血浆5例作为对照组,分析研究外泌体蛋白质组。
1.2 材料
兔抗补体C4a一抗(Fitzgerald公司);兔抗IgG二抗、预染蛋白质分子量标准P1103(北京普利莱基因技术公司);超高速离心机(Optima L-100XP Ultracentrifuge)(Beckman公司);液相色谱仪(EASY-nLC1000)、质谱仪(Orbitrap Fusion Lu⁃mos)(Thermo公司)。
1.3 超高速离心法提取血浆外泌体
超高速离心法主要参照Théry等[11]建立的细胞培养上清及生物学体液外泌体分离方法中相应的血浆外泌体提取方法。取冻融后的血浆样品1 mL,加入等体积的PBS稀释,4℃、2000 r/min离心30 min去除细胞,上清转移至新的离心管中,4℃、12 000 r/min离心45 min去除细胞碎片,小心吸取上清转移至2 mL超高速离心管中,4℃、110 000 r/min离心2 h,弃上清,加入1 mL PBS重悬沉淀后移入新的超高速离心管中,再加入1 mL PBS补至2 mL,重悬液过0.22μm滤网后转移至新的超高速离心管中,4℃、110 000 r/min离心70 min,弃上清,加入1 mL PBS重悬沉淀后移入新的超高速离心管中,再加入1 mL PBS补至总体积2 mL,4℃、110 000 r/min离心70 min,弃上清,沉淀即为外泌体。
1.4 质谱鉴定与数据搜索
采用基于超滤辅助样品制备(FASP)方法,在超滤管中消化提取的蛋白质。加入8 mol/L尿素溶液(含10 mmol/L DTT),56℃还原样品,室温避光用20 mmol/L碘乙酰胺烷基化20 min,尿素洗涤2次,用50 mmol/L NH4HCO3洗 涤3次,加 入40μL胰蛋白酶,37℃孵育13 h。消化得到的肽离心后真空浓缩干燥,重悬于0.1%甲酸溶液中,并经液相色谱-质谱联用分析,在Uniport_sprot人蛋白质序列数据库中检索,选取置信度高的肽段(大于95%)进行查询,每一个查询至少有5个肽段匹配,且覆盖率不低于整个蛋白质序列的15%。
1.5 银染和Western印迹验证蛋白质谱结果
用Pierce IP裂解液裂解超速离心提取的外泌体,吹打混匀,3000 r/min离心5 min,获得含有外泌体蛋白的上清。用Nano Drop 2000紫外分光度计对获得的总蛋白定量,然后进行SDSPAGE,分离胶浓度为10%。一部分凝胶用考马斯亮蓝染色法初步定性提取的外泌体蛋白质种类,但由于外泌体蛋白质含量极低,考马斯亮蓝染色时蛋白质条带显色不明显,因此采用灵敏度更高的银盐染色法(用乙醇、冰醋酸和水的混合液固定蛋白质,0.1%硝酸银溶液染色,2.5%碳酸钠、0.02%甲醛水溶液温育显色)。另一部分进行免疫印迹实验,低温湿法将蛋白质转印到PVDF膜上,用5%脱脂奶粉封闭1 h,用PBST溶液洗3次膜,用一抗(稀释比例为1∶5000)于4℃摇床孵育过夜,用PBST洗3次膜,用二抗(稀释比例为1∶8000)室温孵育1 h,PBST洗3次膜,显影。
2 结果
2.1 血浆外泌体蛋白质组的质谱分析结果
质谱定量分析共鉴定到血浆外泌体蛋白质253个,并确定其中18个在肺癌病人血浆外泌体中表达上调(表1),8个在肺癌病人血浆外泌体中表达下调(表2)。外泌体差异表达的蛋白质涉及参与受体、载体、免疫、糖酵解、基因调控、血管生成、细胞骨架等多种形式。这些蛋白质有的与细胞转导功能及免疫调节相关,在肿瘤的发生发展过程中发挥作用,在不同的病理过程中差异表达,因此具有肿瘤分子标记物的潜能。
2.2 银染和Western印迹验证结果
采用超速离心法提取上述入选病人血浆中的外泌体,裂解后获取外泌体蛋白质并通过紫外分光光度计定量,取250 ng外泌体蛋白质进行SDS-PAGE。一部分凝胶固定后用硝酸银溶液染色(图1),显色后发现每个样品中均出现多种大小不一的条带,证实了外泌体蛋白提取的多样性,也验证了蛋白质谱的分析结果。
为了进一步验证质谱的准确性,挑选质谱分析结果中肺癌病人血浆外泌体样本高表达的蛋白C4a,该蛋白是与免疫相关的补体蛋白,参与多种生理病理过程。用抗C4a抗体进行免疫印迹实验,证实该蛋白在外泌体的表达(图2)。实验结果显示,所有样品均在相对分子质量190×103左右出现一条特异性条带,说明成功提取了外泌体中的补体蛋白C4a,且该蛋白在肺腺癌病人与肺鳞癌病人血浆外泌体中的表达明显高于良性病人,该蛋白有望成为外泌体中肺癌早期诊断的有效分子。结合质谱定量分析与银染、Western印迹结果,说明我们已初步构建了血浆外泌体蛋白质组分析的技术平台,为肺癌早期诊断奠定了良好的实验基础。
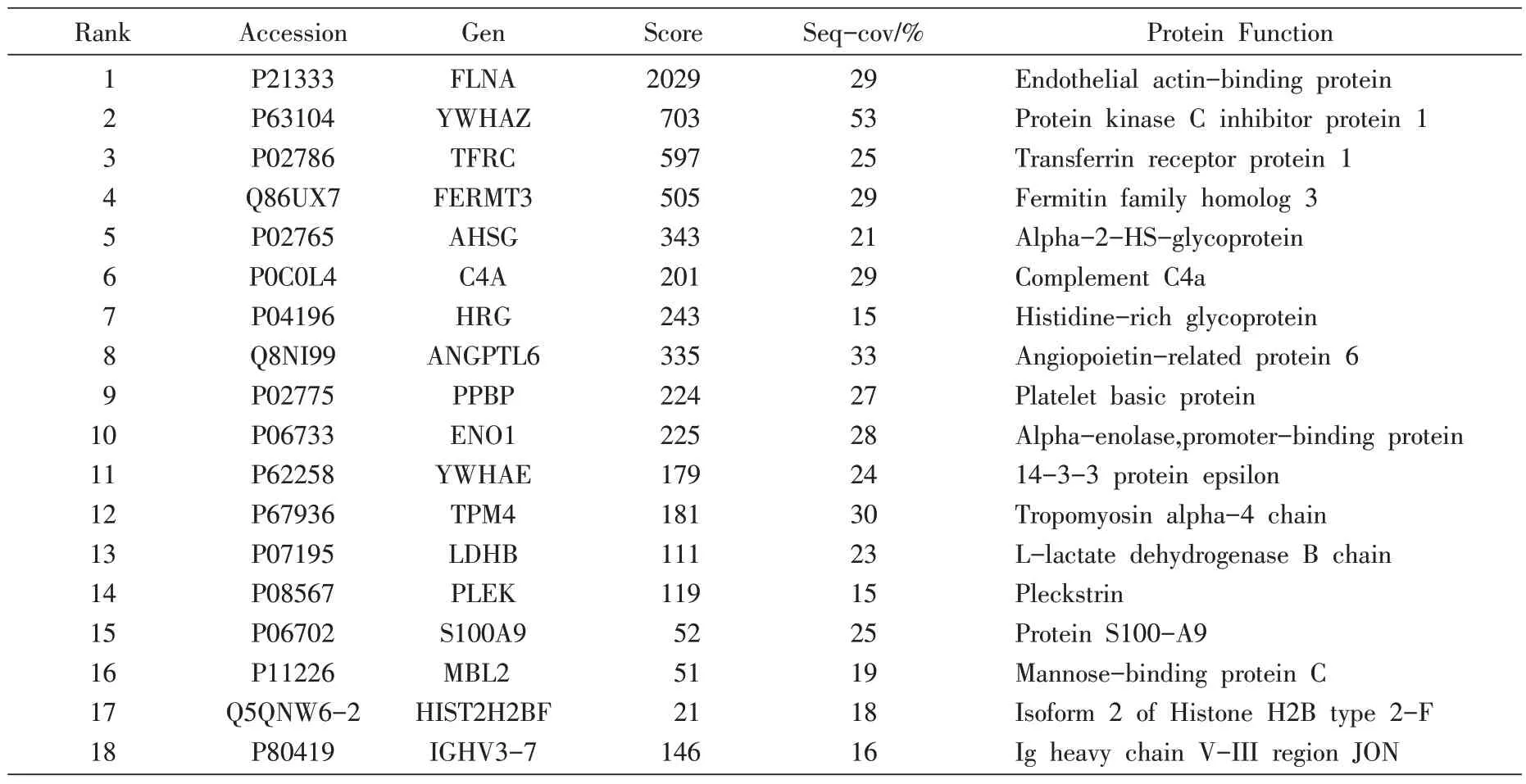
表1 肺癌病人血浆外泌体中表达上调的蛋白质
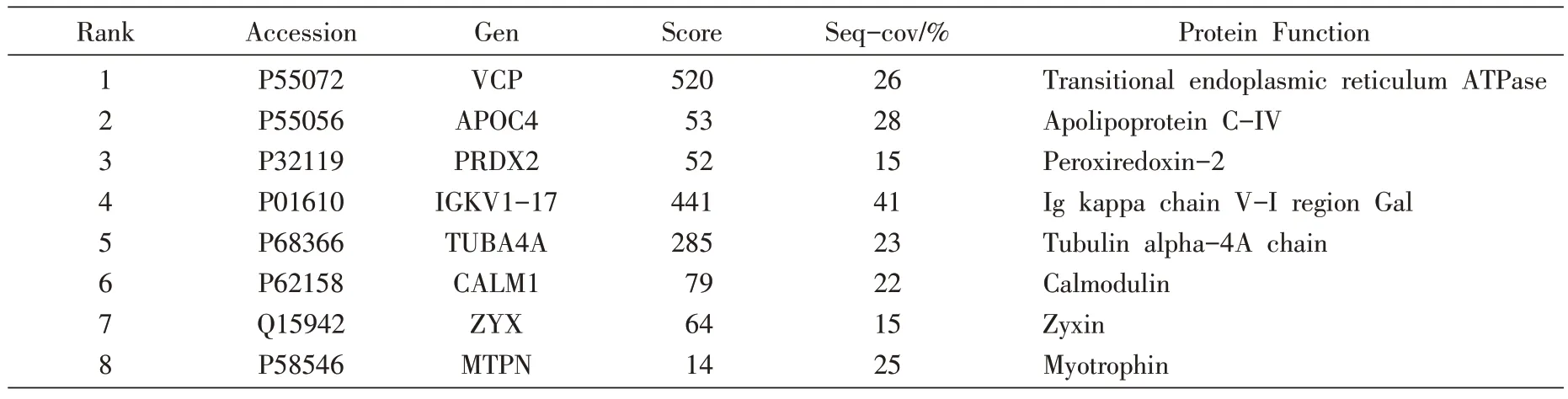
表2 肺癌病人血浆外泌体中表达下调的蛋白质
3 讨论
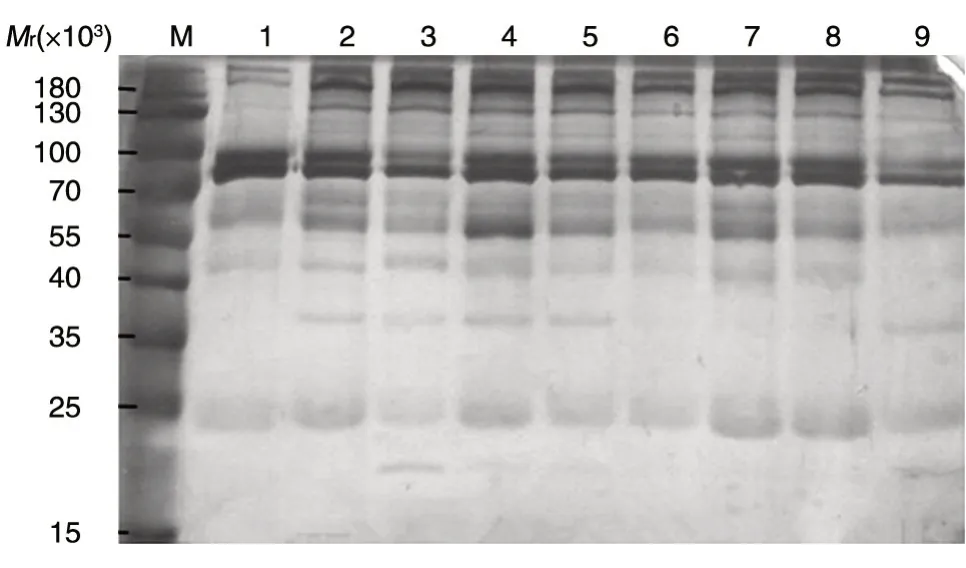
图1 银染验证提取的外泌体蛋白质
本研究检测到血浆外泌体蛋白质在肺癌患者与良性结节病人中存在差异,说明超速离心法提取样品与质谱法联用分析外泌体蛋白质表达的差异性是筛选肺癌潜在分子标志物的有效方法。尽管只用单个差异表达的蛋白质来判断肿瘤发生的可能性很小,但新的蛋白质组学技术还在不断发展,肿瘤分子的复杂性正在层层剖析中。血浆外泌体蛋白质组的分析补充了肿瘤细胞的组织学研究,为筛选更敏感的可临床应用的诊断、预后及分型的肿瘤分子标志物做出贡献。目前,已有多项研究发现肿瘤细胞来源的外泌体中特异性表达的蛋白质在肿瘤诊断方面具有极大的价值。Melo等[12]运用蛋白质组学技术筛选出胰腺癌外泌体中特异表达的蛋白质GPC1,特异性与灵敏度极高,可以作为胰腺癌体外筛查和早期诊断的分子标志物。Vardaki等[13]发现外泌体中的蛋白质periostin可以很好地将乳腺癌淋巴结转移患者与未转移的乳腺癌患者区分开来,peri⁃ostin将是一个重要的乳腺癌转移标志物。

图2 Western印迹验证提取的外泌体蛋白C4a
本实验共筛选到26个血浆外泌体差异表达的蛋白,结合研究背景,我们从中筛选出补体蛋白C4a(P0C0L4)、转铁蛋白受体(P02786)和S100-A9(P06702)3个蛋白质。补体蛋白C4a与机体免疫功能密切相关,它能够参与形成攻击外来抗原的膜相关复合物,也是激活补体经典途径的重要组成部分。最近的研究中,已经发现了补体激活在肿瘤发生和生长中可能发挥的作用,肿瘤细胞在对抗补体介导的细胞毒性作用时会持续释放补体片段导致血浆中更高水平的补体成分[14]。这与本研究中检测到的肺癌患者血浆外泌体样本中C4a的表达情况一致,表明该补体蛋白可能作为诊断肺癌的生物标志物。转铁蛋白受体是调控铁平衡和调节细胞生长的重要蛋白质,它在各类正常细胞中均低水平表达,而肿瘤细胞中的转铁蛋白受体表达水平显著增高[15]。转铁蛋白受体在肿瘤细胞中的表达水平升高可能是因为铁是参与DNA合成的重要辅助因子,肿瘤细胞迅速分裂增加了对铁的大量需求。小分子肽S100钙结合蛋白A9(S100-A9)是S100蛋白家族成员,也是一类天然免疫分子。研究表明S100-A9在多种肿瘤中具有较高表达水平,可能为肿瘤的发生、发展和转移提供了微环境[16]。综上,本研究通过对非小细胞肺癌患者和肺部良性结节病人血浆外泌体蛋白质组定量分析,鉴定出在非小细胞肺癌患者血浆外泌体中的18个高表达蛋白质和8个低表达蛋白质,共26个与肺部良性结节病人血浆外泌体表达存在差异的蛋白质分子。尽管这26个蛋白质分子在非小细胞腺癌和鳞癌中的表达相近,即无法用于区分非小细胞肺癌的表型,但它们在区分非小细胞肺癌和肺部良性结节方面可能具有潜在的诊断价值,为肺癌的早期诊断提供了新的候选分子。
基于色谱-质谱联用的定量蛋白质组学技术的突飞猛进,极大地促进了人们对外泌体的了解,为筛选外泌体来源的分子标志提供了新的视野。然而外泌体蛋白质组信息仅是拥有庞大生物学信息的外泌体中的一部分,把外泌体蛋白质组、基因组和转录组结合才能更好更全面地解读外泌体信息。
