唑来膦酸治疗COPD患者骨质疏松症的疗效及对肺功能影响的分析
2019-03-26袁红李俊翁育清欧阳剑锋
袁红 李俊 翁育清 欧阳剑锋
珠海市人民医院呼吸科,广东 珠海 519000
慢性阻塞性肺疾病(COPD)是一种以呼吸功能障碍、气流不完全可逆受限,呈进行性发展的老年疾患,而骨质疏松症已被广泛认为是COPD的主要并发症,有研究显示COPD患者有20%~58%并发骨质疏松[1], 特别是中、重度COPD患者[2]。目前关于绝经后骨质疏松的研究报道很多,却忽视了COPD合并骨质疏松的抗骨质疏松治疗。唑来膦酸可激活成骨细胞增加骨量,抑制破骨吸收溶解,从而来改善骨质疏松。为了探讨唑来膦酸对合并COPD的骨质疏松症患者的疗效,我们对52例合并骨质疏松症的COPD患者使用唑来膦酸治疗,现报道如下。
1 材料和方法
1.1 资料
选择我院呼吸科及骨科2016年4月至2018年1月期间收治的52例患者为研究对象。男,18例,女,34例;年龄53~85 岁,平均(61.4 ±3.2)岁。患者均行肺功能检查符合COPD诊断,肺功能测定均为阻塞性通气功能障碍,其中FEV1(第1秒钟用力呼气容积)为(1.21±0.38)L、FEV1占预计值的百分比为(47.3 7±14.8)%、FEV1/FVC(用力呼气容积)<70%(60.1±6.4)。患者同时行骨密度测定,并根据WHO诊断标准以T值≤-2.5确诊为骨质疏松。纳入标准:①符合慢性阻塞性肺疾病诊治标准[3];②根据WHO诊断标准,影像学及骨密度检查确诊为骨质疏松症;③临床表现以自发性全身疼痛及轻微活动骨折病史;④无脊髓及神经根受损。排除标准:①需要机械通气的COPD患者;②病理性骨折患者;③严重的内分泌疾病、代谢性疾病者;④严重肝肾疾病者;⑤对唑来膦酸过敏者;⑥治疗期间未规律治疗,中途退出者。
1.2 治疗方法
病人常规予钙尔奇D(600 mg/d),骨化三醇(0.25μg/d)药物治疗基础上,予以静脉唑来膦酸5 mg(Novartis Pharma Stein AG,规格:100 mL/5 mg)滴注,治疗后让患者多饮水,监测输注过程的不良反应。
1.3 观察指标
1.3.1视觉模拟评分法(visual analogue scale/score,VAS):患者治疗前及治疗后1年,采用VAS评估,根据结果予以临床治疗效果评价。
1.3.2活动能力评分[4]:活动能力评分1 分;行动无明显困难;2 分:行走有困难(需帮助);3 分:需使用轮椅或只能坐立;4 分:被迫卧床。
1.3.3骨密度:患者治疗前、治疗12个月后,采用法国Medilink公司生产的XR-600双能X线骨密度仪,测量部位包含腰椎正位(L2-4)和右股骨颈的骨密度(BMD)。
1.3.4肺功能:治疗前、治疗后12个月,采用美国Medgraphics公司生产的ULTIMA肺功能测定仪,测定各项肺功能指标:肺活量(VC)、第1秒用力呼气容积(FEV1)、FEV1占预计值的百分比(FEV1%)、1秒率(FEV1/FVC%)。
1.3.5骨代谢标志物:血磷(Ca)、血钙(P)、血清骨钙素(BGP)、骨源性碱性膦酸酶(bone alkaline phosphatase,BALP)、晨尿游离脱氧吡啶啉排泄率(Dpd/Cr)。治疗期间的血、肝肾功改变及不良反应也同时记录。
1.4统计学处理
采用SPSS19.0统计软件进行数据分析。治疗前后的计量资料的比较应用配对样本t检验,P<0. 05 为差异具有统计学意义。
2 结果
2.1 疼痛评分、活动能力及骨密度
从表1可以看出,患者治疗1年后VAS分值显著低于治疗前,腰椎及股骨颈骨密度(BMD)高于治疗前,活动能力评分较治疗前降低,差异具有统计学意义(P<0.05)。见表1。
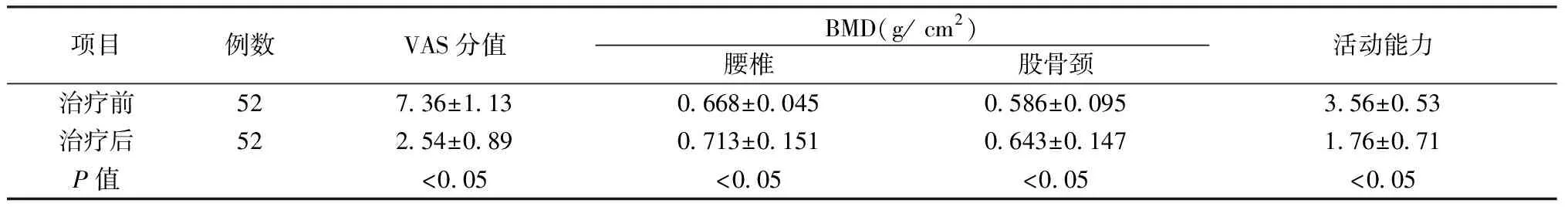
表1 患者治疗前后VAS评分、BMD变化、活动能力评分Table 1 VAS score, BMD change, and mobility score before and after the treatment
2.2 肺功能的评价
治疗1年后复查肺功能结果,FEV1及FEV1%有显著提高,差异具有统计学意义(P<0.05),而FEVl/FVC%也有升高,但与治疗前相比差异无显著性(P>0.05)。见表2。

表2 治疗前后患者肺功能变化Table 2 The change of pulmonary function before and after the treatment
2.3 相关性分析
随着肺活量VC的改善,我们发现VAS分值也呈下降趋势,两者呈负相关(r=-0. 725,P< 0. 05),活动能力评分与VC(r=-0. 725,P< 0.05)则呈负弱相关,但VAS 评分与FEV1%无显著相关性(r=0.216,P>0.05)。
治疗前COPD患者的肺功能与骨密度的相关分析显示,FEV1与腰椎间呈弱正相关,r值为0.216 (P<0.05),FEVl%、FEVl/FVC与骨密度间没有明显的相关。治疗1年后,FEVl的变化值正相关于腰椎骨密度的变化值,r值为0.534(P<0.05)。
2.4 血清ALP、血钙、血磷水平、BGP及晨尿游离脱氧吡啶啉排泄率(Dpd/Cr)的变化
治疗1年后,血钙、血磷未见明显差异,但BGP明显升高、BALP及Dpd/Cr水平值均下降,差异有显著性(P<0.05)。

表3 治疗前后血清骨代谢物水平的变化Table 3 Changes of in serum levels of bone metabolites before and after the treatment
3 讨论
本研究选取52例COPD合并骨质疏松症患者,应用唑来膦酸及协调钙剂治疗,治疗时间为1年。经过治疗后,观察患者前后骨密度、疼痛及活动能力评分、肺功能及血钙、血磷水平、BGP、BALP及晨尿游离脱氧吡啶啉排泄率(Dpd/Cr)的变化。结果显示患者治疗后,骨密度显著提高,同时BGP升高,BALP和Dpd/Cr值均明显降低,肺功能较前改善,而且VAS评分降低,其中治疗后VC、FEV1,FEV1%改善,FEV1变化值与腰椎MBD变化值之间呈正相关,结合临床,说明骨量的增高,提高了患者日常生活能力,因而肺功能也得到进一步改善,这些均说明唑来膦酸对COPD患者骨质疏松的治疗是有效和必要的。
作为老年人高发的疾病,COPD与骨质疏松症之间相互关联,COPD患者常因为机体缺氧及较差的运动能力,使得骨质量下降出现骨质疏松,而骨质疏松症也被确定是COPD的主要并发症[5]。某些细胞因子,如肿瘤坏死椅子-α、IL-6、IL-8等,可使破骨细胞增殖分化受到激发,在骨重塑及代谢中扮演了重要角色,而COPD存在的全身慢性炎症却影响这这些细胞因子[6]。COPD患者中常广泛应用糖皮质激素,糖皮质激素使用后,导致性激素分泌合成降低,甲状旁腺机能相应亢进,成骨细胞活力减少,进一步导致骨量降低;同时激素可直接增强破骨而减弱成骨作用,导致骨代谢失衡,最终导致骨密度明显减少[7-8]。目前已有研究[9]发现女性COPD患者49%可能发生椎骨骨折,激素使用者椎骨骨折发生率高达63%。
当COPD患者合并骨质疏松或发生骨折时,受限的胸廓及膈肌活动,加上本身存在的呼吸肌疲劳,导致呼吸功能进一步限制性障碍,同时由于骨折时产生的疼痛刺激,也会使得呼吸运动及咳嗽反射受抑制,最终影响了肺的通气功能[10]。本文治疗后随着疼痛减轻、活动能力增强,患者肺功能参数VC、FVC、FEV1、FEV1%明显改善,呼吸功能改善伴随VAS及活动能力评分降低反应了两者之间存在显著关联性,并在随访期间得到了进一步改善, 与文献报道基本一致[11]。
唑来膦酸作为新型的治疗骨质疏松药物,因其强大的吸附力,骨组织能够重吸收少量脱落的药物,故其只需1年1次,依从性好,而其对破骨细胞的抑制,使得骨密度得到提升[12],并激活成骨细胞,最终达到抑制骨的破坏及溶解而增加了骨量,改善了骨质疏松[13]。Dpd/Cr是一种反映骨吸收的理想指标[14],其变化反映了骨转换过程中的骨吸收程度。本研究中发现唑来膦酸对患者骨密度降低抑制明显,同时BGP升高,BALP和Dpd/Cr值均明显降低,这也与唑来膦酸抑制了骨溶解,减少骨破坏的原理相符。
本研究中发现43.4%患者在输注后发生发热、肌肉酸痛等反应,而文献报道的急性期不良反应可达80%[13-14],分析原因可能是我们给予非甾体抗炎药预防,另外可能性是COPD患者机体的免疫应答受抑制,反而降低了其不良反应。
综上所述,唑来膦酸治疗不仅提高骨密度,改善骨生化指标,亦能改善患者肺功能及生活质量。针对COPD骨质疏松患者的治疗效果肯定,值得进一步推广。本研究也存在一定不足,纳入病例数少,观察时间短,因此还需要大宗病例和长时间观察来验证。
