损害控制在肠外瘘致严重腹腔感染再次手术中的应用
2019-03-23牙韩清毕连臣王晓通
李 雷,麦 威,牙韩清,毕连臣,王晓通,谢 思,汪 龙,沈 印
肠外瘘是指胃肠道与其他空腔脏器、体腔或体腔外有异常通道,肠内容物经此通道排出体外,并由此而引起感染、体液丧失、内部稳态失衡、器官功能受损等改变。肠外瘘是腹部外科于术后最严重的并发症之一,严重威胁患者的生命安全。随着科技进步,腹部外科技术得到大幅提升,但肠外瘘的发生仍然无法杜绝[1]。
20世纪80年代以来,南京军区总医院(现东部战区总医院)肠瘘治疗中心黎介寿院士团队系统阐述肠外瘘的诊疗过程,使我国肠瘘治疗水平迅速提升,病死率由70年代的50%~60%,下降为目前的5%~25%[2]。但在肠外瘘的治疗过程中出现严重腹腔感染尤其凶险,遵循怎样的手术原则值得手术医师深思。
严重腹腔感染不仅会引起脓毒症感染性休克、无法控制的大出血、急性腹腔间隙综合征,也会引起机体代谢和免疫功能障碍,甚至出现多器官功能障碍,最终导致多器官功能衰竭、死亡。王革非等[3]率先提出在复杂腹腔感染及其规范化治疗中贯彻损害控制理念并建立阶梯式处理方案,为此类肠外瘘患者的再次手术指明了方向。本研究对广西壮族自治区人民医院胃肠外周血管外科2013年6月—2017年1月收治的肠外瘘患者进行分析,回顾性研究其中因肠外瘘致严重腹腔感染行再次手术治疗的病例,评估损害控制的应用效果。
临床资料
1 一般资料
本组因严重腹腔感染行再次手术的肠外瘘患者24例,男性19例,女性5例;年龄18~74岁,平均57.1岁。纳入标准:(1)肠外瘘均经CT及造影检查明确瘘口部位;(2)严重腹腔感染是指合并有重症脓毒症或脓毒症休克的腹腔感染;(3)经有效复苏后能耐受手术麻醉。排除标准:(1)已在外院行2次及2次以上手术病例;(2)合并多器官功能衰竭,经重症监护积极复苏仍无法耐受手术。
2 肠外瘘的治疗
肠外瘘患者均使用消化道造影、引流管造影或CT和B超检查明确瘘的部位、走行,内口、外口的位置以及瘘的远端有无梗阻等情况;使用黎氏双套管建立通畅引流;使用“第三代头孢菌素+奥硝唑”为首先经验用药方案,并根据药敏结果调整抗生素方案;根据肠功能恢复情况,使用肠内肠外营养支持治疗。笔者医院肠外瘘患者的治疗过程中出现严重腹腔感染,需要再次进行手术的适应证:(1)积极抗感染治疗后腹腔感染无法局限,经反复定位穿刺仍无法建立通畅的冲洗、引流,患者出现弥漫性腹膜炎、脓毒性休克;(2)无法控制的大出血,经内镜及介入止血治疗后仍需持续输注红细胞3h≥2U;(3)出现腹腔间隙综合征(abdominal compartment syndrome,ACS),腹内压≥20mmHg,并伴有器官功能障碍;(4)经积极抗休克治疗后评估可耐受手术[3]。
3 损害控制
1993年Michael等[4]在腹部穿透伤患者的救治过程中,首次提出了损害控制手术(damage control surgery,DCS)概念,即根据患者身体状况、病变的范围、术者的技术、现有的诊疗条件等,为危重患者设计最佳的手术方案,将提高存活率作为首要目标。本研究使用的DCS步骤:(1)延长原腹部切口进腹,如原腹腔镜手术则行腹部正中探查切口,切口足够长,避免二次肠管损伤;(2)控制感染源,不追求清除所有坏死组织及脓苔,使用大量等渗液冲洗腹腔(6 000mL),注意两侧膈下的冲洗;(3)不行肠瘘修补术,有条件的低位肠外瘘在瘘口近端提出肠管造瘘,无法造瘘及高位瘘患者在瘘口周围使用黎氏双套管建立足够多并且通畅的冲洗引流途径;(4)建立肠内营养支持途径,有条件者术中留置空肠营养管、三腔营养管,部分高位瘘患者谨慎使用空肠造瘘管由腹壁引出;(5)严格掌握腹腔开放指征,尽可能缩短手术时间(1~2h)、达到缓解病情及改善脏器功能即可。
损害控制性复苏(damage control resuscitation,DCR)是指在损害控制的基础上,使用限制性液体复苏和止血性复苏,纠正患者的凝血功能障碍、酸中毒以及低体温,目的是改善组织低灌注及维持术中麻醉血压[5]。其中限制性液体复苏强调在活动性出血控制之前,控制患者血压低于正常血压,避免凝血功能障碍和再次出血;止血性复苏针对失血性休克患者凝血功能障碍,早期输血和联合使用止血药物,维持血浆和血红细胞比例接近生理水平。
结 果
1 肠瘘部位
肠外瘘原因:胃肠道肿瘤手术21例,腹部创伤1例,消化道穿孔出血1例,胰腺疾病1例。根据肠外瘘的部位分为:小肠瘘13例,其中高位瘘(十二指肠及距离十二指肠100cm以内的空肠)7例;结直肠瘘10例;胃穿孔部位瘘1例。见表1。
2 APACHE-II评分
针对全身疾病的严重程度,使用急性生理与慢性健康评分-Ⅱ(acute physiology and chronic health evaluation-Ⅱ)进行评估,其与预后的相关性见表2。
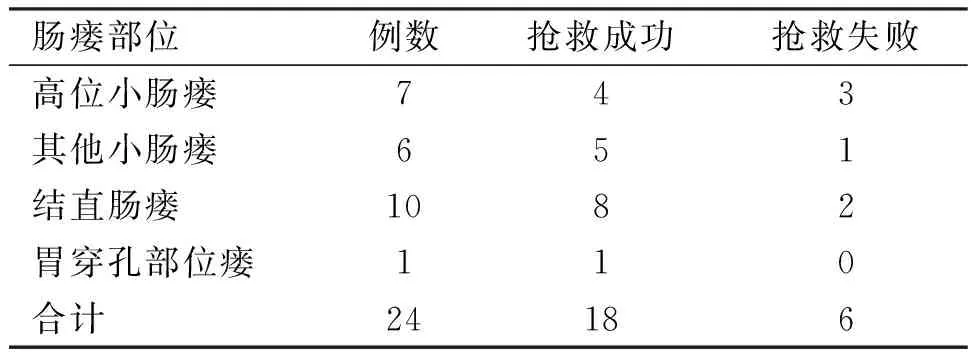
表1 肠瘘部位与结局(n)
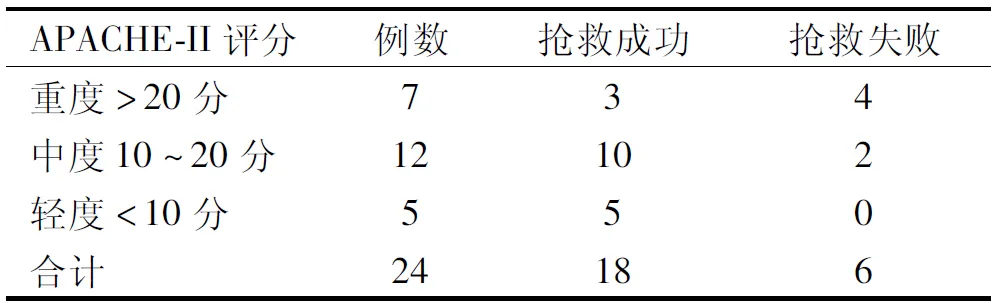
表2 APACHE-II评分与结局(n)
3 再次手术的主要原因
本组患者因肠外瘘致严重腹腔感染再次手术主要原因:弥漫性腹膜炎(14例),腹腔无法控制的大出血(6例),明确有急性ACS(4例)。
4 腹腔开放技术
腹腔开放技术作为DCS的重要组成部分,其目的除了降低腹内压防治ACS外,还包括恢复腹壁生理结构、保护腹腔脏器、减少体液丢失、充分引流避免脓液聚集等,分为腹腔开放和暂时性腹腔关闭,两者缺一不可。笔者医院该类手术患者针对创面是否存在开放瘘口采用两种简单的暂时性关闭方式,一种是当存在可见的开放瘘口时,因肠壁水肿及感染无法行肠切除、肠吻合、瘘口修补,建议首先使用凡士林纱布覆盖肠管,表面放置多根黎氏双套管冲洗引流记出入量,最外层覆肠外营养袋直接与皮肤缝合(图1)。既起到减压效果,也可充分引流瘘液、记录腹腔液体丢失量。

图1患者男性,64岁,直肠癌术后吻合口瘘合并腹壁切口全层裂肠外露。a.腹壁切口全层裂开并肠外露;b.予凡士林纱布及黎式双套管冲洗引流;c.术后3周瘘及腹壁切口愈合
另一种方式为Bogata法,简单易行:当开放伤口没有明确瘘口时,将肠外营养输液袋剪开,其边缘与腹壁皮肤缝合,暂时性关闭腹腔(图2)。待病情稳定后行创面负压引流,促进肉芽组织增生,如治疗过程中出现开放瘘口,则转为第一种方式。

图2患者女性,35岁,乙状结肠癌术后腹壁切口感染裂开。a.予肠外营养输液袋暂时关闭腹腔;b.使用VSD负压膜治疗2周时创面情况;c.术后复查时腹壁切口愈合情况
5 并发症及抢救失败原因
再次手术时使用损害控制虽然能极大缓解疾病进展,但因肠外瘘对各系统生理功能影响巨大,术后的出血、感染、肠空气瘘、肠道功能障碍、内环境紊乱、电解质失衡、持续的高分解代谢状态等并发症仍需认真对待,逐步解决。特别是高龄和体弱患者虽然腹腔感染严重,但无明显腹膜炎体征。本研究中引起抢救失败的原因:6例死亡或放弃治疗患者中,继发腹腔内出血2例,重症胰腺炎1例,多发肠空气瘘1例,肝功能衰竭1例,呼吸机无法脱机自动出院1例。
讨 论
肠外瘘引起的病理生理改变复杂,但感染、内稳态失衡、营养不良是肠外瘘患者的三大主要病理生理改变。随着医学的发展,肠外肠内营养支持治疗、抗感染降阶梯疗法、微创穿刺引流等技术逐渐解决了以上问题,多学科综合诊疗成为肠外瘘标准配置。但是严重的腹腔感染仍然是临床常见危重症,何时手术干预,使用哪种手术方式时时考验着外科医师。目前,肠瘘的手术治疗成为有针对性的选择,需要严格把握手术适应证及积极术前准备[6]。
针对肠外瘘引起的严重腹腔感染,笔者建议围手术期及术中均应用损害控制原则处理,尽可能缓解病情进展,为后续治疗提供基础。因为腹部CT不仅可以客观呈现感染病灶、腹腔脏器的相关改变,也可以准确反映肠道水肿及积气积液等情况,建议肠外瘘再次手术前作为首选检查。
DCS作为严重创伤患者手术救治方案,对再次手术治疗的指征要求非常严格。要以患者生存为目标,以术后生活质量为前提,而不是一味追求手术完美,这一理念适用于外科的各个专业。通过对肠外瘘诊疗的不断实践,李宁[7]提出在存在以下情况时才考虑计划外再次手术:(1)经过内镜及介入治疗后仍难以控制的进行性出血;(2)残留消化道损伤导致全身炎症反应综合征和休克;(3)ACS。而当决定再次手术干预时也需要充分贯彻损害控制的理念,术前需重新评估影像学资料,必要时携带呼吸机、监护仪、血管活性药物等再次外出CT检查。建立以手术医师为主导,重症监护、麻醉科、手术室共同组成的多学科诊疗小组,明确此时手术目的在于控制感染和出血、缓解患者的病情,而不是盲目的去修补瘘口[8]。在围术期积极纠正低体温、休克及凝血功能障碍,维持呼吸、循环系统功能;术前充分备血,重视血浆胶体的应用,避免术中腹内压骤降时引起的致命性损害;术中探查时也需严格遵守损害控制原则及步骤,因腹腔严重感染致肠管、脏器水肿粘连明显,过度分离及追求完全清除感染坏死组织不仅无益于手术结局,而且会诱使大量细菌及内毒素入血,引起多器官功能障碍。术中明确感染灶位置后仅适当清理坏死组织,大量等渗盐溶液冲洗腹腔至清亮,由主刀医师设计、放置多根黎氏双套管、三套管,目的在于建立充分的冲洗引流。而对于严重腹腔感染引起的大出血,因感染所致创面的弥漫性渗血,无法通过结扎、电凝止血,单纯使用纱条、纱布填塞有加重腹腔感染的可能,因此推荐使用黎介寿院士设计的“三明治”法,即在创面填塞纱布的基础上放置黎氏双套管持续冲洗、引流,在观察渗血情况的基础上还可引流脓液,有效控制腹腔感染,术后待病情稍稳定即可进一步行介入血管造影[9]。
严重腹腔感染是感染性疾病的第二大致死病因,上述损害控制理念为外科医师提供了新的思路和方向。如并不能有效控制肠瘘所致的复杂腹腔感染,常合并腹腔高压症(intra-abdominal hypertension,IAH)甚至发生ACS,在ICU中ACS的病死率高达60%,均需要早期的外科手术或放射介入干预[10]。当ACS合并器官功能障碍时,腹腔开放为处理严重腹腔感染提供了新的选择[11],适应证主要包含以下3点:(1)致命性腹腔出血;(2)ACS;(3)严重腹腔感染。在实施腹腔开放时,必须牢记及时关闭腹腔,因肠壁长时间摩擦及接触空气极易引发肠空气瘘,大量体液的丢失、腹腔二次污染、创面出血、腹壁疝等并发症也严重威胁患者的生命。本组即出现1例多发肠空气瘘最终死亡。目前常用的暂时关腹方法有皮肤关闭、筋膜关闭和负压辅助关闭。在应用过程中,如果忽视并发症的防治,其优势便无法体现,甚至会导致治疗失败。近期也广泛采用聚丙烯补片暂时性关腹,但远期并发症可能导致严重后果。有学者报道部分患者放置聚丙烯补片10~15年后出现肠内瘘,具体原因尚需进一步研究[12]。因此,笔者医院采取肠外营养袋做为暂时性腹腔关闭的主要材料,再根据术后腹腔感染情况逐步缩小切口,直至肉芽增生及使用负压吸引及植皮完成腹腔关闭。
综上所述,在肠外瘘的整体治疗中,特别是严重腹腔感染需再次手术的患者,损害控制为外科医师提供了新的手术选择,贯彻损害控制的原则,恰当使用DCS、DCR等技术,可以提高生存率,改变疾病的最终结局。
