固态电子介质Z型光催化剂g-C3 N4/Ag/Ag3 PO4的设计合成与光解水性能研究
2019-03-23毛晨憬司华艳邓祺鑫曹雅兴
毛晨憬,司华艳,2,邓祺鑫,曹雅兴
(1.石家庄铁道大学 材料科学与工程学院,河北 石家庄 050043;2.河北省交通工程材料重点实验室,河北 石家庄 050043)
0 引言
近年来,随着环境污染越来越严重,开发可再生的清洁能源和治理环境污染是人类发展的必然趋势。关于太阳能利用的研究,特别是太阳能光催化研究的发展十分活跃,尤其是在半导体光催化剂研究方面。2006年,C3N4作为有机半导体在材料科学和催化领域作为非金属催化剂的应用被发现[1-2],2009年,Wang X C et al[3]发现C3N4在可见光的照射下可将水分解为氢气和氧气,自此C3N4迅速成为全世界范围内光催化研究领域的热点。C3N4有5种同素异形体结构[4]:α-C3N4、β-C3N4、立方C3N4、准立方p-C3N4和石墨相g-C3N4,其中石墨相g-C3N4是5种C3N4中最稳定的构型[5],它具有以3-三嗪环为结构单元的类石墨的片层结构,C、N原子均发生sp2杂化,且所有原子的p轨道互相重叠形成离域π键,即形成共轭电子能带结构[5]。但是C3N4也有比表面积小、光量子效率低、光生载流子传输慢等缺点,导致光催化效率低。现有报道可以通过改性方法如纳米法扩大比表面积,元素掺杂、构筑复合物异质结等方法来调节能带结构[6-7],但是这些方法都会在一定程度上降低半导体本身氧化还原电势绝对值[8],进而降低催化剂氧化还原能力,同时现有体系在光催化过程中还需要加入牺牲剂(例如:电子牺牲剂Ag+,空穴牺牲剂Na2S/Na2SO3)[9]。
为了克服上述缺陷,人工模拟光合作用提供了很好的思路。通过设计Z型催化体系,将两种半导体光催化剂放入同一个催化环境中,分别为PSI和PSII,用氧化还原介质传递电子和空穴,在两种光催化剂上分别发生氧化和还原反应。为了避免氧化还原介质在反应过程中稳定性较差以及无电子介质欧姆接触电阻较大的不足,金属电子介质Z型光催化体系优势脱颖而出。光激发PS II产生的电子通过电子介质传导与PSI半导体上的空穴复合,不仅保留了PSI较负的导带位置(还原电势)和PSII较正的价带位置(氧化电势),还使得光生电子和空穴富集在不同的半导体上,这样使得催化剂保持了较高的氧化还原电位,而且在空间上将光生电子和空穴分离,避免了电子和空穴之间的复合[10-12]。
2010年叶金花教授课题组在Nature Materials上首次报道了Ag3PO4的光催化性质[13],发现其可见光催化降解或析氧性质远大于其它常用的可见光催化剂如WO3、BiVO4、N掺杂的TiO2。Ag3PO4的催化活性与其晶面结构密切相关,研究发现Ag3PO4的{110}晶面的活性强于{100}晶面[14]。因此选择十二面体结构的Ag3PO4和g-C3N4来构筑Ag金属电子介质Z型光催化体系[15]。半导体材料较负的导带位置、足够正的价带位置以及光生载流子寿命长是实现光催化H2O反应的关键,所以结合两者的导带价带位置来实现类比植物光合作用的Z型光催化剂。
1 实验
1.1 实验材料
尿素(分析纯,天津市永大化学试剂有限工司),硝酸银(分析纯,上海精细化工材料研究所),乙酸银(分析纯,阿法埃莎(中国)化学有限公司),磷酸氢二钠(分析纯,天津市津东天正精细化学试剂厂)。
1.2 样品制备
十二面体Ag3PO4的制备:0.501 g CH3COOAg溶于100 mL水中,在搅拌状态下滴加0.15 M的Na2HPO4溶液,当溶液变成黄色后离心,用去离子水洗涤后用去离子水和乙醇各洗3次,在60℃真空干燥。g-C3N4的制备:取20 g尿素放到氧化铝坩埚中,盖好盖子放在马弗炉中加热至550℃,保持4 h,升温速率为4.5℃/min。g-C3N4薄片制备:将在马弗炉中烧好的g-C3N4再次放入到马弗炉中进行加热,去掉盖子升温至550℃,升温速率为5℃/min,加热4 h后取出。以下实验中用的g-C3N4都为g-C3N4薄片。g-C3N4和Ag3PO4十二面体复合物的制备:取0.002 3 g g-C3N4加入去离子水100 mL,加入0.75 g AgNO3之后暗反应30 min,之后光沉积60 min。加入0.25 g CH3COOAg,在搅拌状态下滴加0.15 M的Na2HPO4水溶液,当溶液变成黄色后离心,用去离子水洗涤后烘干。
1.3 光催化实验
光催化制氧:在光分解水反应器中分别放入单体g-C3N4、Ag3PO4和不同比例的复合光催化剂做光分解水实验来做对比,加入去离子水至120 mL,冷却水温度设置为8℃。做光分解水实验时先把反应器抽真空,然后氙灯光照,每30 min进一次样,总共光照4 h,产生的气体通过色谱仪来测定。
自由基捕获:取样品0.1 g g-C3N4/Ag/Ag3PO4放入60 mL RhB溶液中(10 mg/L),光照前在黑暗条件下搅拌30 min保证RhB在催化剂表面的吸附平衡。其中分别加入1 mM EDTA作为h+捕获剂,1 mM IPA作为·OH捕获剂,1 mM BQ作为·O-2捕获剂。
1.4 表征仪器
扫描电子显微镜(SEM,日本电子公司JSM-5600LV);透射电镜(TEM,日本电子株式会社JEM-2010型);X射线衍射仪(XRD,德国布鲁克公司D8 Advance型);紫外-可见光漫反射光谱仪(hitachiU4100);X射线光电子光谱(XPS,Axis Ultra日本岛津集团全资子公司);光解水制氧装置(LabSolar-ⅢAG,北京泊菲莱科技有限工司);色谱仪(GC7900,上海天美科学仪器有限工司);氙灯光源(PLS-SEX300北京泊菲莱科技有限工司)。
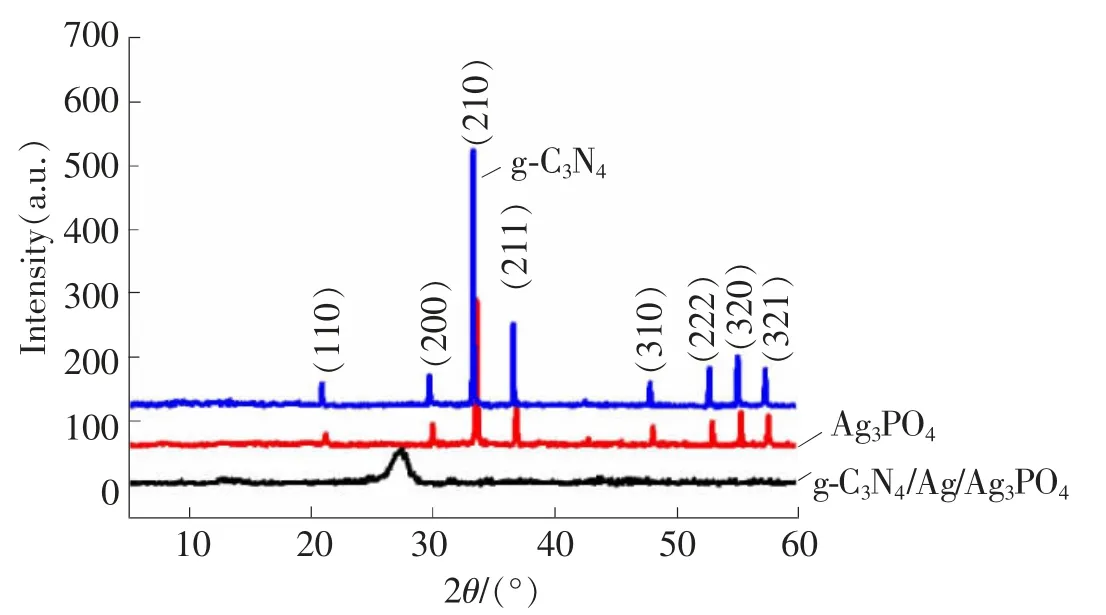
图1 g-C3 N4、Ag3 PO4和g-C3 N4/Ag/Ag3PO4样品的XRD图
2 结果与讨论
2.1 催化剂的表征
图1为类石墨烯g-C3N4、Ag3PO4和g-C3N4/Ag/Ag3PO4复合光催化剂的XRD图谱。从图中可以看出g-C3N42θ=13.1°对应的特征峰为晶面(100),该峰是由夹层结构引起的,为C3N4的面内结构堆积峰,其峰高变得不明显,是由于g-C3N4经过二次热处理后平面尺寸的减少造成的,说明体相C3N4经过二次热处理后,变为少层类石墨烯g-C3N4。2θ=27.3°对应的特征峰为晶面(002),该晶面是为g-C3N4中叠加的共轭芳香体系的吸收峰[16],两个衍射峰均与标准卡片(JCPDS No.87-1526)一一对应。Ag3PO4中所有的衍射峰与标准卡片(JCPDS No.06-0505)晶面特征衍射峰对应,表明纯Ag3PO4为立方晶体结构。对于Z型光催化剂g-C3N4/Ag/Ag3PO4,其中的特征峰和Ag3PO4特征峰相对应,表明加入的g-C3N4并没有改变Ag3PO4的晶体结构。复合光催化剂中并没有显示出g-C3N4的特征峰和Ag的特征峰,这是由于g-C3N4和Ag的含量非常少,导致特征峰不明显。

图2 Ag3PO4的TEM图谱

图3 Ag3PO4的SEM图谱

图4 g鄄C3N4光沉积Ag

图5 g鄄C3N4/Ag/Ag3PO4 TEM

图6 g鄄C3N4/Ag/Ag3PO4 XPS全谱图
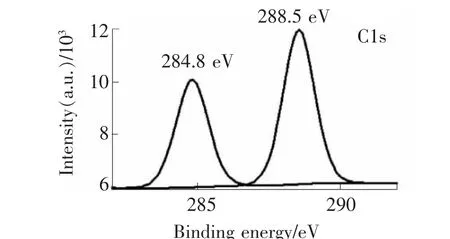
图7 元素C的XPS图谱
图2是Ag3PO4的透射电镜图谱,其形貌为十二面体,十二面体Ag3PO4对应{110}晶面,具有更高的表面能和更多的活性位点。图3为Ag3PO4扫描电镜图谱,整个图谱均为规则的十二面体,Ag3PO4粒径大小为500 nm左右,与TEM结果一致。图4是经过二次热处理过的g-C3N4经过光沉积银的透射电镜图,可以看出热处理后,g-C3N4的厚度均匀,而且表面有光沉积上的银单质,银单质大小为20 nm左右。图5是Z型光催化剂g-C3N4/Ag/Ag3PO4光催化剂的TEM图,Ag3PO4周围的物质是Ag和g-C3N4,表明两种物质复合良好。
图6是g-C3N4/Ag/Ag3PO4X射线光电子能谱图,进一步分析了样品的化学成分以及原子价态,证明g-C3N4/Ag/Ag3PO4中Ag,O,P,C,N的存在。图7是C1s的高分辨率XPS光谱,两个特征峰分别集中在284.8 eV和288.2 eV,其中284.8 eV峰源于外界环境中的碳源。288.2 eV峰源于C3N4框架中典型的C—N—C中的C元素[17]。图8为g-C3N4/Ag/Ag3PO4中的Ag3d特征峰,其分别位于368.4 eV和374.4 eV。虽然在XRD图中找不到银单质的峰,但是在XPS中的374.4 eV对应的峰证明在复合物表面存在银单质,这与TEM图上的Ag结果一致[18]。368.4 eV的峰证明有Ag+的存在,对应Ag3PO4里面的银元素。图9中P2p峰的位置是133.6 eV,对应Ag3PO4的PO3-4里面的磷元素[19-20]。
图10展示了纯相g-C3N4、Ag3PO4和复合材料g-C3N4/Ag/Ag3PO4的UV-vis DRS谱图,从图10中可以看出g-C3N4的吸收边大约在460 nm,Ag3PO4的吸收边大约在550 nm,复合光催化剂的吸收边发生了红移,并且在可见光区域的吸收明显增强,这可能要归功于表面银的表面等离子共振[21-22]。通过g-C3N4、Ag3PO4和复合材料g-C3N4/Ag/Ag3PO4光催化剂的过能带转换作图11,g-C3N4对应的带隙能为~2.7 eV,Ag3PO4对应的带隙能~2.25 eV,与文献的结果相符[23-24]。

图10 UV-vis DRS图谱
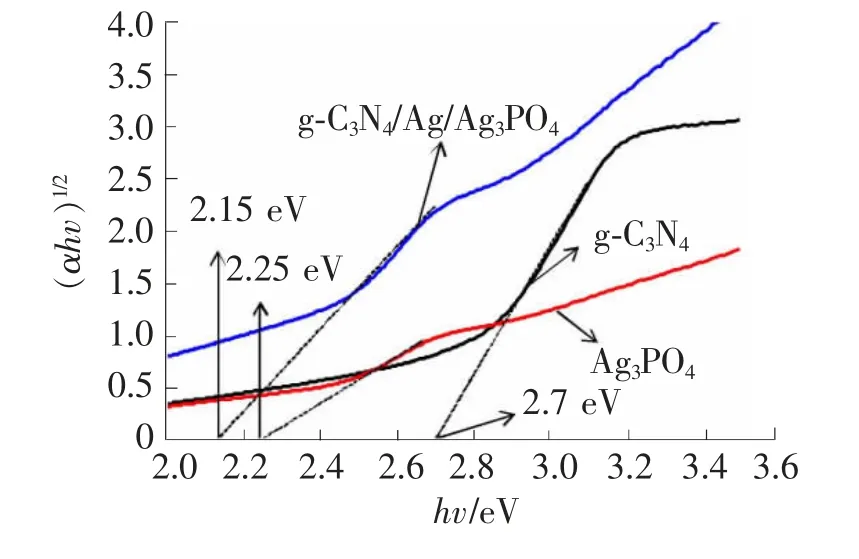
图11 能带转换图谱
图12是光催化剂在光照下的产氧气量对比图,从图中看出光沉积银后的g-C3N4没有氧气产生[8]。Ag3PO4产生的氧气量为24.56μmol·g-1·h-1,复合光催化剂g-C3N4/Ag/Ag3PO4产氧气量是Ag3PO4的10.4倍,为257.45μmol·g-1·h-1,说明Z体系复合物起到了加速分离电子-空穴的作用,并有效抑制了电子-空穴的复合,提高了光催化性能。
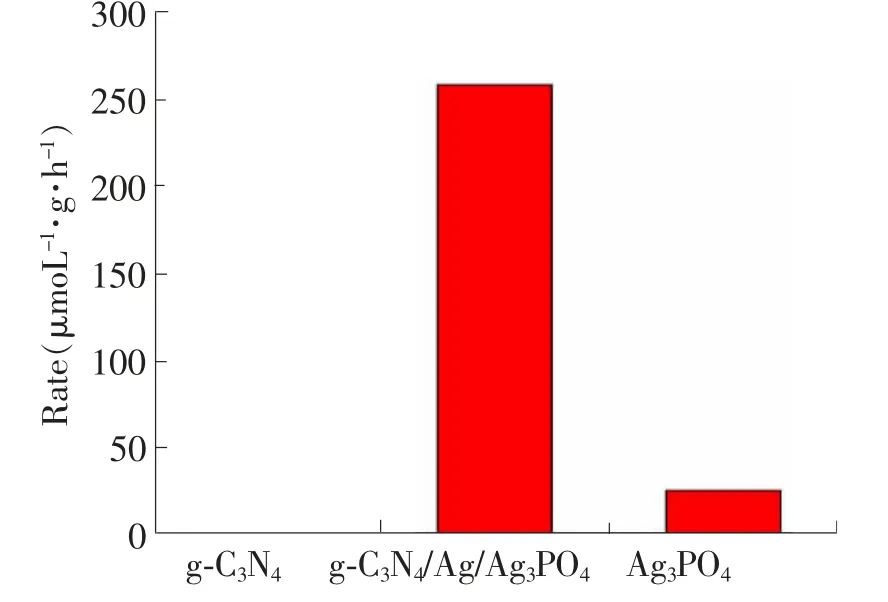
图12 g-C3 N4、Ag3 PO4和复合材料g-C3 N4/Ag/Ag3 PO4的光分解水产氧气量图
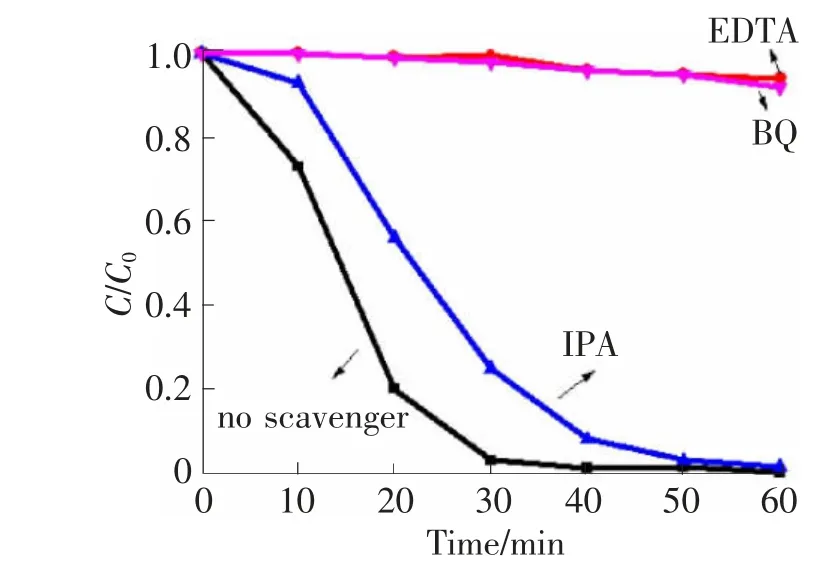
图13 g-C3 N4/Ag/Ag3 PO4在捕获剂作用下降解RhB图
2.3 反应机理
为了验证光催化剂的反应机理,做了g-C3N4/Ag/Ag3PO4降解RhB染料过程中自由基的捕获实验。从图13实验结果可以看出,在加了EDTA和BQ后,g-C3N4/Ag/Ag3PO4降解RhB的速率大大降低,而加入IPA后对g-C3N4/Ag/Ag3PO4降解RhB的速率影响较小,说明反应过程中h+和·O2-是主要的活性物质。结合两者VB和CB位置,其中Ag3PO4的CB是0.34 eV vs NHE,比O2/·O-2(-0.33 eV)更正,所以Ag3PO4不能将O2还原为·O-2自由基[25-28]。
由此做出图14复合光催化剂的反应原理图,如果两者按照图14(b)所示的传统方式转移电子空穴,将不能产生超氧自由基。这与降解RhB和光分解水实验结果相悖[29-30]。说明两者是按照图14(a)所示的方式进行转移电子空穴。其中Ag3PO4的电子转移到银单质上,因为银的费米能级比Ag3PO4的CB更正。同时,g-C3N4VB上的空穴也能转移到银单质上,因为银的费米能级比g-C3N4的VB的费米能级更负[31]。所以银单质作为Ag3PO4CB上的电子和g-C3N4VB上的空穴的复合中心能有效地转移电子和空穴,有效地抑制了电子—空穴复合。
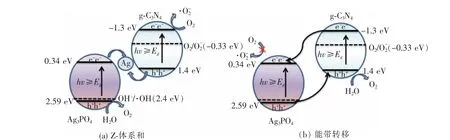
图14 g-C3 N4/Ag/Ag3 PO4的反应机理图
3 结语
通过尿素二次热处理的方法制备出类石墨烯g-C3N4,光沉积银后再通过共沉淀的方法制备出Ag电子介质Z型光催化剂g-C3N4/Ag/Ag3PO4。制备出的复合物光解水的产氧气量是单体Ag3PO4的10倍。这是由于制备的Z型光催化剂不仅有效拓宽了可见光的吸收范围,而且还借助了电子介质Z型光催化剂具有的优势:电子空穴有效的分离,在不同催化剂上分别完成氧化反应和还原反应,抑制了逆反应的进行。
