食品中硒形态测定的不确定度评价①
2019-03-20金婉芳钟莺莺曹国洲
谭 曜 蒋 立 佟 岩 金婉芳 钟莺莺 曹国洲
(宁波海关技术中心 浙江宁波315012)
硒是人体不可缺少的微量元素之一,成人最低日需量为40 μg。由于硒的主要生物活性与人类健康及动植物生长代谢关系密切,硒的药物价值已得到普遍重视。现已知硒具有治癌、抗衰老功能,为治疗地方病(如克山病、大骨节病、大脖子病等)、贫血病、冠心病、糖尿病、心血管病、视力障碍等23 种病变的要药[1]。有研究表明,人体内硒生物活性不仅取决于摄入的总硒量,还与硒的化学形态密切相关[2]。常见的硒形态有亚硒酸盐[Se(Ⅳ)]、硒酸盐[Se(Ⅵ)]、硒代胱氨酸(SeCys2)、硒代乙硫氨酸(SeEt)、硒代蛋氨酸(SeMet)等。由于人与动物对硒的需求量与中毒量间阈值很窄,不同硒形态的毒性亦不同。因此,定性定量分析不同硒形态对硒的安全使用具有重要意义[3]。
由于测量误差的存在,实验中无法得到测量结果的真值。过去对检测结果的准确度用误差表示,现在,国际上通用不确定度反映测量结果的可信程度。不确定度是与测量结果相关联的参数,表征合理赋予被测量值的分散性[4-5]。不确定度是对测定结果的信息补充,反映了测量结果可信程度的高低,是个确定的值。一方面便于评定可靠性,另一方面也增强了测量结果间的可比性。
通过建立食品中硒形态的测定方法,按照JJF 1059.1-2012《测量不确定度评定与表示》[6]《化学分析中不确定度的评估指南》[7]规定的基本方法和程序对食品中硒形态的测试结果给予不确定度评定,一方面为国家质量检测和监督部门提供相关数据支持,尤其当食品中硒形态的含量处于临界值时,用含不确定度的检测报告作为判定依据,可有效规范市场秩序,保障消费者权益[8],另一方面也为实现国际检测数据互认、全球经济交流与发展提供不可缺少的方法和手段。
1 材料与方法
1.1 材料
柠檬酸,国药集团化学试剂有限公司;氨水,国药集团化学试剂有限公司;蛋白酶K,百灵威公司。除另有说明外,所用试剂均为优级纯,实验用水应符合GB/T 6682规定的一级水。
标准储备液:亚硒酸盐[Se(Ⅳ)]、硒酸盐[Se(Ⅵ)]、硒代胱氨酸(SeCys2)和硒代蛋氨酸(SeMet)标准储备液由中国计量科学研究院提供,浓度分别为68.9、75.1、93.5 和97.9 mg/kg,4℃冰箱保存备用。硒代乙硫氨酸(SeEt)由加拿大TRC 公司提供,纯度为98%,25 mg 装。称取0.011 2 g SeEt 固标至标准配备瓶内,去离子水定量至112 g,制成100 μg/g 标准储备液。
标准工作液:分别称取2.000 0 g Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeMet 标准储备液至25 mL 标准配备瓶内,用去离子水分别定量至13.680 0、15.020 0、18.700 0 和19.580 0,制成10 μg/g 标准使用液,再分别吸取10 mL 各形态标准溶液至100 mL 容量瓶中定容,配制成1.0 μg/g 标准工作液。取10 mLSeEt 标准储备液至100 mL 容量瓶中,用去离子水定容至刻度,得10 μg/g SeEt标准工作溶液。
分别吸取一定量的标准工作液,稀释配制SeⅣ和SeCys2 浓度均为10、25、50、100和250 ng/g;SeⅥ为20、50、100、200 和500 ng/g;SeMet 为50、100、200、400 和1 000 ng/g,SeEt 为100、250、500、1 000 和2 000 ng/g,所有溶液为现用现配。
微孔滤膜:0.45 μm,水系(百灵威公司);高效液相色谱议,美国Thermofisher 公司,配有脱气机、二元梯度泵、自动进样器、柱温箱;iCAP Qc 电感耦合等离子体质谱仪,美国Thermofisher公司;水浴恒温振荡器,中国常州杰博森仪器有限公司;Milli-Q 超纯水器,美国密理博公司;高速冷冻离心机,美国Sigma公司;涡旋混合器,德国IKA公司;分析天平,美国梅特勒托利多,精确至0.000 1 g;pH计,美国梅特勒托利多。
1.2 方法
固体试样经粉碎均质后,准确称取适量样品;若是液体样品,则需摇匀液体试样后,准确称取适量样品。加入蛋白酶K溶液,37 ℃水解提取4 h。然后用液相色谱串联电感耦合等离子体质谱仪对食品中的硒形态进行分离测定,与系列标准溶液比较定量。
1.2.1 样品处理
准确称取样品1~2 g(精确至0.000 1 g),加入20 mg 蛋白酶K,20 mL 水,37 ℃水浴震荡4 h,3000 r/min 离心10 min,取上清液经0.45 μm 水性滤膜过滤,然后实验室温度下待测。同样方法做试剂空白。
1.2.2 测定条件
1.2.2.1 高效液相色谱条件
(1)色谱柱 分析柱:Hamilton PRP-x100 柱,长250 mm,内径4.1 mm,粒度10 μm ,或相当者;保护柱:Hamilton PRP-x100。
(2)流动相 流动相B 20 mmol/L 柠檬酸溶液和流动相C 10 mmol/L 柠檬酸溶液分别用20 %氨水调节pH 至4.9。梯度洗脱条件见表1。流速:1.0 mL/min;进样量:100 μL。
1.2.2.2 质谱条件
质谱条件见表2。

表1 液相色谱梯度洗脱条件

表2 ICP-MS仪器条件
1.2.3 建立数学模型
试样中各种硒形态的含量按下式进行计算。

式中:X,试样中不同形态硒的含量,mg/kg;Ci,测试样液中不同硒形态的浓度,ng/mL;C0,试剂空白中不同硒形态的浓度,ng/mL;V,样品定容体积,mL;m,样品称样量,g。
2 结果与分析
2.1 不确定度的来源
不确定度评定可分为不确定度A类和不确定度B 类评定。不确定度A 类评定指用对观测列进行统计分析的方法来评定标准不确定度(以标准差表示的测量不确定度),是由一系列重复观测值计算得到。主要包括以下3个来源:
(1)重复性实验;
(2)最小二乘法拟合标准曲线校准引入的不确定度;
(3)样品回收率。
不确定度B类评定指用不同于对观测列进行统计分析的方法来评定标准不确定度,是根据有关信息来评定,即通过一个假定的概率密度函数得到。主要包括以下3个来源:
(4) 样品前处理:包括样品均匀性、称重(天平的最大允许误差)、移液枪定量、温度引起的水膨胀系数等;
(5)标准物质:包括标准储备液的不确定度和稀释过程引入的不确定度;
(6)检测仪器引入的不确定度。
使用鱼骨图系统分析不确定度A、B 类来源,如图1所示。

图1 不确定度A、B类来源
2.2 不确定度的评定
2.2.1 A类不确定度评定,u(1)
由重复观察(精密度)引入的不确定度属于A类不确定度[9]。
2.2.1.1 重复试验引入的相对不确定度
以Se(Ⅳ) 为例(下同),3 次测量结果ωSe(Ⅳ)为2.86、3.04、2.97 mg/kg,算术平 均值ϖ=2.96 mg/kg,算术平均值的不确定度为uSe(Ⅳ)(ϖ)相对不确定度
依据上述公式计算其他4种硒形态重复试验引入的相对不确定度,结果见表3。

表3 重复试验引入的不确定度
2.2.1.2 最小二乘法拟合标准曲线校准引入的不确定度
测定不同质量浓度的Se(Ⅳ)、Se(Ⅵ)、Se-Cys2、SeEt及SeMet标准工作溶液,每个校准点测定2 次,计数值y见表4 所示。采用最小二乘法拟合标准溶液的浓度与峰面积曲线,可得到方程y=a + bx (a 为截距,b 为斜率,x为浓度)和相关系数r,具体见表4。
依据试验,对一浓度样品进行2 次重复测量,c1Se(Ⅳ)=99.94 ng/g,c2Se(Ⅳ)=99.66 ng/g,平均浓度c0Se(Ⅳ)=99.80 ng/g。残差标准偏差为:

标准溶液平均浓度为:

标准溶液浓度的残差的平方和为:

则c0Se(Ⅳ)的标准不确定度为:

式中:n,标准溶液的测量次数,本例为10;p,c0的测量次数,本例为2。
C0Se(Ⅳ)的标准不确定度为:

依据上述公式计算,其他4种硒形态线性拟合产生的相对不确定度见表5。
2.2.1.3 样品回收率引入的不确定度
加标实验结果显示,5 种硒形态的回收率为a-~a+,其中Se(Ⅳ)为85.2%~94.8%、Se(Ⅵ)为90.5 %~102.2 %、SeCys2 为88.3 %~100.6 %、SeEt 为91.9 % ~101.7 % 、 SeMet 为93.1 % ~99.4 %,样品回收率不确定度按JJF 1059.1-2012《测量不确定度评定与表示》[7]附录A.1.4 节计算。区间半宽度为:

若在区间分布均匀,取矩形分布:

样品回收率引入的不确定度见表6所示。
2.2.1.4 A类不确定度u(1)合成
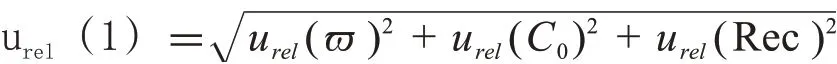
按此公式计算,5 种硒形态Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeEt 及SeMet 的A 类不确定度分 别 为3.347%、4.208%、3.908%、3.533%、2.434%。
2.2.2 B类不确定度评定,u(2)
2.2.2.1 样品前处理过程(包括样品均匀性、天平最大允许误差、移液器定量误差、温度引起的水膨胀系数等)引入的不确定度
(1)样品均匀性引入的不确定度 依照GB/T 5009.1-2003 《食品卫生检验方法理化部分总则》[10]规定,将样品充分混匀后随机取样,可认为样品是均匀、充分具有代表性,由此所引入的不确定度可忽略不计。

表4 最小二乘法拟合标准溶液浓度

表5 最小二乘法拟合标准曲线校准引入的不确定度
(2)称重(天平的最大允许误差)引入的不确定度 准确称取样品1.00 g,天平的最小分度为0.000 1 g。根据鉴定证书,该准确级的天平在0~50 g的最大允许误差为±0.000 5 g,因样品质量由2 次回零(空瓶和样重)称量所得,取矩形分布,称重所导致的不确定度为:

(3)移液管引入的不确定度 依据JJG 646-2006《移液器》[11]规定,20 mL可调移液器取20 mL的容量允差(△)为±0.048%,取矩形分布。移液器引入的不确定度为:

表6 样品回收率引入的不确定度 单位:%

(4) 温度引入的不确定度 实验室温度为25℃,水的膨胀系数为2.1×10-4℃-1,实验室容量瓶和溶液温度与校准时的不同引起体积变化所引入的不确定度u(△T)=(20×2.1×10-4×5)/
urel(△T)=0.012 12/20=0.0606%
(5) 样品前处理过程引入的不确定度urel(pre) 由上述评定可知,样品前处理引入的不确定度由urel(m)、urel(△V)及urel(△T)组成,合并前处理不确定度urel(pre)为:

依此公式计算,5 种硒形态Se (Ⅳ)、Se(Ⅵ)、SeCys2、SeEt及SeMet由样品前处理引入的不确定度均为:0.078 14%。
2.2.2.2 标准物质引入的不确定度
(1)标准储备液的不确定度 根据SeEt 固体标准品纯度不小于98%,取矩形分布,由标准品纯度引入的相对不确定度为1.155 %。其余4 种硒形态标准品为标准储备液,由中国计量科学研究院提供。5 种硒形态标准品不确定度及相对不确定度详见表7。

表7 硒形态标准储备液相对不确定度
(2)标准储备液稀释过程所用天平(天平的最大允许误差)称重引入的不确定度 分别称取2.000 0 g Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeMet标准储备液至25 mL 标准配备瓶内,用去离子水定量至13.680 0、15.020 0、18.700 0和19.580 0 g,制成10 μg/g 4种硒形态标准使用液。分别吸取10 mL各形态标准溶液至100 mL 容量瓶中定容,配制成1.0 μg/g标准工作液。
从SeⅣ和SeCys2 的1.0 μg/g 标准工作液分别取1(1 mL 吸管)、2.5(5 mL 吸管)、5(5 mL 吸管)、10(10 mL 吸管)和25 mL(25 mL 吸管)至100 mL 容量瓶中,用去离子水定容分别得到10 、25、50、100 和250 ng/g 的Se Ⅳ和SeCys2 标 准溶液。
从SeⅥ的1.0 μg/g 标准工作液中分别取2(2 mL 吸管)、5(5 mL 吸管)、10(10 mL 吸管)、20(20 mL 吸管)和50 mL(50 mL 吸管)至100 mL 容量中,用去离子水定容分别得到20、50、100、200和500 ng/g的SeⅥ标准溶液。
从SeMet 的1.0 μg/g 标准工作液中分别取5(5 mL 吸管)、10(10 mL 吸管)、20(20 mL 吸管)和40 mL(20 mL 吸管2 次)至100 mL 容量中,用去离子水定容分别得到50、100、200 和400 ng/g 系列SeⅥ标准溶液;直接使用1.0 μg/g标准工作液,为1 000 ng/g SeⅥ标准溶液。
称取0.011 2 g SeEt 固标至标准配备瓶内,用去离子水定量至112 g,制成100 μg/g SeEt标准储备液;再从100 μg/g SeEt标准储备液中取10 mL至100 mL容量中,用去离子水定容得10 μg/g SeEt标准工作溶液。用吸管分别吸取10 μg/g SeEt标准工作溶液1(1 mL 吸管)、2.5(5 mL 吸管)、5(5 mL吸管)、10(10 mL 吸管)和20 mL(20 mL 吸管)至100 mL 容量中,再用去离子水定容分别得到100、250、500、1 000和2 000 ng/g系列SeEt标准溶液。
使用天平的最小分度为0.000 1 g,根据鉴定证书,该准确级的天平在0~50 g 的最大允许误差为±0.000 5 g,稀释过程各由2 次回零称量所得(储备液由空瓶重、标准储液重称量获得,稀释液由储备液重及稀释液重称量获得),取矩形分布。

则天平的最大允许误差导致的不确定度由以上两个不确定度合成:
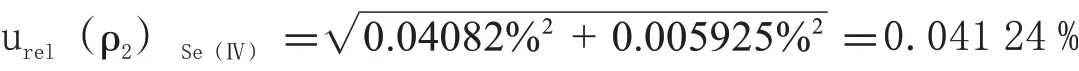
同理,Se(Ⅵ)、SeCys2、SeMet 和SeEt 稀释过程引入的相对不确定度分别为0.041 18%、0.041 05%、0.041 04%和3.645%。
(3)标准储备液稀释过程所用容量器具引入的不确定度 按照标准GB 5009.93-2017 标准曲线制备步骤,配制系列硒标准溶液。测定过程中所用容量器具引入的不确定度[12]见表8所示。
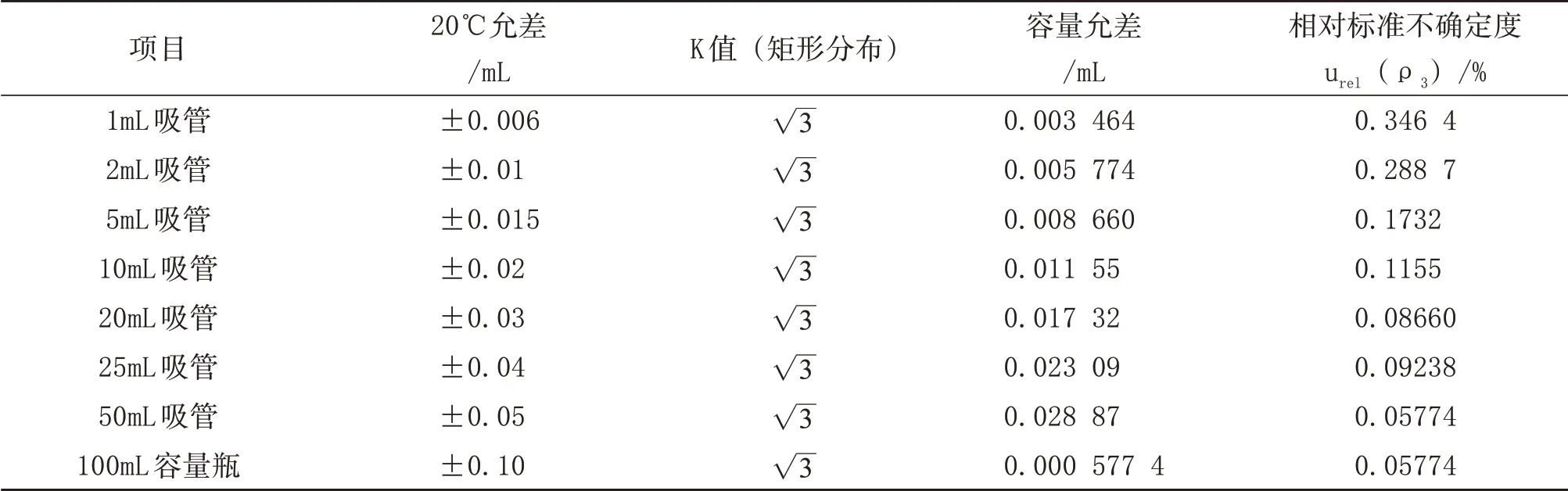
表8 稀释过程中容量器具引入的相对标准不确定度
配制Se(Ⅳ)系列标准溶液使用1 mL 吸管1次,5 mL 吸管2 次,10 mL 吸管2 次,25 mL 吸管1次,100 mL容量瓶6次。

配制Se(Ⅵ) 系列标准溶液使用2 mL 吸管1次,5 mL 吸管1 次,10 mL 吸管2 次,20 mL 吸管1次,50 mL吸管1次,100 mL容量瓶6次。

配制SeCys2系列标准溶液使用使用1 mL吸管1次,5 mL 吸管2 次,10 mL 吸管2 次,25 mL 吸管1次,100 mL容量瓶6次。

配制SeMet系列标准溶液使用5 mL吸管1次,10 mL 吸管2次,20 mL吸管3次,100 mL容量瓶6次。

配制SeEt 系列标准溶液使用1 mL 吸管1 次,5
mL 吸管2 次,10 mL 吸 管2 次,20 mL 吸 管1 次,100 mL 容量瓶6次。

(4)标准储备液稀释过程温度引入的不确定度 由2.2.2.1(4)可知,由于每用一次吸管、容量瓶,温度引入的相对不确定度均为0.060 6%。
配制Se(Ⅳ)系列标准溶液使用1mL 吸管2次,5 mL 吸管2 次,10 mL 吸管1 次,25 mL 吸管1次,10 mL 容量瓶1 次,100 mL 容量瓶5 次,共计12次。

同理,配制Se(Ⅵ)、SeCys2、SeMet、SeEt标准储备液稀释过程温度引入的不确定度均为0.209 9%。
(5)标准物质引入的不确定urel(sta)

依此公式计算,5 种硒形态Se (Ⅳ)、Se(Ⅵ)、SeCys2、SeEt及SeMet由样品前处理引人的不 确 定 度 分 别 为1.146%、 1.664%、 1.438%、3.860%和1.333%。
2.2.2.3 检测仪器引入的不确定度
依据国家计量所提供的校准证书:高效液相色谱的不确定度为0.65%。电感耦合等离子体质谱仪的不确定度9Be 为2.9 %、115In 为1.0%、229Bi 为2.5%,取最大不确定度2.9%,按矩形分布计算不确定度。

2.2.2.4 B类不确定度u(2)合成

按此公式计算,5 种硒形态Se (Ⅳ)、Se(Ⅵ)、SeCys2、SeEt 及SeMet 由B 类引入的相对不确定度分别为2.065%、2.392 %、2.240%、4.225%和2.174%。
2.2.3 总体相对不确定度μ(总)
2.2.4 试样不确定度评价
假设置信概率为0.95,取包含因子k=2,则扩展相对不确定度urel=k×urel(总)
扩展不确定度为u=ϖ×Urel
计算食品样品中5 种硒形态Se (Ⅳ)、Se(Ⅵ)、SeCys2、SeEt、SeMet 浓度分别为(2.96±0.23)、(0.63±0.06)、(4.39±0.40)、(6.52±0.72)、(10.48±0.68) mg/kg
食品中5种硒形态不确定度评定结果见表9。
3 讨论与结论
液相色谱-电感耦合等离子体质谱联用测定食品中硒形态的含量方法简便、快速、准确。对不确定度分量来源评定进行了更加合理的分类评定。A 类评定包括重复性实验引入的不确定度;最小二乘法拟合标准曲线校准引入的不确定度;样品回收率引入的不确定度。B 类评定包括样品前处理:样品均匀性、称重(天平的最大允许误差)、移液枪定量误差、温度引起的水膨胀系数等引入的不确定度;标准物质:包括标准储备液的不确定度和稀释过程引入的不确定度;检测仪器引入的不确定度。

表9 食品中5种硒形态不确定度评定结果
不确定度评定可明确实验室质控管理目标,通过计算食品中硒形态含量测定的扩展不确定度,可为食品中硒形态的实际监测工作提供更科学、完整的检测数据。
实验过程中,由于没有购买到SeEt 的标准储备液,只能以固标SeEt (纯度98%,25 mg 装)来代替。因质量较小,在取样称量过程产生的不确定度较大。因此,应尽量选用标准储备液,以降低不确定度。
通过表9可知,回收率、重复性实验、仪器以及标准物质产生的不确定度较大。因此,在实际测定中,检测人员应熟练掌握实验操作技能、规范具体实验操作,尽可能保证实验结果的稳定性和准确性。为保证仪器处在最佳工作状态,仪器性能的维护和调试也十分重要,这是保证实验结果准确可靠的基础。标准曲线拟合会对不确定度带来一定影响,因此,在实验过程中,应当提高标准溶液配制的技术水平,降低对结果的影响,使测定结果更加准确,更接近真实值。
