釉原蛋白在牙周组织再生中的生物学作用
2019-03-19杨宇轩张海霞王爽
杨宇轩 张海霞 王爽
西安交通大学口腔医院正畸科 西安 710004
牙周炎是发生在牙周组织,在牙石等多种局部因素刺激下,以牙龈炎症、牙槽骨吸收、牙周袋形成、牙齿松动为主要表现的一类疾病,其牙槽骨破坏呈现不可逆性[1]。临床上对于牙槽骨吸收的主要治疗方式有引导组织再生术(guided tissue regeneration,GTR)、牙周植骨术、生长因子治疗等[2]。传统的治疗牙槽骨缺损的方法存在费用高、干细胞来源缺乏以及干细胞移植的伦理问题[3]、远期效果不确定[4]等限制,临床治疗效果并不理想。目前研究表明,釉基质蛋白具有在牙周缺损区诱导形成与牙本质紧密结合的无细胞牙骨质、恢复牙周纤维附着、促进牙周再生的作用[5],是现有治疗手段的有效补充,但是其具体促进牙周再生的机制仍待研究。
牙周组织的再生涉及细胞迁移、细胞黏附、细胞增殖等多种生物学行为,在这些过程中,釉原蛋白均起到一定的调节作用。因组织来源和细胞种类不同,釉原蛋白的调节作用也不尽相同,这些调控作用可以有效调控牙周组织缺损时优先附着和增殖的细胞,具有重要的临床意义。
1 对细胞迁移的调控
1.1 牙周膜成纤维细胞
牙周膜成纤维细胞(periodontal ligament fi-broblasts)是人牙周膜中数量最多、具有重要功能的一种细胞,具有独特且高效的合成细胞外基质中胶原蛋白的能力,是形成牙周膜纤维的主要细胞[6]。牙周膜成纤维细胞可以分化成为成骨细胞样和成牙骨质细胞样细胞,并且被认为在维持和修复牙周组织中起到重要作用[7]。
重组猪釉原蛋白(recombinant porcine amelogenin)作用于原代培养的牙周膜成纤维细胞,可以明显促进牙周膜成纤维细胞的迁移。在无血清培养基中,添加重组猪釉原蛋白,培养牙周膜成纤维细胞,在细胞贴壁生长后,使用毛细管尖端在细胞汇合处制造无细胞划痕,随后48 h内每12 h观察细胞迁移情况,结果显示与对照组相比,牙周膜成纤维细胞的迁移速率显著增加[8]。还有实验[9]表明,在釉原蛋白作用下,牙周膜成纤维细胞通过boyden小室的速率较对照组显著提高,显示釉原蛋白对牙周膜成纤维细胞迁移具有促进作用。
1.2 牙龈上皮细胞和牙龈成纤维细胞
牙龈是牙周组织的另一组成成分,其主要由牙龈上皮细胞(gingival epithelial cell)组成。由于牙龈上皮细胞生长迅速,在牙周组织受损后会抢先迁移至受损的牙槽骨表面,形成上皮附着,阻碍牙周组织的再生[10]。
重组猪釉原蛋白处理后的牙龈上皮细胞在无血清培养基中培养24 h后,使用毛细管尖端在细胞汇合处制造无细胞划痕,结果显示,与对照组相比,24 h后牙龈上皮细胞的迁移速率出现了明显下降[8]。同时,在重组猪釉原蛋白干预下,6 h后牙龈成纤维细胞的迁移速率也出现明显下降。
1.3 牙周膜干细胞
牙周膜干细胞(periodontal ligament stem cell)是存在于牙周膜中的一种未分化的间充质干细胞,具有自我更新及多向分化潜能,在一定条件下能够定向分化为成牙骨质样细胞、成纤维细胞和脂肪细胞。在免疫缺陷小鼠体内,牙周膜干细胞可以产生牙骨质、牙周膜样结构,是维持牙周组织稳态,促进牙周组织再生的重要种子细胞[11]。
釉原蛋白可以促进干细胞迁移。在划痕实验中,实验组以人全长重组釉原蛋白GST-rMI80处理体外培养牙周膜干细胞,并在12和24 h观察其迁移情况。实验[12]结果显示,GST-rMI80处理的牙周膜干细胞的迁移速率显著高于对照组。
1.4 可能的机制
研究[13]显示,细胞膜表面蛋白Grp78可能是釉原蛋白的受体,其可以促使釉原蛋白进入细胞内发挥其促进细胞迁移作用。Toyoda等[12]研究发现,釉原蛋白可以与细胞膜表面葡萄糖调节蛋白Grp78特异性结合,激光共聚焦显微镜显示,这种联结蛋白会诱导细胞的内吞作用,沉默Grp78基因可以抑制其内吞作用(图1)。
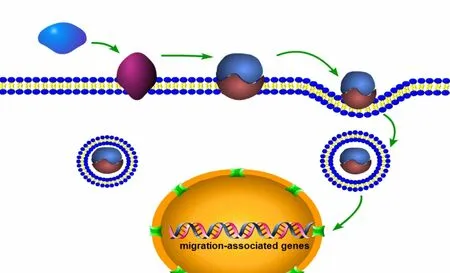
图1 Grp78介导的细胞内吞作用Fig 1 Grp78 mediated endocytosis
进一步研究显示,釉原蛋白可以调节细胞迁移相关基因的表达。在受到釉原蛋白作用时,Grp78过表达的细胞的迁移作用会显著增强,同时不影响其对于细胞增殖的调节作用。沉默Grp78基因会消除釉原蛋白对细胞迁移的促进作用。
2 对细胞增殖的调控
2.1 牙周膜成纤维细胞和牙龈成纤维细胞
一项系统回顾[14]显示,釉原蛋白干预的牙周膜成纤维细胞和牙龈成纤维细胞的增殖速率较对照组明显增加,细胞内DNA合成明显增强,并且促进作用具有浓度依赖性。另有研究[8]以重组猪釉原蛋白处理牙周膜成纤维细胞和牙龈成纤维细胞,用无血清培养液培养24 h后进行细胞计数,实验结果显示,重组猪釉原蛋白可以显著促进牙周膜成纤维细胞和牙龈成纤维细胞的增殖,其促进效果在重组猪釉原蛋白浓度为10 μg·mL-1时具有时间依赖性。
2.2 牙龈上皮细胞
使用重组猪釉原蛋白处理实验组牙龈上皮细胞,细胞计数结果显示,与成纤维细胞相反,重组猪釉原蛋白显著抑制了牙龈上皮细胞的增殖[8]。
2.3 牙周膜干细胞
Kémoun等[15]研究发现,釉原蛋白可以显著促进牙周膜干细胞增殖。Cheng等[16]使用人全长重组釉原蛋白和猪釉基质蛋白处理牙周膜干细胞,在随后8 d内对细胞进行计数。实验结果显示,人全长重组釉原蛋白和猪釉基质蛋白在干预后前3 d均能够显著增强牙周膜干细胞的增殖,在实验观察的8 d中,其促进增殖的效果始终存在,并在第6 d达到最高值。
2.4 可能的机制
有研究[17]显示,釉原蛋白诱导的细胞增殖与丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPK)/细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)通路密切相关。MAPK是细胞内的一类丝氨酸/苏氨酸蛋白激酶,MAPK/ERK通路存在于大多数细胞内,能够将细胞外信号转导至细胞以及细胞核内,引起多种生物学作用[18]。研究[19]表明,重组全长人釉原蛋白作用于人骨髓间充质干细胞时,可以显著增强人骨髓间充质干细胞的增殖,MAPK通路阻滞剂U0126可以显著抑制其促进增殖的作用。Yoshimi等[17]研究显示,重组釉原蛋白作用下的人成牙骨质细胞内ERK1/2磷酸化显著增强,MARK抑制剂可以阻断这一反应。
3 对细胞黏附的调控
3.1 牙周膜成纤维细胞和牙龈成纤维细胞
釉原蛋白可以促进牙周膜成纤维细胞和牙龈成纤维细胞的细胞黏附作用。有研究[8]使用重组猪釉原蛋白处理牙周膜成纤维细胞和牙龈成纤维细胞,对黏附细胞用胰酶消化后进行细胞计数,结果显示,重组猪釉原蛋白在牙周膜成纤维细胞和牙龈成纤维细胞生长的前30 min可以显著促进细胞黏附;但随着时间的延长,这种对细胞黏附的促进作用会逐渐下降,在干预4 h后,重组猪釉原蛋白对细胞黏附的促进作用几乎消失。
3.2 牙龈上皮细胞
有研究[8]显示,重组猪釉原蛋白能够显著抑制牙龈上皮细胞的黏附。另有研究[20]指出,釉原蛋白对牙龈上皮细胞黏附的抑制作用具有浓度和时间依赖性,釉原蛋白浓度越高,作用时间越长,对牙龈上皮细胞黏附的抑制作用越强。
3.3 牙周膜干细胞
釉原蛋白在一定时间内可以促进牙周膜干细胞的细胞黏附。使用重组人全长釉原蛋白和猪釉原蛋白分别处理牙周膜干细胞,随后对黏附细胞进行计数,实验结果显示接种2 h后,牙周膜干细胞的黏附率达到80%左右;重组人全长釉原蛋白和猪釉原蛋白均能够在细胞接种的前60 min显著提高牙周膜干细胞的黏附率,但在60 min之后对细胞黏附的影响与对照组没有显著性差异[16]。
3.4 可能的机制
目前对于釉原蛋白对细胞黏附影响的机制了解较少。Toyoda等[12]发现,沉默Grp78基因后,釉原蛋白诱导的细胞黏附也随之消失,并认为Grp78在釉原蛋白诱导细胞黏附方面具有重要作用。
4 对细胞分化的调控
釉原蛋白在具有调节细胞迁移、黏附、增殖作用的同时,还显示出具有诱导牙周组织细胞成骨分化的作用。在釉原蛋白的诱导下,成牙骨质细胞、间充质干细胞、牙周膜细胞等都会表达成骨相关蛋白质,并产生钙化结节,对牙周组织再生具有重要意义。
4.1 间充质干细胞
牙周组织的牙周膜干细胞和骨髓间充质干细胞均属于间充质干细胞,在体外培养中,釉原蛋白可以诱导其产生钙化结节,并分化成为成骨细胞,这是牙周组织再生的关键环节。研究[21]显示,在含有重组釉原蛋白片段的培养液中培养间充质干细胞,其碱性磷酸酶(alkaline phosphatase)的表达水平显著上升。同时,在成骨环境中,重组釉原蛋白还可以增强碱性磷酸酶的活性,其最大浓度和最大活性都显著高于对照组。
在成骨环境中,重组釉原蛋白片段还可以促进Ⅰ型原骨胶原和骨钙蛋白的表达。实验[22]结果显示,在含有重组釉原蛋白片段的培养基中培养间充质干细胞,其第7和14 d的Ⅰ型原骨胶原和骨钙蛋白的表达量都显著高于对照组。
釉原蛋白对间充质干细胞的成骨分化诱导作用具有浓度依赖性。在诱导牙龈间充质干细胞的实验[23]中,100 μg·mL-1的釉原蛋白在成骨诱导后1~2周就可以检测到染色的钙化结节;而25 μg·mL-1的釉原蛋白诱导时,则至少需要3~4周才可观察到。在25和100 μg·mL-1釉原蛋白干预的牙龈间充质干细胞中,碱性磷酸酶mRNA的表达量都明显提高。
综上,不同生物来源的釉原蛋白均具有促进间充质干细胞成骨分化的能力,并且这种促进能力具有浓度依赖性。
4.2 成牙骨质细胞
成牙骨质细胞是牙骨质细胞间质内一类可以分泌钙化基质和胶原纤维的细胞,其与牙根表面平行,是连接牙周膜和牙骨质的组成部分。茜素红染色显示,釉原蛋白可以显著增加成牙骨质细胞分泌的钙化基质,聚合酶链式反应显示,在釉原蛋白作用下,成牙骨质细胞中的碱性磷酸酶、骨涎蛋白、骨钙蛋白的表达明显增加,具有促进成牙骨质细胞成骨分化的作用[24]。
4.3 牙周膜干细胞
釉原蛋白可以显著增加牙周膜干细胞的碱性磷酸酶表达量,并具有浓度依赖性。加入釉原蛋白抗体可以有效地抑制这种促进作用。加入抗体后,牙周膜干细胞的碱性磷酸酶表达量与对照组没有显著性差异。实验[25]结果显示,釉原蛋白可以促进牙周膜干细胞发生成骨分化。
4.4 可能机制
Olivares-Navarrete等[21]研究显示,釉原蛋白作用于人间充质干细胞,在使其发生成骨分化的过程中,蛋白激酶C、ERK1/2、β-连环蛋白发生了高度磷酸化;进一步研究显示,ERK1/2的抑制剂可以阻断细胞合成碱性磷酸酶、骨钙蛋白、骨形态发生蛋白2等成骨相关蛋白质。因此,釉原蛋白诱导的细胞分化作用与ERK通路、蛋白激酶C和β-连环蛋白的降解密切相关(图2)。
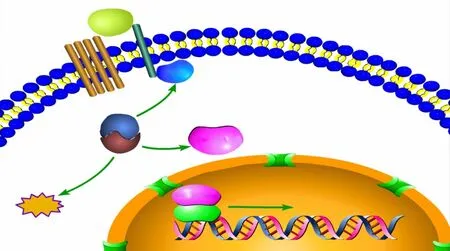
图2 Wnt/β-连环蛋白通路示意图Fig 2 Wnt/β-catenin pathway
重组釉原蛋白诱导细胞发生成骨分化的过程与Wnt/β-连环蛋白通路密切相关。Wnt/β-连环蛋白通路在胚胎发育和成熟机体中均具有重要意义,同时还与肿瘤的发生、发展密切相关,对维持同型细胞的黏附、防止细胞的移动发挥作用。
经典的Wnt/β-连环蛋白通路作用方式是:Wnt分子与细胞膜表面特异性受体Frizzled结合,进而使β-连环蛋白在细胞内的浓度升高。随后β-连环蛋白向细胞核内转移,引起细胞的增殖、分化、成熟[26]。有研究[27]表明,在釉原蛋白处理的胚胎干细胞中,β-连环蛋白的表达量显著上升,Wnt的细胞膜表面受体的表达量也明显上调。同时,应用特异性Wnt抑制剂sFRP-1可完全阻断釉原蛋白介导的胚胎干细胞成骨分化作用。
5 问题与展望
以往的研究证实,釉基质蛋白可以诱导牙周组织的再生。釉原蛋白是釉基质蛋白的主要组成成分,占釉基质蛋白的90%以上,是釉基质蛋白发挥牙周再生作用的主要成分[5]。在牙周组织再生过程中,釉原蛋白在细胞迁移、细胞增殖、细胞黏附、细胞分化等过程中发挥着不同的生物学作用。通过基因芯片分析发现,釉原蛋白作用过程中表达发生变化的基因涵盖信号转导、转录、翻译、细胞周期、细胞增殖、细胞凋亡、免疫应答、囊泡运输、溶酶体活动,以及细胞骨架、细胞黏附和产生细胞外基质等方面[28]。同时,由于牙周组织的复杂性,在牙周组织发生缺损时,抢先黏附于缺损骨组织表面的细胞可以决定牙周组织愈合的性质[10],所以调节细胞迁移和黏附在牙周组织缺损的重建中具有重要的临床意义。釉原蛋白的作用具有细胞特异性,可以抑制牙龈上皮细胞的迁移,促进间充质干细胞、牙周膜成纤维细胞的迁移和增殖,从而有效促进骨组织和牙周膜的再生,诱导牙周缺损的重建,是理想的治疗牙周组织缺损并促进牙周组织再生的药物。
目前,对釉原蛋白的生物学作用研究较多,从不同细胞来源、不同种属和不同作用方式等方面进行了阐述,同时在牙周组织之外的领域也得到了一定的临床应用[29]。目前认为,在牙周组织再生过程中,釉原蛋白对葡萄糖调节蛋白Grp78[12]、MAPK/ERK通路[19]和Wnt/β-连环蛋白通路[27]发挥着重要生物学作用。但是,已有的研究对于釉原蛋白在诱导牙周组织再生的过程中的具体作用方式仍不明确,还需要从以下几个方面进一步探究釉原蛋白生物学效应的机制。
1)釉原蛋白与效应细胞的具体结合位点仍不明确,对如何激活信号通路、与细胞膜表面哪些受体结合而产生生物学效应仍有待研究。
2)对不同通路之间是否存在潜在的联系仍有待研究。
3)由于釉原蛋白是一种复合型蛋白质,可被分为不同大小的片段,目前部分研究使用全长重组釉原蛋白,也有使用不同大小重组釉原蛋白片段进行的研究,尚没有研究探讨釉原蛋白能够发挥最佳生物学效应的最小片段的分子质量。
