腮腺分区勾画方式对鼻咽癌IMRT计划靶区及腮腺剂量的影响
2019-03-15赵彬青东朱红蕾马代远
赵彬,青东,朱红蕾,马代远
川北医学院附属医院 肿瘤科,四川 南充 637000
引言
唾液腺损伤造成的放射性口干症作为鼻咽癌放疗后常见的并发症,主要表现为口干、喉咙痛、味觉失敏、牙龈坏死等,严重影响患者的生活质量[1-2]。腮腺作为最大的唾液腺,对其功能的保护尤为重要。随着精确放疗技术的不断进步,调强放疗(Intensity Modulated Radiotherapy,IMRT)相比于传统二维放疗或者三维适形放疗,虽然已明显降低腮腺的受照剂量,显著改善放疗后口腔干燥症状[3-5],但是对于上颈部存在淋巴结转移的病例,腮腺的剂量限定仍然不尽如人意,仍然有相当一部分患者出现明显的放疗中、后腮腺功能损伤,导致比较顽固的口干症[6-7]。如何更好地优化放疗计划,以达到最大限度保护腮腺功能一直是临床研究的热点问题。临床上常用的IMRT中通常是将腮腺整体作为危及器官进行勾画并给予剂量限制,近年来的研究结果显示如果单侧腮腺平均剂量低于20 Gy或者双侧腮腺平均剂量低于25 Gy就能避免严重的口腔干燥症状[8],Hey等[9]将限制标准放宽至至少一侧腮腺受照平均剂量<26 Gy也能得出相似结论。咽后和Ⅱ区是鼻咽癌淋巴结最常见的转移区域[10],对于这类病例,为了满足靶区的剂量覆盖,腮腺往往不能达到上述的剂量限制标准,现仅有少数研究结论[11-14]显示腮腺分区勾画方式在腮腺受照剂量限制上存在一定剂量学优势,但是到目前为止,关于何种分区勾画方式更好尚未见报道。本研究选取4例鼻咽癌患者,采用4种不同方式勾画腮腺,制作4组调强放疗计划,评估腮腺、靶区、其余危及器官剂量,现将本研究的初步结果报道如下。
1 资料与方法
1.1 病例资料
选取既往于我科行IMRT的鼻咽癌患者4例,其中男性3例,女性1例,年龄19~52岁,中位年龄43岁。治疗前经头颅+鼻咽部+颈部MRI、常规胸片、上腹部B 超、全身骨ECT 完善分期检查,据美国癌症联合委员会分期系统第7版分期,临床分期均为T2N2M0,III期,其中1例病例鼻咽部病灶(GTVnx)及颈部转移淋巴结(GTVnd)如图1所示。

图1 靶区示意图
1.2 靶区及危及器官勾画
参考MRI影像勾画靶区及危及器官。根据国际辐射单位与测量委员会(International Commission on Radiation Units and Measurements,ICRU)50号及62号报告来勾画靶区及确定靶区处方剂量。鼻咽和全颈靶区使用IMRT照射,大体肿瘤体积(Gross Tumor Volume,GTV)分为鼻咽原发肿瘤靶区GTVnx和淋巴结转移病灶靶区GTVnd、咽后淋巴结靶区GTVrpn;在GTVnx的基础上外扩3 mm为P-GTVnx,GTVnd外扩3 mm为P-GTVnd,GTVrpn外扩3 mm为P-GTVrpn,临床靶体积(Clinical Target Volume,CTV)设置2个临床靶区,CTV1为GTVnx外扩5~10 mm,需包括全鼻咽腔黏膜下5 mm、破裂孔软组织、翼腭窝(翼内肌侵犯时);CTV2为 CTV1外扩5~10 mm,需包括鼻腔后1/3,上颌窦后1/3,蝶窦下1/3至 1/2、双侧翼腭窝、颅底所有孔道、全颈淋巴结预防区等;CTV1、CTV2外扩3 mm作为计划靶体积(Planning Target Volume,PTV)。邻近危及器官(Organ At Risk,OAR)结构的勾画包括:脊髓、脑干、垂体、左右晶体、左右视神经、视交叉、视网膜、左右颞叶、左右下颌骨、左右颞颌关节、左右甲状腺、食管、气管、口腔、内耳、肺。
1.3 腮腺分区勾画及剂量限制
计划0:将腮腺作为整体予以勾画(图2a),左侧腮腺(L-Parotid)和右侧腮腺(R-Parotid)计量限制均为D50<35 Gy;计划1:沿下颌支后缘将腮腺分为浅叶与深叶勾画(图2b),整体腮腺剂量限制同计划0,腮腺浅叶(Parotid-S)和深叶(Parotid-D)剂量限制为D50<25 Gy;计划2:以PTV2轮廓线为界将腮腺分为靶区外部分(Parotid-NO)和靶区内重叠部分(Parotid-O)(图2c),整体腮腺剂量限制同计划0,Parotid-NO 和Parotid-O剂量限制为D50<25Gy;计划3:沿下颌后静脉前外缘将腮腺分为前叶(Parotid-F)与后叶(Parotid-B)(图2d),整体腮腺剂量限制同计划0,Parotid-F 和 Parotid-B 剂量限制为 D50<25 Gy。
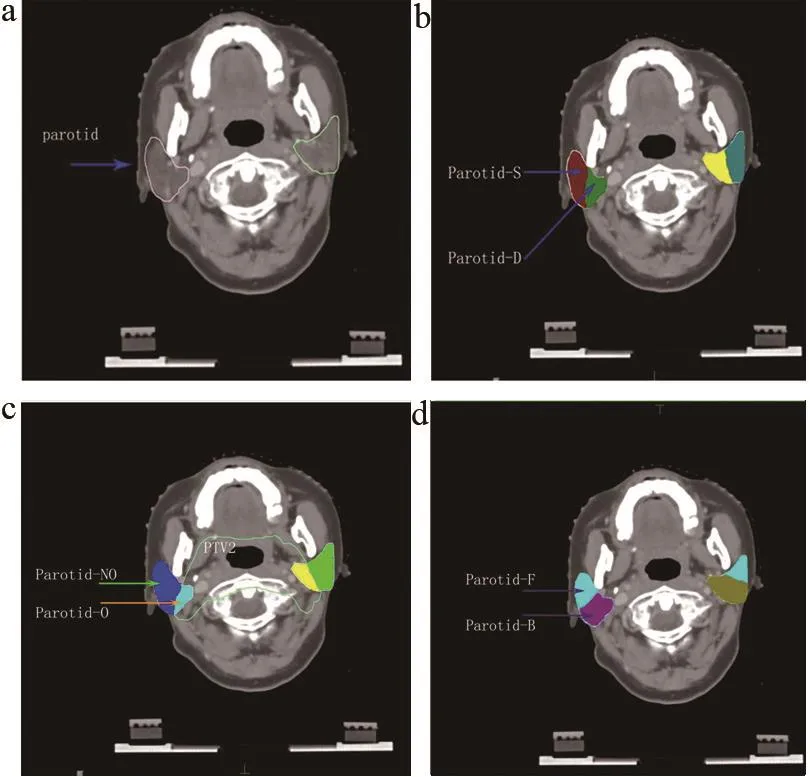
图2 腮腺4种勾画方式示意图
1.4 治疗计划设计
在治疗计划系统(Treatment Planning System,TPS)上设计鼻咽癌的IMRT计划,采用常规分割照射。由同一物理师分别制作4组IMRT计划,除腮腺以外,靶区的处方剂量及其余危及器官限制剂量均相同。4组计划靶区均给予相同的处方剂量:P-GTVnx:70.5 Gy/30 Fx(95%),P-GTVrpn:70.5 Gy/30 Fx(95%),P-GTVnd:69 Gy/30 Fx(95%),P-CTV1:60 Gy/30 Fx(95%),P-CTV2:51 Gy/30 Fx(95%)。重要器官限制剂量为:脊髓D2<45 Gy,脑干 D2<54 Gy,垂体 D2<50 Gy,左右晶体 D2<8 Gy,左右视神经 D2<54 Gy,视交叉 D2<50 Gy,视网膜 D2<40 Gy,左右颞叶D2<60 Gy,左右下颌骨D2<60 Gy,左右颞颌关节 D2<55 Gy,左右甲状腺 D2<45 Gy,食管 V40<40%,气管V40<40%,口腔 D33<40 Gy,内耳 D2<47 Gy,肺 V20<10%。
1.5 靶区、危及器官剂量比较及统计学分析
比较4组计划中靶区P-GTVnx 、P-GTVnd、P-GTVrpn、P-CTV1、P-CTV2 平均剂量(Dmean)及100%处方剂量照射靶体积(V100);整体腮腺及各个亚区的平均剂量(Dmean)及50%体积剂量(D50);根据RTOG 0615的剂量要求,比较其余危及器官如脑干、脊髓、视神经、视交叉、晶体、口腔、颞颌关节、下颌骨等的特殊剂量体积参数。结果用x-±s表示,采用SPSS 17.0软件进行分析,4种放疗计划剂量学参数进行方差分析。P<0.05为差异有统计学意义。
2 结果
2.1 腮腺剂量及体积比较
4组计划中整体腮腺及各个亚区腮腺平均剂量(Dmean)和50%体积剂量(D50)剂量学参数如表1所示,4例患者整体腮腺及各亚区腮腺体积如表2所示。
2.2 靶区剂量及体积比较
4组计划中P-GTVnx、P-GTVnd、P-GTVrpn、P-CTV1、P-CTV2平均剂量(Dmean)及100%处方剂量照射靶体积(V100)如表3所示,所有的靶区剂量均达到计划优化的目标要求;4例患者靶区体积如表4所示;其中1例病例靶区70、60、50 Gy剂量分布,见图3;4组计划剂量体积直方图(Dose Volume Histogram,DVH),见图4。
2.3 其余危及器官剂量比较
晶体、视神经、视交叉、脊髓、脑干、下颌骨等危及器官剂量如表5所示,所有危及器官剂量均符合剂量限制要求。
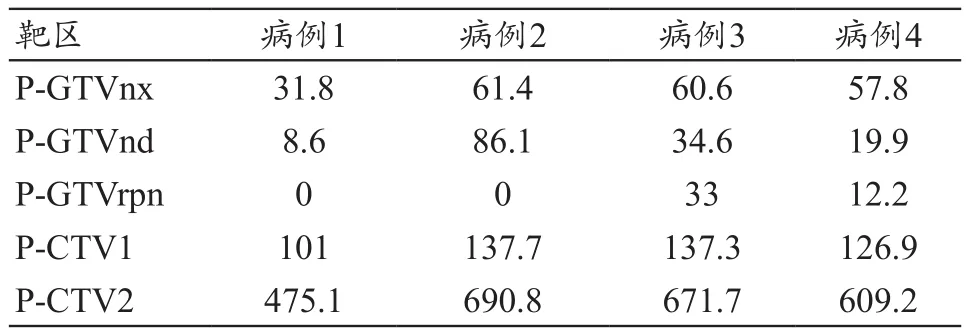
表4 四例患者靶区体积(cm3)
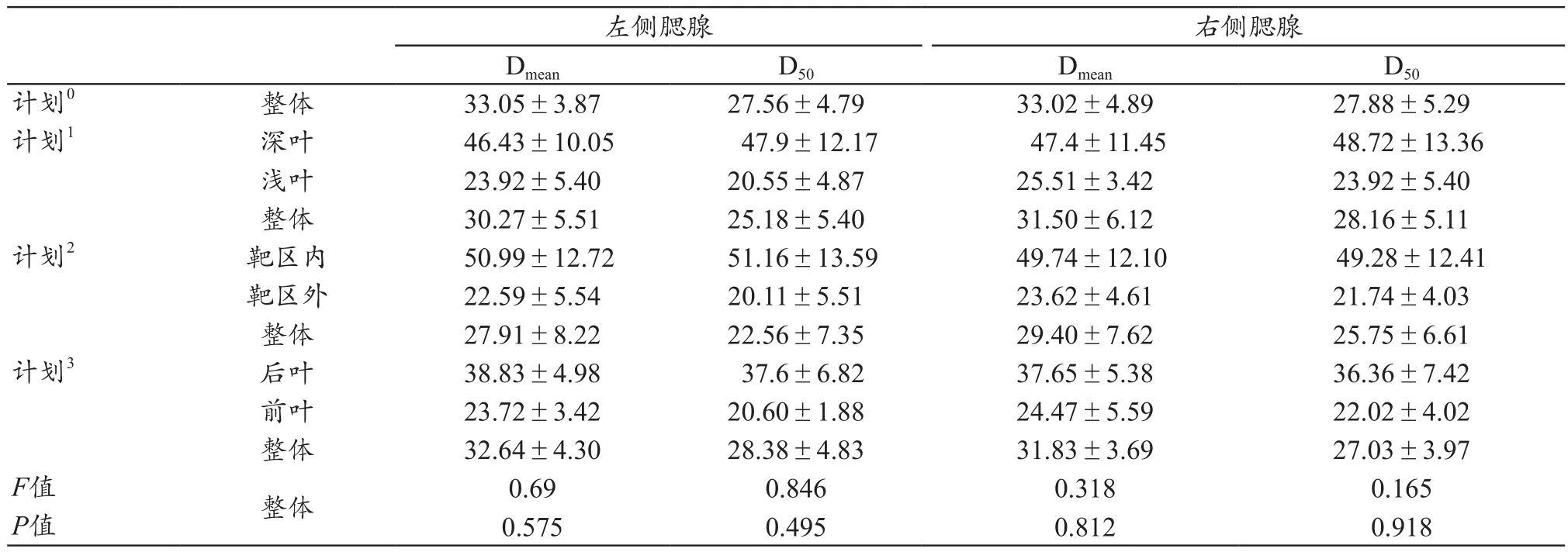
表1 四组计划中腮腺剂量比较(x-±s,Gy)

表2 四例患者整体腮腺及各亚区腮腺体积(cm3)

表3 四组计划中靶区剂量比较(x-±s)

图3 1例病例4组计划靶区剂量分布图
3 讨论
腮腺分区勾画方法是鼻咽癌等头颈部肿瘤放疗临床工作中持续关注的问题,恰当的分区勾画方式探索一直在进行。Xiao等[11]选择有咽旁间隙侵犯和Ⅱa区淋巴结转移的鼻咽癌病例作为研究对象,在CT图像上以下颌后静脉前外缘为界将腮腺分为前外叶和后内叶,其研究结果显示无论是整体腮腺还是前外侧腮腺,平均剂量都明显低于常规勾画方式(即腮腺整体勾画),并且这种差异在咽旁间隙与Ⅱa区淋巴结同时受累时表现得更为明显。邵明海等[14]基于上述腮腺分区勾画方法来研究伴有双侧颈部Ⅱ区淋巴结转移鼻咽癌病例,也得到了相似的结论。Zhang等[12]采用另一种分区方式,即在颅底层面,以茎乳孔和下颌支后缘的连线为界,当茎乳孔消失时,以胸锁乳突肌前缘和下颌支的后缘为界将腮腺分为浅叶和深叶,其研究结果显示对于T1-3的鼻咽癌,在没有明显影响靶区剂量的情况下,分区勾画使整体腮腺的平均剂量相比整体勾画下降了4 Gy,腮腺浅叶的平均剂量低于30 Gy,但对于一些T4的鼻咽癌病例分区勾画却不能满足靶区和脑干的剂量要求。Chau等[13]则以PTV轮廓线为界将腮腺分为与靶区重叠区域和靶区以外区域两部分分区勾画腮腺,研究结果显示无论是靶区以外区域腮腺还是整体腮腺平均剂量都明显低于将腮腺作为整体予以勾画的方式。上述三种腮腺分区勾画方式结论相似,即将腮腺分区勾画,分区予以剂量限制相比于腮腺整体勾画,能够不同程度降低腮腺受照剂量。但上述三种腮腺分区勾画方式到底哪一种更有利于腮腺保护,未见三种方式的对比研究报道。
本研究将三种分区勾画方式应用于同一患者的计划设计,横向比较对腮腺及靶区剂量的影响。腮腺分区勾画方式对靶区、其余危及器官剂量学影响如表3和5所示,所有靶区和危及器官的剂量改变都很小,并且均能满足靶区剂量覆盖和各危及器官剂量限制。对腮腺剂量学影响如表1所示,腮腺分区勾画组(计划1,计划2,计划3)两侧腮腺Dmean均低于腮腺整体勾画组(计划0);计划2两侧腮腺Dmean<30 Gy,D50<26 Gy,且能最大程度降低左右侧腮腺Dmean和D50。张羽等[15]研究结果显示,在鼻咽癌调强放疗中,两侧腮腺Dmean在36 Gy左右,明显超过了RTOG的鼻咽癌腮腺剂量限制标准[16](两侧腮腺Dmean≤26 Gy或至少一侧腮腺Dmean≤26 Gy)。本研究选择的病例均有较大颈部Ⅱ区淋巴结或者咽后淋巴结转移,故肿瘤靶区(PTV)更大,且更靠近腮腺,因此腮腺更难以满足上述剂量限制标准。采用本研究3种腮腺分区勾画方式后,当给予腮腺不同亚区D50<25 Gy剂量限制后,如图3b~d所示,靶区等剂量曲线内收,在前后方向上延伸,使得高剂量区相对远离腮腺,这可能归功于对于远离靶区的腮腺亚区如浅叶、靶区外区域、前叶的额外的剂量限制。这种变化在腮腺分区勾画方式2上表现更为明显。

图4 1例病例4组计划DVH

表5 四组计划中危及器官剂量比较(x-±s,Gy)
本研究分区勾画方式中腮腺Dmean和D50的平均值较整体勾画方式有不同程度下降,特别是勾画方式2下降趋势明显,针对存在Ⅱ区淋巴结或者咽后淋巴结转移的鼻咽癌病例,腮腺分区勾画具有降低腮腺受照剂量潜能。上述3种分区勾画方式相互比较,勾画方式1和3没有确切解剖学依据,勾画过程中人为误差较大,勾画方式2以PTV2轮廓线为界,分区依据更明确,临床工作中可行性更高。因此腮腺分区勾画方式2可能是Ⅱ区淋巴结或者咽后淋巴结转移鼻咽癌腮腺保护中值得推广的勾画方法。但由于本研究仅仅探讨了4例鼻咽癌病例,未能得出统计学上的差异,同时不能排除靶区勾画以及计划制作等试验误差的影响,同时鼻咽癌其他分期的病例是否具有相似的结论,均需要更多病例来验证。另外,此种腮腺分区勾画方式带来的腮腺保护的剂量学优势能否真正转化为临床对腮腺功能的实实在在的保护,还需要进一步开展腮腺功能评估的研究予以证实。
