壳聚糖絮凝法纯化牛蒡多糖的工艺优化
2019-02-18侯静宇王立安
许 昕,侯静宇,王立安
(河北师范大学生命科学学院,河北石家庄 050024)
牛蒡(ArctiumlappaL.)属菊科两年生草本植物[1]。据《本草纲目》记载,牛蒡性温味甘,可“通十二经脉,洗五脏恶气”,“久服轻身耐老”[2]。牛蒡多糖是由呋喃构型的D-2果糖经β(2→1)糖苷键脱水聚合而成的一种果聚糖,末端有葡萄糖残基,其聚合度一般在2~60[3]。牛蒡根中的多糖含量高达45%[4],而且牛蒡多糖作为一种水溶性膳食纤维,具有清除自由基[5]、增强免疫力[6]、降血脂[7]、改善心血管疾病[8]等功效。
壳聚糖是一类天然的阳离子型高分子絮凝剂[9]。由于分子中含有氨基,壳聚糖在酸性条件下带有正电荷,因此具有中和电荷与吸附架桥的双重絮凝作用[10-11],可有效除去多糖中的蛋白质、色素等杂质。它作为甲壳素的脱乙酰化产物,具有良好的生物相容性、无毒性、可降解特性等[12]。近年来,壳聚糖已逐渐运用到猴头菇[13]、大枣[14]、合欢皮[15]、香菇[16]、翅果油树叶片[17]等多糖的纯化中,并取得良好的效果。
目前,对于牛蒡多糖提取工艺的研究很多[18],如超声[19]、微波[20]、酶法[21]、超高压技术[22]等均可得到较热水浸提更高的多糖提取率。但纯化工艺的相关研究较少。按照传统方法,从多糖提取液中纯化多糖需要先经过除小分子杂质、脱色和去蛋白等处理,然后进行乙醇沉析,离心收集滤饼,真空冷冻干燥后制得多糖成品[23]。此传统工艺步骤繁琐,杂质均需逐步去除,实验周期长,生产效率较低而且易造成多糖等有效成分的损失[24]。为了更好地保留有效成分和缩短工艺周期,本文以牛蒡根为材料,采用壳聚糖对牛蒡多糖提取液进行絮凝纯化,以多糖保留率、蛋白清除率以及脱色率为评价指标,用正交试验的方法探讨壳聚糖絮凝的最佳工艺,以期为牛蒡多糖的研究开发奠定科学试验基础。
1 材料与方法
1.1 材料与仪器
鲜牛蒡根 河北省宁晋县牛蒡生产基地;壳聚糖、BCA蛋白浓度测定试剂盒、1-二苯基-2-三硝基苯肼(DPPH)、抗坏血酸(VC)、丁基羟基茴香醚(BHA)、过氧化氢 北京索莱宝科技有限公司;干酵母 安琪酵母股份有限公司;95%乙醇、盐酸、氢氧化钠 中国医药集团化学试剂有限公司;酵母粉、蛋白胨、葡萄糖、琼脂粉 北京奥博星生物技术有限公司;实验所使用水 均为超纯水;其余有机试剂 均为国产分析纯。
MULTISKAN GO酶标仪 美国Thermo;FW177型中草药粉碎机 天津市泰斯特仪器有限公司;MIKRO-22R型台式冷冻离心机 德国Hettich公司;YH-M10001型电子天平 瑞安市英衡电器有限公司;RE-52AA 51011型旋转蒸发仪 上海亚荣生化仪器厂;HH-4数显恒温水浴锅 国华电器有限公司;WKH-7-A型热风循环烘箱 青州市精诚医药装备制造有限公司;KQ-500E超声波清洗仪 昆山市超声波仪器有限公司;FD-1C-50冷冻干燥机 上海比朗仪器制造有限公司。
1.2 实验方法
1.2.1 壳聚糖絮凝法制备牛蒡多糖
1.2.1.1 牛蒡多糖提取液的制备 将新鲜牛蒡根于55 ℃下烘干后粉碎,过80目筛,得到牛蒡根干粉。称取一定量牛蒡粉,按照1∶10 (g/mL)的料液比于70 ℃浸提90 min,3500 r/min离心15 min,取滤渣,按照相同步骤再浸提一次,合并前两次的提取液得到牛蒡多糖提取液[23]。
1.2.1.2 壳聚糖絮凝 精确称取10.0000 g壳聚糖加入1%(v/v)乙酸溶液溶解并定容至1000 mL,充分搅拌均匀,于4 ℃条件静置6 h后使用。取1.2.1.1中的40 mL牛蒡多糖提取液(pH5.4),加入4 mL壳聚糖醋酸溶液,混匀后在一定温度下静置一定时间后,12000 r/min离心15 min后,取少量上清液检测蛋白质、多糖、色素含量的变化。
1.2.1.3 牛蒡多糖制备 将在特定条件下絮凝纯化后的多糖上清液减压浓缩、真空冷冻干燥,得到牛蒡多糖粉末,称重备用。
1.2.2 壳聚糖絮凝法纯化牛蒡多糖单因素实验
1.2.2.1 壳聚糖用量对絮凝纯化效果的影响 在26 ℃条件下,固定絮凝时间为45 min,向多糖提取液中分别加入不同用量壳聚糖溶液(0、0.4、0.8、1.2、1.6、2.0 mL/g,壳聚糖用量定义为:1%壳聚糖醋酸溶液体积/生药材质量),考察壳聚糖用量对絮凝纯化效果的影响(换算后1%壳聚糖醋酸溶液量不足4 mL的用超纯水补足)。
1.2.2.2 壳聚糖絮凝时间对牛蒡多糖纯化效果的影响 在26 ℃条件下,固定壳聚糖用量为1.2 mL/g,通过改变絮凝时间(15、45、75、105、135 min),考察絮凝时间对于牛蒡多糖纯化效果的影响。
1.2.2.3 提取液pH对牛蒡多糖絮凝纯化效果的影响 调节多糖提取液pH,在26 ℃条件下,固定壳聚糖用量为1.2 mL/g,絮凝时间45 min,考察多糖提取液不同pH(2、3、4、5、6、7)对絮凝效果的影响。
1.2.2.4 絮凝温度对絮凝纯化效果的影响 固定壳聚糖用量为1.2 mL/g,絮凝时间45 min,多糖提取液pH为4,考察不同温度(26、30、40、50、60、70 ℃)对牛蒡多糖提取液絮凝效果的影响。
1.2.3 正交试验 考虑到在26 ℃条件下絮凝效果最佳,后续试验在室温(26 ℃)条件下进行。选取提取液pH、絮凝时间和壳聚糖用量为考察因素,以多糖保留率、蛋白清除率、脱色率为评价指标,采用L9(34)正交试验表(表1)进行正交试验,从而得出壳聚糖絮凝的最佳工艺条件。

表1 L9(34)正交试验因素水平表Table 1 L9(34)orthogonal experimental design and factors
1.2.4 传统水提醇沉工艺制备牛蒡多糖方法 多糖提取液的制备方法同1.2.1.1,将所得牛蒡多糖提取液60 ℃真空浓缩至原体积的1/3,采用Sevag法去蛋白,即将氯仿与正丁醇以4∶1 (v/v)混合加入4倍体积多糖提取液中,充分振荡10 min后4000 r/min离心10 min,重复去蛋白3次之后,取上层液体加入4倍体积的95%乙醇,边加边快速搅拌,于4 ℃条件下静置10 h后,3500 r/min离心15 min,以无水乙醇洗涤沉淀,后真空冷冻干燥,即可得到牛蒡多糖[25-27]。将其用超纯水配制成0.1 mg/mL的多糖溶液,测定多糖含量,计算得率以及纯度,并与正交试验得出的最佳絮凝工艺条件下制得牛蒡多糖的各项指标比较。
1.2.5 指标测定
1.2.5.1 多糖标准曲线的绘制及多糖含量的测定 参照马宁等[28]的方法并稍作修改。精密称取10.0 mg葡萄糖,加入适量超纯水溶解,并定容至100 mL,摇匀即得0.1 mg/mL的标准葡萄糖溶液。分别精密量取0、0.1、0.2、0.3、0.4、0.5、0.6 mL的标准葡萄糖溶液,并用水补至1 mL,然后依次加入1.6 mL 5%苯酚溶液和7 mL浓硫酸,迅速摇匀,30 min后于490 nm处测定吸光度。以质量浓度为横坐标,吸光度值为纵坐标,绘得葡萄糖标准曲线,得回归方程Y=a1X+b1。将牛蒡多糖样品用超纯水稀释1000倍后,依照上述方法,测定其490 nm处的吸光度值,结合以下公式测得多糖含量。
式中,F表示多糖含量,μg;A490为490 nm处吸光度;a1、b1均为葡萄糖标准曲线中的系数值;N为稀释倍数;V为样品溶液的定容体积,mL。
1.2.5.2 蛋白标准曲线的绘制及蛋白含量的测定 参照李海玲等[29]的方法,按BCA试剂A∶B=50∶1的比例配制工作液,将0.5 mg/mL的标准BSA溶液按照0、1、2、4、8、12、16 μL加入96孔板,并用PBS溶液补至20 μL。然后每孔加入200 μL工作液,37 ℃孵育30 min后于562 nm处检测吸光度。以蛋白质质量浓度为横坐标,吸光度值为纵坐标,绘得蛋白标准曲线,得回归方程Y=a2X+b2。将牛蒡多糖样品稀释10倍,依照1.2.2的方法,测定562 nm处的吸光度值,并由蛋白标准曲线方程求得蛋白质含量:
式中,P表示蛋白含量,μg;A562为562 nm处吸光度,a2、b2均为蛋白质标准曲线中的系数值;N为稀释倍数;V为样品溶液的定容体积,mL。
1.2.5.3 多糖保留率、蛋白清除率、脱色率的测定 在按照1.2.5.1和1.2.5.2的方法求得多糖含量、蛋白含量后,按照以下公式计算即可得到多糖保留率、蛋白清除率。
式中,F1表示絮凝纯化前多糖含量,μg;F2表示絮凝纯化后多糖含量,μg。
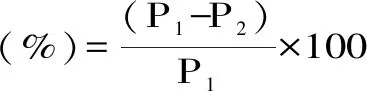
式中,P1表示絮凝纯化前蛋白含量,μg;P2表示絮凝纯化后蛋白含量,μg。
取絮凝后上清液直接检测420 nm处吸光度值,作为色素含量检测方法。脱色率计算公式如下:

式中,A1表示多糖提取液絮凝纯化之前的420 nm处吸光度值,A2表示多糖提取液絮凝纯化之后的420 nm处吸光度值。
1.2.5.4 多糖得率和纯度的测定

式中:m2表示在最佳的絮凝条件下按照1.2.1.3步骤纯化的多糖样品质量,g;m1表示原料质量,g。
纳什在《旅游作为人类学的一个主题》中指出:在人类社会中,旅游是普遍存在的一种人类活动,而旅游包含着不同文化、亚文化之间的接触[3]。
将按照1.2.1.3中制备的多糖粉末配制成浓度为100 μg/mL的多糖溶液,取1 mL的多糖溶液用1.2.5.1的方法进行检测,得到吸光度值,多糖纯度计算公式如下:

式中,A490表示490 nm处的吸光度;a1、b1均为葡萄糖标准曲线中的系数值。
1.2.6 多糖的抗氧化活性检测
1.2.6.1 DPPH·清除能力检测 参考Sharma等[30]的方法,并做若干修改。用无水乙醇配制0.2 mmol/L的DPPH·溶液,并将之与不同浓度(0.2、0.4、0.6、0.8、1.0、1.2 mg/mL)的样品溶液分别混合,37 ℃暗反应30 min,在517 nm处测定吸光度值。同时,采用维生素C作为阳性对照。以下为DPPH·清除率计算方法:

式中,A0为100 μL DPPH·溶液+100 μL水的517 nm处的吸光度值;A1是100 μL DPPH·溶液+100 μL样品的517 nm处的吸光度值;A2是100 μL样品+100 μL无水乙醇的517 nm处的吸光度值。
1.2.6.2 酵母细胞保护试验 实验参照并优化了Joshi等[31]的研究方法,实验操作步骤如下:将培养到对数期的酵母细胞经离心后混悬于100 mmol/L(pH=7.4)的磷酸盐缓冲液中,并调整细胞浓度至1×107~2×107个/mL[32]。取不同浓度(5、10、15、20、25、30 mg/mL)的多糖样品溶液加入酵母细胞悬浮液中,于37 ℃温浴2 h后,再加入一定量H2O2温浴1 h。经过上述处理的反应体系稀释适当倍数后,采用YEPD平板进行活菌计数[33],BHA做阳性对照,抗氧化剂对酵母细胞的保护作用按照以下的公式进行计算:

式中:Ai为3 mL细胞悬液+1 mL样品溶液+2.1 mL 0.14% H2O2溶液的平板活菌计数;Aj为3 mL细胞悬液+3.1 mL蒸馏水的平板活菌计数;Ao为3 mL细胞悬液+1 mL蒸馏水+2.1 mL 0.14% H2O2溶液的平板活菌计数。
1.3 数据处理

2 结果与分析
2.1 多糖和蛋白质标准曲线
2.1.1 葡萄糖标准曲线 以葡萄糖质量浓度(μg/mL)为横坐标,490 nm处的吸光度值为纵坐标,进行线性回归,得到回归方程Y=0.00368X-0.00464(R2=0.9989),线性范围为10~60 μg/mL,标准曲线见图1。
2.1.2 蛋白质标准曲线 以蛋白质质量浓度(μg/mL)为横坐标,562 nm处的吸光度值为纵坐标,进行线性回归,得到回归方程Y=0.00315X+0.0402(R2=0.9884),说明25~400 μg/mL范围内线性关系良好,本研究中所有蛋白测定均使用该标准曲线。

图1 葡萄糖标准曲线Fig.1 Calibration curve for glucose determination

图2 蛋白质标准曲线Fig.2 Calibration curve for protein determination
2.2 单因素实验结果
2.2.1 壳聚糖用量对牛蒡多糖纯化效果 如图3所示,随着壳聚糖用量的增加,牛蒡多糖提取液的脱色率和蛋白清除率不断升高,当壳聚糖用量达1.2 mL/g以后,二者增幅变缓。另外,随着壳聚糖用量的增加,牛蒡多糖保留率呈逐步下降趋势。这可能是由于壳聚糖作为一种吸附剂,在絮凝色素和蛋白质的同时,也会对与蛋白质紧密结合的多糖起到一定的吸附沉降作用[34]。综合考虑上述因素,选择壳聚糖浓度为1.2 mL/g为适宜壳聚糖用量。

图3 壳聚糖用量对牛蒡多糖保留率、 蛋白清除率和脱色率的影响Fig.3 Effects of chitosan dosages on polysaccharide retention rate,protein removal rate and decolorization rate
2.2.2 絮凝时间对牛蒡多糖纯化效果的影响 如图4所示,在15~45 min阶段,蛋白质清除率逐渐增长,在45 min后,蛋白质的去除率增势趋缓。脱色率同样在絮凝开始阶段上升,而在45 min后基本不变。另外,多糖保留率在15~135 min范围内略有下降但不明显(图4)。这可能是因为随着絮凝时间的延长,蛋白质和色素已与壳聚糖充分接触并结合为絮团,即壳聚糖对蛋白胶粒吸附饱和[35],综合考虑选择45 min为适宜絮凝时间。

图4 壳聚糖絮凝时间对多糖保留率、 蛋白清除率和脱色率的影响Fig.4 Effects of treating time of chitosan on polysaccharide retention rate,protein removal rate and decolorization rate
2.2.3 提取液pH对牛蒡多糖纯化效果的影响 实验结果表明(图5),在提取液pH从2升至4的过程中,壳聚糖蛋白质清除率逐渐增大,此后逐渐变小。这可能是由于壳聚糖在偏酸性的溶液中,分子上的氨基被质子化,使得壳聚糖带有正电荷,较易与牛蒡多糖提取液中呈阴离子型的杂质结合[36]。从图5还可看出,在pH在2~7之间,多糖保留率和脱色率有微小波动,但整体变化不大。综合考虑选取提取液pH4为适宜pH。

图5 pH对多糖保留率、蛋白清除率和脱色率的影响Fig.5 Effect of pH on polysaccharide retention rate, protein removal rate and decolorization rate
2.2.4 絮凝温度对牛蒡多糖纯化效果的影响 实验结果表明(图6),随着絮凝温度的升高,多糖保留率和脱色率基本不变,而蛋白质清除率均逐渐下降,这可能是温度升高使得分子热运动加快,絮凝剂分子老化,架桥长度变短,不利于形成大的絮团[34]。所以,絮凝纯化温度在室温26 ℃即可。

表2 壳聚糖絮凝实验结果与分析Table 2 Result and analysis of chitosan-based flocculation of polysaccharides
注:R表示因素的极差。

图6 温度对多糖保留率、蛋白清除率和脱色率的影响Fig.6 Effects of temperature on polysaccharide retention rate,protein removal rate and decolorization rate
2.3 正交试验结果
正交试验结果及极差分析见表2,多糖保留率、蛋白质清除率和脱色率方差分析分别见表3。从表2及表3可知,若以多糖保留率作为评价指标,通过极差分析可知,各因素的影响效果A>C>B,即提取液pH>壳聚糖用量>絮凝时间,最佳工艺条件为A1B1C3。另外,方差分析结果(表3)显示,A、B、C因素对多糖保留率均无显著影响。
若以蛋白清除率作为评价指标,通过极差分析可知,各因素的影响效果B>C>A,即絮凝时间>壳聚糖用量>提取液pH,最佳工艺条件为A2B1C3。另外,方差分析结果显示,A因素对蛋白清除率的影响达显著水平,B、C因素对蛋白清除率的影响达到极显著水平。
若以脱色率作为评价指标,通过极差分析可知,各因素的影响效果C>B>A,即壳聚糖用量>絮凝时间>提取液pH,最佳工艺条件为A2B1C3。另外,方差分析结果显示,A、B、C因素对脱色率均无显著影响。
综合以上三个考察因素,最终确定牛蒡多糖壳聚糖絮凝法最佳条件为A2B1C3,即提取液pH为4,絮凝时间15 min,壳聚糖用量1.2 mL/g,、此时,多糖保留率为87.15%±0.24%,蛋白清除率为54.15%±0.48%,脱色率为79.43%±0.31%。

表3 絮凝实验方差分析表Table 3 Variance analysis of flocculation experiment
2.4 絮凝法和传统水提醇沉法的比较
2.4.1 纯化工艺的比较 由表4可以看出,絮凝法耗时少,生产周期短,而且在最佳絮凝条件下,多糖得率和纯度分别比传统水提醇沉工艺提高了33%,15%,因此壳聚糖絮凝法是一种较好的纯化牛蒡多糖的方法。

表4 絮凝法和水提醇沉法的比较Table 4 Comparison of chitosan-and ethanol-based purification of polysaccharides
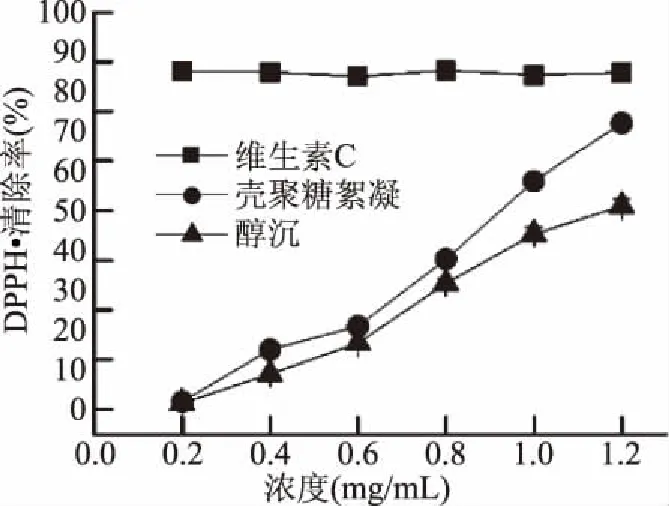
图7 两种方法制备牛蒡多糖的DPPH·清除率Fig.7 Results of DPPH· scavenging capacity of polysaccharide prepared by two methods
2.4.2 DPPH·清除活性的比较 壳聚糖絮凝法和醇沉法制备多糖样品的DPPH·清除能力如图7所示,DPPH·清除率和样品浓度之间存在明显的量效关系,且壳聚糖絮凝法制得的牛蒡多糖比水提醇沉制备的多糖DPPH·清除能力强。当壳聚糖絮凝法制备的多糖样品浓度达1.2 mg/mL时,DPPH自由基清除率已达77.61%。
2.4.3 对氧化应激酵母细胞保护作用的比较 如图8所示,随着样品浓度的增加,其对酵母细胞的保护率呈升高趋势,说明两种多糖样品均对H2O2氧化损伤的酵母细胞有剂量依赖性。当样品浓度为30 mg/mL,絮凝法制得的多糖对氧化损伤酵母细胞的保护率为40.04%±1.60%,传统水提醇沉制得的多糖样品对氧化损伤的酵母细胞的保护率为33.83%±0.81%,说明絮凝法制得的牛蒡多糖的抗氧化活性优于水提醇沉法多糖。

图8 两种方法制备牛蒡多糖 对氧化损伤酵母细胞的保护作用Fig.8 Protective effects of polysaccharide prepared by two methods on oxidative damaged yeast
3 讨论与结论
本文通过正交试验得到壳聚糖絮凝法纯化制备牛蒡多糖的工艺条件:壳聚糖用量为1.2 mL/g,絮凝时间为15 min,提取液pH为4。在此条件下,多糖得率和纯度均在传统水提醇沉工艺的基础上有一定提高,并证实絮凝法制备牛蒡多糖不仅用时短,而且抗氧化活性更强,为进一步开发利用牛蒡多糖提供了新方法。但絮凝法制备的牛蒡多糖仍为粗多糖,若后期需要继续提高多糖纯度或进一步对多糖进行分级纯化[37],则可结合超滤[38]等方法进行。
本文为比较两种多糖的抗氧化活性采用了两种方法。其中DPPH自由基清除能力检测是体外抗氧化实验中最经典的,也是使用最广泛的方法[39]。而选取酵母细胞对多糖的抗氧化活性进一步检测是因为酵母细胞和人有很多的同源基因,所以二者的抗氧化机制可能有相似之处[40],酵母细胞可以较好地模拟人体细胞受到氧化应激的状态。两种方法均显示,壳聚糖法制得的牛蒡多糖均具较好的抗氧化活性,为制备牛蒡多糖产品的功能定位指明了方向。
另外,壳聚糖作为一种有抗菌、抗氧化[41]等作用的食品添加剂,即使少量残留在多糖产品中也不会影响其品质。而且,壳聚糖来源于虾蟹外壳等水产废料,是世界上产量仅次于纤维素的第二大天然可再生资源[42]。采用壳聚糖作为絮凝剂是对生物资源的合理利用,充分体现了资源节约、环境友好的发展理念。
综上,本研究结果为牛蒡的精深加工提供了科学依据。
