新生儿重症监护患儿机械通气撤机失败的胸部CT图像特点分析
2019-02-13孙利芳陈志平时胜利
孙利芳,陈志平,时胜利
(郑州大学附属儿童医院放射科,河南 郑州450000)
机械通气是目前救治重症呼吸衰竭的重要辅助手段。研究[1]表明,达到撤机标准的患儿约40%需再次上机,一般认为撤离呼吸机48 h内患儿自主呼吸不能满足自身气体交换需再次使用呼吸机辅助通气者称为撤机失败,撤机失败成为困扰临床医师的重要问题。本文回顾性分析临床提示呼吸机撤机失败新生儿的胸部CT图像特点,旨在为临床提供帮助。
1 资料与方法
1.1 一般资料 回顾性分析2014年8月至2016年12月临床提示呼吸机撤机失败在我院行CT检查的患儿33例,其中男14例,女19例;年龄10~50 d,中位年龄27 d;早产儿19例,平均胎龄30.5周,均有出生后长期用氧史。33例均有呼吸衰竭呼吸机机械通气病史,且撤机后不耐受出现呼吸窘迫,48 h内需重新上机插管。
1.2 仪器与方法 采用Philips 16排或256排螺旋CT扫描仪行胸部CT检查,其中10例加行气道三维重建。患者取仰卧位,不配合患儿用10%水合氯醛灌肠镇静,剂量0.5 mL/kg体质量,总量≤10 mL。扫描参数:80 kV,自动管电流,层厚、层距均为5.0 mm。扫描范围从胸锁关节至膈肌层面,加行气道重建。扫描野外使用铅橡皮护具防护。
1.3 图像处理 胸部CT图像用肺窗及纵隔窗观察,由2名主治以上影像诊断医师采用双盲法,分别对肺的透亮度、肺纹理、肺实质及气管、支气管等CT征象进行分析、记录,如有异议,则由另1名影像副主任或主任医师进行评判。
2 结果
33例中,肺炎32例。28例表现为两肺野多处或局部斑片状、絮状薄片影,其中吸入综合征3例,表现为两肺广泛分布薄片影,以右侧及两下肺野背侧较著(图1);实变或不张4例,主要表现为片状致密影,主要累及某个段或亚段,1例累及整个肺叶,3例可见支气管充气相;泡性气肿和局限肺气肿6例,其中3例表现为胸膜下、肺野内多发直径1.5 mm的泡状透亮影,3例为肺段、亚段的片状低密度影,其内肺纹理稀疏。
急性呼吸窘迫综合征2例,表现为两肺透光度减低呈磨玻璃样改变,两肺野背侧可见大片实变影,并可见充气支气管征(图2)。
支气管肺发育不良(bronchopulmonary dysplasia,BPD)17例,表现为两肺局限性及广泛的线状、网格状改变;其中磨玻璃样改变10例,为两肺局灶性和弥漫性分布薄片影;实变影7例,呈肺段、亚段分布;囊泡状样影7例,双肺多发分布及局限散在分布(图3)。
先天性心脏病3例,均表现为心影饱满,进一步超声检查为先天性心脏病;两肺可见多处斑片影3例,2例肺野透光度不均匀,1例合并左肺上叶肺气肿。
气管狭窄1例,CT平扫表现为气管狭窄,增强扫描气管后壁见半环状强化影,提示血管瘤,两肺未见异常片影(图4)。
3 讨论
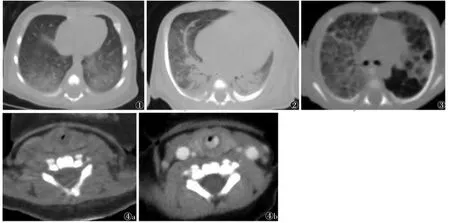
图1 男,足月,出生后6 d,羊水吸入史。CT平扫轴位示两肺下叶背侧肺野絮状薄片影 图2 女,20 d,出生后呼吸困难,急性呼吸窘迫综合征。CT平扫轴位示两肺背侧大片实变影,内可见支气管充气征 图3女,35 d,31周早产,支气管肺发育不良晚期(Ⅳ期)。CT平扫轴位示双肺透光度降低,双肺呈网格状间质性改变,左肺可见多个囊泡影及局限肺气肿 图4女,28 d,出生后呼吸困难、喘鸣音 图4a CT平扫示气管近端管腔狭窄 图4b 增强扫描气管后壁可见半环状强化影,提示血管瘤
临床上关于新生儿机械通气撤机失败的原因主要有原发病难以控制、机械通气时间过长、早产儿呼吸道发育不完善、并发症未能控制及医务人员因素等[2]。胸部影像检查因患儿上机移动困难仍以床边胸片为主,但其密度分辨力较低,显示病变局限。MSCT扫描时间短,可减少患儿呼吸及心跳运动伪影,特别是其强大的图像后处理技术,MPR可分析病变特点、位置及解剖毗邻关系,MinIP可显示气道有无狭窄和畸形,VR则可立体直观显示气道全貌。CT轴位扫描图像是各种后处理技术的基础,运用不同的后处理技术分析撤机失败患儿的肺部疾病特点,可更大可能地帮助临床医师找出撤机失败的原因从而降低其发生率。
原发病大多为肺部感染,机械通气患儿有一“肺部感染控制窗”[3],此时撤机成功率较高[4]。 目前,大多数临床医师仍以临床表现、血气分析、胸片作为撤机的常规指标,缺乏可靠的统计学依据,临床上常出现撤机后自主呼吸不能满足自身需要而重新上机[5-6]。本研究中足月患儿多为新生儿感染性肺炎,CT主要表现为支气管肺炎、大叶性或节段性实变、炎性渗出及间质性浸润,并伴不同程度的肺气肿。新生儿吸入综合征包括羊水、胎粪的吸入,以及吸入奶液、胃内容物引起的吸入性肺炎,表现为急性肺水肿和肺实变。新生儿呼吸窘迫综合征可表现为两肺透光度减低,呈磨玻璃样改变,显示弥漫性间质水肿,晚期可表现为白肺,需结合患儿临床与肺出血、新生儿湿肺鉴别,肺出血患儿插管内会有血液溢出,及时治疗短期可明显吸收;新生儿湿肺为早期呼吸窘迫原因之一,多见于足月儿,出生后2~3 d临床症状及影像异常征象消失。
先天性心脏病患儿,特别是血流动力学改变较大或复杂型先天性心脏病,肺部感染较重且难以控制,X线及CT检查应注意心影形态大小及肺血改变,提示临床进一步检查。另有1例气管狭窄出现通气障碍,增强扫描显示为气管壁血管瘤。因此,足月儿呼吸机不能撤离的原因除肺部感染加重外还应考虑心脏及气管赘生物等,且后者患儿肺部感染征象不一定严重。
另外,早产儿胎龄越小,撤机失败率越高[7]。本组早产儿平均胎龄30.5周,均有出生后长期用氧史。早产儿的肺发育不成熟是引起BPD的重要原因。传统经典型BPD主要病理特征为早期肺泡和呼吸道损伤及晚期纤维化,CT表现为两肺透光度减低、肺内广泛间质性改变以及多发小囊状改变。而新型BPD则定义为任何氧依赖(>21%)超过28 d的新生儿,且规定X线片不再作为疾病严重程度的评估依据[8],其病理改变以肺泡和肺微血管发育不良为主要特征,气道损伤和间质纤维化较轻,但弹力蛋白增多,肺泡数目减少、体积增大及肺泡结构简单化。CT主要表现为两肺过度充气,纹理粗多模糊,偶有小囊出现。Northway法将胸部影像改变分为4期[9]:Ⅰ期(1~3 d),双肺磨玻璃影,呈肺透明膜样改变;Ⅱ期(4~10 d),肺实变明显;Ⅲ期(11~30 d)两肺多发囊状低密度影,伴肺不张;Ⅳ期(1个月后),肺广泛纤维化伴肺气肿。早期X线及CT胸部表现无特异性,主要表现为原发病变的征象。赵晨等[10]认为CT上的多发囊泡影是诊断BPD的主要依据。早期应与肺水肿、肺出血鉴别,晚期影像表现应与肺发育不成熟(Wilson Mikity综合征)鉴别,后者无机械通气用氧史,可完全恢复。
综上所述,胸部MSCT检查可多方位观察病变,为确定临床分析撤机失败原因提供帮助,但其辐射量大,不宜作为常规检查方法,应在保证图像分辨力的基础上使用低剂量扫描技术,控制照射范围,并严格注意患儿防护,在非照射区域做到最大化使用防护用品[11]。
