双能量与单能量CT 扫描及重建影像在头颈部肿瘤粒子治疗计划靶区显示的差异
2019-02-12龚雪明StefanieKaess苗华栋
蒋 磊 龚雪明 Stefanie Kaess 鹿 蓉 苗华栋
国外很多研究机构发表了“Dual-Energy Computed Tomography(DECT)扫描和影像重建技术应用在以放射治疗为目的,改善质子Stopping Power Ratio 和提高照射剂量统计准确性”的研究性文献以及大量理论性数据,并且这些数据已经被临床逐步推广。然而国内很少将DECT 扫描和重建技术引入临床放射治疗计划(TPS),原因是DECT 设备整机价格较SECT 设备昂贵,国内DECT 扫描技术的主要临床应用都集中在以心脏及血管增强为诊断目的的检查。另外,和国内放射物理师临床经验缺乏也有一定关系。
作为放射治疗计划设计最重要的组成部分,清晰地勾画肿瘤区域与正常组织之间解剖轮廓、通过组织的Hounsfield Unit(HU)值[1]准确地计算出与之相关的Stopping Power Ratio(SPR)[2]以及最优化的照射剂量(as low as reasonable achievable, ALARA)都是关键[3],而这些数据的获得必须以CT扫描作为基础。国内目前常用单一能量(120kVp)的X 线束扫描,对于衰减系数相对较小的正常组织与肿瘤区域之间,因为缺乏足够的对比度,导致临床靶区轮廓勾画不清晰。另外,人工金属伪影及血管强化影像无法消除,导致影像无法用于评估,照射剂量计算误差大。双能量CT使用两种不同千伏值(80/140kVp)的X 线束,扫描范围相同的FOV,并且将两种能量获得的影像合并重建,得到一个可任意地选择范围在40 ~190keV 内的能谱曲线影像。相比SECT 的影像,在不增加辐射剂量的前提下,DECT 获得了更丰富的影像信息和最理想的重建影像条件,同时也改善了显示人体不同组织构造密度与肿瘤特征之间变化的准确性。对制定放射治疗计划(TPS),勾画靶区的具体位置和体积,以及临床靶区(CTV)和相邻危及器官(organs at risk, OAR)之间的关系,都能提供清晰的影像和准确的数据。
本文旨在分析和比较20 例头颈部肿瘤放射治疗(包括质子、重离子治疗)患者的SECT(管电压120kVp)影像与DECT(管电压80kVp/140kVp)影像以及DECT 模式下使用“Dual-Energy”软件重建出不同千电子伏(kilo electron voltage, keV)水平能谱的单能量影像(扫描部位,层厚一致)[4]。探讨两种扫描模式获得的影像和双能量能谱CT 重建的单能量影像,在改善衰减系数相近的正常组织与肿瘤组织显示分辨率和对比度上的差异,以及差异对改善和提高三维适形放射治疗设计中肿瘤区(GTV)、临床靶区(CTV)和危及器官(OAR)之间自动勾画的准确性是否具有临床价值,并通过统计两种扫描方式共三种能量的扫描剂量、容积CT 剂量指数CTDIvol(mGy)、剂量长度乘积DLP(mGy.cm),计算出头颈部有效剂量D=k·DLP(头 部K 值0.0023mSv·mGy-1·cm-1,颈 部K 值0.0054mSv·mGy-1·cm-1),研究双能量扫描在头颈部肿瘤CT 放射治疗计划设计应用的可行性。
方 法
1.设备及材料
西 门 子SOMATOM Definition AS128 排 和64 排 螺 旋CT 扫 描,安 装Dual-Energy“Monoenergy”3D 软 件 的Syngo.via,VersionVA30B 工 作站和物理师勾画靶区使用的MIMVersion6.5.9 工作站,UNIDOSWebline 高精度剂量仪和参数校正使用的Phantom。
2.DECT 和SECT 扫描协议,重建参数设定
DECT: 采 用 管 电 压80kVp, 参 考 电 流380mAs,CTDIvol7.1mGy 和 管 电 压140kVp, 参考电流90mAs,CTDIvol9.08mGy。扫描参数:准直32×1.2mm,层厚1.5mm,旋转时间1 秒,螺距0.55,FOV500mm。重建技术:使用软组织重建函数D34S Medium Smooth BHC Bone,窗位Cerebrum。SECT:采用管电压120kVp,参考电流300mAs,CTDIvol49.76mGy。扫描参数:准直32×1.2mm,层厚1.5mm,旋转时间1 秒,螺距0.55,FOV500mm。重建技术:使用软组织重建函数H30S Medium Smooth,窗位Cerebrum。
3.CT 剂量指数(CTDI),容积CT 剂量指数(CTDIvol)和剂量长度乘积(DLP)记录和比较
将一端连接UNIDOSWebline 高精度剂量仪的长杆电离室探头分次放入L(体部)=32diameter/S(颈部)=16diameter)CTDI Phantom 中心及12 点钟位置,使用已设置的DECT 和SECT 扫描参数扫描,经剂量仪检测和计算,得到剂量指数CTDI 值。同时通过设备扫描软件自身携带的剂量检测软件,统计容积CT 剂量指数(CTDIvol)和剂量长度乘积(DLP),并根据上述数值计算出CTDI 有效剂量ED 值:ED= k·DLP(颈部K 值0.0054 mSv·mGy-1·cm-1)。同样使用DECT 和SECT 扫描参数,扫描人体头颈部体模(model of human body phantom),统计容积CT 剂量指数(CTDIvol)和剂量长度乘积(DLP),并根据上述数值计算出CTDI 有效剂量ED 值。比较两种扫描模式下四组数据的差异性,确认DECT 扫描是否符合辐射正当化原则(ALARA)。
4.扫描参数
根据《Catphan® 600 技术手册》所提供的相关目标CT 标准值和显示要求,确定最佳能谱CT重建单能量影像keV 值分布范围。根据选定的keV值和线性融合参数对按照人体头颈组织构造设计的Phantom 进行影像重建。
分别对CAT Phantom 和人体头颈Phantom 采用已设置参数DECT 和SECT 扫描[5],将得到CAT Phantom DECT 影像数据传入Siemens SyngoVia工作站,使用“Dual-Energy”软件“Mono-energy”功能重建出能谱值从40 ~190keV 范围内的单能量影像[6]。通过测量、统计CAT Phantom(CTP404, CTP486)相关目标在能谱曲线影像(以40keV 为基础,每次以10 个keV 递增[7]),80kVp、120kVp 和140kVp 影像的CT 值,确定能谱keV 值的范围。并与《Catphan® 600 技术手册》所提供的标准值比较,选取与标准值接近的能谱keV 值影像。同时,评价CAT Phantom(选择CTP404,CTP528,CTP515, CTP486)在SECT 和DECT 扫描影像、能谱CT 重建单能量影像显示效果是否达到《Catphan® 600 技术手册》规定(空间分辨率、密度分辨率、噪声)的显示要求。按照人体头颈组织构造设计的Phantom,采用预先设置的DECT 和SECT 参数扫描,并根据上述方法扫描和重建影像。然后,放射物理师将影像导入放射治疗计划工作站,确定扫描和重建影像是否符合临床放射治疗要求。
5.临床实施阶段
5.1 一般资料:对2017 年1 ~4 月于上海市质子重离子医院拟头颈部肿瘤放射治疗(质子、重离子治疗)患者20 例,其中女性9 例、男性11 例,平均年龄42.2 岁,其中一位患者右眼摘除术后,另一位右侧腮腺切除术后,其余均无手术史。
5.2 治疗计划设计阶段:采用热塑性塑料面罩对头颈部固定,扫描基线以制模时在面罩上留有的定位线为准,并且以面罩所覆盖范围作为扫描范围。采用已通过验证的常规SECT(管电压120kVp)扫描参数,记录下每个病人容积CT 剂量指数(CTDIvol)和剂量长度乘积(DLP),计算出有效剂量ED。将扫描后的影像数据导入本院放射物理师使用的专业放射治疗计划设计系统(MIM Version 6.5.9)工作站,由放射物理师勾画出肿瘤区域(GTV),临床靶区(CTV)的范围,以及OARS (包括Brain Stem、Chiasm、Spinal Cord、Cochlea、EYE、LENS、Opticnerve、Parotid),并以文件名(RTstruct)保存勾画影像在系统中,为放射治疗后的验证阶段做好准备。
5.3 治疗计划验证阶段:固定方法,扫描基线,扫描范围,层厚与常规SECT 相同。采用DECT(管电压80kVp 和140kVp)双能量扫描,同样记录下每个病人容积CT 剂量指数(CTDIvol)和剂量长度乘积(DLP),计算出有效剂量ED。根据经过验证得到的能谱keV 值对双能量影像重建。同样,将扫描影像数据和重建影像数据导入该系统工作站,由同一位放射物理师操作,采用放疗计划设计系统工作站自带的Adaptive Recontour-Deform 功能,由计划设计软件根据RTstruct 影像,自动在7 组影像中勾画出同层,同部位靶区,以及器官,统计8 组影像数据在GTV、CTV 和OARs 的3D 容积(Volume),以及软件根据3D 容积范围自动计算所得平均CT 值(HU)。
5.4 影像主观评价法:由2 名主治医师对SECT(120kVp) 和DECT(80kVp/140kVp), 以及DECT 重建的能谱keV 值影像,采用双盲法进行独立评价,统一图像的窗宽和窗位。采用四分法对影像进行评价,评价内容包括以下方面:
5.1 肿瘤边缘锐利度评分:4 分,边缘清晰锐利;3 分,边缘较锐利;2 分,边缘模糊;1 分,边缘显示不清或与伪影无法分辨。
5.2 影像主观噪声:4 分,影像噪声小;3 分,影像噪声较小;2 分,影像噪声偏大;1 分,影像噪声大。
5.3 勾画靶区评分:4 分,影像总体质量优,有信心清晰勾画出靶区;3 分,影像总体质量较好,有较高信心勾画出靶区;2 分,影像总体质量较差,影像勾画靶区;1 分,影像总体质量极差,无法勾画靶区。2 名医师判断不一致时,经第3 名主任医师进行评分后采用多数者评分值。
6.统计学方法
使用SPSS17.0 进行统计学分析。CAT Phantom 所含化学成分材料AIR、PMP、LDPE、Water、Polystryrene、Acrylic、DelrinTM、Teflon的CT 定量参数值以表示,采用单样本t 检验,P<0.05 表示差异具有统计学意义。临床实施阶段DECT 及能谱重建勾画出GTV、CTV 和OARs 的3D 容积和CT 值(HU)以表示,符合正态分布者,采用独立样本t 检验,P<0.01 表示差异具有统计学意义。SECT 与DECT 及能谱重建勾画区域3D容积(Volume)和CT 值(HU)的比较采用配对样本t 检验,不符合正态分布者采用秩和检验。主观评分采用非参数检验(Friedman test)。P<0.05 表示差异具有统计学意义。
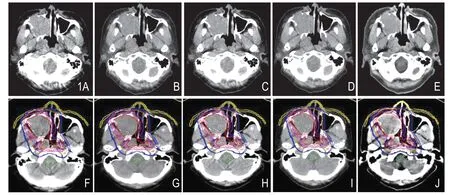
图1 A ~D.头颈部采用DECT(80/140kVp)扫描及部分能谱重建轴面图像。E.头颈部采用SECT(120kVp)扫描轴面图像。F ~J.上述扫描及部分重建影像在放射治疗计划设计系统中勾画肿瘤靶区图像。50 KeV(图F)、90KeV(图G)、80kVp(图H)、140kVp(图I)、120kVp(图J)头颈部轴位影像肿瘤区域GTV(红线)、CTV(蓝线)和OARS(绿线等) 的3D 容积,并且系统根据容积计算出相关区域的平均CT 值(HU)。
结 果
扫 描 参 数: 比 较SECT(120kVp) 与DECT(80kVp/140kVp) 扫描模式下测得CTDI Phantom 中心点和12 点方向的剂量指数CTDI,以及CTDI Phantom 和人体头颈部体模Model of human body Phantom 的 扫 描 剂 量、CTDlvol *(mGy)、DLP(mGy.cm)和有效剂量D,DECT 较SECT 辐射剂量明显降低,符合辐射实践正当化原则,该扫描协议可以在临床扫描检查中使用。
最佳能谱keV 值分布范围:比较使用DECT 扫描影像重建能谱从40 ~190keV 单能量影像所测得CATPhantom(CTP404)各材料成分CT 值,除在Polystryrene 材料成分CT 值无统计学意义(P>0.05)外,其余7 种材料成分CT 值差异均有统计学意义(P<0.05)(表1)。并且,数据显示能谱从50 ~90keV 所测得CT 值最接近厂家提供的标准CT值,影像评价显示(CTP515)能谱低于50keV 的重建影像虽然具有较高的密度分辨率,但能量过低噪声也随之明显升高,导致空间分辨率低,影像质量不能满足诊断要求。显示(CTP528)能谱高于90keV 的重建影像虽然具有较高的空间分辨率,但高能量降低不同组织之间的有效衰减,导致密度分辨率低,同样影像质量也不满足诊断要求。因此,我们在临床实施阶段,除选择2 组DECT 扫描影像外,能谱值为50keV、60keV、70keV、80keV、90keV 共5 组重建影像作为对照组,SECT(120kVp)扫描影像作为标准组。
表1 CTP404 各材料成分在能谱重建影像中CT 值分析
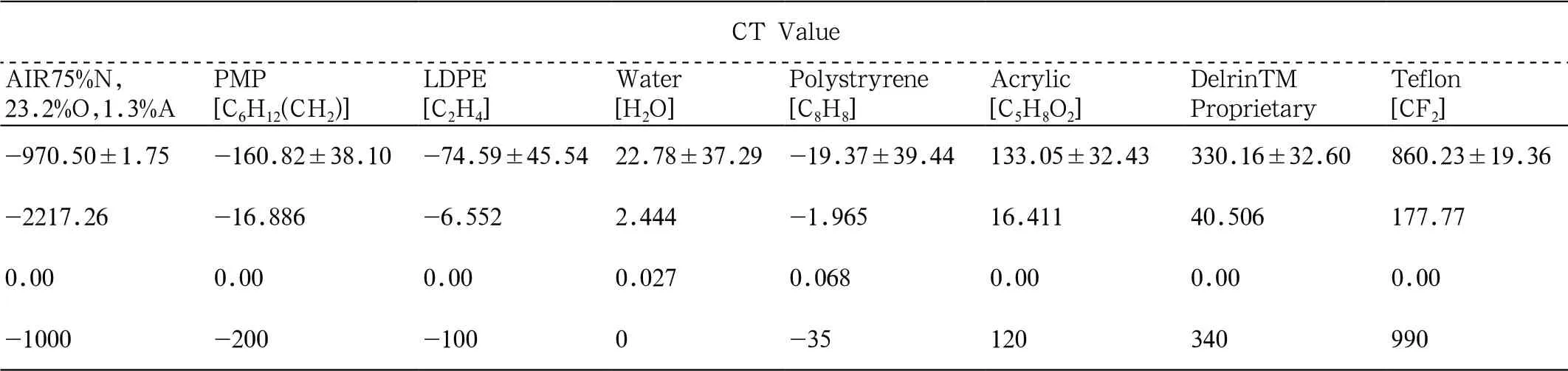
表1 CTP404 各材料成分在能谱重建影像中CT 值分析
CT Value AIR75%N,23.2%O,1.3%A PMP[C6H12(CH2)]LDPE[C2H4]Water[H2O]Polystryrene[C8H8]Acrylic[C5H8O2]DelrinTM Proprietary Teflon [CF2]-970.50±1.75 -160.82±38.10 -74.59±45.54 22.78±37.29 -19.37±39.44 133.05±32.43 330.16±32.60 860.23±19.36-2217.26 -16.886 -6.552 2.444 -1.965 16.411 40.506 177.77 0.00 0.00 0.00 0.027 0.068 0.00 0.00 0.00-1000 -200 -100 0 -35 120 340 990
表2 DECT 及能谱重建3D 容积范围(Volume)和平均CT 值(HU)的关系
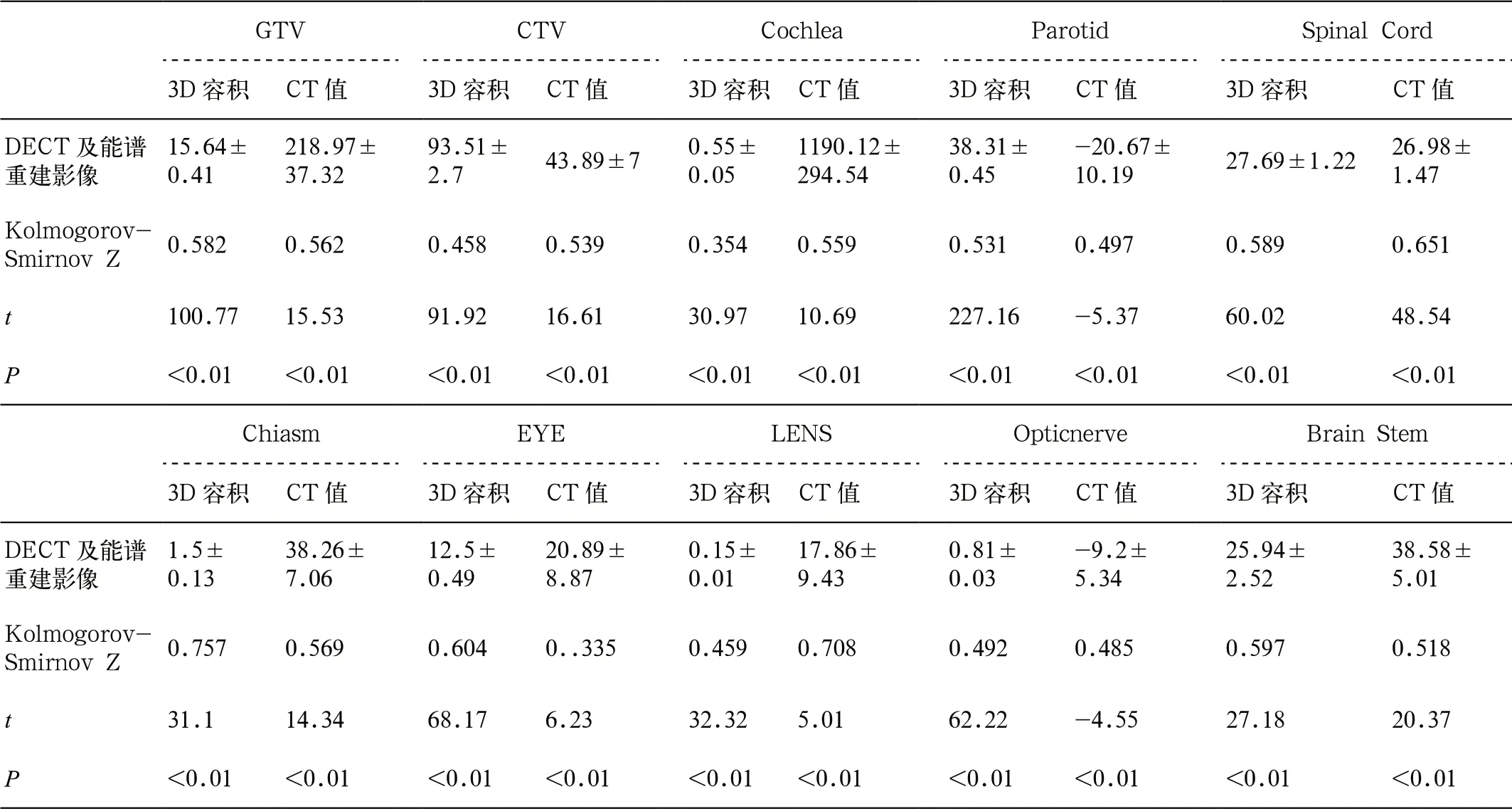
表2 DECT 及能谱重建3D 容积范围(Volume)和平均CT 值(HU)的关系
GTV CTV Cochlea Parotid Spinal Cord 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值DECT 及能谱重建影像15.64±0.41 218.97±37.32 93.51±2.7 43.89±7 0.55±0.05 1190.12±294.54 38.31±0.45-20.67±10.19 27.69±1.22 26.98±1.47 Kolmogorov-Smirnov Z 0.582 0.562 0.458 0.539 0.354 0.559 0.531 0.497 0.589 0.651 t 100.77 15.53 91.92 16.61 30.97 10.69 227.16 -5.37 60.02 48.54 P<0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 Chiasm EYE LENS Opticnerve Brain Stem 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值DECT 及能谱重建影像1.5±0.13 38.26±7.06 12.5±0.49 20.89±8.87 0.15±0.01 17.86±9.43 0.81±0.03-9.2±5.34 25.94±2.52 38.58±5.01 Kolmogorov-Smirnov Z 0.757 0.569 0.604 0..335 0.459 0.708 0.492 0.485 0.597 0.518 t 31.1 14.34 68.17 6.23 32.32 5.01 62.22 -4.55 27.18 20.37 P<0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01
影像质量主观评价:对20 例头颈部肿瘤放射治疗患者标准组SECT 和对照组DECT 扫描影像,能谱从50 ~90keV 重建影像共160 组影像主观评价分数统计,肿瘤边缘锐利度和勾画靶区信心评分在不同能量扫描和能谱重建影像,总体分布是不相同的,影像评分差异有统计学意义(P<0.01)。但是,影像主观噪声评分在不同能量扫描和能谱重建影像,总体分布是相同的,影像评分差异无统计学意义(P>0.05)。
3D 容积范围和平均CT 值:分析和检验20 例头颈部肿瘤放射治疗患者DECT 扫描和能谱从50-90keV 重建影像勾画出GTV、CTV 和OARs 的3D容积范围和计算出的平均CT 值,数据值呈现正态分布,并且差异具有统计学意义(P<0.01)(表2)。
比较20 例头颈部肿瘤放射治疗患者标准组SECT 扫描影像和对照组DECT 扫描及能谱从50-90keV 重建影像勾画出GTV、CTV 和OARs 的3D容积范围和平均CT 值:Brain Stem 和Spinal Cord平均CT 值,Chiasm、EYE、LENS 3D 容积范围和平均CT 值差异具有统计学意义(P<0.05)。Brain Stem 和Spinal Cord3D 容 积 范 围,GTV、CTV、Chiasm、Cochlea、Optic nerve、Parotid 3D 容 积范围和平均CT 值差异均无统计学意义(P>0.05)(表3)。
比较20 例头颈部肿瘤放射治疗患者标准组SECT 和对照组DECT 扫描剂量、CTDlvol(mGy)、DLP(mGy.cm)和有效剂量D(表3),显示对照组均低于标准组,差异有统计学意义(P<0.05)。
表3 表3 两组能量扫描及5 种能谱重建3D 容积范围、平均CT 值(HU)和辐射剂量比较(±)( )

表3 表3 两组能量扫描及5 种能谱重建3D 容积范围、平均CT 值(HU)和辐射剂量比较(±)( )
分组GTV CTV Cochlea Parotid Spinal Cord Total mAs DLP 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值标准组 59±38.43 54.34±98.25 190.42±153.65 100.14±191.95 0.35±0.24 1129.99±151.64 35.26±15.83 3.67±25.3 20.26±8.38 6.56±5.6 7291.9±533.64 2229.9±169.2对照组 59.6±38.07 43.08±115.94 188.65±148.17 96.24±161.49 0.37±0.25 1192.97±332.14 36.81±17.02-9.63±33.99 19.62±7.75 43.45±11.2 6145.3±140.39 752.87±18.57 F 0.001 0.06 0.01 0.04 0.07 17.53 0.45 2.65 0.11 6 13.42 20.39 P >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 <0.05 <0.05 <0.05分组Chiasm EYE LENS Opticnerve Brain Stem有效剂量E CTDIvol 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值 3D 容积 CT 值标准组 1.33±0.53 25.42±13.83 9.6±1.37 45.42±3.73 0.27±0.07 95.94±9.95 0.71±0.29 36.62±38.52 26.68±6.47 26.85±1.54 12.04±0.91 50.06±000对照组 1.1±0.42 33.88±17.81 10.61±1.66 17.37±7.95 0.21±0.05 21.73±9.62 0.72±0.3 31.28±38.31 25.21±6.65 38.01±5.67 4.07±0.1 16.08±0.47 F 2.64 0.11 1.3 14.97 2.41 0.28 0.03 0.01 0.05 16.56 20.36 4.46 P <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 >0.05 >0.05 >0.05 <0.05 <0.05 <0.05
讨 论
本研究结果发现DECT 扫描及能谱重建影像测得颈部肿瘤组织和正常组织的CT值呈现出正态分布,能量在60 ~80keV 时CT 值最高,相对应的3D 容积也最大,同时影像的噪声最低,分辨率最高,肿瘤与正常组织的边界,以及肿瘤组织的内部结构显示更加清晰,从而增加物理师准确地勾画肿瘤靶区的信心。相比SECT(120kVp)一次扫描只能获得一种能量结果,DECT 采用高(140kVp)、低(80kVp)两种管电压扫描,并且将扫描后的影像合并重建,得到能谱值从40 ~190keV 范围内的单能量影像。根据统计数据,DECT 测得肿瘤组织和正常组织的CT 值均涵盖了SECT 的CT 值,相对应的3D 容积也同样涵盖。也正是因为DECT 扫描的这个特点,对X 线束的衰减系数接近正常组织和肿瘤,可以调节能谱能量,获得影像显示差异的最佳密度分辨率和空间分辨率。特别是在除金属伪影方面效果更显著。对于DECT 扫描外界一直存在两种能量扫描会增加患者接受辐射的剂量,容易引起被照射器官辐射损伤。在本研究中,DECT 扫描参数是通过对CTDI Phantom 和人体体模扫描后,由高精度剂量仪测得的辐射剂量计算得出,并且专业扫描软件监测显示的结果证明:DECT辐射剂量明显低于SECT。在接下来临床实施阶段,这个结果也进一步得到了证实。因此,遵循辐射防护最优化原则(as low as reasonable achievable, ALARA),设置低辐射剂量的CT 检查扫描参数尤为重要。
综上所述,头颈部肿瘤粒子治疗计划靶区设计显示中,在辐射剂量明显降低的前提下,DECT 扫描影像以及基于DECT 影像重建的不同能谱值影像可以获得可变量的CT 值,对改善衰减系数相近的正常组织与肿瘤组织显示分辨率和对比度具有优于SECT扫描影像获得单一的CT 值,一定程度上提高了临床三维适形放射治疗设计中肿瘤区(GTV)、临床靶区(CTV)和危及器官(OR)之间自动勾画的准确性。
