脑转移瘤的影像学诊断
2019-01-25,,
, ,
中山大学肿瘤防治中心放射科、华南肿瘤学国家重点实验室、肿瘤医学协同创新中心(广东广州 510060)
颅脑是恶性肿瘤常见的远处转移器官之一,最常见发生脑转移的恶性肿瘤有肺癌、乳腺癌、恶性消化道肿瘤等,最常见的转移途径为血行转移,脑转移瘤约占颅内肿瘤20%~40%。好发部位为脑实质内,其中幕上好发于大脑半球(约占80%), 以大脑中动脉分布区多见;幕下转移常见于小脑。脑转移瘤亦可见于脑膜(硬脑膜、软脑膜)、脑干、垂体、视神经及眼球、颅骨。本文结合中山大学肿瘤防治中心的相关典型病例影像图片说明脑转移瘤的影像诊断。
1 脑转移瘤影像学检查技术概述
中枢神经系统的常用影像学检查方法包括计算机断层扫描成像(CT)、核磁共振成像(MRI)、数字减影血管造影(DSA)、核医学成像(PET-CT)等,这些检查方法各有其优缺点,应根据临床需要有效选择。
1.1 MRI 是目前中枢神经系统检查最重要的影像诊断方法,亦是临床怀疑有脑转移瘤的首选检查方式。其优点是无辐射、软组织分辨率高、多参数成像、灵敏度高。缺点是成像较慢,部分体内有磁敏感金属的患者、幽闭恐惧症患者不适宜进行MRI检查。
MRI检查可利用血管成像(MRA)检查肿瘤与血管的关系,以及弥漫加权成像(DWI)、扩散张量成像(DTI)、灌注加权成像(PWI)、磁敏感加权成像(SWI)、磁共振波谱成像(MRS)、功能性磁共振成像(fMRI)等技术进一步评估脑组织的功能和代谢改变,有利于脑转移的诊断及鉴别诊断。
1.2 CT 是颅内病变诊断应用较广泛的影像检查方法,其优点是扫描速度快,密度分辨率高,后处理图像重建能力强,缺点是存在电离辐射,软组织分辨率低。CT扫描根据占位效应和密度改变可以发现大多数脑转移病灶,CT骨窗可显示转移瘤与颅脑骨质的关系,增强CT扫描可以更好地提高脑转移瘤诊断灵敏度。
1.3 DSA DSA是诊断颅内血管性病变的金标准。其优点是对脑血管成像清晰、直观,不受颅骨及血流动力学改变影响,缺点是有创检查、操作环境存在电离辐射。DSA在脑转移瘤的诊断上较少应用。
1.4 PET-CT 肿瘤细胞葡萄糖、核苷酸、氨基酸等物质代谢异常活跃,肿瘤代谢显像就是放射性核素标记代谢底物,利用核素示踪技术体外显像,探测体内肿瘤组织的代谢情况。其优点是灵敏度高,对于微小病灶有较高的检出能力和确诊率,缺点是存在核辐射。
2 脑转移瘤影像学表现及诊断
2.1 脑实质转移 脑转移瘤好发部位为脑实质内,其中幕上好发于大脑半球, 以大脑中动脉分布区多见;幕下转移常见于小脑。常见表现为颅内多发实质病变,少数可单发[1]。其位置多发生于灰白交界区(约占74.5%),是由于受脑内动脉血液供应的特殊性影响:大脑皮层的血供多为皮质下白质的3~4倍,在解剖结构上可知供血动脉在灰白质区变细,故癌栓常停留于此[2]。形态上脑转移瘤以类圆形及圆形多见,因原发肿瘤病理基础不同,可不同程度发生囊变、坏死、出血、钙化等。
2.1.1 CT表现 平扫表现为颅内多发或单发的圆形或类圆形病灶,以多发病灶多见,可呈高、中、低或混杂密度,肿瘤小者为实性结节,大者中间多有坏死,呈不规则环状[3],一般囊壁厚薄均匀一致, 外部清晰、内壁模糊,偶可见壁结节。以常见的肺癌转移瘤为例,肺癌脑转移瘤中腺癌以多发转移瘤常见,鳞癌以单发转移瘤多见,与其病理特性有关。
脑转移瘤增强扫描病灶多呈结节状、环形或不规则明显强化,见图1。腺癌脑转移瘤以结节性强化多见,鳞癌则以环形强化多见,见图2。

A:CT增强扫描横断位示右侧额叶、基底节区、双侧小脑半球多发环形、结节状强化灶(箭头),边界欠清;B:增强扫描明显强化,周围少量低密度水肿区
图1肺癌脑转移瘤CT影像(60岁男性)
另外,“小肿瘤大水肿”为脑实质转移瘤特征性表现,单发病灶以中重度水肿多见,呈大片指样水肿。多发病灶无水肿或轻度水肿,病灶数较多、中重度水肿较少。瘤周水肿通常不累及胼胝体和大脑皮质, 这一点有别于胶质瘤。瘤周水肿程度可能与转移瘤的分化程度相关,分化程度越低,转移瘤恶性程度越高,水肿越严重[4]。
2.1.2 MR表现 脑转移瘤在MR上主要表现为脑实质多发或单发的类圆形异常信号灶,无囊变坏死或出血病灶在T1WI上呈等或低信号,在T2WI上呈稍高或高信号,少数病灶可呈等信号。如瘤体内出现囊变坏死,在T1WI上呈低信号,在T2WI上呈高信号,少数可见在T2WI上呈低信号环。出血者信号表现为混杂(短、长)T1,混杂(长、短) T2信号,在T2WI图像上呈现厚薄不一、或不完整的不规则含铁血黄素环[5]。绝大多数脑转移瘤在MR平扫T1WI及T2WI图像上即可显示,极少数病例在转移早期,或病灶位于皮层,或者同时有脑萎缩的患者,MR平扫未能显示异常信号。增强扫描,85%的病例发现比平扫更多的病灶,能显著提高灵敏度[6]。在进行MR增强扫描时可见均匀的结节样或环形的强化影像,以环形强化多见,瘤内坏死时,囊壁呈厚薄不均或壁结节强化;见图3。
A:CT平扫横断位示做顶叶一环状转移瘤,病灶中央坏死,边界清,周围脑实质见大片状低密度水肿区;B:增强扫描病灶明显环形强化(箭头),中央液化坏死区及周围脑实质水肿区无强化
图2肺癌脑转移瘤CT影像(50岁男性)
瘤周水肿在MRI上表现为在T2WI上呈斑片状、条片状高信号,在T1WI上呈等或稍低信号,一般表现为“小肿瘤大水肿”。董鹏等[7]对影响肺癌脑转移灶瘤周水肿范围的一系列临床及影像因素做了对比分析,结果发现瘤周水肿程度与转移灶大小及发生部位有关,而与原发病灶强化形式及肿瘤的组织学类型无关联性。而马茜等[8]研究则认为不同原发肿瘤脑转移瘤瘤周水肿程度比较差异有统计学意义,所以,瘤周水肿的程度与原发肿瘤类型是否有相关性,目前意见尚不统一。
在DWI上脑转移瘤实质部分为等或高信号,见图4-C,坏死囊变部分低信号,在图4-A、B、D上实质部分显示为等或稍低信号,坏死囊变部分明显高信号[9]。闫斌等[10]研究中脑转移瘤的MRS主要表现:肿瘤实质的胆碱(Cho)峰值增高、N-乙酰天门冬氨酸(NAA)峰值降低、Cho/肌酸(Cr)及Cho /NAA明显增高、NAA/Cr降低;见图5-D。瘤周水肿与正常脑实质代谢物比较,Cho /NAA增高。另外,脑转移瘤MRS常可出现脂质峰及可流动脂质[11]。

A:MRI平扫横断位显示颅内多发结节异常信号,在T2WI上呈稍高信号,部分结节内见坏死,瘤周见大片状水肿;B:水肿在FLAIR上呈明显高信号;C:增强扫描病灶呈环形强化,瘤周水肿无强化
图3乳腺癌脑转移瘤MR影像(43岁女性)

A:MRI平扫横断位显示右侧顶叶类圆形异常信号,在T1WI上呈等信号为主,内见小斑片状高信号影,提示瘤内出血。瘤周见大片状低信号水肿区;B:在T2WI上病灶呈混杂稍高信号,水肿呈明显高信号;C:在DWI上,病灶呈等信号,瘤内出血呈低信号;D:增强扫描病灶呈明显不均匀强化,瘤周水肿无强化
图4胃癌脑转移瘤MRI影像(65岁女性)
2.1.3 PEC/CT主要表现 临床上最常用的PET/CT正电子药物为18F-FDG,是葡萄糖的类似物。达到一定体积的脑转移瘤在18F-FDG PET/CT上一般显示为代谢活跃结节,伴周围代谢低下的水肿区,见图6。但由于脑灰质以葡萄糖代谢为主,正常脑组织放射性本底过高,包括转移瘤在内的脑肿瘤与周围正常脑组织对比不明显,使得肉眼分辨肿瘤有一定难度,必须结合PET/CT的结构影像特点进行分析。11C-MET是目前临床应用最多的氨基酸类显像药,其摄取多少主要与组织细胞表面的氨基酸转运体分布多少有关,而与肿瘤细胞的蛋白质合成关系不十分明显。由于氨基酸不是脑组织的常规能源,正常脑组织摄取少,而脑肿瘤摄取11C-MET多,因此,11C-MET PET/CT图像组织对比度佳,图像清晰,有助于观察肿瘤组织。
18F-FDG PET/CT还可以观察大脑转移瘤所致的交叉性小脑神经机能联系不能(crossed cerebellar diaschisis,CCD),CCD指脑内某一局灶损伤区域的兴奋性传出冲动丧失,致神经系统其他特异性区域对刺激的反应性减弱,这种功能障碍是突发性的,损伤灶与受累的远隔区域间有神经解剖的关联。引发CCD有多种因素,最常见是由脑血管疾病引起,然而其发生机制仍不是很清楚。主要表现为一侧小脑半球18F-FDG摄取明显低于对侧,见图7。
2.2 脑膜转移 肿瘤脑膜转移相对脑实质转移少见,其发生概率虽然低,但由于早期诊断困难,容易漏诊,导致患者预后不良。脑膜转移的诊断主要依靠有明确的原发恶性肿瘤病史、出现脑实质转移难以解释的神经系统症状和体征、影像学检查、脑脊液细胞学检查。
肿瘤的脑膜转移一般包括血行转移、蛛网膜下腔播散和直接侵犯。中枢神经系统以外的肿瘤如肺癌、乳腺癌、淋巴瘤、消化道肿瘤等多经血行转移,中枢神经系统肿瘤常见经蛛网膜下腔播散,鼻咽癌则可通过颅底自然孔道直接侵犯硬脑膜[12-13]。
恶性肿瘤的脑膜转移一般分为硬脑膜-蛛网膜型和软脑膜-蛛网膜型,硬脑膜-蛛网膜型较多见。软脑膜-蛛网膜型脑膜转移表现为广泛性脑回表面、脑沟、脑裂、脑池及室管膜下等部位弧线状强化,且形态不规则,亦可形成结节,见图8。硬脑膜-蛛网膜型脑膜转移MRI表现为大脑凸面或小脑幕连续不均匀线样脑膜增厚或“鼠尾征”,一般不伸入脑沟、脑裂内生长,范围多较广泛,严重者可局部形成结节或不规则肿块,增强扫描明显强化,见图9;如侵犯邻近脑组织,可引起局部脑实质水肿;少数脑膜转移仅表现为脑积水,而无脑膜强化[14]。

A:MRI平扫横断位显示左侧颞叶不规则异常信号,在T1WI上呈环形等信号,中央坏死区呈低信号;B:在T2WI上病灶囊变坏死区呈明显高信号,瘤周见大片状高信号水肿区;C:在增强扫描上病灶呈环形强化为主,边界结节样强化,坏死区无强化;D:在MRS上,IOS区取病灶强化部分,曲线显示:Cho明显增高、NAA降低、Cho /Cr及Cho /NAA明显增高、NAA/Cr降低;并可出现脂质峰
图5肺癌脑转移瘤MRI影像(55岁女性)

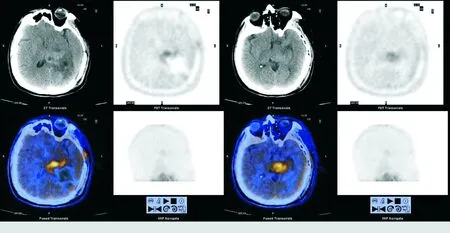
A:颅脑18F-FDG PET/CT显示左侧顶叶大片状水肿区代谢低下;B:颅脑11C-MET PET/CT显示左侧顶叶近大脑镰结节代谢活跃,周围大片状水肿区低下;C:颅脑18F-FDG PET/CT显示左侧顶枕叶结节代谢活跃,周围水肿区代谢低下;D:颅脑11C-MET PET/CT显示左侧顶枕叶结节代谢活跃
图6肺癌脑转移11C-MET PET/CT图像

右侧小脑半球18F-FDG摄取明显低于对侧

A:冠状位;B:横断位;C:矢状位; 双侧额部、右侧颞部软脑膜不均匀弧线状增厚、明显强化;部分脑回见条带状强化
脑部MRI成像,特别是增强MRI是诊断和定位脑膜转移瘤的重要手段。
3 鉴别诊断
3.1 胶质瘤 单发常见,需与单发的脑转移瘤鉴别,高级别胶质瘤与脑转移瘤鉴别较为困难。胶质瘤多位于脑深部脑白质,可有扩散灶,多数位于原发灶附近,浸润生长,边界不清,可沿脑白质扩散至邻近脑白质或经胼胝体累及对侧,呈环形强化时壁厚薄不均,常有壁结节,瘤周水肿相对较轻,水肿可累及胼胝体;见图10。

A:横断位;B:冠状位:右侧额部硬脑膜呈不均匀增厚、明显强化;可见“鼠尾征”
图9肺癌硬脑膜转移MRI增强扫描(51岁男性)
胶质瘤水肿区在MRS图像上NAA减低,Cho升高,胶质瘤的瘤周Cho/Cr值升高[15],而转移瘤在MRS图像上无此特点。

A:MRI平扫横断位示右侧枕叶不规则肿块,边界不清,在T1WI上呈混杂等稍低信号,病灶沿脑白质扩散; B:病灶在T2WI上呈混杂稍高信号,周围脑实质斑片状高信号水肿区; C:在增强扫描上病灶呈明显不均匀强化,水肿区不强化,邻近见小斑片样强化扩散灶
图10胶质母细胞瘤(Ⅳ级)MRI(69岁女性)
图11左丘脑间变星形细胞瘤Ⅲ级术后11C-MET PET/CT显像,可见术区结节代谢活跃,为胶质瘤术后复发的PET/CT表现。
3.2 血管母细胞瘤 血管母细胞瘤好发于成年人16~48岁,男性多于女性,多发生于小脑。其分型有囊结节型(大囊小结节)、实质型、单纯囊性型,囊壁一般不强化,结节显著强化,在DWI上实质部分不受限,结节及邻近脑组织可见流空血管,见图12。而单发脑转移瘤以囊变多见,囊壁可见强化,在DWI上实质部分受限,无流空血管,可兹鉴别。
显示术区结节代谢活跃
3.3 脑脓肿 常有感染病史是重要鉴别依据,脑脓肿病理上分为三期:急性脑炎期、化脓期、包膜形成期(1~2周),其中包膜形成期(图13)最需要跟脑转移瘤相鉴别,其在T2WI上表现为在高信号环壁外可见低信号环征,形成“双环征”,在DWI上囊内呈高信号,强化环内外壁均较光滑整齐, 壁厚薄均匀;有时可有“切迹征”、“囊中囊”等征象,无壁结节。而后者强化环外壁光滑内壁模糊、壁厚薄不均匀,可有壁结节,在DWI上囊内弥散不受限。
3.4 脱髓鞘病变
3.4.1 多发性硬化 需要与多发的脑转移瘤鉴别,多发性硬化多见于青年女性病灶,病程以缓解与复发交替为特征,常发生在侧脑室周围及深部脑白质,最大径常与侧脑室垂直(即直角征),活动期病灶可呈环形、半环形(开口向外,开环征)强化及结节强化;无占位效应、缺乏指状水肿;病灶多发新旧不一;病灶内有走行正常髓静脉穿过。图14显示1例多发性硬化患者的颅脑MRI表现。

A:右侧小脑半球见一囊实性占位,在T2WI上囊性部分呈高信号,实性壁结节呈稍高信号,周围见少量水肿;B:在T1WI上囊性部分呈低信号,实性成分呈等信号;C:在DWI上结节呈低信号;D:增强扫描结节明显强化,囊壁不强化;E:在PWI上,病灶呈低灌注
图12囊结节型血管母细胞瘤(34岁女性)

A:MRI横断位示右侧顶叶病灶,在T1WI上呈低信号,边缘见环形高信号;B:在T2WI上呈混杂高信号,周围脑实质见大片状高信号水肿区;C:在DWI上囊内弥散受限,呈高信号;D:增强扫描病灶呈环形强化灶,见“囊中囊”征象
图13脑脓肿MRI(59岁男性)

A:MRI横断位双侧侧脑室旁多发病灶,部分病灶长径与侧脑室垂直,在T2WI上呈高信号;B:在T1WI上呈低信号;C:在FLAIR上呈高信号;D:增强扫描病灶无强化
图14多发性硬化(42岁女性)
3.4.2 脱髓鞘假瘤 女性多见,平均年龄37岁。影像特征表现为脑白质内单发团块,占位效应多较轻,在T1WI上呈低信号,在T2WI上呈高信号,非闭环形强化(开口朝向灰质),环形强化或结节样强化,有时可见垂直于侧脑室的线条样强化(梳齿样扩张静脉血管)。在MRS上Cho、Cho/Cr均可增高,常见乳酸峰和谷氨酸盐峰,对脱髓鞘假瘤的诊断有一定特异性。见图15。

A:MRI平扫示右侧额顶叶病变,边界不清,在T1WI上呈低信号;B:增强扫描病灶呈非闭环形强化(开口朝向灰质);C:在DWI上病灶呈低信号,周围见高信号环;D:在MRS上见Cho峰明显升高,Cr、NAA峰减低,可见Lip峰
图15脱髓鞘假瘤
3.5 脑结核 脑结核多见于青壮年,以血行播散为主,脑结核病变可见以下4种类型:肉芽肿型;干酪型;弥漫性粟粒样型;脑膜炎型。与脑转移瘤的鉴别要点主要是,前者囊变区在T1WI上稍高信号,在DWI上受限,内壁常常较为光整,见图16;后者囊变区在T1WI上呈低信号,在DWI上不受限,且囊壁厚薄不均匀,可有壁结节。

A:MRI平扫示左侧小脑半球见不规则病灶,边界不清,病灶中央在T1WI上呈等稍高信号,病灶边缘呈稍高信号;B:在T2WI上病灶呈混杂等稍高信号,边缘呈高信号,病灶周围脑实质见大片状水肿区;C:增强扫描病灶呈环形明显强化,壁厚薄不均匀,中心囊变区无强化
图16脑结核瘤(21岁女性)
3.6 寄生虫感染 中枢神经系统最常见的寄生虫感染性疾病是脑囊虫病,是猪绦虫的囊尾蚴寄生于人脑内所引起的疾病,占全身囊虫病的80%。可分为:脑实质型、脑室型、脑膜型、混合型;脑实质型又细分为脑炎型、囊泡型、多发环形或结节强化型、慢性钙化型。其中多发小囊泡型需要与多发脑转移瘤相鉴别。多发小囊泡型CT表现为脑实质内多发圆形、类圆形低密度影,分布不均,典型者可见小结节状等密度囊虫头节,增强扫描多不强化,见图17-A;在MRI上,囊尾蚴存活时,病灶在T1WI上呈低信号,在T2WI上呈高信号,周围无水肿,头节呈等信号,见图17-B;囊尾蚴死亡后,病灶周围出现水肿,钙化期,病灶在T1WI及T2WI均呈低信号。典型的头节与钙化,是两者主要的鉴别点。

A:CT平扫示双侧脑实质多发类圆形低密度灶及结节状钙化,边界欠清,病灶内密度不均;B:右侧颞叶、左侧枕叶见结节状异常信号灶,在T1WI上病灶呈低信号,内见小条状高信号,在T2WI上病灶呈高信号,增强扫描病灶呈环形强化
图17脑囊虫病
4 总结
脑转移瘤在临床上发病率高,影像学上具有一定特征性表现,在临床诊断的基础上,结合相关影像学检查,特别是CT或MRI增强扫描对脑转移瘤病灶的发现具有重要的意义。
