我国公立医院干细胞临床研究及其相关伦理委员会的现状*
2019-01-25王剑萍白莉华马晨光
王剑萍,白莉华,马晨光,林 云,张 勘,薛 迪**
(1 上海市卫生健康委员会,上海 200125,lucywang@outlook.com;2 上海交通大学医学院附属同仁医院,上海 200336;3 复旦大学公共卫生学院,国家卫生健康委卫生技术评估重点实验室,上海 200032)
2015年8月,我国国家卫健委发布了《干细胞临床研究管理办法(试行)》,2016年10月又公布了全国首批通过备案的30所干细胞临床研究机构。干细胞临床研究相关管理规定的出台,有助于我国加强干细胞临床研究机构管理,落实我国干细胞临床研究机构的主体责任,确保符合条件的医疗机构能够规范地开展干细胞临床研究,促进我国干细胞临床研究健康发展。本文旨在分析我国公立医院干细胞临床研究与相关伦理管理的基本状况,探讨我国干细胞临床研究的发展。
1 研究内容与方法
本研究选取了上海市、天津市和贵州省作为调查的省级行政区域,选择此3个区域首批通过国家干细胞临床研究的备案机构9所和目前刚通过国家第二批干细胞临床研究的备案机构1所(共10所)公立医院作为被调查的机构。针对被调查的10所公立医院(上海市、天津市和贵州省分别为5所、3所和2所),开展了机构问卷调查、伦理委员会的问卷调查和现场关键知情者访谈。本研究邀请了被调查的10所公立医院干细胞及相关生物样本库的负责人、科研部门负责人和伦理委员会秘书进行了关键知情者访谈,以了解干细胞临床研究的现况与伦理管理状况。
2 研究结果
2.1 被调查公立医院的基本状况分析
分析显示,本次被调查的10所公立医院中,9所为三级甲等综合性医院,1所为三级甲等专科医院;2017年10所被调查公立医院实际开放床位616~3400张;拥有卫生人员1212~4090人,其中卫生技术人员占79.87%~89.24%。2016年10所被调查公立医院的总医疗服务人次数为17.16万次~436.30万人次,其中住院人次数为2.02万次~12.12万人次;平均承担省部级项目数为49.2项(5~93项),平均承担国家级项目数为56.6项,平均拥有市级、省部级和国家级重点学科数分别为5.7个、9.0个和5.4个。此外,医院备案或准备备案的干细胞临床研究项目平均为1.5个(0个~6个),有6所公立医院尚无备案或准备备案的干细胞临床研究项目。
2.2 被调查公立医院干细胞临床研究状况
分析显示,被调查的10所公立医院中,仅1所公立医院在调查时有1个干细胞临床研究项目在国家卫健委备案,4所公立医院有14个干细胞临床研究项目申请备案。15个备案或申请备案的干细胞临床研究项目中,9个项目采用间充质干细胞,2个项目采用脂肪干细胞,2个项目采用诱导多能干细胞,采用支气管基底层细胞和人视网膜色素上皮细胞的各有1项。干细胞临床研究针对的疾病主要是目前无有效治疗方法的难治性疾病,详见表1。
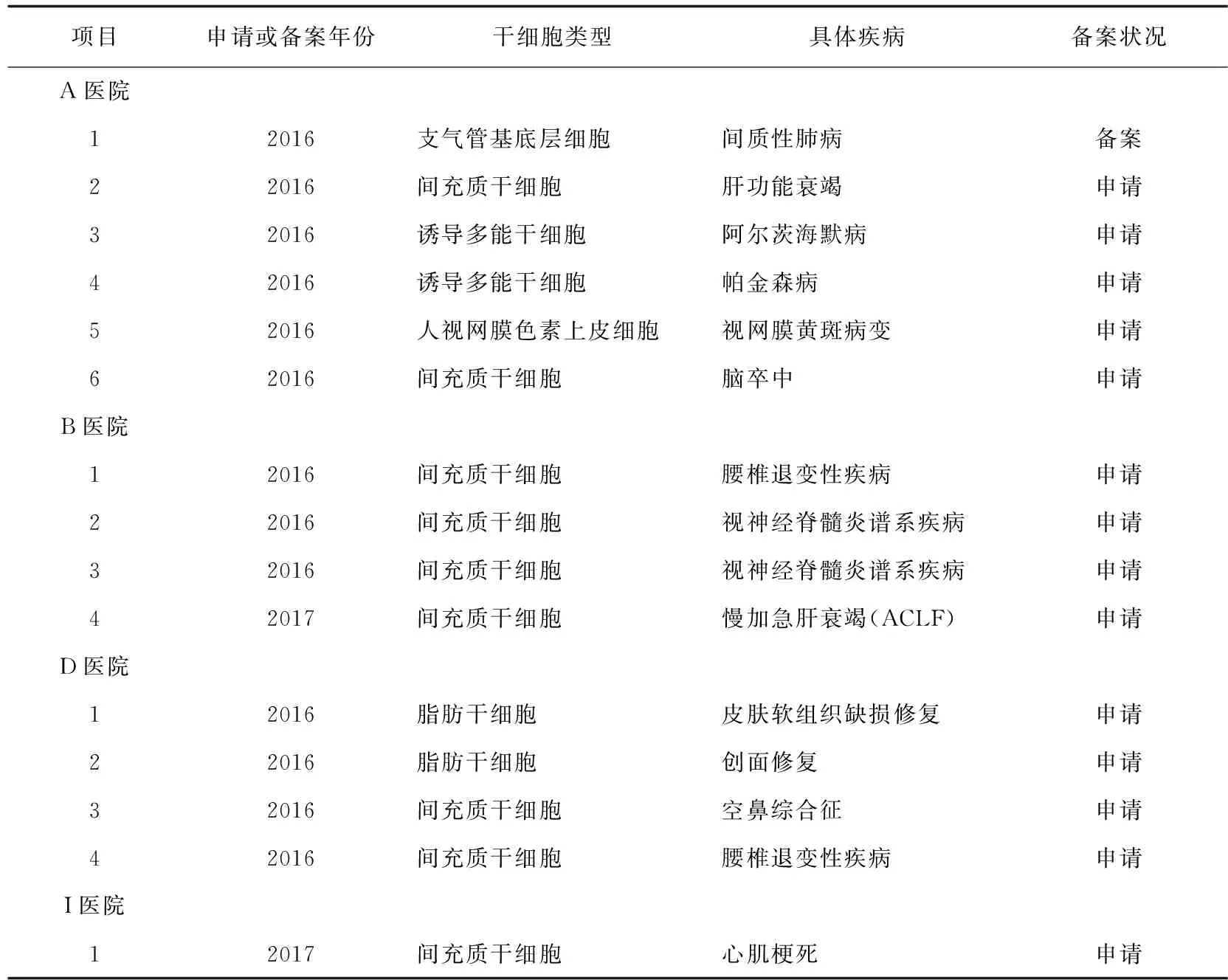
表1 被调查公立医院干细胞临床研究的基本状况
2.3 干细胞临床研究相关伦理委员会的基本状况
本次被调查的10所公立医院均建立了机构伦理委员会,其中1所医院专门建立了干细胞临床研究的伦理分会;伦理委员会建立时间为1993-2017年;伦理委员人员数为11~19人,其中院外委员人数为2~ 5人(主要是律师、社会表、临床药理和卫生统计研究者、社会与伦量学专家)。除有3所医院未制定有专门针对干细胞伦理审查的标准操作程序(SOP)外,其余医院制定有干细胞伦理审查的标准操作程序(见表2)。
分析显示,涉及干细胞临床研究的伦理委员会136名委员和秘书中,女性占60.29%,45岁及以上者占72.79%,正高级职称者占70.59%;院级或中层领导占52.94%;临床研究人员、行政管理人员、医技人员、伦理专家分别占59.56%、12.50%、9.56%和4.41%。

表2 涉及干细胞临床研究相关的伦理委员会基本状况
2.4 关键知情者的意见和建议
本研究的关键知情者对我国干细胞临床研究的看法与建议是:①由于干细胞具有自身生物学特性,理论上可应用于医疗领域的多个方面;②目前干细胞临床研究主要针对的是难治性疾病,例如周围血管疾病、红斑狼疮、多发性硬化症和风湿性关节炎、帕金森病、阿尔茨海默病、脑卒中、脊髓损伤、视网膜黄斑变性、骨关节损伤及退化、糖尿病、肺部感染、肺慢性纤维化疾病以及肿瘤等;③我国干细胞临床研究常用的是间充质干细胞、神经干细胞和脂肪干细胞,胚胎干细胞主要用于基础研究,诱导多能干细胞则仍停留在学术探讨阶段;④我国干细胞临床研究目前还处于初步发展阶段,首批通过备案的30所公立医院干细胞临床研究备案项目数量较少,备案机构也正在积极组织干细胞临床研究项目的备案申报;⑤我国曾出现干细胞临床研究的乱象,一些社会机构或医疗机构为谋取利益,出现虚假宣传、夸大干细胞疗效,使患者承担了较大的风险;⑥为了保障干细胞临床研究在医疗机构规范有序开展,完成项目备案的医疗机构还需不断改进和完善干细胞临床研究的质量管理(包括干细胞制剂质控),加强对干细胞临床研究的日常监管。
此外,访谈的关键知情者认为:目前我国干细胞临床研究相关的伦理委员会中,具有干细胞及相关专业知识背景的人员缺乏;仅少部分备案的公立医院成立了干细胞临床研究的伦理委员会;建议我国可建立区域性或联合性的干细胞临床研究伦理委员会,优化伦理委员会委员的人员配置,适当增加干细胞临床研究的相关专业人员。访谈的关键知情者还认为,我国应从国家层面进一步制定细化、可操作的干细胞临床研究伦理管理规范(如指导原则、指南、实施细则等),严格干细胞临床研究机构和项目的准入制度,有步骤地引导医疗机构干细胞临床研究伦理管理的规范化和制度化;认为为了保护干细胞临床研究受试者的权益,医疗机构应严格按照《干细胞临床研究管理办法(试行)》的要求,继续重视机构学术委员会和伦理委员会对干细胞临床研究的立项审查与监管,重视干细胞研究的特殊风险,做好潜在风险与预期收益的评估与权衡,重视干细胞临床研究知情同意的实施,强化干细胞临床研究受试者的隐私保护和数据安全,积极组织干细胞临床研究相关法规、政策、专业知识和伦理培训,提升干细胞临床研究相关人员的业务水平和伦理素养。
3 讨论与建议
3.1 积极稳健地推动我国干细胞的临床研究
本次机构调查发现,10所被调查的通过国家干细胞临床研究的备案机构均为三级甲等综合或专科医院,从医院规模(实际开放床位616~3400张,卫生人员1212~4090人)、医疗服务(总医疗服务人次数为17万人次~436万人次)、医学科研(平均承担省部级和国家级科研项目分别为49.2项和56.6项,平均拥有市级、省部级和国家级重点学科数分别为5.7个、9.0个和5.4个)等方面均有较强的综合能力。但是,在本研究调查时,被调查医院备案或准备备案的干细胞临床研究项目平均为1.5个,有6所公立医院尚无备案或准备备案的干细胞临床研究项目;仅1所公立医院在调查时有1个干细胞临床研究项目在国家卫健委备案,有4所公立医院有14个干细胞临床研究项目申请备案。这一调查结果与关键知情者访谈结果相似,我国干细胞临床研究目前还处于初步发展阶段,首批通过备案的30所公立医院干细胞临床研究备案项目数量较少。我国需积极稳健地推动干细胞临床研究。
3.2 难治性疾病是目前干细胞临床研究的主要方向
干细胞临床研究为一些常规治疗方法难以治愈的疾病带来了新的治疗手段,为阿尔兹海默病、帕金森病、等重大疾病的有效治疗带来了希望[1-4]。本次机构调查发现,15个备案或申请备案的干细胞临床研究项目中,9个项目采用间充质干细胞,2个项目采用脂肪干细胞,2个项目采用诱导多能干细胞,采用支气管基底层细胞和人视网膜色素上皮细胞的各有1项;干细胞临床研究针对的疾病主要是目前无有效治疗方法的难治性疾病,如肝功能衰竭、阿尔兹海默病、帕金森病、视网膜黄斑病变、脑卒中、腰椎退变性疾病、视神经脊髓炎谱系疾病,其他还有间质性肺病、心肌梗死、空鼻综合征、皮肤软组织缺损修复和创面修复。本次关键知情者访谈也了解到,目前干细胞临床研究主要针对的是难治性疾病,即常规手段治疗无效、疾病日益加重而无替代治疗方法的疾病。
3.3 提升干细胞临床研究相关伦理委员会的审核能力
本次被调查的10所公立医院虽然均建立了机构伦理委员会,但仅1所公立医院专门建立了干细胞临床研究的伦理委员会;虽然委员和秘书的总体结构基本符合伦理委员会伦理审核的要求,有院外人员(主要是律师、社会代表、临床药理和卫生统计研究者、社会与伦理学专家),有临床研究人员、行政管理人员、医技人员等,但关键知情者访谈中了解到干细胞临床研究相关伦理委员会委员中具有干细胞临床研究背景的人员相对缺乏。为了更好控制干细胞临床研究的伦理风险,笔者建议我国公立医院可根据医院实际情况,通过建立干细胞临床研究的伦理委员会分会、增加具有干细胞临床研究背景的委员、聘请干细胞临床研究专家作为伦理委员会的独立顾问或建立区域性或联合性的干细胞临床研究伦理委员会,以提高干细胞临床研究相关伦理委员会的伦理审核能力。
3.4 完善和落实我国干细胞临床研究的伦理规范
本研究发现,10所被调查的公立医院中,有3所医院未制定有专门针对干细胞伦理审查的标准操作程序(SOP)。鉴于干细胞临床研究的特殊风险,我国开展干细胞临床研究伦理审核的机构应建立干细胞伦理审查的SOP。正如关键知情者所指出的,我国曾出现干细胞临床研究的乱象,使患者承担了较大的风险。虽然2015年我国出台了《干细胞临床研究管理办法(试行)》,但还应从国家层面进一步制定可操作的干细胞临床研究伦理管理规范(如指导原则、指南、实施细则等),指导干细胞临床研究伦理审核机构制定SOP和开展规范的伦理审核,指导干细胞临床研究机构规范开展干细胞临床研究,有效控制干细胞研究风险,加强干细胞临床研究机构和行政监管部门的监管和监督。
