E515-A对猪流行性腹泻病毒灭活疫苗的佐剂作用
2019-01-24麻勇棋王越珉胡松华
麻勇棋,徐 伟,王越珉,胡松华
(浙江大学 动物科学学院,浙江 杭州 310058)
猪流行性腹泻是由猪流行性腹泻病毒(porcine epidemic diarrhea virus, PEDV)感染引起的一种急性、高度接触性肠道传染病[1]。PEDV可感染各年龄的猪,导致动物出现呕吐、水样腹泻及脱水等临床症状,以仔猪的感染最为严重,病死率可达80%~100%,给养猪业造成巨大的经济损失[2]。疫苗注射是预防PEDV感染的常用方法之一。目前,已有PEDV的灭活疫苗、减毒活疫苗和基因工程疫苗等[2]。但在养猪生产中常见动物注射疫苗后不能产生有效的免疫反应,其原因之一是疫苗的免疫原性不高[3-4]。因此,研究如何提高PEDV疫苗的免疫效果在生产上具有重要意义。为提高疫苗免疫效果,常将含疫苗抗原的水相和油相佐剂混合制成油乳剂疫苗。最近研究发现,将人参茎叶皂苷和油乳剂疫苗混合可提高疫苗的免疫效果。例如,包省军等[5]报道,在以白油为佐剂的口蹄疫油乳剂疫苗中加入人参茎叶皂苷可显著提高动物对疫苗的免疫应答水平;李禹涛等[6]报道在以白油为佐剂的鸡新城疫油乳剂疫苗中加入人参茎叶皂苷可显著提高疫苗的免疫效果。但以白油为油相,和水相混合时通常要在高剪切力作用下才能形成稳定的乳剂。例如,实验室条件下制备油乳剂时,乳化机的剪切转速高达10 000 r·min-1时,才能形成稳定的乳剂,制备工艺要求相对较高[7]。E515-A是一种主要含人参茎叶皂苷(GSLS)的白油佐剂,该佐剂和水相混合时在低剪切力(剪切转速仅需200 r·min-1)作用下就可形成稳定的乳剂,疫苗制备工艺要求相对较低。本研究探讨E515-A对PEDV疫苗的免疫佐剂作用,为进一步采用E515-A作为病毒性疫苗佐剂提供依据。
1 材料与方法
1.1 材料
含20%氢氧化铝胶的0.9% NaCl溶液购自齐鲁动物保健品有限公司;10号白油购自中国石化集团杭州炼油厂;GSLS(含Re 16.36%、Rd 9.0%、Rg1 6.0%、Rb2 3.8%、Rc 3.7%、Rb1 2.4%和Rf 0.1%)购自吉林省宏久生物科技股份有限公司;E515-A(主要成分为含GSLS的白油)由本实验室研制;K562靶细胞购自中国科学院上海细胞库;PEDV(106.75TCID50mL-1)抗原及其抗体检测试剂均由浙江大学动物科学学院李肖梁研究员惠赠。
1.2 PEDV疫苗的制备
将稀释5倍后的PEDV抗原与铝胶佐剂、E515-A佐剂或生理盐水等体积混合,即每mL PEDV疫苗中抗原量相当于105.75TCID50。制备油乳剂疫苗时,在油相(白油或E515-A)中缓慢加入等体积含PEDV抗原的水相,置31 ℃恒温摇床,于200 r·min-1混合乳化15 min。
1.3 含E515-A的PEDV疫苗的性状检验
采用染色法进行油乳剂疫苗的类型鉴定,即分别用水溶性染料曙红-Y和脂溶性染料苏丹Ⅲ进行染色,观察内外相染色情况;采用离心法进行油乳剂疫苗的稳定性检测,即吸取10 mL油乳剂疫苗于离心管中,3 000 r·min-1离心15 min,观察其析出与分层情况;采用NDJ-8S型旋转黏度计和Nano ZS型纳米粒度电位分析仪分别检测油乳剂疫苗的黏度和粒径大小及分布情况。
1.4 动物分组和处理
雄性ICR小鼠,6~8周龄,18~20 g,购自上海史莱克实验动物有限责任公司。将72只小鼠随机分成6组,每组12只,腹部皮下分别注射0.2 mL 0.9% NaCl溶液、PEDV抗原+0.9% NaCl溶液、PEDV抗原+GSLS溶液、PEDV抗原+白油、PEDV抗原+E515-A和PEDV抗原+氢氧化铝胶,免疫2次,间隔2周,以0.9% NaCl溶液为阴性对照,氢氧化铝胶为阳性对照。每组随机取6只小鼠于一免后24 h采血分离血清用于检测IFN-γ水平,并无菌分离脾脏制备淋巴细胞,用于检测NK细胞杀伤活性。每组的另外6只小鼠于二免后的2周和3周采血分离血清,用于检测PEDV特异性IgG抗体及其亚类IgG1和IgG2a水平及细胞因子IL-5的含量,并于二免后3周无菌分离脾脏制备淋巴细胞进行淋巴细胞增殖试验。
1.5 NK细胞杀伤活性试验
无菌分离脾脏,于研钵中磨碎后过200目滤网,滤液于1 500 r·min-1离心8 min,弃上清后,加入红细胞裂解液于冰上处理3 min,然后于1 500 r·min-1离心8 min,弃上清,用Hank’s溶液洗涤3次,加入配好的细胞培养液(含10%胎牛血清和1%青霉素/链霉素双抗溶液),调整淋巴细胞浓度至1 × 108和5 × 107mL-1,作为效应细胞备用。调整K562细胞浓度至2 × 106mL-1作为靶细胞。于96孔细胞培养板中分别加入100 μL两种不同浓度的效应细胞和100 μL靶细胞(效靶比分别为50∶1和25∶1),效应细胞和靶细胞对照孔分别补充加入100 μL 1640培养液,置于CO2浓度为5%的细胞培养箱,37℃ 培养5 h,然后加入2 μg·μL-1的MTT溶液50 μL,继续培养4 h后于1 500 r·min-1离心10 min,弃上清,加入150 μL的DMSO,避光振荡15 min,测量D570值,并计算NK细胞杀伤活性。
NK细胞杀伤活性=[1-(效应细胞+靶细胞孔D570值-效应细胞孔D570值)/靶细胞孔D570值]× 100%。
1.6 脾淋巴细胞增殖试验
脾淋巴细胞的制备同1.5节,调整细胞浓度为5 × 106mL-1。在96孔培养板中分别加入100 μL淋巴细胞,然后分别加入100 μL 1640培养液、5 μg·mL-1的刀豆蛋白(Con A)或4 μg·mL-1的脂多糖(LPS),置于CO2浓度为5%的细胞培养箱,于37℃ 培养44 h,采用MTT法检测D570值,并计算淋巴细胞刺激指数(SI)。
SI=(刺激孔D值-空白孔D值)/(未刺激孔D值-空白孔D值)。
1.7 血清IgG抗体及其亚类检测
采用间接ELISA方法检测,在预包被PEDV抗原的96孔板中,加入100 μL 1∶1 600稀释的待测血清,于37 ℃ 孵育60 min,洗板后加入100 μL HRP标记的山羊抗小鼠IgG(1∶40 000稀释)、IgG1(1∶1 500稀释)或IgG2a(1∶1 500稀释)抗体,于37 ℃ 孵育30 min,洗板后加入100 μL TMB显色液,显色时间为10 min,然后加入50 μL终止液后检测D450值。
1.8 血清细胞因子测定
采用武汉博士德生物工程有限公司生产的ELISA试剂盒检测小鼠血清IFN-γ水平,具体操作按说明书进行。
1.9 数据统计
试验结果表示为平均值±标准方差,采用SPSS 24.0统计软件中One-way ANOVA post-hoc多重比较的Duncan法进行检验,P<0.05为差异显著。
2 结果与分析
2.1 含E515-A的PEDV油乳剂疫苗的一般特征
含E515-A的PEDV油乳剂疫苗外观呈乳白色。用水溶性染料曙红Y染色时,表现为外相被染色,用脂溶性染料苏丹红Ⅲ染色时,表现为内相被染色;3 000 r·min-1离心15 min后不分层;黏度为(18 ± 2) cP;粒径分布在106~122 nm(92%)和6~8 nm(8%),平均粒径为106.9 nm(图1)。
2.2 E515-A提高了小鼠早期免疫水平
各组小鼠在免疫后24 h检测NK细胞杀伤活性。疫苗中添加佐剂的小鼠NK细胞杀伤活性显著高于对照组(P<0.05),以E515-A佐剂组的杀伤活性最高(P<0.05)。按照NK细胞杀伤活性大小,各组的排列次序依次为:E515-A组>白油组和铝胶组>GSLS组>对照组(图2-A)。疫苗中添加佐剂对小鼠血清IFN-γ的产生也有促进作用,其中E515-A组的IFN-γ水平显著高于其他各组(P<0.05)(图2-B)。按照血清中检出IFN-γ的水平高低,各组的排序为:E515-A组>白油组>铝胶组>GSLS组和对照组。

图1 含E515-A的PEDV油乳剂疫苗的粒径分布Fig.1 Diameter distribution of PEDV oil emulsion vaccine containing E515-A
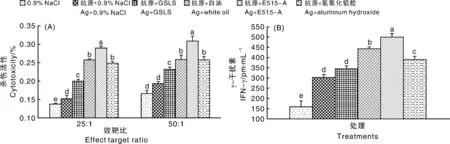
A,NK细胞杀伤活性;B,小鼠血清IFN-γ水平。柱上无相同小写字母表示差异显著(P<0.05)。下同。A, NK cytotoxicity; B, Serum IFN-γ level. Data on the bars marked without the same lowercase letter indicated significant differences at P<0.05. The same as below.图2 E515-A对机体早期免疫的影响Fig.2 Effects of E515-A on the early immune response
2.3 E515-A提高了血清特异性抗体水平
各组的血清特异性抗体水平见图3。GSLS单独使用不能提高IgG水平(P>0.05);白油和铝胶能够显著促进IgG的产生(P<0.05);当GSLS和白油联合使用(即E515-A佐剂)时对IgG的促进作用优于两者单独使用(P<0.05)。佐剂作用从大到小依次为E515-A>白油>铝胶>GSLS(图3-A)。如图3-B所示,抗体亚类的结果与之相似,但铝胶佐剂偏向于促进IgG1水平(P<0.05),而对IgG2a水平无显著促进作用(P>0.05)。
2.4 E515-A促进淋巴细胞增殖反应
如图4所示,E515-A佐剂组小鼠的脾淋巴细胞在体外对Con A刺激的应答能力显著(P<0.05)高于其他组,对LPS刺激的应答能力显著(P<0.05)高于0.9% NaCl溶液、PEDV抗原+0.9% NaCl溶液及PEDV抗原+氢氧化铝胶组。
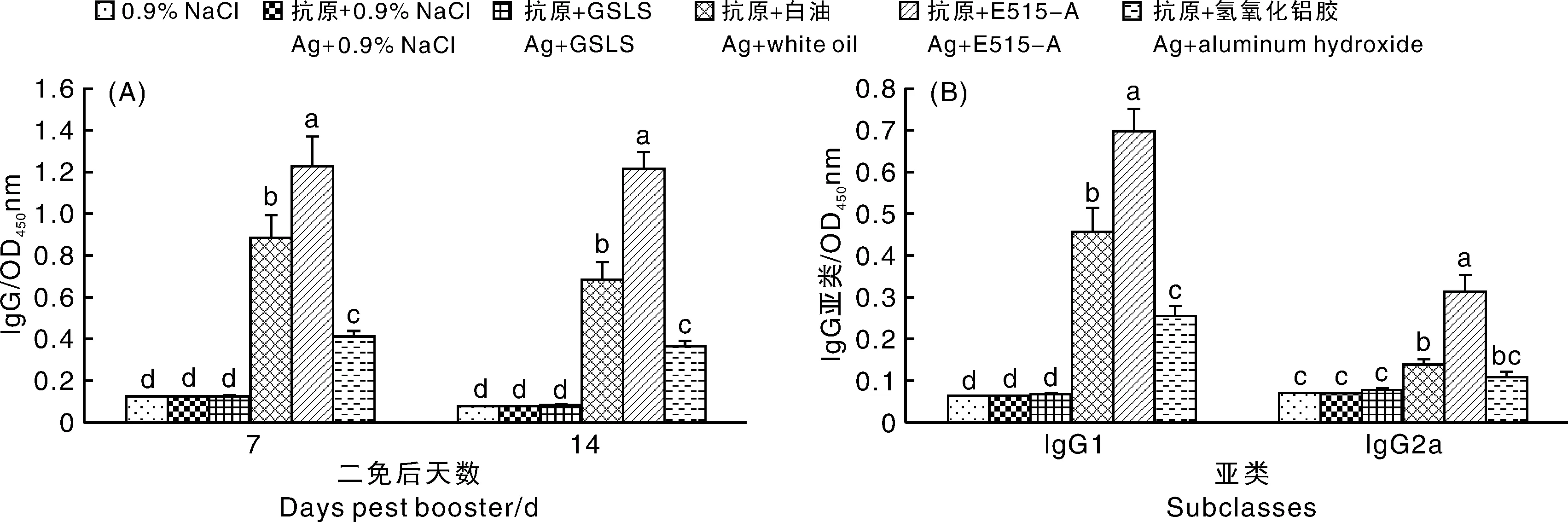
A,IgG抗体水平;B,IgG亚类水平。A, IgG level; B, IgG subclasses level.图3 E515-A对血清特异性抗体IgG及其亚类水平的影响Fig.3 Effects of E515-A on the serum specific IgG and its subclasses
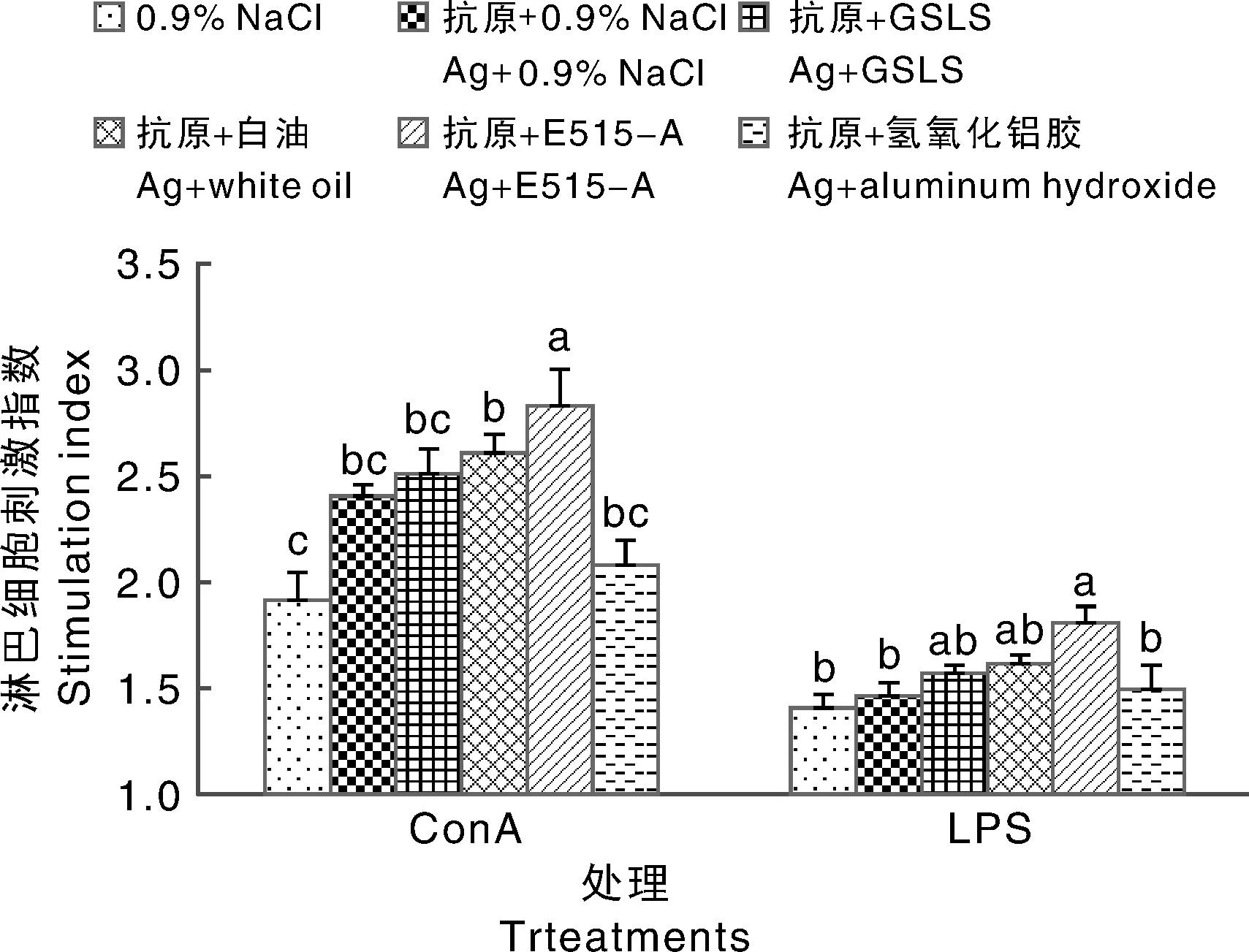
图4 E515-A对脾淋巴细胞增殖的影响Fig.4 Effects of E515-A on spleen lymphocytes proliferation
3 讨论
本研究表明,含人参皂甙的油佐剂E515-A可以和含PEDV抗原的水相在低剪切力下混合,形成稳定的油乳剂PEDV疫苗。经3 000 r·min-1离心15 min后乳剂不分层;黏度为(18±2)cP,符合兽药典对注射用疫苗的要求。E515-A对PEDV疫苗诱导的免疫反应具有显著的促进作用,免疫促进效果优于铝胶佐剂。和对照组比较,E515-A油佐剂可以显著促进免疫小鼠的NK细胞杀伤活性,促进细胞因子IFN-γ的产生,增强脾淋巴细胞对Con A和LPS刺激的增殖应答能力,提高血清IgG及其亚类IgG1和IgG2a水平。
病毒侵入机体后首先刺激免疫系统产生天然免疫应答,激活NK细胞并促进IFN-γ产生[8]。本研究发现,含E515-A的PEDV疫苗免疫小鼠24 h后即可显著增强NK细胞的杀伤活性,促进血清IFN-γ的生成,表明E515-A可以提高机体的早期免疫水平。PEDV疫苗诱导的体液免疫水平与机体抗病毒感染的能力密切相关[9]。E515-A可大幅度提高PEDV抗原诱导的IgG水平,提示该佐剂可通过提高体液免疫应答增强机体的抗感染能力。淋巴细胞体外增殖反映了机体细胞免疫应答水平。Con A主要刺激T淋巴细胞增殖,LPS主要刺激B淋巴细胞增殖[10]。本研究发现,含E515-A佐剂显著增强了细胞对Con A和LPS刺激的反应能力,表明E515-A可通过增强T和B淋巴细胞功能来提高细胞免疫应答。不同的淋巴细胞可促进不同类型的免疫反应。Th1类淋巴细胞刺激IgG2a的产生,促进细胞免疫反应;Th2类淋巴细胞刺激IgG1的产生,促进体液免疫反应[11]。本研究中E515-A可显著提高IgG1和IgG2a水平,而铝胶佐剂仅对IgG1有显著促进作用,对IgG2a无显著促进作用。这说明E515-A佐剂可促进细胞免疫(Th1)和体液免疫(Th2)应答,而铝胶佐剂仅对Th2类免疫反应有促进作用,对Th1类免疫反应几乎无作用。这与Zhang等[12]和王萌等[13]报道的E515佐剂能显著促进金黄色葡萄球菌疫苗和口蹄疫疫苗诱导的Th1和Th2型免疫应答的结果相似。
本研究用E515-A配制PEDV油乳剂疫苗,制备条件温和,乳剂的稳定性和黏度符合药典要求,注射后局部吸收良好,未发现任何不良反应。鉴于该佐剂对Th1和Th2型免疫具有显著促进作用,该佐剂用于PEDV疫苗的生产,可提高疫苗免疫效果,值得进一步研究。
