恩替卡韦联合聚乙二醇干扰素或胸腺素治疗代偿期乙型肝炎肝硬化2年疗效随访*
2019-01-23曹艳平隋洪婷曲宝聚朴红心
曹艳平,隋洪婷,潘 猛,曲宝聚,朴红心
全球大约有2.4亿人为慢性HBV感染者,中国每年有超过100万人死于HBV感染所致的肝硬化、肝细胞癌(HCC)和肝衰竭[1,2]。HBV 持续感染且高水平复制是造成肝硬化发生及病情进展的重要因素,抗病毒治疗代偿期肝硬化的首要目标是阻止或延缓肝功能失代偿和肝癌的发生[3,4]。目前,有效治疗慢性乙型肝炎的药物包括核苷(酸)类似物【nucleos(t)ide analogues,NAs】和 α- 干扰素(interferon-α,IFN-α)两大类[5]。NAs能直接抑制 HBV DNA复制,而IFN-α在具有免疫调节作用的同时也能直接抑制HBV DNA复制[6,7]。胸腺素是具有免疫调节作用的多肽,能够增强机体的抗病毒免疫应答,同时也能延缓肝纤维化的进展[8]。我们应用恩替卡韦联合聚乙二醇化干扰素(PEG-IFN)α-2a或联合胸腺素治疗代偿期乙型肝炎肝硬化患者,观察了临床疗效的差异,现将结果报道如下。
1 资料与方法
1.1 一般资料 自2013年10月至2015年1月就诊于延边大学附属医院的代偿期乙型肝炎肝硬化患者106例,经筛选后纳入国家科技重大专项课题,即病毒性肝炎临床治疗方案研究专题者88例,入选标准:年龄18~65岁、内镜检查提示存在食管或胃底静脉曲张,超声或CT等影像学检查提示肝脏呈肝硬化改变,肝脏表面不规则,肝实质颗粒或结节状、伴或不伴脾肿大和HBeAg阳性者血清HBV DNA>2×103IU/ml或HBeAg阴性者血清HBV DNA>2×102IU/ml。排除标准:有失代偿期肝硬化的表现、对恩替卡韦、PEG-IFNα-2a或胸腺素过敏者、合并HCV或HIV感染、酒精性肝病、自身免疫性肝病等其他慢性肝病、血清AFP>100 ng/ml且影像学检查提示肝脏占位可能、合并其他恶性肿瘤、心、肺、脑、肾等严重疾病、孕妇或哺乳期妇女。研究方案遵循赫尔辛基宣言和相关研究法规,并通过医院医学伦理委员会审议及批准,患者签署知情同意书。
1.2 治疗方法 将患者分成三组,分别给予恩替卡韦分散片(江苏正大天晴药业股份有限公司)0.5 mg口服,1次/d或在口服恩替卡韦分散片26 w后,给予PEG-IFNα-2a(上海罗氏制药有限公司)180 μg皮下注射,1次/w,连续52 w。之后继续口服恩替卡韦至104 w或在口服恩替卡韦分散片26 w后,给予胸腺素(意大利赛生制药有限公司)1.6 mg皮下注射,2次/w,连续52 w,之后继续口服恩替卡韦至104 w。
1.3 检测与检查 使用ARCHITECT-i2000SR全自动化学发光免疫分析仪检测HBV血清标志物(美国Abbott公司);使用 COBAS TaqMan HBV Test实时定量检测血清HBV DNA(美国罗氏公司);使用Cobas E702全自动生化分析仪检测血生化指标(美国罗氏公司);使用FibroTouch检测肝脏硬度值(LSM,无锡海斯凯尔医学技术有限公司);使用东芝Apilo500超声诊断仪行腹部超声检查。
1.4 统计学分析 应用SPSS 22.0软件进行统计分析,计量资料以(±s)表示,组间比较采用 t检验,多组均数的比较采用单因素方差分析,样本均数之间的两两比较采用LSD法,计数资料采用x2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 三组基线资料比较 恩替卡韦联合PEGIFNα-2a治疗组血清HBeAg阳性率显著高于恩替卡韦联合胸腺素治疗组(x2=6.455,P=0.011),其他方面组间差异无统计学意义(P>0.05,表1)。
2.2 三组血清HBV DNA水平变化情况 治疗前,恩替卡韦组、恩替卡韦联合PEG-IFNα-2a组和恩替卡韦联合胸腺素组患者血清HBV DNA水平分别为【(5.6±1.7)IU/ml、(5.8±1.3)IU/ml和(6.1±1.9)IU/ml,P>0.05】;三组患者血清 HBV DNA 定量水平均在26周内迅速下降且低于检测下限(检测下限是20 IU/ml),随访至104周时无明显反弹(图1)。
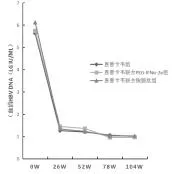
图1 三组血清HBV DNA水平变化
表1 三组基线资料(%,±s)比较
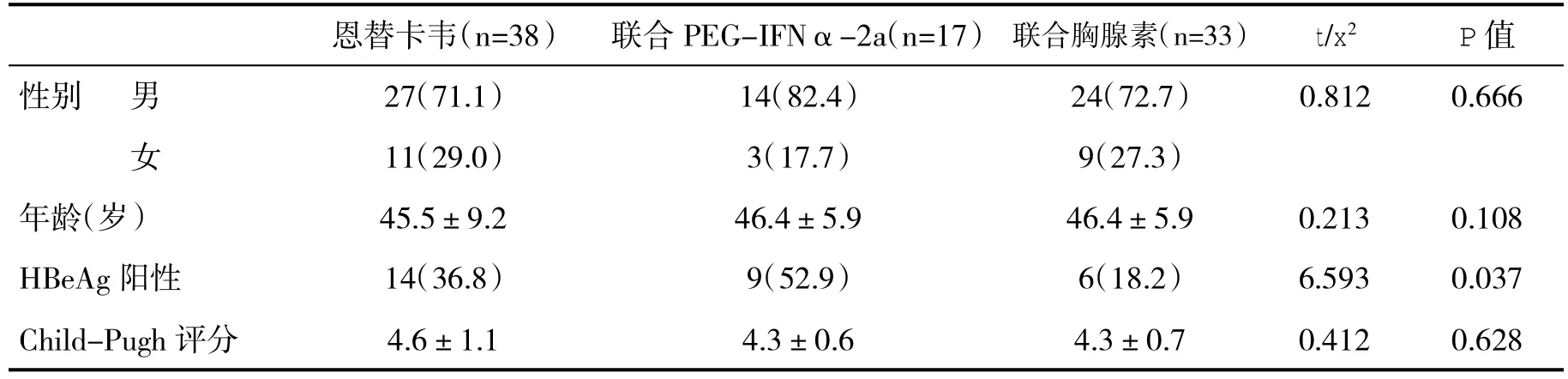
表1 三组基线资料(%,±s)比较
恩替卡韦(n=38) 联合PEG-IFNα-2a(n=17) 联合胸腺素(n=33) t/x2 P值性别 男 27(71.1) 14(82.4) 24(72.7) 0.812 0.666女11(29.0) 3(17.7) 9(27.3)年龄(岁) 45.5±9.2 46.4±5.9 46.4±5.9 0.213 0.108 HBeAg 阳性 14(36.8) 9(52.9) 6(18.2) 6.593 0.037 Child-Pugh 评分 4.6±1.1 4.3±0.6 4.3±0.7 0.412 0.628
2.3 肝功能和肝脏硬度值变化情况 三组患者治疗104w末,血清TBIL水平及MELD评分均无明显变化(P>0.05);单药组和联合胸腺素用药组血清ALB水平治疗104 w末较治疗前显著升高,有统计学差异(P<0.05);三组患者在治疗104 w末INR比值均较治疗前明显下降,有统计学差异(P<0.05)(表2)。利用肝脏弹性值评价肝脏硬化程度,三组均在治疗104w末肝脏弹性值较治疗前下降,但是只有联合胸腺素用药组有统计学意义(P<0.05),其余变化无统计学差异。
2.4 HBeAg转阴情况 在治疗结束时,恩替卡韦组发生HBeAg血清学转换1例,恩替卡韦联合PEGIFNα-2a组发生HBeAg血清学转换2例,恩替卡韦联合胸腺素组未发生HBeAg血清学转换病例。
表2 三组肝功能指标和肝脏硬度值(±s)比较

表2 三组肝功能指标和肝脏硬度值(±s)比较
与联合干扰素治疗组比,①P<0.05
例数 TBIL(μmol/L) ALB(g/L) INR MELD评分 LSM(kPa)恩替卡韦 治疗前 38 23.4±14.7 43.1±5.4 1.2±0.2 20.0±2.9 16.0±9.5治疗 104 w 24.3±9.3① 45.9±2.9 1.0±0.1 19.9±2.0 11.0±8.5联合IFNα 治疗前 17 15.5±4.5 45.1±4.1 1.1±0.2 18.5±3.1 16.5±5.9治疗 104 w 18.3±6.7 45.9±4.2 0.9±0.1 17.4±2.7 9.4±5.0联合胸腺素 治疗前 33 18.1±6.9 43.0±4.0 1.2±0.1 19.4±2.9 17.6±8.6治疗104 w 24.3±14.3① 45.8±3.4 0.9±0.1 16.0±3.3 11.5±5.6
3 讨论
恩替卡韦已广泛应用于慢性乙型肝炎及肝硬化患者的治疗,但是对于单一用药治疗与联合治疗的报道结果还很不一致。本研究结果显示,恩替卡韦单药治疗与恩替卡韦联合PEG-IFNα-2a或联合胸腺素治疗后,总体效果无显著区别,血清HBV DNA呈下降趋势,在前26周明显,以后进入低水平期,说明对代偿期肝硬化患者使用恩替卡韦单药或者是恩替卡韦联合PEG-IFNα-2a或联合胸腺素治疗方案均能在短时间内降低乙型肝炎病毒载量,控制HBV复制活动,改善肝功能,同时持续治疗能够使HBV DNA水平维持在较低的稳定状态。恩替卡韦单药治疗与联合PEG-IFNα-2a或联合胸腺素对代偿期乙型肝炎肝硬化患者血清HBeAg影响较小,三组研究对象在治疗104周末血清TBIL水平及MELD评分均无明显变化,血清ALB水平均显著升高,INR和肝脏硬度值均下降,但是三组肝功能指标及肝脏弹性值在同一访视点均无统计学差异,表明应用单药还是联合用药在改善肝功能及肝纤维化程度方面无明显疗效差异。
尤红[9]等研究恩替卡韦对代偿期肝硬化2年抗病毒疗效,发现与对照组比,血清HBV DNA载量的动态变化无统计学差异,与本文研究结果一致。张洪玲[10]等研究报道恩替卡韦联合胸腺素治疗代偿期乙型肝炎肝硬化52 w疗效,结果显示联合胸腺素能够有效抑制HBV DNA复制,改善肝纤维化程度,与本文观察结果一致。研究报道[11],胸腺素联合恩替卡韦治疗HBeAg阳性代偿期乙型肝炎肝硬化患者,HBeAg转阴率显著高于对照组,差异有统计学意义,且胸腺素联合恩替卡韦组与恩替卡韦单药组的药物不良反应发生率分别为7.5%和17.5%,差异有统计学意义。本文研究显示三种抗病毒治疗方案治疗患者血清HBeAg转阴率无显著差别,可能与纳入受试患者治疗前HBeAg阳性率不高有关。通过在治疗第3个月末监测病毒学应答来评估恩替卡韦疗法的疗效,并试图找出基线因素是否有助于预测代偿性乙型肝炎肝硬化患者的疗效,结果显示基线HBV DNA,HBeAg阴性和ALT水平是预测第3个月病毒学应答的独立因素[12]。经多元回归分析显示,在该肝硬化队列中,早在第3个月时血清HBV DNA水平就是预测完全病毒学应答的唯一参数。重新评估联合胸腺肽α1治疗乙型肝炎患者的疗效试验表明,使用胸腺肽α1联合高效的核苷(酸)类似物在抑制HBV复制的同时,对清除HBsAg和HBeAg也有效,但是该研究是建立在慢性乙型肝炎队列的基础上[13]。有人对自1993年至2017年1月有关慢性乙型肝炎和肝硬化患者抗病毒治疗的相关文献进行了综述,应用NAs可降低失代偿期肝硬化和HCC的发病率,通过成功的病毒抑制可以实现组织学改善和纤维化消退,联合PEG-IFNα-2a是治疗代偿期肝硬化患者一种良好的治疗选择[14]。然而,干扰素治疗在失代偿期肝硬化患者是禁忌的,目前的结果尚不足以证明HCC发生减少了。
NAs和PEG-IFN-α是目前应用最广且安全性相对优异的两类治疗药物,NAs通过抑制病毒逆转录酶有效抑制HBV复制至无法检测的水平,PEG-IFN-α具有双重作用,直接抑制病毒复制和间接增强宿主抗病毒免疫力[15]。在服用NAs停止治疗后频繁复发或再次激活病毒感染导致患者依从性差而需要无限期反复用药,主要是由于HBV共价闭合环状DNA(cccDNA)的活性转录模板的持续存在,而PEG-IFN-α耐受性较差且有频繁的副作用,因此要达到长期控制或治愈HBV的目的,两者都不是最佳的[16]。胸腺素是人工合成的具有免疫功能调节的多肽,通过髓样和浆细胞样树突状细胞中的Toll样受体起作用,导致信号通路的激活和刺激以促进免疫细胞亚群的分化和增殖、免疫相关细胞因子合成和分泌,促进HBV的清除[17,18]。抗HBV治疗的最大挑战是清除受感染肝细胞核中的高度耐药的HBV cccDNA,并能逃避免疫应答监测,未来的治疗需要针对HBV cccDNA有效清除HBV,并预防 HBV 慢性感染引起的 HCC[5,19,20]。
因此,针对代偿期乙型肝炎肝硬化患者,临床治疗上可以优先选择恩替卡韦单药治疗,既可避免因PEG-IFNα-2α和胸腺素引起的不良反应,同时减少患者的经济负担。但是,本研究未能充分比较三种方案持续抗病毒治疗在改善代偿期乙型肝炎肝硬化患者肝纤维化程度、免疫调节功能、药物不良反应等方面是否有差别,这些尚需要进一步明确,以及长期治疗在抗病毒方面是否有疗效的差异等,仍然需要进一步随访观察。