体外培养乳牙牙髓干细胞向血管内皮细胞定向分化的实验研究*
2019-01-18刘琼文军吴小明钱虹
刘琼,文军 ,吴小明,钱虹
[南方医科大学口腔医院(广东省口腔医院)1.儿童口腔科,2.牙体牙髓科,广东 广州 510280]
近年来提出的干细胞治疗是指利用干细胞来替代、修复,并且加强受损组织与器官的生物学功能,最终达到临床组织再生或修复的目的[1]。干细胞是一群具有自我更新和多向分化潜能的细胞,在组织器官生长、发育及损伤修复过程中发挥重要作用。许多组织器官的更新是通过干细胞来维持的。迄今为止,在诸多组织器官中都发现了成体干细胞,如骨骼肌、脂肪、神经、软骨滑膜团等[2]。在干细胞治疗中,种子细胞是组织工程研究中的核心问题之一。
迄今分离到的6种牙源性干细胞包括:乳牙牙髓干细胞、成人牙髓干细胞、根尖乳头干细胞、牙周膜干细胞、根尖乳头干细胞及牙囊细胞[3]。本研究中用于研究的乳牙牙髓干细胞起源于神经嵴外胚层,当其移动迁徙到颌面部后形成了外胚间充质[4]。乳牙牙髓干细胞的首次分离是MIURA等[5]在2003年完成的,其具有自我更新和高度增殖的特性,并且具有间充质干细胞的典型生物学特征。诸多文献报道骨髓间充质干细胞和内皮细胞具有一定的相关性,且具有向内皮细胞分化的潜能[6]。既往研究表明,乳牙牙髓干细胞可以在体外完成向神经细胞、成骨细胞、脂肪细胞、软骨细胞及血管内皮细胞的分化[7],诱导物决定其分化方向。在不同诱导物提供的具有不同细胞外基质、转录因子、生长因子,以及信号分子的微环境中,牙髓干细胞可根据不同条件分化为不同类型的组织细胞[8]。本研究选取的乳牙牙髓干细胞具有以下优点:①乳牙牙髓干细胞的增殖活性高于成人牙髓干细胞及其他牙源性干细胞[9];②取材容易,可实现无创取材;③降低医疗成本;④可在短期内获得组织工程需要的细胞量[10];⑤患儿及家长易接受,所受伦理争议较少;⑥具有较低的凋亡性和衰老性,有研究表明其第10代细胞仍可保持细胞形态[11];⑦可用于自体移植,理论上可有效避免免疫排斥反应[12];⑧用于自体移植时,可降低交叉感染的风险[13]。
理论上牙髓干细胞可以分化为血管内皮细胞[14]。牙髓中的血管系统可以通过提供营养物质及运输代谢废物质来维持牙髓代谢的平衡,目前血管移植技术已广泛应用于临床,在肿瘤、创伤、心血管疾病、显微外科手术及器官移植中都有着重要地位[15]。在血管性疾病的组织工程学研究中,自体血管移植虽然具有组织相容性好、无免疫排异反应等优势,是最为理想的血管移植物,但是自体血管移植具有一定的局限性[16]。血管内皮细胞是一类具有诸多生理功能的细胞,包括维持机体内环境稳定、维持正常免疫功能等;此外,其在心脑血管疾病的发生、发展等方面也具有重要作用[17]。若血管内皮细胞发生功能障碍,则可能引起血管痉挛、血管增生、血管异常收缩及血栓形成等典型的病理生理变化[18]。血管内皮细胞可以移植用于修复血管内膜及重建血管网[19],血管内皮细胞是血管组织工程化的核心,但由于其来源有限且增殖能力不强,在临床应用中仍存在一定阻碍。故具有上述优点的乳牙牙髓干细胞如果能在体外诱导分化为血管内皮细胞,对其在细胞及组织工程学中的应用具有重要意义。
1 资料与方法
1.1 一般资料
选取2015年7月—2017年9月南方医科大学口腔医院牙科29例健康儿童的滞留乳牙。充分消毒牙体周围组织后拔牙,置于预冷的含有高倍双抗的α-DMEM培养基转运到实验室,在4 h内进行原代提取。纳入标准:①所有研究对象及其家属对本研究知情同意,并签署知情同意书;②所有研究对象年龄在6~10岁。排除标准:①牙根吸收>1/2乳前牙标本;②存在牙体牙髓疾病的标本;③存在遗传性疾病的研究对象;④存在严重呼吸、循环、消化及其他系统疾病的研究对象。本研究经本院医学伦理委员会批准。
1.2 主要试剂与仪器
倒置相差显微镜(日本Olympus公司),细胞培养孵箱(美国Thermo Scientific公司),Multiskan Mk3酶标仪(美国Thermo公司),水浴箱(上海中新仪器设备公司),SWCJ-1FD型净化工作台(苏州净化设备厂),EPICS-XL型流式细胞仪(美国Beckman Corlter公司),胎牛血清(fatal bovine serun, FBS)(美国Gibco公司),达尔伯克改良伊格尔培养基(Dulbecco's modified eagle's medium,DMEM)(美国Sigma公司),胰蛋白酶(美国Gibco公司),双抗(美国Hyclone公司),基质蛋白酶1单克隆抗体(stromal cell antigen-1,Stro-1)(美国Santa Cruz公司),Vimentin单克隆抗体(美国Santa Cruz公司),包被抗小鼠IgM Micro Beads的免疫磁珠试剂盒(德国Miltenyi Biotec公司),人血管来源内皮细胞(南京凯基生物有限公司)。
1.3 方法
1.3.1 原代细胞提取 参考文献的经典方法[20],将标本置入超净台中用磷酸盐缓冲溶液(PBS)反复冲洗,采用拔髓针拔取出牙髓组织。完全培养液浸润下剪碎,将终浓度为3 g/L的Collagenase Type I(美国Gibco公司)和4 g/L的Dispase(美国Gibco公司)混合,在37℃水浴中消化1 h牙髓组织,1 000 r/min离心5 min,弃上清液,加入培养液混匀沉淀,轻柔吹打,用70μm的滤网过滤后获得细胞悬液,加入含20% FBS的α-DMEM培养液接种,置于37℃、5%二氧化碳CO2敷箱中培养。当达到生长融合时以1∶2的比例进行细胞传代。
1.3.2 乳牙牙髓干细胞的分选 选取生长状态良好的第3代乳牙牙髓细胞,胰酶消化制成细胞悬液后过30μm细胞筛,以含1% FBS的FBS重悬,调整细胞密度为1×106个/ml。向细胞悬液中加入FcR封闭液,置于4℃中孵育20 min。再加入Stro-1单克隆抗体),置于4℃中孵育1 h。用含0.1% FBS的PBS清洗3次后过30μm细胞筛。加入包被抗小鼠IgM MicroBeads的免疫磁珠,其是一种用于牙髓干细胞磁性标记的与Stro-1单克隆抗体相特异性偶联的超顺磁化微粒,严格按照试剂盒说明书进行分选操作,收集从分选柱流出的乳牙牙髓细胞置于37℃、5%CO2敷箱中培养以供后续实验使用。
1.3.3 乳牙牙髓干细胞的鉴定 采用免疫组织化学染色法对分选出的乳牙牙髓干细胞进行鉴定。将分选后的乳牙牙髓干细胞用PBS清洗3遍,取95%乙醇固定20 min,用0.3%过氧化氢H2O2灭活内源性过氧化物酶10 min。用10% FBS封闭20 min,选取Vimentin单克隆抗体及Stro-1单克隆抗体作为其表面标记物,根据不同实验将一抗室温孵育2 h,之后严格按照试剂盒说明书进行染色。
1.3.4 乳牙牙髓干细胞向血管内皮细胞的定向分化 血管内皮细胞向诱导:选取分选后生长状态良好的乳牙牙髓细胞,调整密度为1×105个/孔,采用常规培养液将其接种到6孔板上,待乳牙牙髓细胞完全贴壁融合后,将培养液更换为血管内皮细胞向诱导培养基,更换培养液1次/2 d。
1.3.5 血管内皮细胞定向诱导培养基成分[21]α-DMEM培养基:2% FBS,50 μg/L的血管内皮生长因子(VEGF),10 μg/L的bFGF,0.1 mg/L的地塞米松,2 g/L的牛血清白蛋白,1%的抗生素。
1.3.6 乳牙牙髓干细胞及血管内皮细胞定向诱导后的细胞的镜下形态观察 分别取第3代的乳牙牙髓干细胞及血管内皮细胞定向诱导14 d后的细胞置于倒置显微镜下观察其形态结构并拍照留存。
1.3.7 乳牙牙髓干细胞及血管内皮细胞定向诱导后的细胞血管生成实验 分别取第3代的乳牙牙髓干细胞及血管内皮细胞向诱导14 d后的细胞,在4℃冰上融化Matrigel胶(美国Sigma公司),50 μl Matrigel胶包被96孔板,注意不要有气泡,37℃、含5% CO2饱和湿度的敷箱中孵育培养30 min,加入1×105个/孔的细胞悬液,在倒置显微镜下观察其体外血管生成过程。
1.3.8 乳牙牙髓干细胞及血管内皮细胞定向诱导后的细胞免疫表型鉴定 采用免疫组织化学染色法来鉴定细胞的免疫表型,具体步骤如下:①分别取第3代的乳牙牙髓干细胞及血管内皮细胞向诱导2周后的细胞接种于预先已经置入玻片的12孔板上,待细胞贴壁融合1 h后,向12孔板内加入常规培养液;②24 h后取出玻片,PBS冲洗后采用甲醇固定20 min,再用PBS充分清洗;③加入兔抗人Ⅷ因子相关抗原抗体,37℃、5% CO2敷箱中培养1 h,PBS冲洗3次;④加入辣根过氧化物酶标识的羊抗兔二抗,37℃、5%CO2敷箱中培养30 min,PBS冲洗3次;⑤DAB显色5 min,蒸馏水冲洗10 min,苏木精衬染2 min;⑥采用盐酸复染,吹干,并用中性树胶封片;⑦在显微镜下进行对比观察并拍照存档。
另取一组人血管来源内皮细胞,采用相同的方法制作切片作为参照组。计数免疫组织化学染色阳性细胞所占百分率。每组细胞随机观察切片5个不同视野,取5个视野的平均值,根据细胞着色判断。①阴性:不着色;②弱阳性:浅黄色;③中等阳性:中黄色或棕色且无背景着色,或深棕色,但背景色为浅棕色;④强阳性:深棕色或棕褐色,且无背景着色。阳性表达率(%)=阳性(弱阳性+阳性+强阳性)表达例数/总例数×100%。
1.4 统计学方法
数据分析采用SPSS 17.0统计软件,计量资料以均数±标准差(±s)表示,比较用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 人乳牙牙髓干细胞的鉴定结果
人乳牙牙髓干细胞免疫组织化学染色可见波形蛋白染色和Stro-1染色呈强阳性。见图1、2。
2.2 镜下形态观察结果
镜下未经诱导的乳牙牙髓干细胞呈长梭形,少数为多角形椭圆形,胞体丰满,体积较小(见图3A)。经过血管内皮定向诱导14 d后的乳牙牙髓干细胞呈多角形或梭形相互嵌合排列,呈典型的鹅卵石或铺路石样,细胞间相互连接紧密(见图3B)。

图1 人乳牙牙髓干细胞表达 (波形蛋白染色×10)

图2 人乳牙牙髓干细胞表达 (Stro-1染色×40)
2.3 血管生成实验结果
经过血管内皮定向诱导14 d后的乳牙牙髓干细胞接种于基质胶后,6 h后在镜下可呈现明显的血管样结构(见图4A)。而未经诱导的乳牙牙髓干细胞在血管生成实验中,接种于基质胶后6 h细胞集聚成团状,不能形成血管样结构(见图4B)。
2.4 免疫表型鉴定结果
乳牙牙髓干细胞血管内皮细胞定向诱导后的细胞染色阳性率为(80.377±4.489)%,与作为参照组的人血管来源内皮细胞的细胞染色阳性率(82.191±5.012)%比较,差异无统计学意义(t=0.645,P=0.479)。
免疫组织化学染色结果显示,乳牙牙髓干细胞血管内皮细胞定向诱导14 d后其细胞表型发生变化,倒置显微镜下可见胞浆内存在棕褐色沉淀,其中核周最为明显(见图5A);未经诱导的乳牙牙髓干细胞细胞因子相关抗原染色呈阴性(见图5B)。

图4 血管生成实验结果 (×10)
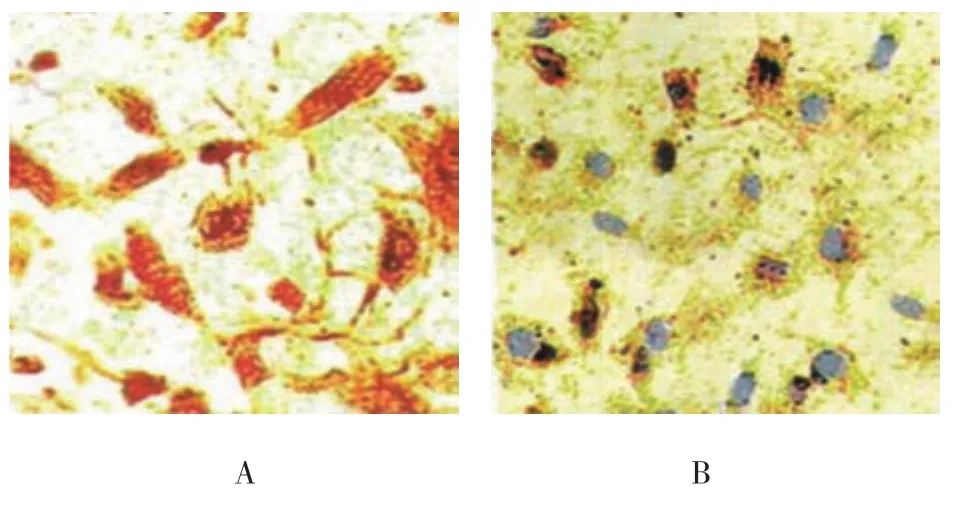
图5 免疫表型鉴定结果 (×10)
3 讨论
乳牙牙髓组织中含有牙本质细胞、未分化间充质细胞,以及成纤维细胞等多种细胞成分,因此想要分离得到纯化的乳牙牙髓干细胞进行后续实验,就需要从这些混合细胞中分离出所需要的细胞。目前针对干细胞的分离方法主要包括流式细胞仪分选法、单细胞克隆法、密度梯度离心法、贴壁筛选法、免疫磁珠分选法等[22]。免疫磁珠分选法是指将偶联在抗体上的磁珠标记在细胞上,利用抗体对细胞表面抗原的特异性识别,在磁场的作用下分选需要的细胞,其具有细胞处理量大、分离纯度高、分选后细胞活力好等优点[23]。本研究采用此法成功分离出纯化的乳牙牙髓干细胞。
在国外研究中,KARBANOVÁ等[24]选择20 μg/L质量浓度的VEGF诱导牙髓干细胞,7 d后检测到血管内皮细胞标志物vWF的表达。ISHKITIEV等[25]发现,乳牙牙髓干细胞形成的微血管可以与宿主的脉管系统相吻合。SAKAI等[26]发现,乳牙牙髓干细胞在VEGF的作用下可表达血管内皮细胞特有的表面标志物。
但在这一领域国内相关研究数量甚少,针对乳牙牙髓干细胞的分化多为成骨以及成脂向的研究。血管内皮细胞呈扁平多角形,边界清楚,典型形态为倒置显微镜下呈鹅卵石或铺路石样。本研究中的诱导培养基条件为:α-DMEM培养基,2% FBS,0.1μmol/L地塞米松,50μg/L VEGF,10μg/L bFGF,2 g/L牛血清白蛋白,1%抗生素,在此条件下对乳牙牙髓干细胞进行血管向诱导并分别对乳牙牙髓干细胞及血管内皮细胞定向诱导后的细胞的镜下形态观察,进行血管生成实验以及免疫表型鉴定。结果表明镜下未经诱导的乳牙牙髓干细胞镜下呈长梭形,少数为多角形椭圆形,胞体丰满,体积较小,与既往研究中报道的相一致[27]。经过血管内皮定向诱导14 d后的乳牙牙髓干细胞,呈多角形或梭形相互嵌合排列,呈典型的鹅卵石或铺路石样,细胞间相互连接紧密,说明其已经具有血管内皮细胞的形态特征。在血管生成实验中,未经诱导的乳牙牙髓干细胞不能形成血管样结构,而经过血管内皮定向诱导14 d后的乳牙牙髓干细胞可呈现明显的血管样结构,表明经过诱导后的细胞具有了血管内皮细胞的血管生成这项生物学功能。在免疫表型鉴定的研究中,未经诱导的乳牙牙髓干细胞细胞因子相关抗原染色呈阴性,而乳牙牙髓干细胞血管内皮细胞定向诱导后的细胞的细胞染色阳性率为(80.377±4.489)%,说明经过诱导后的细胞具有了血管内皮细胞的免疫表型。以上结果证实在本研究中的诱导条件下,成功将乳牙牙髓干细胞诱导为血管内皮细胞,证明乳牙牙髓干细胞具有血管生成的分化能力。
虽然在国内外已经有很多研究关于牙髓干细胞的血管生成研究,但在国内针对牙髓干细胞多为成骨研究,针对血管生成领域仍属于摸索研究阶段。在本研究的基础上,本课题组可进行血管生成后续相关的研究,如分化后的细胞人乳牙牙髓干细胞在牙科材料学上的应用等,牙髓干细胞的血管生成这一基础性研究为明确牙髓干细胞的特性特点并使其进一步得到实际应用奠定了基础。目前尚有以下几点问题待进一步研究解决:一是诱导乳牙牙髓干细胞血管生成的最佳VEGF浓度尚待探索,是否存在优于本研究方案的诱导培养基条件;二是诱导后的血管内皮细胞在组织工程中实际应用是否可达到预期的效果。随着对乳牙牙髓干细胞向血管内皮细胞诱导分化的深入研究,并建立起乳牙牙髓干细胞分离培养的统一标准,乳牙牙髓干细胞有可能成为血管生成的理想种子细胞。
