颞骨放射性骨坏死行人工耳蜗植入的经验分析
2019-01-14赖彦冰陈抗松谭玲梅刘振林枫虞幼军
赖彦冰陈抗松 谭玲梅刘振林枫虞幼军*
1佛山市第一人民医院耳侧颅底外科
2广东省听觉与平衡医学工程技术研究开发中心
人工耳蜗植入(cochlear implantation,CI)是重度/极重度感音神经性聋患者的重要康复手段之一。鼻咽癌(nasopharyngeal carcinoma,NPC)患者接受头颈部放射性治疗后,颞骨放射性骨坏死(osteoradionecrosis,ORN)和听力损失是常见的并发症。颞骨ORN的临床症状常见反复或持续性耳漏、耳痛、耳闷,不同程度的听力下降,检查可见外耳道积聚痂皮,不同程度外耳道骨壁坏死、裸露,伴渗液或坏死物[1]。放射治疗后外耳道骨坏死可能导致电极裸露,中耳反复感染的环境可能因电极植入致内耳感染,以上因素可能影响经典人工耳蜗植入手术的远期疗效,故我们对有鼻咽癌放射治疗病史而需人工耳蜗植入的患者采用了岩骨次全切除术(subtotal petrosectomy,STP)联合人工耳蜗植入术(CI)这一手术方法。
1 手术技巧
在过去,人工耳蜗植入受到某些中耳病理和解剖变异的限制。如果中耳有感染,或中耳与颅内相通,人工耳蜗植入是被禁止的,但利用岩骨次全切除技术,通过将鼓室乳突与外部环境隔离,是可以安全的植入人工耳蜗的[2]。岩骨次全切除术(STP)联合人工耳蜗植入(CI)已经得到越来越多学者的肯定及应用[3-5],是治疗复杂人工耳蜗植入的一种有效替代方法。颞骨ORN出现中耳反复感染,骨质渐进性受到侵犯腐蚀,阿姆斯特丹学术医疗中心的研究结果[6]显示,岩骨次全切除术加外耳道及咽鼓管封闭能很好的切断中耳感染源,治愈率高,推荐作为颞骨ORN的手术治疗方案。我们对该技术的一些细节进行改进并进一步探讨。
皮肤切口:耳后皮肤切口,距耳后沟约1cm,上与耳颅角水平持平,绕耳后,到达乳突尖后方,略向后下延长至胸锁乳突肌表面。(如图1 a)
制作肌骨膜瓣:制作基于前方带蒂的耳后肌骨膜瓣,预设耳后肌骨膜瓣长度向前翻转后能覆盖外耳道口(如图1 b),蒂部上方位于颞线水平,下方到达外耳道下壁。
STP:在开放式乳突根治[7]的基础上,术中判断放射性骨坏死的范围,可以扩大范围切除包括颈内动脉区域、颈静脉球区域、迷路间气房及上鼓室前间隙内侧气房,解剖面神经[8]。如果术中所见,放射性骨坏死范围局限于乳突气房及中耳,在确保彻底切除感染的腐骨的情况下,以上解剖区域结构可保留(如图1 c)。使用游离肌瓣碎块及骨皮质填塞咽鼓管口。外翻缝合外耳道口残端。在鼓骨前壁钻孔,向前翻转耳后肌骨膜瓣,缝扎固定于鼓骨前壁,确保覆盖外耳道口残端,作为第二层加强封闭外耳道口。
制作植入体骨槽:取头夹肌及部分胸锁乳突肌作为游离肌瓣备用。在顶切迹区域分离头皮及皮下组织,向后上延长切口,确保足够的皮下组织及肌瓣完全覆盖人工耳蜗接收/刺激器前端部分,切开皮下组织,向后剥离头皮,按标记距离磨出植入体骨槽。
人工耳蜗植入:放好植入体,行耳蜗开窗或开放圆窗龛,将人工耳蜗电极植入耳蜗鼓阶(如图1 d)。盘好电极线贴附于术腔内侧骨壁(如图1 e),将游离肌瓣碎块逐渐封闭耳蜗开窗或圆窗、鼓室及整个岩骨术腔(如图1 f)。注入生物蛋白胶封闭组织腔隙。病例分析
研究纳入了9例患者,进行STP联合CI,观察术后并发症,并随访听力康复效果。人工耳蜗品牌为诺尔康。参数如下:电极阵列长度20.5mm,电极点数24。表1总结了所有病例的情况。

图1 a显示皮肤切口范围Fig.1 a Incision of the skin
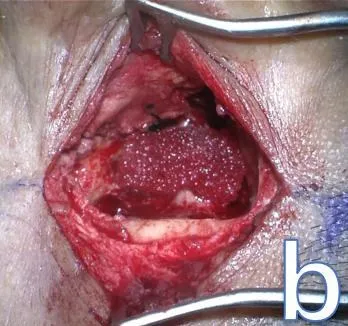
图1 b显示肌骨膜瓣向前翻转作为第二层封闭外耳道Fig.1 b Asecond layer of closure is achieved by turning the retroauricular fascial flap.
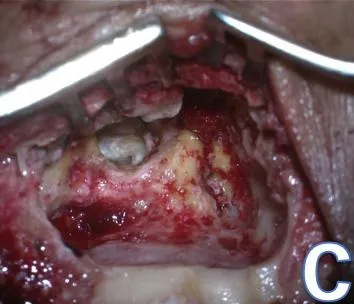
图1 c岩骨次全切除术术腔包括切除感染的腐骨Fig.1 c Subtoal petrosectomy includes complete exenteration of rotten bone

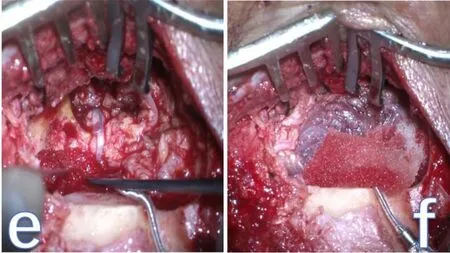
图1 e/图1 f显示人工耳蜗电极贴附骨壁及游离头夹肌肌瓣填塞术腔Fig.1 e/f The electrode is clung to the medial bone.Free muscle flap harvested from splenius capitis is to obliterate the cavity
2 结果
所有患者人工耳蜗电极为全植入。术后随访时间为4月-38月,平均为13.3月,1例在术后2周出现小并发症[4](外耳道口渗液)。5例双侧聋患者表示术后可清楚听到环境声音,并可进行日常简单交流。2例单侧聋患者表示术后能适应双耳聆听并耳鸣减轻。1例患者(病例6)表示辨别言语声比较困难。1例(病例2)拒绝使用并要求取出植入体。
3 讨论
3.1 CI在颞骨ORN所面临的问题
骨组织放射性损伤有两种病理改变,一是放射性动脉内膜炎、血管闭塞,导致营养障碍;二是直接导致骨细胞坏死,抑制成骨细胞的增值,并以纤维组织代替。放射线导致骨组织低细胞、低血管、低氧状态,抗感染能力差,“三低”状态可导致骨组织崩解或慢性不愈性创伤,骨坏死的进程加速[9-12]。颞骨由于其表面位置、皮肤覆盖薄,在鼻咽癌放射治疗中接受的射线剂量很高。中耳与上呼吸道通过咽鼓管相通,极其容易因感染出现骨坏死[12]。外耳道表面软组织覆盖较少,放射性骨坏死的风险更高,出现外耳道皮肤感染坏死并骨质裸露。此类患者联合径路术后可能会因中耳乳突感染和外耳道炎而出现外耳道后壁缺损。同时放射治疗后中耳和呼吸道黏膜功能受损,中耳感染机率增加,也可能影响到植入电极后的耳蜗。所以不建议在ORN病例中采用经典的耳后入路人工耳蜗植入技术。
Formanek等在1988年报道第一例为放射性耳聋患者成功植入人工耳蜗的病例[13]。文中考虑因耳蜗纤维化,Combi 40电极假体植入深度仅为17mm,改为植入短版的11mm Combi 40。有文献显示[20],高分辨率CT及病理学提示放射线能导致耳蜗内上皮组织萎缩、退化,纤维化甚至耳蜗骨化。我们的病例接受放射治疗年限在7-20年,选取诺尔康人工耳蜗,术中均为全植入,未出现植入困难病例。我们推测,鼻咽癌放疗后出现耳蜗纤维化或骨化的情况少见。
3.2 STP填充材料和技术要点
关于术腔填塞材料的选择,按文献报道[4,14]有以下几种材料:1、带蒂颞肌瓣,2、腹部脂肪,3、带蒂颞肌瓣联合腹部脂肪,4、游离头夹肌瓣联合腹部脂肪。术腔填塞包括两个要点:一是封闭咽鼓管口及外耳道口,阻断感染途径;二是填塞材料具备良好的抗感染能力。腹部脂肪抗感染能力较弱,容易液化感染,不建议选用。人工耳蜗植入体需要颞肌的保护,因此在颞骨放射性骨坏死的病例,我们保留颞肌,选取游离头夹肌肌瓣填塞术腔。肌瓣填塞术腔时,需注意将人工耳蜗电极线压至紧贴术腔内侧骨壁,避免发生因加压包扎和术后肌瓣萎缩牵拉电极造成电极线移位而使电极脱出。
关于术腔冲洗和伤口缝合。颞骨ORN长期反复出现感染,厌氧菌或多重耐药病原菌出现概率高,术腔填塞之前使用大量的双氧水、甲硝唑/抗生素溶液、安尔碘及生理盐水依次冲洗,加强术腔的抗菌能力。术腔填塞之后,耳廓复位,直接缝合耳后切口,注入生物蛋白胶止血并封闭组织间隙,加压包扎。如果术后出现皮下积血或积液,采用穿刺抽液及加压包扎。
本文中,除病例1术后2周出现外耳道口渗液,给予局部换药及口服抗生素治疗后痊愈,未见严重并发症,显示STP在ORN手术治疗的可靠性,确保人工耳蜗植入体及电极的安全,有效避免内耳感染,是颞骨ORN手术治疗的关键。
3.3 NPC放射治疗后听觉损伤的因素分析
在以往动物实验及人体试验的研究中,NPC放射治疗对听觉损伤的影响,在早期表现为血管内皮的炎性反应,在晚期,表现为黏膜萎缩/退化及骨组织坏死[15]。Bhide 等[16]和 Borsanyi等[17]研究发现,在放射治疗早期咽鼓管水肿以及分泌性中耳炎是早发型传导性耳聋的主要因素。外耳道狭窄、慢性中耳炎、咽鼓管退化以及耳蜗损伤是迟发型传导性聋、感音神经性聋或者混合性聋的因素。

表1 颞骨放射性骨坏死行STP同期CI的临床资料Table 1 Radiation-induced Osteonecrosis Of Temporal Bone With Cochlear Implants
在解剖定位上,有学者认为[18],鼻咽癌患者放疗后听力下降主要以内耳病变为主,并伴有中耳损伤。J Singh等通过ABR研究发现,调强放射治疗后I波潜伏期明显延长,而I~Ⅲ波、I~V波、Ⅲ~V波之间的峰间潜伏期无明显变化。Lau等人的研究进一步论证,耳蜗毛细胞损伤可能导致I波的延长,辐射诱发的中耳也会产生类似的效应。动物实验证实放射治疗存在内耳出血或膜迷路积水,Corti器内外毛细胞的缺失,血管纹萎缩、螺旋神经节退化[19]。
NPC放疗后听觉损伤的因素很多,但还没有确定耳蜗及神经放射损害的发病机制、病理生理学和随后的临床表现之间的关系[20]。孙映凤等[18]观察到,放疗结束后时间的长短是放疗后听力损失发生的相关因素,这与本文纳入的9例患者听力损失情况相当。重度/极重度混合性聋以及感音神经性聋导致患者生存质量明显下降,而CI是目前改善听力最有效的方法之一,其效果能够与未接受放射的患者相媲美[21]。
3.4 NPC放疗后单侧语后聋的人工耳蜗植入
建议对非对称听力损失和单侧聋进行干预。传统的方法为验配环绕信号助听器或佩戴软带固定骨导助听器或植入BAHA获得“双耳”听力,但这些干预并不能给患者带来真正的双侧听力。因此,CI是唯一能帮助单侧极重度语后聋患者恢复听力的选择[22]。
病例资料中有2例NPC放疗后单侧聋患者,因日常交流场合要选择好耳朝向声源,往往造成尴尬和不便。聋耳接受人工耳蜗植入后,均反应能适应双耳聆听,在噪音环境中言语理解能力提高,植入耳耳鸣症状较前缓解。目前未将单侧聋纳入人工耳蜗植入适应证,但我们的2例NPC放疗后单侧聋患者目前获得满意效果,因此更加证实CI是可能恢复双侧听力的有效方法,同时提示人工耳蜗能抑制极重度耳聋出现的耳鸣症状[23],也为NPC放疗后单侧聋的人工耳蜗植入领域迈出了重要的一步。
3.5 人工耳蜗植入与放射性脑病的关系
NPC放射性治疗不可避免的出现放射性脑损伤(也称放射性脑病)。放射性脑病大脑半球型为临床多见[24],以额颞叶损伤的症状为主,其中认知功能障碍是NPC放疗后较早出现且较为突出的症状。认知功能障碍包括听觉功能的减退,听力障碍可以作为预测认知功能是否下降的指标[25]。临床上针对以认知功能障碍为主要表现的临床疾病如阿尔茨海默病或老年痴呆,Stern[26,27]等认为建立丰富的社交关系,增加认知储备可推迟阿尔茨海默病和老年痴呆的发病。
听力损失尤其达到重度以上,患者社交能力将受到显著影响,不良的负面情绪随之出现。CI是改善重度/极重度聋患者听力的有效方法。Mo[28]等研究发现,成人语后聋患者的生存质量,在术前和术后最大的改善表现在交流、情绪控制和与朋友及家庭关系处理等方面。
我们目前进行STP联合CI的病例,8例在随访时均表示日常交流能力提高,病例9甚至可以进行会议交流。其中病例2患者可听到声音,但以为佩戴人工耳蜗能听到正常声音,怀疑产品质量,拒不配合言语康复训练。考虑耳聋时间过久和放射性脑病对植入的预期值不理解。
我们推测,提高听力或声音感知,可改善患者的认知功能,从而延缓放射性脑病的病程。但是放射性脑病患者如出现情绪障碍或严重的认知功能障碍,也会导致人工耳蜗植入术后言语训练及社交训练的困难,所以我们评估NPC放疗后人工耳蜗植入的适应证,必须考虑放射性脑病对手术效果的影响。
4 结论
岩骨次全切除术(STP)是颞骨放射性骨坏死(ORN)手术治疗的核心技术。岩骨次全切除术同期人工耳蜗植入是可行的。听力改善能够提高NPC放疗后重度/极重度聋患者言语交流能力。我们认为,提高听力或声音感知,可改善患者的认知功能,从而延缓放射性脑病的病程。其次,考虑到鼻咽癌放射性治疗后可能出现放射性脑病,将可能影响人工耳蜗植入的言语康复效果,术前应谨慎评估。
