还原剂浓度对化学还原法制备纳米锡银合金粉末颗粒生长的影响
2019-01-05王瑶马运柱刘文胜唐思危黄宇峰
王瑶,马运柱,刘文胜,唐思危,黄宇峰
还原剂浓度对化学还原法制备纳米锡银合金粉末颗粒生长的影响
王瑶,马运柱,刘文胜,唐思危,黄宇峰
(中南大学 粉末冶金国家重点实验室,长沙 410083)
采用化学共还原法制备纳米级Sn-3.5Ag(质量分数,%)合金粉末,分析粉末的微观形貌、物相组成和熔化行为,着重研究还原剂溶液的浓度对粉末粒径的影响,探究液相中颗粒形核长大机制。结果表明:还原剂浓度控制液相中颗粒形核和长大的速率,粉末平均粒径随还原剂浓度降低而增大,还原剂溶液的浓度为0.25 mol/L时粉末平均半径达到最小值约为13 nm;粉末由β-Sn和Ag3Sn两相组成,熔点约为206 ℃;还原剂浓度升高,溶液中大量金属离子用于瞬间形核从而抑制纳米颗粒的后续长大;液相中Ag3Sn优先形核生长,随着溶液中银原子的饱和度下降,粉末的物相组成转由β-Sn占主导,最终形成由Ag3Sn相和β-Sn相组成的纳米合金粉末。
化学共还原法;Sn-Ag纳米颗粒;微观形貌;合金化;形核长大
共晶锡银(Sn-3.5Ag)焊膏因其优良的润湿性能、抗蠕变性能和结合强度在电子封装领域得到广泛应用[1]。随着电子元器件向着小型化、微型化发展,以往电子封装中可忽略的溶解扩散、微区应力应变等问题变得突出[2],且高密度和超细间距的封装发展趋势对焊膏中金属粉末的粒径提出了更高的要求。传统焊膏中添加的合金粉末粒径达微米级,为了降低粉末尺寸,通常采用球磨法制备。TANG等[3]利用机械合金化法制备了Sn-Ag粉末,粉末多呈大块片层状,将粉末尺寸减小至约3 μm,其粒径仍然无法满足未来对超细间距封装的要求。纳米材料在小尺度下表现出异于寻常材料的物理和化学性能[4],代替传统焊膏中微米级金属粉末可满足超细间距封装的要求,并拓宽锡银焊膏的应用领域。杨明等[5]采用化学还原法制备纳米锡粉末,发现还原剂浓度对粉末的粒度分布和平均粒径至关重要。CHEE等[6]制备Sn-Ag纳米合金时首先还原Sn颗粒,再将其作为形核中心还原Ag颗粒,这种分步还原法所需试剂较多且实验操作较复杂,增加了成本并降低实验的可重复性。采用化学共还原法制备合金粉末,液相中难以控制的还原速率和元素间还原电势的差异对共还原过程的顺利进行提出了挑战[7],粉末颗粒的生长机理和合金化能否完成需要进行深入的研究。本文采用化学共还原法一步制备完全合金化的Sn-3.5Ag纳米粉末,通过研究还原剂浓度对Sn-Ag纳米粉末形貌及粒径分布的影响以及分析纳米颗粒的相组成和熔点,探究液相中颗粒形核长大的机制,为Sn-Ag纳米合金粉末的制备和性能研究提供理论依据。
1 实验
1.1 原料
AgNO3,阿拉丁试剂(上海)有限公司生产,纯度99.99%;SnCl2,麦克林生化科技(上海)有限公司生产,纯度99.99%;1,10-菲罗啉(phen,分子式C12H8N2∙ H2O),国药集团化学试剂有限公司生产,纯度99%;NaBH4,阿拉丁试剂(上海)有限公司生产,纯度98%。无水乙醇(EtOH),恒兴化学试剂制造(天津)有限公司生产;去离子水(DI water),采用重庆颐洋企业发展有限公司生产的AQP-10-U型超纯水机制备。
1.2 Sn-3.5Ag合金粉末制备
选用AgNO3和SnCl2提供金属银离子和锡离子,用1,10-菲罗啉作为保护剂,用NaBH4作还原剂,采用化学共还原法制备银含量(质量分数)为3.5%的纳米级Sn-3.5Ag合金粉末,选择还原剂溶液的浓度为变量进行实验。首先将3×10−5mol AgNO3,7.4×10−4mol SnCl2和3.78×10−3mol phen分别加入到3个装有20 mL无水乙醇的烧杯中;然后用去离子水配制4组还原剂溶液,NaBH4的用量为5×10−3mol,去离子水的用量分别为20,30,40和50 mL,4组溶液中NaBH4的浓度(NaBH4)分别为0.25,0.167,0.125和0.1 mol/L。将AgNO3和SnCl2溶液混合,用江苏科析仪器有限公司生产的HJ-2A数显恒温磁力搅拌器搅拌均匀,作为前驱体溶液,然后以1.5 mL/s的速率注射到NaBH4和phen的混合溶液中。为使反应充分进行,整个过程都伴随强烈的搅拌。反应结束后收集溶液,以4 500 r/min的速度离心15 min,倾倒上层液体,加入无水乙醇对离心管内及内壁附着的粉末进行超声洗涤。重复离心和乙醇超声洗涤3次后,取少量粉末均匀分散于无水乙醇中保存,以避免其进一步团聚,用胶头滴管取出适量滴至超薄碳膜上,待40 ℃烘干无水乙醇后作为透射电镜观察样品。剩余粉末40 ℃真空干燥8 h,得到锡银纳米合金粉末。
1.3 性能检测
用JEM-2100F型场发射透射电镜(TEM)对透射电镜分析样品进行微观形貌、晶格条纹观察以及衍射斑点的标定。采用瑞士布鲁克公司的Advance D8型X射线全自动衍射仪(XRD)对锡银合金粉末进行物相分析,扫描角度为5°~80°,扫描速度为4 (°)/min。用美国Nicolet6700智能型傅立叶红外光谱仪(FT-IR)对合金粉末进行表面官能团分析。用美国SDT Q600型同步热分析仪对粉末进行DSC分析,研究粉末的熔化行为。参数为:样品质量小于15 mg,Ar气氛保护,室温为起始温度,峰值温度为500 ℃,升温速率为10 ℃/min,随设备冷却。
2 结果与讨论
2.1 粉末形貌与粒径
图1和图2所示为还原剂溶液的浓度(NaBH4)分别为0.25,0.167,0.125和0.1 mol/L条件下制备的银锡合金粉末的TEM形貌与粒径分布。由图2可见,随还原剂浓度降低,银锡合金粉末的平均粒度增大,(NaBH4)分别为0.25,0.167,0.125和0.1 mol/L条件下的平均粒度分别为13,26,28和30 nm。当(NaBH4)为0.25 mol/L时,粉末粒径集中在10~15nm之间,平均粒径约为13 nm,颗粒大小不均匀,且相互粘连。(NaBH4)降低到0.167 mol/L时,颗粒的平均粒径增大至约26 nm,粒径分布为10~30 nm,团聚现象严重。当(NaBH4)为0.125 mol/L和0.1 mol/L时,粉末进一步长大,平均粒径分别为28 nm和30 nm。这是因为还原剂浓度较低时,金属离子的还原速率低,在形核阶段仅有少量晶核形成,在后续扩散长大阶段形成较大的颗粒,并且较慢的反应速率使得溶液中源源不断地出现新的小晶核,颗粒因有充足的时间和金属离子供给而长大,所以粉末粒径较大;随NaBH4浓度升高,更多电子从BH4-转移到金属离子[8],单位时间内参与反应的金属离子大量被用于瞬间形核,这些数量庞大的晶核消耗溶液中一大部分金属离子,剩下的金属离子难以维持后续纳米颗粒的长大,所以锡银合金粉末粒径减小。(NaBH4)为0.125 mol/L时,粉末颗粒虽然平均粒径增大至约28 nm,但粒径分布集中于20~25 nm之间,团聚现象得到明显改善。纳米粉末的团聚主要由生长过程中粉末的表面能和粒径分布所控制,纳米颗粒料由于比表面积大且表面能高而处于不稳定的状态,容易相互聚集达到稳定状态。因此,当(NaBH4)为0.125 mol/L时,虽然粉末颗粒尺寸较(NaBH4)为0.25 mol/L的样品明显增大,由于粉末表面相对趋于稳定,团聚现象得到缓解。另外,在粉末颗粒生长的动态过程中,主要由奥斯瓦尔德熟化效应控制团聚,小于临界形核半径的颗粒分解以供给大于临界形核半径的颗粒继续长大,溶液中存在“大吃小”的生长过程从而出现团聚,当还原剂浓度为0.125 mol/L时,由于粉末粒径分布较均匀,因此团聚现象得到缓解。最终当(NaBH4)降低到0.1 mol/L时,颗粒尺寸较(NaBH4)为0.25 mol/L的样品增大2倍,并且粒径分布达到30 nm的跨度。

图1 不同还原剂溶液浓度下制备的Sn-3.5Ag合金粉末TEM形貌
(a) 0.25 mol/L; (b) 0.167 mol/L; (c) 0.125 mol/L; (d) 0.1 mol/L
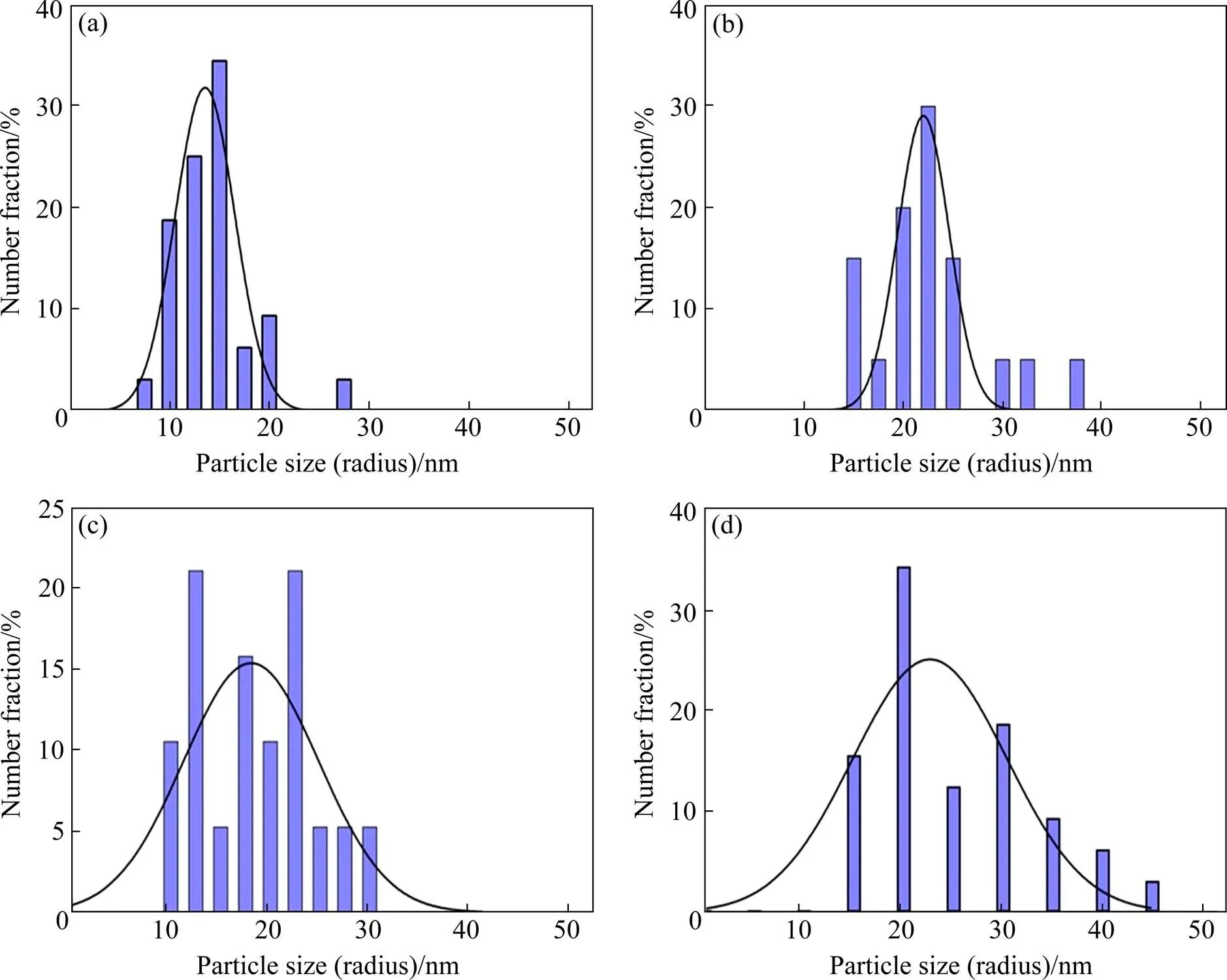
图2 不同还原剂溶液浓度下制备的Sn-3.5Ag合金粉末粒径分布
(a) 0.25 mol/L; (b) 0.167 mol/L; (c) 0.125 mol/L; (d) 0.1 mol/L
2.2 物相组成和熔点
图3所示为不同还原剂浓度下制备的银锡合金粉末XRD谱。4个样品均由晶化程度很高的β-Sn和Ag3Sn相组成,没有出现杂质相,Ag3Sn的存在说明粉末完成了良好的合金化过程。观察β-Sn和Ag3Sn的衍射峰强度发现,随还原剂浓度降低,Ag3Sn占比逐渐减少。图4所示为不同(NaBH4)下制备的粉末高分辨透射电镜图片及衍射斑点标定,证明粉末包含PDF卡片号为04-4673四方结构的β-Sn和卡片号为44-1300正交结构的Ag3Sn,与XRD结果吻合。从图4看出,粉末颗粒表面均由一层厚度约为4nm的菲罗啉保护剂非晶层包覆。在利用化学还原法制备纳米粉末时,为了得到尺寸均一的颗粒,通常需要添加保护剂,通过空间位阻效应将官能团与金属粒子配位,使得颗粒表面被一层配体外壳包裹,避免在颗粒密度较大的时候出现团聚。WANG等[9]在制备SnO2纳米棒时,发现SnCl4与phen充分混合搅拌后生成 (phen) SnCl4配体。其它研究者也提出phen通过N原子与金属配位[10]。

图3 不同还原剂溶液浓度下制备的Sn-3.5Ag合金粉末物相组成
(a) 0.25 mol/L; (b) 0.167 mol/L; (c) 0.125 mol/L; (d) 0.1 mol/L

图4 不同还原剂溶液浓度下制备的Sn-3.5Ag合金粉末高分辨透射电镜照片及衍射斑点标定
(a) 0.25 mol/L; (b) 0.167 mol/L; (c) 0.125 mol/L; (d) 0.1 mol/L
Sn-Ag二元合金相图中锡银合金(Sn-3.5Ag)共晶熔点为221.6 ℃。进一步对还原剂浓度为0.125 mol/L条件下制备的Sn-Ag粉末进行DSC分析,DSC曲线如图5所示。由图可知Sn-Ag纳米粉末的熔点约为206 ℃,低于共晶锡银块体合金的熔点。
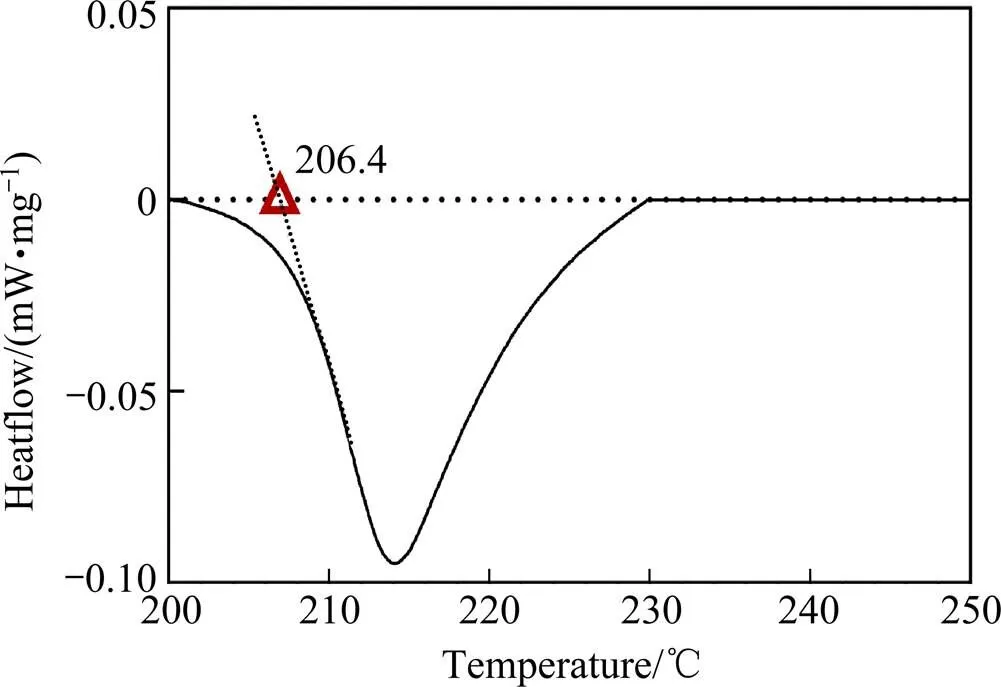
图5 Sn-3.5Ag合金粉末的DSC曲线
纳米粒子的熔点与粒子尺寸的关系可用式(1)所示的同质熔化模型[11](HMM 模型)表示:
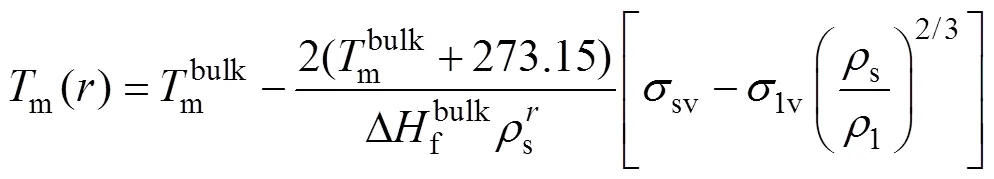
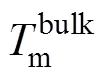
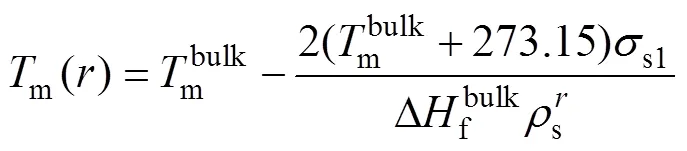
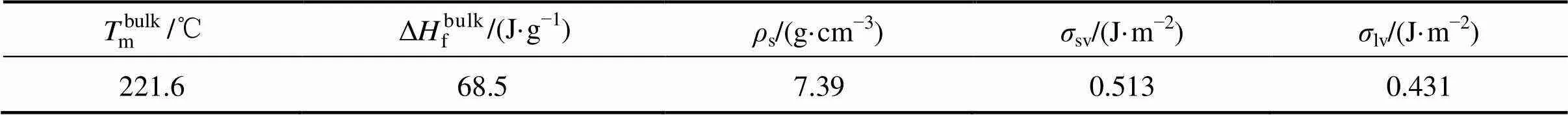
表1 用式(2)计算纳米颗粒熔点所需的参数[13]
根据式(2)的计算结果,得到图6所示纳米颗粒的熔点与粒径的关系图。上部虚线为共晶Sn-3.5Ag块体焊料的熔点,下部虚线为传统共晶SnPb块体焊料的熔点。可以看到根据HMM公式计算的纳米颗粒熔点与粒径关系曲线明显处于Sn-Ag块体熔点下方,说明本实验制备的Sn-Ag纳米粉末具有明显的熔点降低效应。
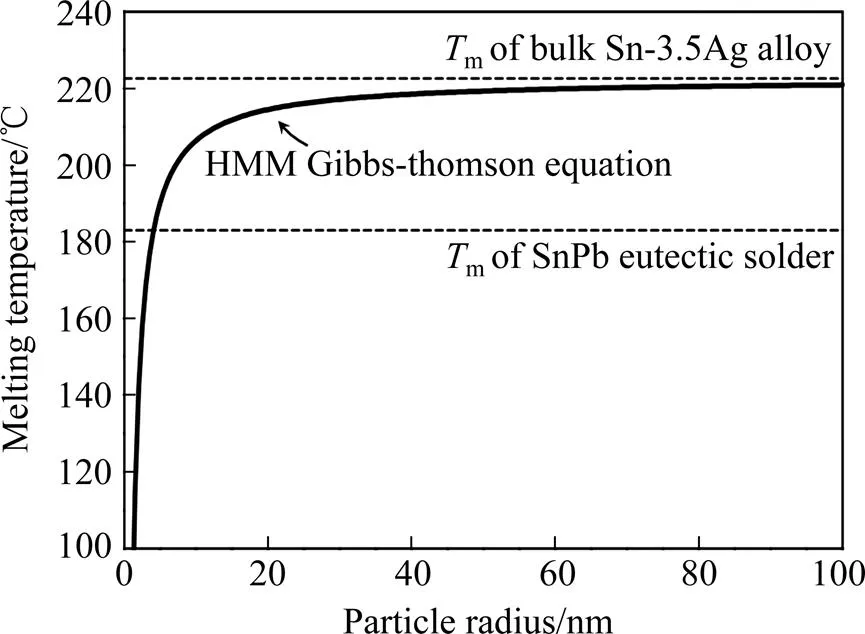
图6 Sn-3.5Ag纳米颗粒的理论计算熔点曲线
2.3 液相过程粉末形核、长大原理
共晶Sn-3.5Ag由β-Sn和Ag3Sn两相组成,这两相在共还原过程中处于竞争Sn离子的状态。氧化还原电位Ag+/Ag(0=0.799 V)高于Sn2+/Sn(0=−0.140 V)[14],因此Ag+在溶液中优先被还原(式(3)所示)。可以通过调整银和锡这2种金属的摩尔比来减小这种电势带来的差异,从而达到一步共还原的目的。SUN 等[15]在制备Au-Ag合金时,发现提高混合溶液中氧化还原电势较低的银离子浓度可获得与金离子近乎一致的形核长大速率。本实验制备的共晶粉末银含量(质量分数)仅为3.5%,对Sn的还原劣势给予了补偿。同时处于亚稳态的Sn2+也参与Ag+的还原[16],自身变成4价的锡离子(式(4)所示),然后Sn4+被还原成Sn原子(式(6),(7)所示)。活泼的锡原子与银原子结合成为合金相Ag3Sn,当银原子耗尽时,剩余的锡原子转化为稳定的β-Sn(式(5)所示)。所以反应初期以生成Ag3Sn为主,后期由于Sn和Ag原始比例差距很大,转变为以形成β-Sn为主。当溶液中反应物耗尽的时候不再出现新的晶核,在菲罗啉的保护下,反应温度下搅拌2 h后溶液中的β-Sn和Ag3Sn达到稳定平衡,不再相互转化。化学还原法制备纳米颗粒的反应模型图如图7 所示。
2Ag++2BH4−—2Ag+H2+B2H6(3)
Sn2+(aq)+2Ag+—Sn4+(aq)+2Ag (4)
Ag(reacted)+Sn(reacted)—Ag3Sn+Sn(unreacted)(5)
Sn4+(aq)+2e–—Sn2+(aq) (6)
Sn2++2BH4−—Sn+H2+B2H6(7)
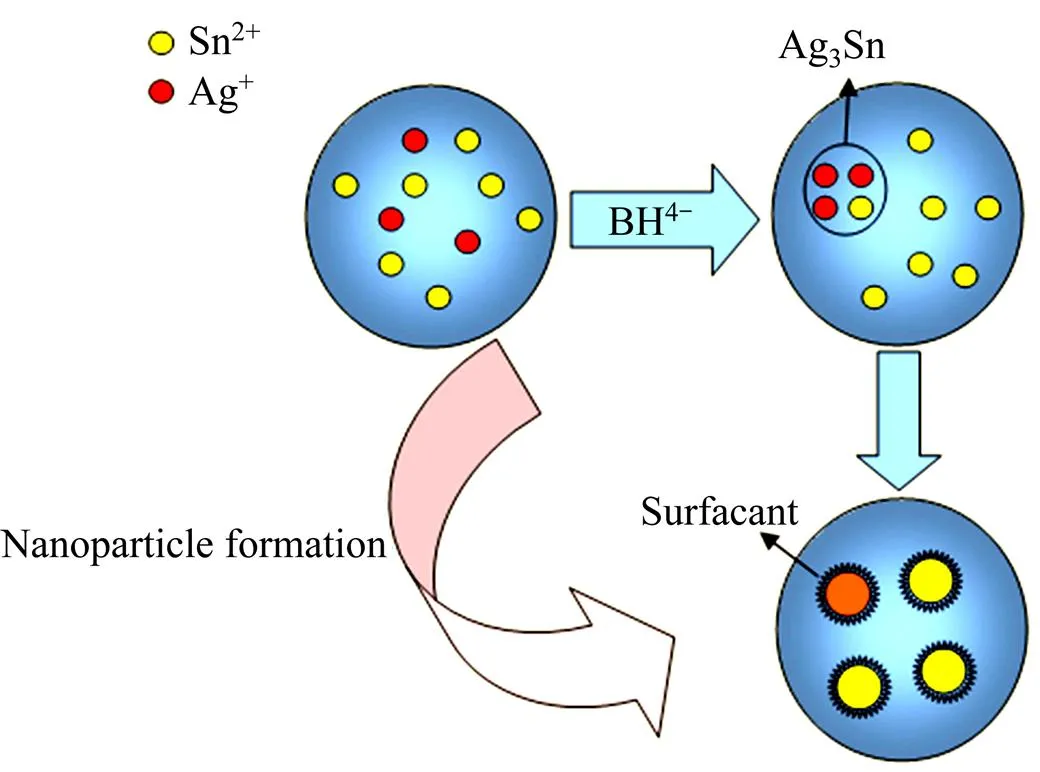
图7 化学还原法制备Sn-3.5Ag纳米颗粒的反应模型图
化学还原法可分为形核和长大2个阶段。第一阶段溶液中的自由单体迅速增加,原子开始聚集成原子簇,当金属离子被还原的速率超过消耗速率时,过饱和程度增大到可以突破能量壁垒时开始均质形核,此时溶液中形核和生长同时存在,生长过程持续到金属离子被耗尽(本实验所用还原剂为过量)。溶液中自由单体一直被消耗,当消耗速率大于被还原的速率时,金属离子浓度达不到临界形核浓度,不再出现新的晶核,然后稳定的晶核开始长大形成纳米晶,溶液中饱和度和临界形核半径的关系可用下式表示[17]。
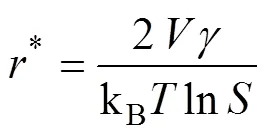
式中;*为临界形核半径;为摩尔体积;为单位表面积的表面自由能;kB为玻尔兹曼常数;为绝对温度;为饱和度。在反应初期,反应物浓度很高,使得溶液中饱和度()较大,此时临界形核半径很小,容易形成晶核(>1)。随着反应的进行,浓度降低,饱和度减小,临界形核半径随之增大,这意味着难以突破形核所需最小能量壁垒。Ag3Sn 的临界形核半径小于Sn,所以相比之下Ag3Sn可能优先形核生长,这与由于Ag+氧化还原电势更负从而溶液中Ag+首先被还原的预测相符。
第二阶段长大的过程可用奥斯瓦尔德熟化来解释,这是一个由热力学驱动的自发过程。根据Young– Laplace公式[18],
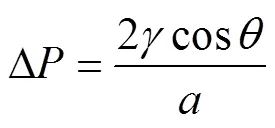
式中:是液态表面张力;Δ是液体表面的压力差;为颗粒半径;为固液界面夹角。从式(9)可知,内部压力与粒子半径成反比,粒径大的颗粒因比表面积较小而具有较低的表面能。当体系试图通过降低其整体能量以达到稳定状态时,拥有较大比表面积的小颗粒不如大颗粒稳定,对于小颗粒来说表面粒子不如内部粒子稳定,因此小颗粒表面粒子倾向于分解并通过溶液扩散,然后附着到粒径较大的颗粒表面。因此,小颗粒的数量继续减少,而大颗粒继续增长,如此反复直到体系达到稳定状态[19]。
4 结论
1) 采用化学共还原法制备纳米级Sn-3.5Ag合金粉末,还原剂浓度影响Sn-Ag粉末的粒径分布和平均粒径。随还原剂溶液的浓度减小,粉末粒径逐渐增大。还原剂浓度为0.25 mol/L时,粉末平均粒径最小,约为13 nm;还原剂浓度为0.125 mol/L时粉末粒径分布较均匀,平均粒径约28 nm,无明显团聚。
2) 共晶锡银粉末由β-Sn和Ag3Sn组成,完成了良好的合金化过程,Ag3Sn的占比随还原剂浓度降低而减少。还原剂浓度为0.125 mol/L时制备的粉末熔点约为206 ℃。
3) Ag+的氧化还原电位高于Sn2+,溶液中优先被还原并形核,随着反应的进行,溶液中Ag原子饱和度降低,最终粉末由β-Sn占主导。
[1] 朱奇农. 电子封装中表面贴装焊点的可靠性研究[D].上海:中国科学院上海冶金研究所, 2000. ZHU Qinong.Reliability of surface mount solder joints in electronic packaging[D]. Shanghai: Chinese Academy of Sciences Shanghai Metallurgical Institute, 2000.
[2] 李操. 3D封装工艺及可靠性研究[D]. 武汉: 华中科技大学, 2015. LI Cao.3D packaging process and reliability study[D]. Wuhan: Huazhong University of Science and Technology, 2015.
[3] ZHANG H, TANG W M, XU G Q, et al. Synthesis of Sn-Ag binary alloy powders by mechanical alloying[J]. Materials Chemistry and Physics, 2010, 122(1): 64−68.
[4] QI W H, HUANG B Y, WANG M P. Size and shape-dependent formation enthalpy of binary alloy nanoparticles[J]. Physical B: Condensed Matter, 2009, 404(12/13): 1761−1765.
[5] 杨明, 韩蓓蓓, 马鑫, 等. 纳米无铅焊料的研究进展[J]. 电子工艺技术,2014, 1(35): 1−5. YANG Ming, HAN Beibei, MA Xin, et al. Current status of nanolead-free solder alloys[J]. Electronics Process Technology, 2014, 1(35): 1−5.
[6] CHEE S S, CHOI E B, LEE J H. Fabrication of Sn-3.5Ag eutectic alloy powder by annealing sub-micrometer Sn-Ag powder prepared by citric acid-assisted Ag immersion plating[J]. Journal of Nanoscience and Nanotechnology, 2015, 15(11): 8407−8413.
[7] KUMAR A, OJHA D P. Theoretical study of size dependent properties of CdSe quantum dots[J]. Indian Journal of Physics, 2016, 90(9): 1041−1047.
[8] GILROY K D, RUDITSKIY A, PENG H C, et al. Bimetallic nanocrystals: Syntheses, properties, and applications[J]. Chemical Reviews, 2016, 116(18): 10414−10472.
[9] WANG Y, LEE J Y, DEIVARAJ T C. Controlled Synthesis of V-shaped SnO2Nanorods[J]. The Journal of Physical Chemistry B, 2004, 108(36): 13589−13593.
[10] ABEBE A, HAILEMARIAM T. Synthesis and assessment of antibacterial activities of ruthenium (III) Mixed ligand complexes containing 1,10-phenanthroline and guanine[J]. Bioinorganic Chemistry and Applications, 2016: 1−9.
[11] WRONSKI C R M. The size dependence of the melting point of small particles of tin[J]. British Journal of Applied Physics, 1967, 18(12): 1731−1737.
[12] HASHIMOTO R, SHIBUTA Y, SUZUKI T. Estimation of solid-liquid interfacial energy from gibbs-thomson effect: a molecular dynamics study[J]. ISIJ International, 2011, 51(10): 1664−1667.
[13] GAO Y, ZOU C, YANG B, et al. Nanoparticles of SnAgCu lead-free solder alloy with an equivalent melting temperature of SnPb solder alloy[J]. Journal of Alloys and Compounds, 2009, 484(/2): 777−781.
[14] ZHANG W, ZHAO B, ZOU C, et al. Investigating the formation process of Sn-based lead-free nanoparticles with a chemical reduction method[J]. Journal of Nanomaterials, 2013: 1–9.
[15] WANG C, YIN H, CHAN R, et al. One-Pot synthesis of oleylamine coated AuAg alloy NPs and their catalysis for CO oxidation[J]. Chemistry of Materials, 2009, 21(3): 433–435.
[16] ROSHANGHIAS A, YAKYMOVYCH A, BERNARDI J, et al. Synthesis and thermal behavior of tin-based alloy (Sn-Ag-Cu) nanoparticles[J]. Nanoscale, Royal Society of Chemistry, 2015, 7: 5843–5851.
[17] FISENKO S P, ROSTAMI A A, Kane D B, et al. Modeling of formation and growth of nanodroplets at high nucleation rate[C]// BORISENKO V E, GAPONENKO S V, GURIN V S, et al. Physics, Chemistry and Application of Nanostructures: Reviews and Short Notes to Nanomeeting-2017. Minsk, Belarus: World Scientific, 2017: 422−424.
[18] LIU H, CAO G. Effectiveness of the Young-Laplace equation at nanoscale[J]. Scientific Reports, 2016, 6(1): 23936.
[19] YUNG K C, LAW C M T, LEE C P, et al. Size control and characterization of Sn-Ag-Cu lead-free nanosolders by a chemical reduction process[J]. Journal of Electronic Materials, 2012, 41(2): 313−321.
Effect of reducing agent concentration on the growth of Sn-Ag nanoparticles synthesized by chemical co-reduction method
WANG Yao, MA Yunzhu, LIU Wensheng, TANG Siwei, HUANG Yufeng
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Sn-3.5%Ag (mass fraction, %) nanoparticles were synthesized by chemical co-reduction method and the morphology, phase composition and thermal behavior were studied. The effects of reducing agent concentration on nanoparticles size and the mechanism of nucleation and growth in the solution were studied. The results show that the concentration of reducing agent controls the rate of particle nucleation and growth in the solution, and the average particle size decreases with increasing the reducing agent concentration. The average radius of the nanoparticles reaches a minimum value of about 13nm when the reducing agent concentration is 0.25 mol/L. The nanoparticles consist of β-Sn and Ag3Sn phases. The minimum melting point is about 206 ℃. The increasing concentration of the reducing agent consumes a large amount of metal ions for instantaneous nucleation and inhibits further growth of the nanoparticles. Ag3Sn nucleates and grows in the solution preferentially. With the decrease of Ag atoms saturation in the solution, the composition of the nanoparticles is dominated by β-Sn. Finally forms nano-alloy consisting of Ag3Sn and β-Sn phases.
chemical co-reduction; Sn-Ag nanoparticles; morphology; alloying; nucleation and growth
TG425.1
A
1673-0224(2018)06-607-07
国家高技术研究发展计划资助项目(2012AA03A704)
2018−03−26;
2018−05−30
马运柱,教授,博士。电话:18163708188;E-mail: zhuzipm@csu.edu.cn
(编辑 汤金芝)
