3D腹腔镜在腹腔镜辅助胃癌根治术中的应用价值
2018-12-26李家新缪刚刚毛须平
李家新 缪刚刚 毛须平
(南通大学附属丹阳医院胃肠外科,丹阳 212300)
随着腹腔镜技术的发展及应用,3D腹腔镜技术在胃癌根治术的应用逐渐开展和日趋成熟。3D腹腔镜引进了三维的概念,是腹腔镜技术向机器人手术过渡的类型,三维视野是通过两眼视野的偏差,产生立体影像,对术野构建景深,对于荷包包埋、吻合口加固、血管游离、淋巴结清扫提供更加清晰和身临其境的真实感,更加高清的视野和分辨率提供精细安全操作的基础[1]。由于3D腹腔镜价格昂贵,三维视野引起术者眼部不适以及视觉死角的存在,对3D腹腔镜在胃癌根治术中是否优于2D腹腔镜尚存在争论。我们采用前瞻性研究对2014年1月~2015年7月我科3D腹腔镜与传统2D腹腔镜行腔镜辅助胃癌根治术(D2)进行比较,旨在探讨3D腹腔镜在腔镜辅助胃癌根治术的优势。
1 临床资料与方法
1.1 一般资料
本研究经医院伦理委员会备案。2014年1月~2015年7月51例术前胃镜病理诊断胃癌,根据单双号日期行3D腹腔镜胃癌,根治术(3D组,n=27)或2D腹腔镜胃癌根治术(2D组,n=24)。临床表现:进食哽咽感3D组5例,2D组4例,上腹隐痛不适症状3D组8例,2D组6例,呕血、黑便3D组2例,2D组2例,恶心、反酸、嗳气3D组4例,2D组5例,其余病人无明显症状。均无急腹症及腹膜炎体征。重度营养不良(BMI<19.0)3D组2例,2D组2例,均经过营养支持及空腹营养配方纠正。影像学检查无脏器明显外侵及远处转移,无腹膜后淋巴结转移及腹水,无心肺功能不全及严重基础疾病。实验室检测无重度贫血,无电解质紊乱,血红蛋白<7 g 3D组2例,2D组2例,术前通过输注红细胞纠正。2组一般资料比较无显著性差异(P>0.05),有可比性,见表1。
病例选择标准:术前胃镜病理活检明确诊断,增强胸腹部CT排除远处转移、肝脏及腹膜后转移,排除广泛的浆膜面侵犯,术前均未行辅助化疗及放疗,无开放性上腹部手术史,排除严重心肺基础疾病不能耐受手术者。术前无明显胃潴留、严重的营养不良和电解质紊乱。

表1 2组一般资料比较
*Fisher精确检验
1.2 方法
均经过术前营养状况评估,经过术前营养要素饮食改善术前营养状况。手术遵循肿瘤根治的原则,强调肿瘤与周围组织切除的完整性,肿瘤的操作遵循非接触原则,要有足够的切缘;术中根据规定的淋巴结清扫范围进行根治术治疗。3D组采用Snake EinsteinVision 3D腹腔镜系统,2D组采用Stryker 2D腹腔镜系统。根据胃癌部位及分期,分别行腔镜辅助下近端胃切除联合食管、残胃吻合,全胃切除联合食管空肠Roux-en-Y吻合术,远端胃切除联合毕Ⅰ式或毕Ⅱ式吻合。腔镜下完成游离及淋巴结清扫,所有吻合均采取中腹部小切口直视下完成。
平卧位,全麻麻醉,建立CO2气腹,气腹压力维持在 13~15 mm Hg,在脐部下缘 1 cm 置入 10 mm trocar 操作穿孔,其余 3 孔分别在上腹锁骨中线、左右中腹部锁骨中线,主操作孔为左上腹孔,然后分别置入器械。游离大网膜、横肠结以及胃结肠韧带,清除第6组淋巴结;游离胃十二指肠韧带,清除第5、12、8组淋巴结;游离十二指肠上部,在距离幽门 3 cm 的位置,使用直线切割器将十二指肠切断,将胃向左上方牵拉,暴露脾动脉、腹腔动脉等,于胃左动脉根部上肽夹后切断,清除第 7、9、11组淋巴结。沿肝下缘将小网膜清扫至贲门右侧,并将第1、3组淋巴结清除。如为全胃或近端胃切除,游离脾曲时离端胃短血管,清扫第2组淋巴结,在腹部正中做一切口,长4~5 cm,用无菌塑料薄膜将切口保护起来,然后将胃提出腔外,根据2015年V1版《NCCN胃癌临床实践指南》进行[2],行胃大切或胃全切。术后抗生素防止感染,术后第2天过渡到肠内营养,常规放置引流管。
1.3 观察指标
术中出血量[显性(吸引器吸出量-冲洗液体量)与隐性失血量(纱布吸收)之和。将带血纱布称重减去原纱布重量,即纱布的含血量(g),过滤液减掉水分就是血液质量(g),除以血液比重(1.050)即为纱布失血量(ml)]、淋巴结清扫数目、手术时间(从开始建立气腹至关闭切口)、术后排气时间、术后住院时间(出院标准:无需要住院处理的并发症,无胃肠道症状,营养状况良好,可生活自理,进食与排便良好)、术后3 d平均引流量(术后拔管标准:连续3 d引流液<20 ml/d,无可疑吻合口漏及残余感染存在)、术后早期并发症(术后腹腔出血、吻合口漏、胃排空障碍、肺部感染等)、术后无瘤生存(disease free survival,DFS)情况。
1.4 统计学处理
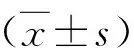
2 结果
3D组手术时间、淋巴结清扫数目、术后排气时间、术后住院时间、术后并发症发生率与2D组比较差异无显著性(P>0.05),3D组出血量、术后3 d平均腹腔引流量显著少于2D组(P<0.05),见表2。3D组术后胃排空障碍1例,肠内营养结合肠外营养28 d治愈;术后肺部感染1例,术后高热,加强抗感染、排痰等治疗后痊愈。2D组术后淋巴漏1例,经腹腔引流21 d拔管后痊愈;术后第5天腹腔出血1例,经过血管造影考虑为超声刀损伤脾动脉致术后假性动脉瘤破裂出血,经介入脾动脉栓塞止血后痊愈;胃排空障碍1例,术后肠内营养结合肠外营养35 d治愈。2组均未发生吻合口漏。术后随访6~24个月(平均21个月),死亡4例,失访1例。2组各有2例死亡:3D组2例术后8、15个月肿瘤复发转移,分别于术后13、18个月后死亡;2D组2例术后9、13个月胃癌局部复发及腹腔转移,分别于术后12、17个月死亡。术后2年内复发3D组4例,2D组6例,2组术后DFS log-rank检验无明显差异(χ2=0.780,P=0.377),见图1。

表2 2组观察指标比较

图1 2组术后无瘤生存Kaplan-Meier曲线
3 讨论
1994年Kitano等[3]首次成功应用腹腔镜行胃切除术,腹腔镜技术在胃癌根治术中应用逐渐得到普及与发展,较开腹胃癌根治术更少的近期并发症,促进术后恢复,在淋巴清扫数与远期生存取得与开腹胃癌根治术效果相似[4~6]。普通腹腔镜有视野放大的优势,但二维视野使术野缺乏景深及立体感,易损伤细小血管,解剖定位与判断上出现偏差,在根治术的效果上受到质疑。胃癌手术D2淋巴结清扫较为困难,3D腹腔镜系统能够提供更大的放大倍数,更强的手术图像的立体感和纵深感,遥控机器臂扶镜的应用也增加视野的稳定性,增加操作的精准度,兼具微创优势及根治效果[7]。
3D腹腔镜引进三维的概念,通过两眼视野的偏差产生的立体影像,提供更加清晰和身临其境的真实感[8],更加高清的视野和分辨率提供了精细操作的基础。腔镜的移动可通过遥控操作,减少术者眼部的不适以及眩晕感。3D腹腔镜还有一些问题尚需解决,由于3D腹腔镜的摄像头及光源系统相对固定,无法像2D腹腔镜那样通过旋转光源系统来增加视野观察角度,导致某些操作具有一定死角。3D腔镜术前准备与维护相对复杂,价格较为昂贵。
本研究3D组淋巴结组清扫(32.6±5.3)枚,与2D组(29.9±4.3)枚,无显著性差异(t=1.982,P=0.053),但已显示出增加的趋势,考虑与该3D腔镜不能随意通过旋转光源转换视角以及人机之间的配合有关,随着器械的改进以及人机配合的熟练,在D2根治效果上必将显示出显著的优势。手术时间上3D组与2D组无显著差异(t=1.332,P=0.189),考虑3D组较为复杂的术前准备及机组安装,以及对三维视野的适应,虽然在血管解剖、淋巴游离及缝合缩短了时间,但整体时间上并未明显缩短。3D组在术中出血量及术后引流量明显少于2D组(P<0.05),体现3D腹腔镜具有更加高清的视野及纵深感,定位更加精准,从而减少术中出血,由于减少细小淋巴管和血管的损伤,术后的渗出明显减少。由于胃周血管丰富,淋巴结层次复杂,普通2D腹腔镜由于对解剖位置和深度辨别不足,易损伤细小血管发生出血,或淋巴结清扫不彻底。通过3D腹腔镜对系膜间的颜色轻微差别和深度透视感可以提高层面的分辨。3D腹腔镜手术中,可以更好地贯彻和执行层面优先、血管为导向的理念[9],对于进展期胃癌更易达到胃癌根治及D2 淋巴结清扫要求[10]。3D组术中出血量明显少于2D组(t=2.759,P=0.008),2组手术时间差异无显著性(t=1.332,P=0.189),考虑3D腹腔镜需要更多的准备和调整时间,更加精细的操作,手术时间上与2D腹腔镜相比无明显差别。3D组清扫淋巴结数略多于2D组,我们使用的Snake EinsteinVision 3D腹腔镜系统尚存在角度调整困难遗留死角的问题,故淋巴清扫显露可能存在某些盲区。目前,新一代3D腔镜技术已解决角度调整的问题,随着经验的增加及3D腔镜技术的改进,淋巴结清扫的优势会逐步体现出来。2组术后住院时间和排气时间明显差异(P>0.05),但3D腹腔镜在辅助性胃癌根治术上较2D腔镜显示出了优势,更符合肿瘤根治的需要。由于本研究样本量少,在分层研究上尚不足以提供明确结论,尚需大样本的前瞻性研究进一步证实3D腹腔镜在胃癌根治术淋巴结清扫中的优势。
由于3D腹腔镜手术一般在普通腹腔镜已熟练掌握的基础上开展,凡能熟练掌握普通腹腔镜胃癌根治术者均可开展3D腹腔镜手术。Cicione等(11]报道相对2D腹腔镜,3D腹腔镜视野下腹腔镜初学者能更好地施展外科技能。由于3D腹腔镜需要熟悉机器的准备与流程,故在腔镜工程师的指导下开展可缩短手术时间,加快适应过程。
为减少操作者的眩晕感,避免扶镜手因长时间扶镜疲劳所造成的视野晃动,或因调整视野时幅度过大,不能精细调节视野及视距,遥控机器臂的使用使视野更加稳定,加上更加高清的视野及纵深感,增加淋巴结清扫、血管解剖、间隙辨认的精确性,符合根治原则。虽然3D腔镜术前准备与维护价格较为昂贵,但治疗总体费用与2D腔镜手术相比并未明显增加[7,8,12]。
术后2D组出现1例淋巴漏,考虑在腹腔镜清扫淋巴结的过程中,区域淋巴循环途径被破坏,引起淋巴液外漏,术中未能正确处理离断的淋巴管造成医源性损伤是重要原因之一。3D腔镜通过更加清晰的三维视野,在清扫区域淋巴结方面具有潜在优势。2D组出现腹腔出血1例,血管造影证实为脾动脉假性动脉瘤破裂出血,考虑超声刀误伤所致,在游离脾动脉、肝动脉及沿血管清扫淋巴结时,应做到暴露清楚及精细化操作,以避免热传导损伤血管。2组各出现1例胃排空障碍,由于胃大部手术后胃的完整性受到破坏,消化道内环境改变、紊乱,导致胃蠕动节律失常,减弱残胃的收缩,故在术前准备及术中、术后管理上应注意胃功能的维护。3D组1例肺部感染,因此,术前对存在潜在心肺基础疾病的病人应加强围手术期管理及心肺功能的维护。
本研究中3D组术中出血量、术后3 d平均腹腔引流量显著少于2D组(P<0.05),在淋巴清扫数量和手术时间上并未显示出明显优势(P>0.05),2组术后2年无瘤生存率无统计学差异(χ2=0.780,P=0.377)。由于本研究样本量少,且混杂因素较多,有待多中心以及更大样本量的研究以进一步评价3D腹腔镜在胃癌根治术的优势。
