CuO/硅藻土催化苯酚羟化制苯二酚的研究
2018-12-25舒世立王建茹刘晓玲杨晓宇
舒世立,王 琳,王建茹,刘晓玲,杨晓宇
CuO/硅藻土催化苯酚羟化制苯二酚的研究
舒世立,王 琳,王建茹,刘晓玲,杨晓宇
(唐山师范学院 化学系,河北 唐山 063000)
以浸渍法制备CuO/硅藻土催化剂,采用XRD、SEM、FTIR、氮气吸附脱附等表征手段对CuO/硅藻土进行表征。以此催化剂催化苯酚双氧水羟化反应合成苯二酚,考察了反应温度、CuO/硅藻土催化剂用量、反应物配比、反应时间等因素的影响,确定了催化剂的再生方法。结果表明,在CuO/硅藻土为0.1 g,反应温度为70 ℃,反应时间1 h,苯酚为2 g,苯酚双氧水的物质的量之比为1:1,水为溶剂的条件下,苯酚的转化率为40%左右,邻苯二酚的选择性为20%,对苯二酚的选择性为76%。
苯酚;CuO/硅藻土;双氧水
苯二酚(主要指邻苯二酚和对苯二酚)是重要的化工原料和中间体,主要用于农药、阻聚剂、香料、橡胶、染料等工业。随着苯二酚需求量的增加,国内外生产苯二酚的方法越来越多,主要有苯胺氧化法、对二异丙苯过氧化法、苯酚羟化法等,其中苯酚羟化法具有工艺简单、符合绿色化学发展方向等优点,被认为是最有发展前途的苯二酚合成工艺。苯酚直接羟化制苯二酚所用的氧化剂之一为双氧水,而双氧水为非羟基化试剂,需要利用催化剂的辅助才能与苯酚进行羟化反应,获得高的苯酚转化率。
非均相催化剂以其分离简单,回收方便等优点得到研究者的广泛关注。已工业化的苯酚直接羟化制苯二酚工艺所用非均相催化剂往往比较昂贵,长期以来,科研人员一直致力于研制高效、低廉、环保的新型催化剂。
硅藻土作为一种多孔性硅质沉积岩,主要由硅藻及其它微生物的硅质遗骸组成,具有质轻、多孔、吸附能力强、比表面积大、价格低廉等优点,可以为化学反应提供优良的接触空间,主要用于助滤剂、吸附剂和催化剂载体等。Jia等利用盐酸溶液浸泡过的硅藻土进行苯酚双氧水羟化反应,得到苯酚转化率为54.19%,苯二酚选择性为99.34%[1]。
铜及其氧化物作为活性组分催化苯酚双氧水羟化反应的研究较多[2-7],但以CuO/硅藻土为催化剂进行苯酚羟化反应的较少。将铜负载于硅藻土上,以CuO/硅藻土为催化剂进行苯酚羟化反应。在苯酚羟化反应时,活性中心氧化铜的催化性能与硅藻土的稳定性结合起来,硅藻土的吸附性能使反应液与活性中心接触得更充分,催化剂展现出优良的催化效果。
1 实验部分
1.1 催化剂的制备
硅藻土的预处理:每10 g硅藻土中加入20 mL 5 mol·L-1的盐酸,搅拌1 h,过滤,洗涤至中性,110 ℃干燥10 h,备用。
采用浸渍法制备CuO/硅藻土催化剂。称取4.83 g的Cu(NO3)2·3H2O溶于100 mL去离子水,将5 g预处理后的硅藻土浸入硝酸铜溶液中,搅拌24 h,过滤,置于110 ℃干燥10 h,于500 ℃焙烧3 h,即得所需催化剂CuO/硅藻土。
1.2 催化剂的表征
样品表面官能团用Bruker FENSOR37傅立叶红外光谱仪进行表征;氮气吸附脱附用SSA-4300孔径比表面积分析仪测定;表面形貌用Quanta-200扫描电子显微镜表征; XRD分析用Bruker D8 Discover的X射线衍射仪。
1.3 苯酚羟化反应
苯酚羟化反应在配有冷凝管和温度计的三口瓶中进行,通过带有磁力搅拌的加热套控制温度和进行搅拌。在100 mL三口圆底烧瓶中加入2 g苯酚,20 mL溶剂,一定量的催化剂,搅拌下加热到指定温度,待温度稳定后匀速滴加相应量的30w%H2O2,反应一定时间后取样,过滤,采用高效液相色谱进行分析。高效液相色谱仪采用C18柱,甲醇/水(体积比:40/60)作流动相,流速为1.0 mL·min-1,紫外检测器波长270 nm,进样量为20 μL。外标法定量得出反应液中苯酚、邻苯二酚和对苯二酚的量,以反应开始加入的苯酚量来计算苯酚转化率和苯二酚的选择性,其计算式如下:
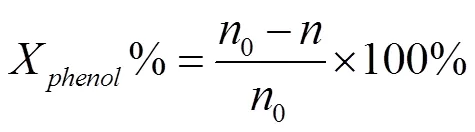
以上各式中,phenol表示苯酚的转化率,0表示苯酚初始物质的量(mol),表示反应后剩余苯酚物质的量(mol);CAT表示邻苯二酚的选择性,CAT表示反应后邻苯二酚的物质的量(mol);HQ表示对苯二酚的选择性,HQ表示反应后对苯二酚的物质的量(mol)。
2 结果与讨论
2.1 催化剂的表征
2.1.1 XRD
图1为硅藻土、CuO/硅藻土的XRD谱图。

图1 样品XRD图
由图可见,2在22o出现明显的无定形SiO2衍射峰,为硅藻蛋白石特征衍射峰。浸渍后硅藻土颜色由纯白变为蓝色,说明铜负载到了硅藻土上,但在CuO/硅藻土的XRD图中并未发现CuO的衍射峰,说明CuO负载量较少,没有发生团聚,均匀分散在硅藻土表面,没有改变硅藻土的孔径结构[8]。
2.1.2 SEM
图2为硅藻土和CuO/硅藻土的SEM图。
从图2可以看出,纯硅藻土呈圆盘状为圆筛藻,壳体直径约为37 μm,具有发达的孔隙结构,表面洁净,杂质附着较少。氧化铜主要负载于硅藻土表面,颗粒分布较均匀,粒径约为800 nm,壳体的部分孔道被填充,孔隙结构不明显[9]。

图2 硅藻土和CuO/硅藻土SEM
2.1.3 FTIR
图3为样品的FTIR谱图。在487 cm-1处的峰为硅氧四面体中O-Si-O反对称伸缩振动,617 cm-1、793 cm-1处的峰为Si-O对称伸缩振动,1 090 cm-1处的吸收峰属于Si-O反对称伸缩振动吸附峰[10]。在CuO/硅藻土的谱图中1 400 cm-1处出现了Cu-O振动峰,说明氧化铜已经负载到硅藻土上,但铜的负载量较少。
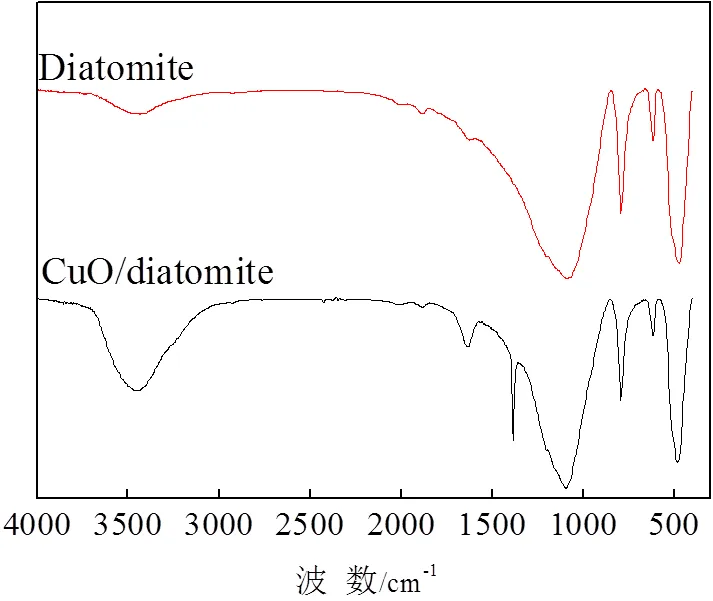
图3 硅藻土和CuO/硅藻土FTIR谱图
2.1.4 氮气吸附脱附
N2吸附-脱附等温线如图4所示。由图4可知,硅藻土和CuO/硅藻土的吸附-脱附等温线均属于具有微弱H3型回滞环的II型等温线,表明硅藻土和CuO/硅藻土中含有少量介孔。在/0低于0.9的范围内,硅藻土和CuO/硅藻土的N2吸附随着相对压力的上升增加缓慢,且吸附、脱附曲线重合。当/0高于0.9时,N2吸附量快速增加,表明硅藻土和CuO/硅藻土具有大孔结构,且产出毛细管凝聚现象导致吸附、脱附曲线分离,但二者分离程度不同,表明氧化铜颗粒对硅藻土的孔径造成了部分影响,但影响较小[11]。用BET法计算比表面积,可得负载前后硅藻土的比表面积分别为9.038 m2·g-1和6.667 m2·g-1,孔容为0.053 7 cm3·g-1和0.036 4 cm3·g-1,平均孔径分别为11.38 nm和10.90 nm,可见硅藻土负载铜以后其比表面积、孔容有所下降,但其平均孔径变化不明显,说明氧化铜颗粒没有进入硅藻土的孔道或者是进入孔道的数量非常少,仅造成孔道的少部分阻塞,该结果与SEM结果一致。

图4 N2吸附-脱附等温线
2.2 CuO/硅藻土催化苯酚羟基化反应
2.2.1 反应温度对苯酚羟基化反应的影响
CuO/硅藻土催化苯酚制苯二酚,考察了反应温度对羟化反应的影响。CuO/硅藻土0.1 g,反应2 h,苯酚与双氧水的物质的量之比为1:1,水作溶剂,结果如图5。
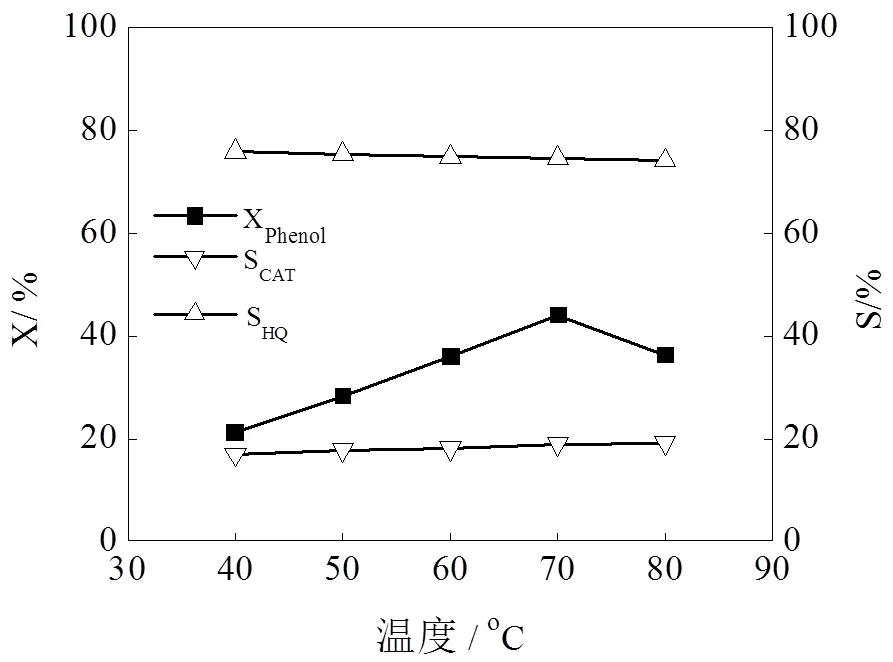
图5 反应温度对苯酚羟化反应的影响
由图5可见,随着反应温度的升高,苯酚转化率增加,当温度升高到70 ℃以后,转化率随温度的升高有所降低。一方面,反应温度较低时,催化剂的活化能力较低,不能有效活化双氧水;当温度升高,催化剂的活化能力上升。另一方面,反应温度较低时,分子在催化剂表面和孔道内的扩散速度较慢,因此苯酚的转化率也较低,随温度升高,分子扩散速度上升,反应速率上升。同时,部分被活化的双氧水用于氧化苯二酚,因此苯酚的转化率有所降低。此外,随着反应温度的提高,双氧水的无效分解加剧,也导致苯酚转化率降低。随着反应温度的升高,邻苯二酚和对苯二酚的选择性变化不大,说明苯二酚的选择性受温度影响较小,表明产物组成只受热力学平衡控制,而不受扩散动力学的控制[5]。因此,后续实验采用70 ℃作反应温度。
2.2.2 催化剂用量对苯酚羟化反应的影响
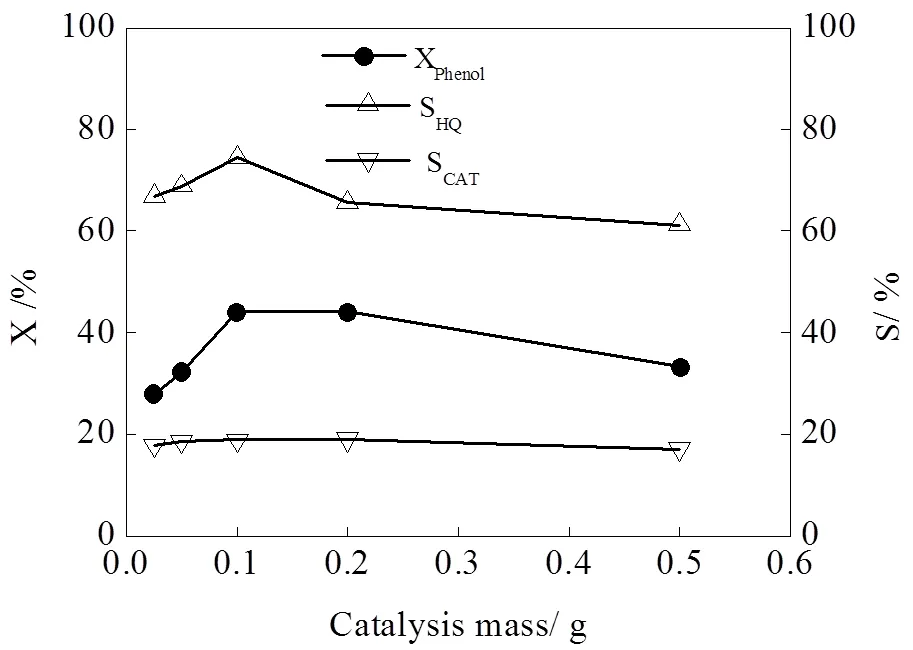
图6 催化剂用量对苯酚羟化反应的影响
图6为催化剂用量对苯酚羟化反应性能的影响。由图可知,在相同反应温度下,随着CuO/硅藻土用量的增加,苯酚的转化率逐渐增加,当催化剂用量增加到0.2 g后,苯酚的转化率开始下降。邻苯二酚的选择性在所选用催化剂用量范围内,基本不变;对苯二酚的选择性随着催化剂用量的增加,先增大后减小。该结果说明当催化剂用量较小时提供的有效活性位比较少,不足以活化双氧水,苯酚的转化率较低,随着催化剂用量的增加,催化剂的活性位增多,双氧水的活化率提高,有利于提高苯酚的转化率[12]。随着苯酚转化率的提高,反应体系中苯二酚的量增大,其被进一步氧化的可能性也随之增加,对苯二酚更容易被氧化,导致苯二酚的选择性下降。催化剂用量过大,双氧水直接分解的同时,也会生成更多的副产物,这些副产物中的焦油会覆盖部分活性位,使催化剂部分失活,从而降低催化剂的催化活性,致使苯酚转化率下降。催化剂用量超过一定值后,提供的活性位达到一定数量,没有足够的双氧水与之反应,造成活性位浪费,因此,过多或过少的催化剂用量,都会降低苯酚的转化率,其合适用量为0.1 g。
2.2.3 苯酚/双氧水对苯酚羟化反应的影响
通过改变双氧水加入量来改变苯酚双氧水的物质的量之比,考察苯酚/双氧水物质的量之比对苯酚羟化反应的影响。实验结果如图7所示。
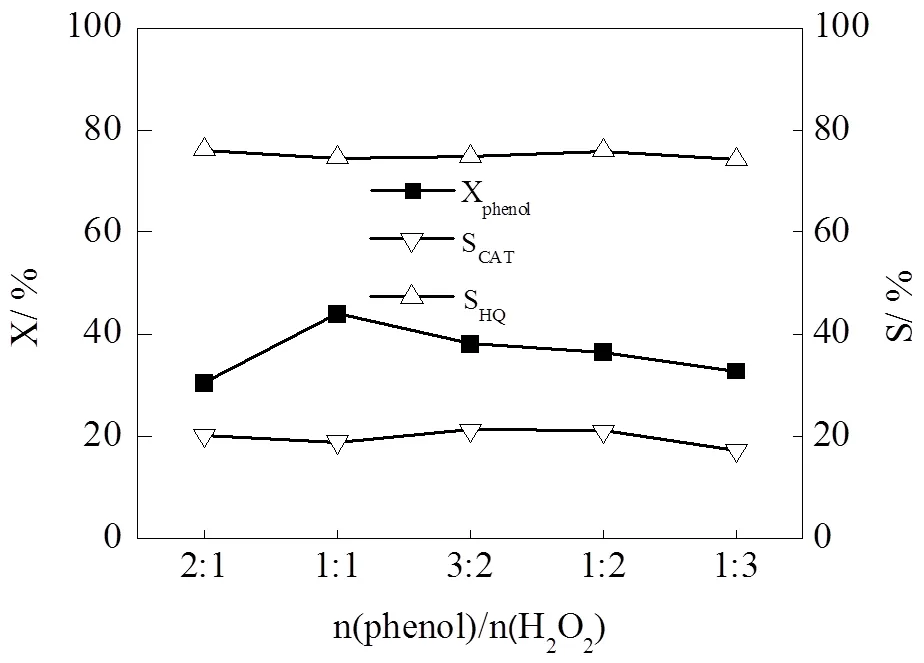
图7 n(苯酚)/n(双氧水)对苯酚羟化反应的影响
随着双氧水用量增加,苯酚的转化率升高,邻苯二酚和对苯二酚的选择性均有降低。这是因为双氧水的分解速度与其浓度成正比,在反应过程中苯酚和溶剂的量是固定的,随着双氧水用量的增加,反应体系中双氧水的浓度也增加。反应体系中双氧水浓度越大,其分解速率越快,实验现象也说明了这一点,随着双氧水用量的增大,反应体系中产生大量气泡,反应液颜色也逐渐加深,在三口瓶底部可见褐色油状液滴。根据实验结果,苯酚/双氧水物质的量之比选择1:1为好。
2.2.4 反应时间对苯酚羟化反应的影响

图8 反应时间对苯酚羟化反应的影响
时间对苯酚羟化反应的影响如图8所示。苯酚的转化率在开始1 h之内逐渐增加,当反应时间超过1 h后苯酚的转化率基本不变。说明在反应开始阶段,反应物量大、催化剂活性位较多,反应速率很快。随着反应时间的延长,反应物的量减少,部分产物或副产物覆盖催化剂,导致催化剂活性位减少,因此反应速率有所下降。而苯二酚的产量随反应时间的延长而增加,部分活化后的氧化剂与苯二酚反应,产生醌类或焦油[13]。这些从反应液的颜色可以看出,随着反应时间的延长,反应液的颜色逐渐加深,三口瓶底部产生褐色油状物质。反应时间超过1 h后,尽管苯酚的转化率不变,但双氧水的消耗量仍在增加,说明双氧水主要用于氧化苯二酚。因此,本实验条件下,反应时间控制在1 h为宜。
2.2.5 溶剂对苯酚羟化反应的影响
在苯酚羟化反应过程中,苯酚与双氧水呈两相存在,只有在反应体系中加入适当的溶剂,才能使苯酚与双氧水互溶。研究者认为在苯酚羟化过程中溶剂的作用主要是:提供苯酚和双氧水充分接触形成均相的场所,影响反应物和产物在催化剂孔内及孔外的扩散,通过与活性中心及反应过渡态的相互作用影响苯酚的转化率及产物选择性[14]。同时,溶剂还具有清洗催化剂表面的有机物和焦油,减少结焦,提高产物选择性的作用。图9为溶剂对苯酚羟化反应的影响,由图可见,溶剂的性质明显影响苯酚羟化反应的结果。水作溶剂时,苯酚的转化率为36%,乙腈作溶剂时,苯酚的转化率为23%左右。在水中邻苯二酚和对苯二酚的选择性分别为23%和70%左右,乙腈中邻苯二酚和对苯二酚的选择性分别为24%和63%左右,在水中邻苯二酚的选择性略高。由文献报道,可以认为CuO/硅藻土催化苯酚羟化反应为自由基机理,因为水的极性大于乙腈,自由基在极性溶剂中更加稳定。水将苯酚与双氧水形成互溶体系的同时有利于羟基自由基·OH的形成,从而促进了苯酚双氧水羟基化反应的进行。乙腈虽然也可以将苯酚与双氧水形成互溶体系,但是有机溶剂不利于羟基自由基·OH的形成,阻碍了苯酚分子进行氧化反应。随着溶剂极性的下降,邻苯二酚的选择性略有提高,说明溶剂的极性还会影响产物的分布[15]。
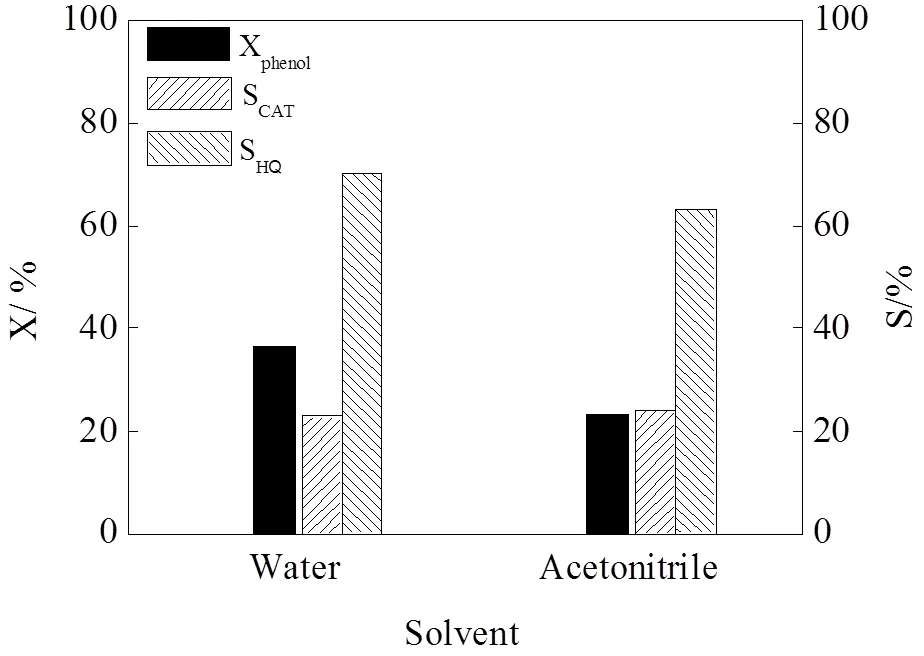
图9 溶剂种类对苯酚羟化反应的影响
2.2.6 催化剂的回收利用

表1 Cu/硅藻土催化剂的回收再利用
表1为CuO/硅藻土催化剂回收再利用的实验结果。从表1可以看出,使用过一次的催化剂,仅仅经过水洗、乙醇清洗后,基本上没有活性。经过清洗,100 ℃干燥后再于500 ℃焙烧2 h,其催化活性和选择性则可以恢复到90%以上。说明催化剂失活原因可能与苯二酚氧化产生的焦油类有关[16]。这些物质进入到催化剂孔道内或粘附在催化剂的表面,水或乙醇很难将其洗掉,造成催化剂失活。经过高温空气气氛焙烧,焦油类物质被烧掉,催化剂活性位得以释放。经过三次再生后催化剂的活性和选择性下降30%。
3 结论
采用浸渍法制备CuO/硅藻土催化剂,水为溶剂,催化苯酚双氧水羟化合成邻苯二酚和对苯二酚。当实验条件为:2 g苯酚,苯酚双氧水的物质的量之比为1:1,20 mL水,0.1 gCuO/硅藻土,反应温度70 ℃,反应1 h,苯酚的转化率可达40%左右,邻苯二酚的选择性为20%,对苯二酚的选择性为76%。催化剂经过洗涤、焙烧处理后可将活性位充分释放,恢复其催化活性。
[1] Jia Yuxin, Han Wei, Xiong Guoxing, et al. Diatomite as high performance and environmental friendly catalysts for phenol hydroxylation with H2O2[J]. Sci Techol Adv Mater, 2007, 8(1-2): 106-109.
[2] Shi Fengwei, Zheng Jinlong, Xu Kai, et al. Synthesis of binary Cu-Pd-alginates dry bead and its high catalytic activity for hydroxylation of phenol[J]. Catal Commun, 2012, 28: 23-26.
[3] Shi Fengwei, Chen Yaguang, Sun Linpin, et al. Hydroxylation of phenol catalyzed by different forms of Cu-alginate with hydrogen peroxide as an oxidant[J]. Catal Commun, 2012, 25: 102-105.
[4] 刘慧慧,蒋天龙,王艳芹.CuO/Al-SBA-15催化剂的合成及其对苯酚羟基化反应的催化性能[J].应用化学,2014,31(3):274-278.
[5] 胡昌建,伏再辉,宋小平,等.Cu-HMS的合成和催化苯酚羟基化反应研究[J].工业催化,2004,12(11):45-49.
[6] Qi Xingyi, Zhang Lili, Xie Wenhua, et al. Synthesis of copper-substituted aluminaophosphate molecular sieves (CuAPO-11) and their catalytic behavior for phenol hydroxylation[J]. Appl Catal A, 2004, 276(1-2): 89-94.
[7] Zhu Kaizheng, Liu Chibiao, Ye Xingkai, et al. Catalysis of hydrotalcite-like compounds in liquid phase oxidation: (I) phenol hydroxylation[J]. Appl Catal, A, 1998, 168(2): 365-372.
[8] 施周,袁明洋,杨秀贞,等.磁性壳聚糖改性硅藻土吸附去除水中的铅离子[J].环境工程学报,2017,11(2):787- 792.
[9]袁巍巍.硅藻土基多孔矿物复合材料制备及其对有机污染物的吸附/催化性研究[D].广州:中国科学院广州地球化学研究所,2016:37-38.
[10]刘川川.Cu掺杂TiO2/硅藻土复合光催化材料的制备及性能研究[D].北京:中国地质大学,2013:58-60.
[11] Tang Jianting, Xin Hongchuan, Su Weiguang, et al. Synthesis of hierarchical copper-containing silicas under near neutral conditions and their catalytic properties in phenol hydroxylation[J]. Chin J Catal, 2010, 31(4): 386-393.
[12] 高肖汉,吕雪川,陈平,等.Cu/FSM-16催化苯酚与双氧水反应合成苯二酚[J].石油学报(石油加工),2012, 28(1):133-136.
[13] Jian Lijun, Chen Chao, Lan Fan, et al. Catalytic activity of unsaturated coordinated Cu-MOF to the hydroxylation of phenol[J]. Solid State Sci, 2011, 13(5): 1127-1131.
[14] Lou Lanlan, Liu Shuangxi. CuO-containing MCM-48 as catalysts for phenol hydroxylation[J]. Catal Commun, 2005, 6(12): 762-765.
[15] 石勇,曹贵平,张明华,等.钛硅分子筛催化剂条件下苯酚羟化制苯二酚的过程[J].上海师范大学学报(自然科学版),2005,34(4):59-64.
[16] Sun Jianmin, Meng Xiangju, Shi Yanhui, et al. A novel catalyst of Cu-Bi-V-O complex in phenol hydroxyl- ation with hydrogen peroxide[J]. J Catal, 2000, 193(2): 199-206.
Catalytic Performance of CuO/Diatomite for Phenol Hydroxylation
SHU Shi-li, WANG Lin, WANG Jian-ru, LIU Xiao-ling, YANG Xiao-yu
(Department of Chemistry, Tangshan Normal University, Tangshan 063000, China)
The CuO/diatomite catalysts were prepared by impregnation method and characterized by XRD, SEM, FTIR, and N2adsorption-desorption. The reaction temperature, the dosage of Cu/diatomite catalyst, reaction time and the ratio of phenol to hydrogen peroxide were investigated to study their effects on the phenol hydroxylation. The performance for repeated use of the catalysts on the catalytic behavior was studied. The results indicated that the conversion of phenol, selectivity of catechol and selectivity of hydroquinone reached 40%, 20% and 76% when the catalytic dosage was 0.1 g, the reaction temperature was 70oC, reaction time was 1 h, the mass of phenol was 2 g, the molar ration of phenol/H2O2was 1:1 and water was a solvent.
phenol; Cu/diatomite; hydrogen peroxide
O0643
A
1009-9115(2018)06-0019-06
10.3969/j.issn.1009-9115.2018.06.004
唐山师范学院博士基金项目(11A06),唐山师范学院教育教学改革项目(2015001004),唐山师范学院大学生创新创业训练计划项目
2017-11-01
2018-06-09
舒世立(1979-),女,满族,河北唐山人,博士,讲师,研究方向为吸附。
(责任编辑、校对:琚行松)
