二氧化钛/还原氧化石墨烯复合材料的制备及其光催化降解脱色性能
2018-12-22吴海培高晓红刘其霞
吴海培, 高晓红, 方 婧, 刘其霞, 何 平
(1. 南通大学 纺织服装学院, 江苏 南通 226019; 2. 江苏金秋弹性织物有限公司, 江苏 南通 226001)
随着纳米科技的进步,众多净水方法中,光催化是一种非常有前景和有效的方法,其中,TiO2具有宽带隙、高氧化还原电位、廉价无毒和化学稳定等特性,受到广泛关注。TiO2对印染废水具有光催化净化活性[1-2],但由于其带隙较宽,只有在紫外光照射下才能有效地光催化降解,且光生电子-空穴对复合能力较高,导致其光催化效率较低。目前提高TiO2光催化效率的常用方法是将其负载在合适的基质上,例如以纳米级多孔结构的沸石、介孔SiO2和碳基材料(如活性炭、碳纳米管和石墨烯)等做载体,与TiO2复合可增大光催化反应面积,提高反应效率[3-6]。
石墨烯属于零带隙半导体,电子迁移率较高,理论比表面积高达2 630 m2/g,是光催化剂的良好载体[7-8]。利用石墨烯这种特有的能带结构与TiO2复合,可使TiO2的光生电子进入石墨烯中,将电子与空穴分别限制在不同的物相中,达到对光生电子-空穴复合的抑制作用,同时扩大了TiO2的光响应范围,使TiO2具有更稳定的光催化性能[9]。
本文以钛酸丁酯为钛源,采用水热法制备了不同晶型TiO2和TiO2/rGO(rGO为还原氧化石墨烯)复合材料,借助紫外漫反射吸收光谱仪、傅里叶红外光谱仪、拉曼光谱仪、X射线衍射仪和扫描电镜等对TiO2及其复合材料进行了表征,分析了混晶TiO2和混晶TiO2/rGO复合材料对活性红3BS染料废水的降解脱色效果。
1 实验部分
1.1材料与仪器
材料:钛酸丁酯,化学纯,江苏强盛功能化学股份有限公司;无水乙醇,分析纯,上海振兴化工一厂;氢氟酸、氢氧化钠,分析纯,西陇化工股份有限公司;活性红3BS,工业级,浙江龙盛化工染料有限公司;氧化石墨烯、超纯水,自制。
仪器:DF-101S型集热式恒温加热磁力搅拌器,郑州长城科工贸有限公司;800-1型离心机,金坛市城东新瑞仪器厂;KQ-300VDB型双频数控超声波清洗器,昆山市超声仪器有限公司;马弗炉,上虞市道墟镇燕光仪器设备厂;TU-1901型紫外漫反射仪,北京普析通用仪器有限责任公司;IS10型傅里叶红外光谱仪,赛默飞世尔科技分子光谱;LabranHR800型拉曼光谱仪,法国Horiba Jobin Yvon公司;D8 ADVANCE型X射线衍射仪,德国布鲁克公司;JSM-6510型扫描电子显微镜,日本电子公司;GHX-3型光化学反应仪,250 W氙灯,主波长为420 nm,扬州大学城科教仪器有限公司。
1.2 实验方法
1.2.1锻烧法制备TiO2
将一定量的钛酸丁酯与无水乙醇混合均匀,边搅拌边缓慢滴加无水乙醇、氢氟酸的混合液,形成乳白色溶胶,再持续搅拌1~1.5 h后,将溶胶转移至高温高压反应釜中,在150 ℃下水热反应 12 h,接着用无水乙醇和超纯水离心洗涤,烘干研磨成粉,在马弗炉中分别于450、650 ℃煅烧4 h,制得锐钛矿型和金红石型TiO2。
1.2.2水热法制备TiO2
将一定量的钛酸丁酯与无水乙醇混合均匀,边搅拌边滴加超纯水,并调节溶液的pH值为11.5,持续搅拌2 h,然后转移至高温高压反应釜中,于 140 ℃水热反应 72 h后取出,用超纯水洗至pH值呈中性,烘干研磨得到板钛矿型TiO2。
1.2.3TiO2/rGO复合材料的制备
在无水乙醇和超纯水的混合液中加入GO,超声分散1 h,溶液呈黄棕色。称取TiO2粉体加入GO水溶液中,超声分散3 h,溶液呈亮灰色。然后将混合液转移至高温高压反应釜中,于120 ℃水热反应 3 h,冷却至室温,离心水洗,干燥后即可得到 TiO2/rGO复合材料。
1.2.4光催化降解脱色染料和脱色率的计算
配制质量浓度为20 mg/L的活性红3BS染液,测试染液的初始吸光度A0。取100 mL染液,加入10 mg的TiO2或TiO2/rGO粉体,超声分散,在 250 W氙灯下光催化反应2 h,离心分离取上层清液,每20 min取一次样,测试其吸光度At。光催化降解脱色测试重复5次,求降解脱色率的平均值。计算公式为:
D=(A0-At)/A0×100%
式中:D为样品的降解脱色率,%;A0为光催化前染液的吸光度;At为光催化t时间后染液的吸光度。
1.3测试方法
1.3.1紫外漫反射吸收性能测试
采用紫外漫反射光谱仪,用BaSO4压片法测试不同方法制得的TiO2和TiO2/rGO粉体样品的紫外漫反射吸收性能,扫描范围为230~800 nm。
1.3.2化学结构测试
为考察TiO2/rGO复合材料形成前后的官能团变化,采用傅里叶红外光谱仪对GO、TiO2和TiO2/rGO粉体进行了红外光谱测试。取一定量样品与KBr混合均匀,压片制样进行测试,测试范围为 4 000~400 cm-1。
1.3.3晶体结构测试
采用拉曼光谱仪对TiO2粉体和TiO2/rGO复合材料降解前后的染液进行测试,测试范围为 3 000~80 cm-1。
1.3.4TiO2粉体晶型测试
采用X射线衍射仪对TiO2粉体进行测试。采用CuKα辐射源,扫描范围2θ为20°~80°,测试速率为5 (°)/min。
1.3.5rGO和TiO2/rGO复合材料的形貌观测
将样品滴在硅片上,用红外灯烘干喷金处理后,采用扫描电子显微镜表征rGO和TiO2/rGO的形貌及对应的能谱图。
2 结果与讨论
2.1 TiO2的性能分析
按照1.2.1节和1.2.2节方法制备的锐钛矿型、金红石型和板钛矿型3种类型的TiO2粉体,用X射线衍射仪、拉曼光谱仪、紫外漫反射吸收光谱仪进行表征。
2.1.1晶体结构分析
图1、2分别示出450、650 ℃条件下煅烧的TiO2粉体和水热法制备的TiO2粉体的X射线衍射光谱图和拉曼光谱图。

图1 TiO2的X射线衍射光谱Fig.1 XRD pattern of TiO2

图2 TiO2的拉曼光谱Fig.2 Raman spectra of TiO2
由图1可知,在450、650 ℃条件下煅烧的TiO2的衍射峰基本符合锐钛矿型TiO2的特征衍射峰,且随着煅烧温度从450 ℃提高至650 ℃,XRD谱图在69.02°、70.26°处出现越来越明显的金红石型TiO2的特征衍射峰,说明随着煅烧温度的升高,锐钛矿型TiO2正在逐渐转化为金红石型TiO2。此外,从图2可知,450、650 ℃下煅烧的TiO2均在143、397、516、639 cm-1处有明显的锐钛矿型TiO2的拉曼特征振动峰。将400~700 cm-1范围内的拉曼光谱放大研究可发现,650 ℃下煅烧的TiO2在435、602 cm-1处有微小的振动峰,为金红石型TiO2的拉曼特征振动峰[10],也可说明650 ℃煅烧样品中出现金红石型TiO2。
图1中水热法制备的TiO2的XRD衍射峰基本都归属于板钛矿型TiO2的晶面衍射,说明此法制得了较为纯净的板钛矿型TiO2。另外,由图2还可知,水热法制备的TiO2的拉曼光谱图有15个可分辨的振动峰,分别属于A1g(648、407、200、153、124 cm-1);B1g(506、442、321、218、131 cm-1);B2g(586、395、359 cm-1);B3g(455、281 cm-1)振动模式。其中153 cm-1处的振动峰最强,符合板钛矿型TiO2的拉曼特征峰。
2.1.2TiO2紫外漫反射吸收性能分析
图3示出450、650 ℃下煅烧的TiO2粉体和水热法制备的TiO2粉体的紫外漫反射吸收光谱。

图3 TiO2的紫外漫反射吸收光谱Fig.3 UV-diffuse reflectance absorption spectra of TiO2
由图3可知,3种TiO2粉体在230~410 nm范围内均对紫外光有一定的吸收。水热法制备的TiO2对紫外光吸收能力较弱,在290 nm处存在强吸收。450、650 ℃下煅烧的TiO2均在310 nm处有最强吸收峰;与450 ℃煅烧的TiO2相比,650 ℃煅烧的TiO2对紫外光的吸收波长发生了红移,且峰强也有提高,这可能是由于煅烧温度提高至650 ℃,TiO2粉体为锐钛矿型和金红石型的混晶体系,且金红石型TiO2的存在,增加了锐钛矿型TiO2之间的不对称性和缺陷,导致混晶对紫外光拥有更强的吸收能力,这种现象被称为混晶效应[11]。
2.2 TiO2/rGO复合材料的综合分析
根据2.1节对3种TiO2粉体的综合分析表明,650 ℃煅烧的TiO2粉体属于锐钛矿型和金红石型的混晶体系,对紫外光有更强的吸收能力,因此,选取混晶TiO2与GO按照1.2.3节方法制备复合材料,通过紫外漫反射吸收光谱仪、傅里叶红外光谱仪、扫描电镜等综合分析了TiO2/rGO复合材料。
2.2.1紫外漫反射吸收性能分析
图4示出混晶TiO2和混晶TiO2/rGO复合材料的紫外漫反射吸收光谱。可知,混晶TiO2在310 nm处存在特征吸收峰,而混晶TiO2/rGO复合材料在320 nm附近有最强吸收峰,且混晶TiO2/rGO复合材料与混晶TiO2相比发生红移,这可能是材料复合使TiO2的带隙变窄。

图4 样品的紫外漫反射吸收光谱Fig.4 UV-diffuse reflectance absorption spectra of samples
2.2.2化学结构分析
GO、混晶TiO2和混晶TiO2/rGO复合材料的红外光谱如图5所示。可知,GO在3 396、1 718、1 620、1 392、1 229、1 028 cm-1处存在特征峰,分别为水或复合材料中—OH伸缩振动、羧基中CO伸缩振动、CC伸缩振动、C—OH伸缩振动、烷氧基中C—O—C伸缩振动和C—O伸缩振动。混晶TiO2/rGO复合材料中GO特征峰峰强显著减弱,这可能是由于GO在高温水热过程中部分含氧官能团被分解。从混晶TiO2/rGO复合材料的谱图可以看出,在800~400 cm-1范围内存在2个特征峰,这是Ti—O—Ti和Ti—O—C的振动叠加造成的,说明复合材料中混晶TiO2与rGO之间存在化学相互作用。

图5 样品的红外光谱图Fig.5 FT-IR spectra of samples
2.2.3rGO和混晶TiO2/rGO复合材料形貌分析
按照1.2.3节方法制备了rGO,通过扫描电镜表征了rGO和混晶TiO2/rGO复合材料的形貌,结果如图6所示。

图6 样品的扫描电镜照片和能谱图Fig.6 SEM images and EDX spectra of samples. (a) SEM image of rGO (×20 000); (b) SEM image of mixed crystal TiO2/rGO composites (×20 000); (c) EDS of mixed crystal TiO2/rGO composites
由图6(a)可知,所制得的rGO为片层结构,且存在很多褶皱。由图6(b)可以看出,混晶TiO2/rGO复合材料中TiO2颗粒的粒径约为50~100 nm,且复合物中大量TiO2较好地负载在rGO上。
由图6(c)可知,复合材料中存在C、Ti、O元素。C元素主要来源于rGO,Ti元素来自TiO2颗粒,O元素可能来源于TiO2颗粒和rGO上的少量含氧基团。
2.3 活性红3BS染液的光催化降解脱色
2.3.1脱色前后染料溶液的拉曼光谱分析
采用TiO2/rGO复合材料光催化降解脱色 20 mg/L的活性红3BS染液,并对光催化降解脱色前后和脱色降解不同时间的染料进行了拉曼光谱测试,结果如图7所示。可以看出:加入混晶 TiO2/rGO复合材料0~5 min后,活性红3BS染料分子的一些吸收峰强度正在慢慢降低甚至消失;光照 60 min后,对应于活性红3BS染料分子的大部分基团的吸收峰已经消失;光照120 min后对应于活性红3BS染料分子的所有吸收峰均消失,并且没有出现其他染料降解中间体的特征峰。这说明活性红3BS染料分子慢慢被混晶TiO2/rGO复合材料光催化降解脱色。

图7 活性红3BS染液降解脱色前后的拉曼光谱Fig.7 Raman spectra of reactive red 3BS dye before and after degradation and decolorization
2.3.2降解脱色率分析
按照1.2.4节方法制备的混晶TiO2粉体和混晶TiO2/rGO复合材料对活性红3BS染液进行光催化降解脱色,并计算其降解脱色率,结果如图8所示。可知:光催化降解120 min时,rGO对染料的脱色率小于10%,这可能是因为rGO具有较大的比表面积,对染料有较好的吸附作用所致;混晶TiO2对染料具有一定的降解脱色效果;混晶TiO2与rGO制成复合材料后,对染料的降解脱色率大大提高,高达99%。这可能是因为一方面混晶体系增加了锐钛矿之间的不对称性和缺陷,导致其对紫外光具有更强的吸收能力,另一方面,实验过程中发现混晶TiO2/rGO复合材料加入到染液中后,红光慢慢减弱,最后完全消失,这可能是因为rGO对TiO2光催化作用的协同增效,进一步提高了光催化活性所致。
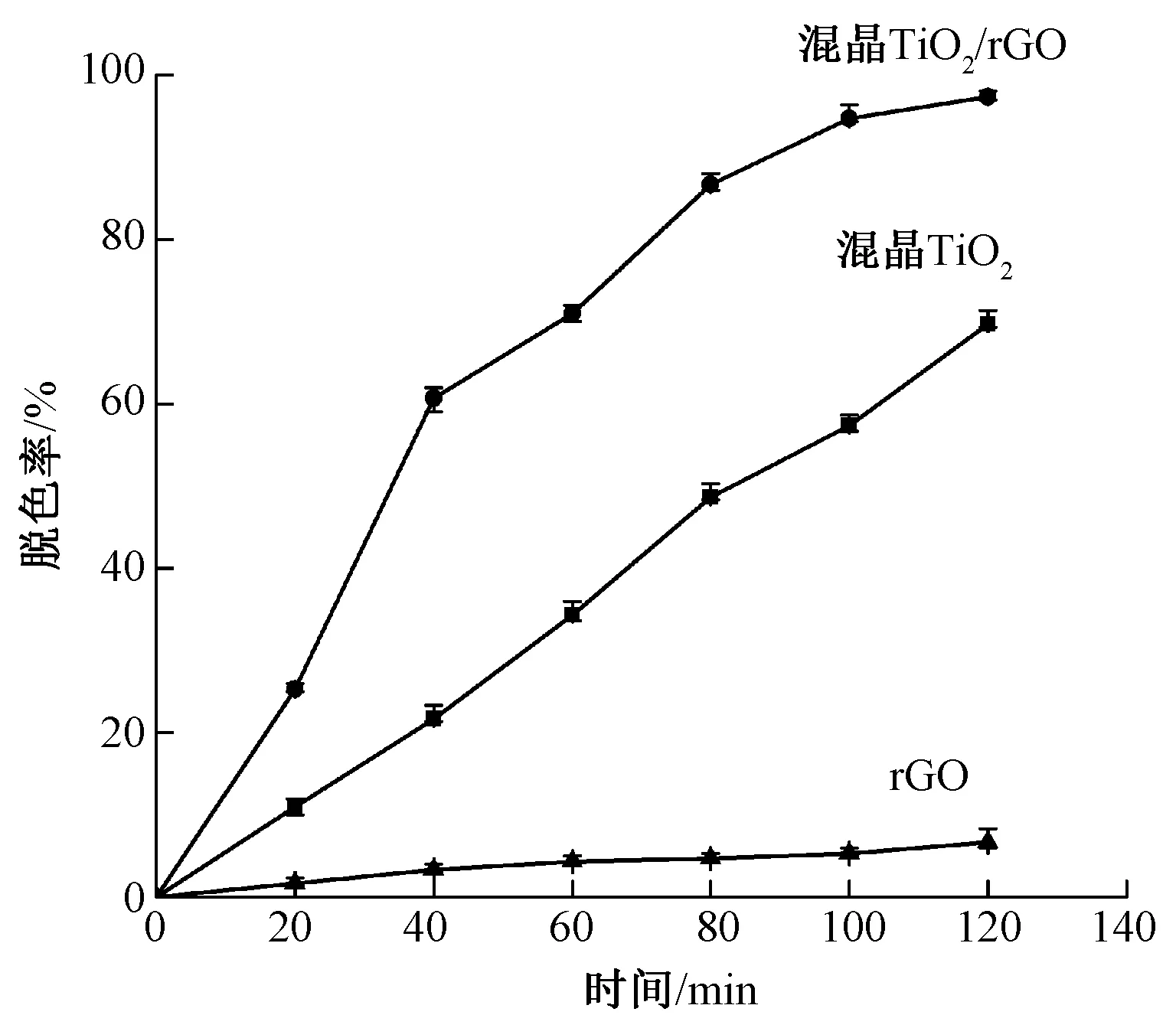
图8 样品对活性红3BS染液光催化降解脱色Fig.8 Photocatalytic degradation and decolorization of reactive red 3BS dye by samples
3 结 论
1)在150 ℃水热12 h,再经过650 ℃煅烧4 h,制得锐钛矿型和金红石型同时存在的混晶TiO2体系;碱性条件下,140 ℃水热72 h,不经过煅烧,可制得较为纯净的板钛矿型TiO2。
2)锐钛矿型和金红石型混晶结构的TiO2体系对染液有一定的降解脱色效果,当混晶TiO2与rGO制成复合材料后,对染液的降解脱色能力大大提高,光催化降解染料120 min后,降解脱色率高达99%。
FZXB
