利拉鲁肽联合胰岛素治疗2型糖尿病骨质疏松的疗效
2018-11-24张志梅张倩辉李彩英齐翠娟朱亚军
张志梅,张倩辉,李彩英,齐翠娟,朱亚军*
(1.河北省人民医院内分泌二科,石家庄 050000;2.河北省人民医院心血管内一科,石家庄 050000)
2型糖尿病由于胰岛素相对缺乏或胰岛素抵抗导致血糖升高,对骨形成可产生影响[1-2]。利拉鲁肽是一种胰高血糖素样肽-1(GLP-1)受体激动剂,体外研究表明,GLP-1对诱导干细胞向β细胞分化,对β细胞的增殖、抑制β细胞凋亡有作用,增加β细胞的数量,改善功能,能快速调节血糖[3-4],并对骨代谢指标:Ca、ALP、BMD、PINP和β-CTX等产生影响。本研究旨在探讨利拉鲁肽联合外源性胰岛素治疗2型糖尿病骨质疏松患者的疗效及对糖代谢、骨代谢的影响,为该病的临床治疗提供依据。
1 资料与方法
1.1一般资料 2014年8月~2015年8月,随机选择在本院诊治的2型糖尿病合并骨质疏松患者106例,男60例,女46例。按照随机数字表法分为观察组和对照组,各53例。观察组男31例,女22例,年龄57~80岁,平均病程3~15年;对照组男29例,女24例,年龄56~82岁,平均病程2~15年。2组患者的年龄、性别、病程、平均身高、平均体质量、BMI、HbA1c和BMD一般资料比较差异无统计学意义(P>0.05),具有可比性,见表1。所有患者及家属知情并签署同意书,本研究经我院伦理委员会批准。
表12组患者的一般资料比较


组别性别女/例男/例年龄/岁平均病程/年平均身高/cm平均体质量/kgBMI/kg·cm -2HbA1c/%BMD/g·cm -2观察组223165.52±3.037.31±1.21162.90±10.6468.42±6.7128.51±3.637.54±0.820.68±0.10对照组242965.05±3.087.49±1.25163.25±10.4268.99±6.4528.76±3.407.60±0.880.67±0.10χ2/t0.1500.7920.7530.2380.4460.2460.1250.082P0.6950.4300.4530.8130.6570.8060.9010.935
1.2标准 纳入标准:①按照2013年的《中国2型糖尿病防治指南》的诊断标准确诊为2型糖尿病[5];②按照WHO推荐的骨密度T值的测定指定的诊断标准,骨质疏松时T值≤-2.5[6]。排除标准:1型糖尿病者;有肝肾功能损害者;合并有糖尿病急性并发症、慢性并发症者;妊娠、哺乳者及有精神疾病者;恶性肿瘤者;长期应用激素类药物或者对骨有作用的药物者;合并其他内分泌疾病者。
1.3方法 2组患者均给予常规治疗,包括:糖尿病的饮食、运动指导等。每周口服阿仑膦酸钠(石药集团,批号266140201)70 mg、维生素D3注射液(上海通用药业股份有限公司,批号H31021404),肌肉注射,7.5~15 mg,早晚餐前15 min皮下注射门冬胰岛素30注射液0.3~0.5 u·kg-1·d-1(丹麦诺和诺德,批号201403027F)。患者自行监测血糖变化,每日7次,监测3餐前、3餐后2 h及睡前血糖,患者根据血糖变化、医师的指导调整胰岛素的注射量。观察组在对照组的基础上皮下注射予利拉鲁肽0.6 mg(丹麦诺和诺德,批号CP51998),每日1次。2组均治疗12周。
1.4观察指标
1.4.1糖代谢指标及BMI 2组患者均在治疗前、治疗后检测空腹血糖(FPG)、餐后2 h血糖、糖化血红蛋白及BMI。空腹及餐后2 h均使用血糖仪测指尖末梢的血糖。采空腹静脉血5 mL测定HbA1c。HbA1c测定使用日本Tosoh公司的G7全自动糖化血红测定仪及试剂。比较治疗前和治疗后2组患者的BMI变化情况。
1.4.2骨密度及骨代谢指标 检测治疗前后患者的骨密度(DPX-LBMD双能X线骨密度测定仪,美国LUNARA公司),所有患者均扫描左侧股骨。治疗前后,采空腹静脉血5 mL,测定(日立7600A-020全自动生化分析仪)钙(Ca)以及碱性磷酸酶(ALP)。治疗前后,采集空腹静脉血5 mL,测定PINP和β-CTX(酶联免疫检测仪,美国Bio-Rad;β-CTX、PINP试剂盒均由武汉云克隆科技股份有限公司提供)。
1.4.3随访骨质疏松情况 对2组患者随访观察2年,观察骨质疏松情况,根据骨密度测定值分为稳定(骨密度减少30%~60%)、改善(骨密度减少<30%)和恶化(骨密度减少>60%)[7],对严重骨质疏松或发生骨折患者及时采取有效的治疗措施。
1.4.4不良反应 治疗期间观察2组患者有无低血糖、恶心、呕吐和腹泻等不适症状。

2 结果
2.1糖代谢指标及BMI 治疗前2组患者的HbA1c、BMI、FPG及餐后2 h血糖差异无统计学意义(P>0.05);治疗后2组的HbA1c、BMI、FPG及餐后2 h血糖较治疗前显著下降,差异有统计学意义(P<0.05),观察组的HbA1c、BMI、FPG及餐后2 h血糖较对照组下降显著,差异有统计学意义(P<0.05),见表2。
2.2骨密度及骨代谢指标 治疗前2组患者的Ca、ALP和BMD差异无统计学意义(P>0.05);治疗后2组患者的Ca、ALP和BMD均较治疗前显著升高,差异有统计学意义(P<0.05),观察组Ca、ALP和BMD较对照组升高显著,差异有统计学意义(P<0.05),见表3。
2.32组患者骨的代谢指标(骨吸收和骨生成情况) 治疗前2组患者的PINP和β-CTX差异无统计学意义(P>0.05),治疗后2组患者的PINP和β-CTX较治疗前显著下降,差异有统计学意义(P<0.05),观察组的PINP较对照组高,差异有统计学意义(P<0.05),β-CTX下降较对照组显著,差异有统计学意义(P<0.05),见表4。
2.4随访骨质疏松情况 2年后观察组的预后良好率显著高于对照组,差异有统计学意义(P<0.05),见表5。
2.5不良反应 2组患者均未出现低血糖、腹泻、恶心和呕吐等不良反应。
表2糖代谢指标及BMI


组别HbA1c/%治疗前治疗后tPBMI/kg·m -2治疗前治疗后tP血糖水平/mmol·L-1FPG治疗前治疗后tP餐后2 h治疗前治疗后tP观察组7.549±0.8216.683±0.5636.3330.00028.519±3.63926.547±2.5433.2340.0028.784±0.9656.673±0.79812.2730.00014.327±1.2168.674±1.12524.8430.000对照组7.609±0.8817.283±0.4392.4110.01828.961±3.40427.669±3.0912.0460.0438.563±0.9638.132±0.9852.2780.02514.328±0.94713.479±0.8754.7940.000t0.3636.1180.6462.0411.1808.3790.00524.544P0.7180.0000.5200.0440.2410.0000.9960.000
表32组患者的生化指标比较

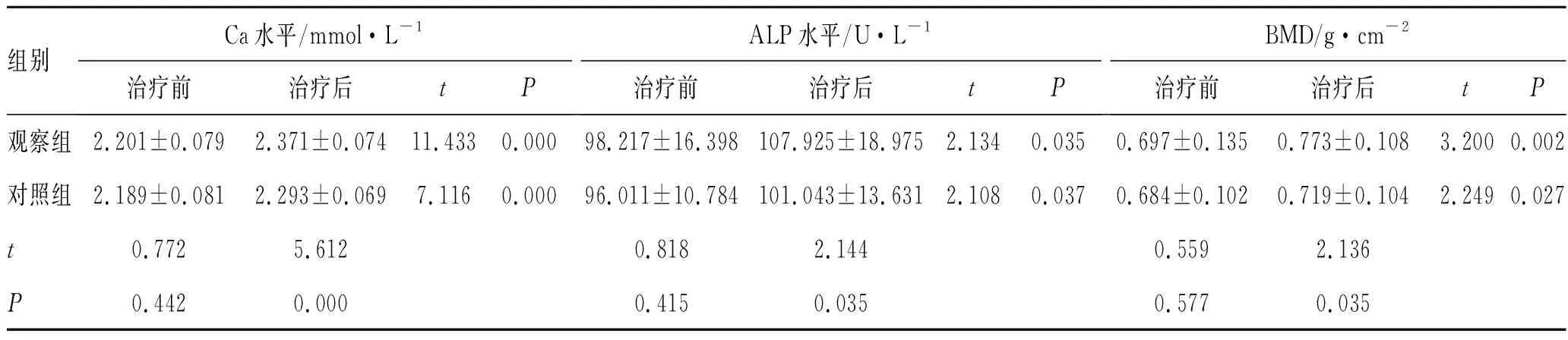
组别Ca水平/mmol·L-1治疗前治疗后tPALP水平/U·L-1治疗前治疗后tPBMD/g·cm -2治疗前治疗后tP观察组2.201±0.0792.371±0.07411.4330.00098.217±16.398107.925±18.9752.1340.0350.697±0.1350.773±0.1083.2000.002对照组2.189±0.0812.293±0.0697.1160.00096.011±10.784101.043±13.6312.1080.0370.684±0.1020.719±0.1042.2490.027t0.7725.6120.8182.1440.5592.136P0.4420.0000.4150.0350.5770.035
表42组患者骨吸收和骨生成情况


组别PINP水平g·mL-1治疗前治疗后tPβ-CTX水平g·mL-1治疗前治疗后tP观察组1 326.081±991.3491 020.293±503.0692.0030.049522.099±51.988342.591±70.73114.8870.000对照组1 320.059±959.168753.672±452.8413.8870.000525.451±51.714398.143±52.15812.6180.000t0.0322.8680.3334.602P0.9750.0050.7400.000
表5观察2组患者的骨质疏松情况
Tab.5 Observation of osteoporosis in the 2 groups

组别稳定/例(%)改善/例(%)恶化/例(%)预后良好率/例(%)观察组31(58.491)19(35.849)3(5.660)50(94.340)对照组25(47.170)9(16.981)19(35.849)34(64.151)χ2/UU=2.260χ2=14.680P0.0280.000
3 讨论
2型糖尿病继发骨质疏松是糖尿病患者较常见的骨骼系统并发症之一。研究表明[8-9],胰岛素不足或敏感性降低是糖尿病骨质疏松发生的主要原因。成骨细胞的表面有胰岛素受体,胰岛素可直接刺激成骨细胞,使成骨细胞内的氨基酸蓄积增加,骨胶原合成,分泌骨基质增加,促进骨形成[10-11]。胰岛素还可以激活25-羟化酶,使腺苷酸环化酶与环磷酸腺苷合成的作用受到抑制,使高血糖对成骨细胞的分化、增殖的毒性作用受到抑制[12-13]。
利拉鲁肽是一种GLP-1类似物,GLP-1类似物是进食后通过食物刺激小肠黏膜L细胞分泌的一种激素[14]。利拉鲁肽可与胰岛β细胞的GLP-1受体结合起作用。利拉鲁肽可使胰岛素分泌增加,并降低食欲、抑制胃排空,同时调节血糖、血脂,可控制体质量。利拉鲁肽还可抑制胰岛α细胞分泌胰高血糖素,使胰岛素、胰高血糖素呈生理稳态。利拉鲁肽还对肝糖的输出起抑制作用,加强外周组织对葡萄糖的利用,提高了胰岛素的敏感性[15-16],在本研究中治疗后2组患者的糖代谢、BMI均显著降低,差异有统计学意义,观察组较对照组降低显著,与其他学者的研究结果一致[17],可见利拉鲁肽联合外源性胰岛素对2型糖尿病患者的糖代谢改善有较好的疗效。
一般认为胰岛素是一种有多种生物学效应的激素,可调节血糖水平和骨形成等,对骨量的维持、防止骨量丢失有较重要的作用。利拉鲁肽是一种肠促胰素,有研究表明其与骨代谢有关[18-19]。Pacheco-Pantoja E L[18]等表明GLP-1R在TE-85和MG-63细胞中表达,对成骨细胞的增殖起促进作用,说明GLP-1可直接对骨细胞起作用,且发现GLP-1R可能存在于人成骨细胞的前体细胞中。GLP-1可调节成骨细胞的活性。PINP以及β-CTX是骨细胞在代谢活动中分泌的。PINP由成骨细胞分泌,是骨形成的标志物之一,其浓度变化可反映Ⅰ型胶原的变化,升高表示Ⅰ型胶原合成的速率加快,骨形成比较活跃。β-CTX是Ⅰ型胶原的分解产物,是骨吸收的特异标志物,β-CTX升高表示骨质吸收增加[20]。高血糖可能使成骨细胞在胶原蛋白上的黏附,使成骨细胞发生障碍,使骨吸收与骨形成不平衡,使 PINP和β-CTX均升高,表现为骨的吸收增加,骨的形成减少。在本研究中2组患者在治疗后Ca、ALP和BMD均显著升高,观察组较对照组升高显著,观察组的PINP较对照组高,说明观察组患者骨形成活跃程度高于对照组,β-CTX较对照组降低显著,说明观察组的骨吸收强度低于对照组,有助于改善骨质疏松症状。在本研究中,2年后观察组的预后良好率显著高于对照组,且无不良反应发生。其原因可能是,胰岛素可使糖尿病患者的胰岛功能衰退减慢,外源性的胰岛素可使体内胰岛素保持一定水平,可保护骨代谢,且外源性胰岛素进入血液循环后可分布到全身肝脏、肌肉、肾脏、脂肪组织等,也可直接作用于成骨细胞,促进成骨细胞的增殖。利拉鲁肽可更有效的改善胰岛功能,即使停止使用外源性胰岛素后也能够维持正常的胰岛素水平,减少了复发的风险。
综上所述,利拉鲁肽联合外源性胰岛素治疗2型糖尿病骨质疏松患者的疗效较好,能够有效改善糖代谢、骨代谢,改善预后,在临床上可广泛使用。
