顶空气相色谱法测定头孢唑兰原料药中的5种有机溶剂残留量
2018-11-24易梦娟刘燕华田太平李豫园
易梦娟,许 军,刘燕华,王 晨,田太平,李豫园
(江西中医药大学药学院,南昌 330004)
头孢唑兰(cefozopran)是由日本武田公司最先研究开发的第四代注射用头孢菌素[1-4]。头孢唑兰对葡萄球菌和铜绿假单胞菌等革兰阳性菌及厌氧菌均显示广谱抗菌活性,头孢唑兰的毒性很低[5-6],临床可用于新生儿和低体质量患者难治性重症感染的治疗[7-9]。其化学名称是1-[[(6R,7R)-7-[(Z)-2-(5-氨基-1,2,4-噻二唑-3-基)-2-(甲氧亚氨基)乙酰氨基]-2-羧基-8-氧代-5-硫杂-1-氮杂双环[4,2,0]辛-2-烯-3-基]甲基]咪唑并[1,2-b]哒嗪鎓内盐盐酸盐[8],结构式见图 1。由于头孢唑兰合成过程中使用了甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯等挥发性溶剂,为了有效控制药品的质量,保证用药安全,依据《中国药典》2015年版四部中残留溶剂测定法[10]和文献方法[11-16],建立了顶空气相色谱法测定头孢唑兰中5种挥发性溶剂残留量的方法。该方法灵敏度高、操作简便、准确度高、重复性好,可用于实际生产中产品残留有机溶剂的质量控制。
1 仪器与试药
1.1仪器 Agilent 7890B型气相色谱仪和Agilent 7697A顶空进样器(安捷伦科技(中国)有限公司);BS124S型电子分析天平(北京赛多利斯仪器有限公司)。
1.2试药 头孢唑兰(自制,批号:20160501,20160502,20160503,质量分数>99.0%);溶剂二甲基亚砜(DMSO)为色谱纯(上海星可高纯溶剂有限公司);对照品甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯均为分析纯(国药集团化学试剂有限公司,质量分数≥99.0%)。

图1头孢唑兰的化学结构式
Fig.1 The chemical structure of cefozopran
2 方法与结果
2.1色谱条件 色谱柱:DB-624毛细管色谱柱(30 m×0.32 mm,1.8 μm);进样口温度:220 ℃;FID检测器温度:250 ℃;程序升温:初始温度40 ℃,维持5 min,以20 ℃·min-1升温至220 ℃,维持10 min;载气:高纯氮气;流量:1.0 mL·min-1。
顶空条件:顶空平衡温度:90 ℃;平衡时间:30 min;进样体积:1 mL;定量环温度:120 ℃;传输线温度:130 ℃;分流进样,分流比:20∶1。
2.2溶液的制备 混合对照品溶液:分别精密量取甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯59.7,120.9,31.7,120.8和29.4 mg,置于50 mL量瓶中,加二甲基亚砜稀释至刻度,摇匀,即得。
供试品溶液:取供试品(批号20160501)100 mg,精密称定,置于20 mL顶空瓶中,精密加入2 mL二甲基亚砜,加盖密封,室温下超声溶解1 min,即得。
2.3系统适用性实验 取2.2项下制备的混合对照品溶液和供试品溶液进样分析,结果测得甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯的分离度均大于1.5,理论塔板数均大于10 000,符合要求,其保留时间分别为4.035,5.403,6.096,6.780和8.378 min,色谱图见图2。
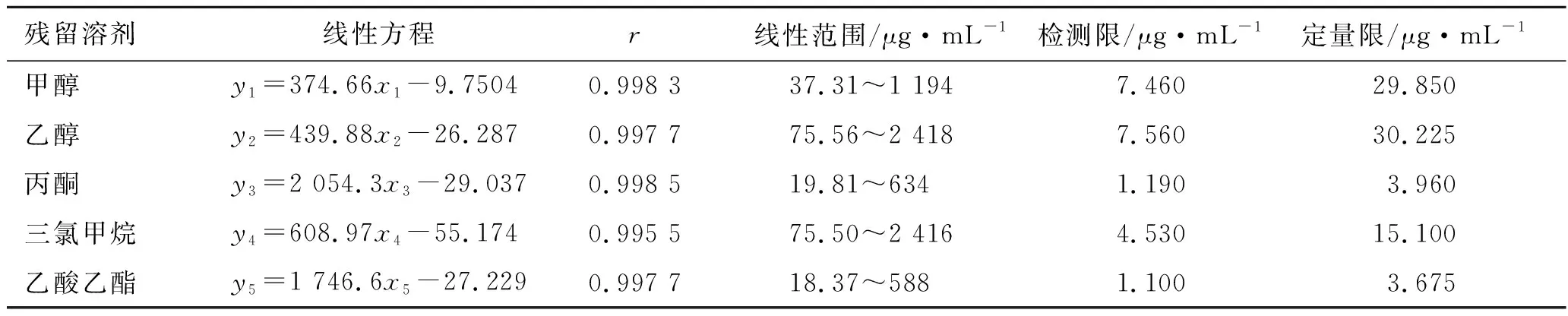
2.4线性关系、定量限与检测限考察 精密吸取5 mL 2.2项下制备的混合对照品溶液,置于10 mL量瓶中,加二甲基亚砜溶解并稀释至刻度,摇匀,作为对照品溶液②;精密吸取对照品溶液②5 mL,置于10 mL量瓶中,加二甲基亚砜溶解并稀释至刻度,摇匀,作为对照品溶液③;精密吸取对照品溶液③5 mL,置于10 mL量瓶中,加二甲基亚砜溶解并稀释至刻度,摇匀,作为对照品溶液④;精密吸取对照品溶液④5 mL,置于10 mL量瓶中,加二甲基亚砜溶解并稀释至刻度,摇匀,作为对照品溶液⑤;精密吸取对照品溶液⑤5 mL,置于10 mL量瓶中,加二甲基亚砜溶解并稀释至刻度,摇匀,作为对照品溶液⑥;取样2.0 mL,置于20 mL顶空瓶中,密封。按照2.1项下色谱条件进样测定。各对照品溶液进样2次,计算各溶剂的平均值。分别以5种残留溶剂的质量浓度为横坐标(x)、峰面积为纵坐标(y),建立回归方程;结果见表1。

图2GC图
A.混合对照品;B.供试品;C.空白溶液;1.甲醇;2.乙醇;3.丙酮;4.二氯甲烷;5.乙酸乙酯;6.二甲基亚砜。
Fig.2 GC chromatograms
A.mixed control;B.sample;C.blank control;1.methanol;2.ethanol;3.acetone;4.dichloromethane;5.ethyl acetate;6.dimethyl sulfoxide.
将上述对照品溶液⑤依次用二甲基亚砜稀释,并按照2.1项下色谱条件进样分析,以信噪比S/N=3计算检测限,以信噪比S/N=10计算定量限。结果见表1。
表15种有机溶剂的线性关系、检测限和定量限
Tab.1 The linear relationship,limit of detection and quantitation of 5 kinds of organic solvents (n=2)
2.5精密度实验 取2.2项下制备的混合对照品溶液2.0 mL,置于20 mL顶空瓶中,密封,按照2.1项下色谱条件重复进样6次。结果甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯的RSD值分别为2.09%,1.92%,1.79%,1.93%和2.21%(n=6),表明该仪器精密度良好。
2.6加样回收率实验 精密称取已知各溶剂含量的头孢唑兰原料药(批号20160501)共9份,每份0.1 g,置于10 mL量瓶中,第1~3份分别加入混合对照品溶液1.6 mL,第4~6份分别加入混合对照品溶液2 mL,第7~9份分别加入混合对照品溶液2.4 mL,加二甲基亚砜溶解并稀释至刻度,摇匀,作为供试品溶液。精密量取2.2项下制备的混合对照品溶液2 mL,置于10 mL量瓶中,加二甲基亚砜稀释至刻度,摇匀,作为对照品溶液。取样2.0 mL,置于顶空进样瓶中,密封,按照2.1项下色谱条件进行测定,按照外标法以峰面积计算加样回收率,结果见表2。
2.7稳定性实验 精密量取2.0 mL 2.2项下制备的混合对照品溶液,置于20 mL顶空瓶中,密封,共6份,分别于0,2,4,6,8和10 h,按照2.1项下色谱条件进样测定,分别计算出甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯的RSD值分别为2.75%,3.50%,3.73%,3.57%和4.19%(n=6),结果表明,混合对照品溶液在室温下10 h内稳定性良好。
2.8样品测定 取3批样品(批号:20160501,20160502,20160503)各适量,按照2.1项下色谱条件进样分析,记录峰面积并以外标法计算甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯的残留量,结果3批样品残留量均符合《中国药典》规定残留溶剂限量要求。见表3。
表25种溶剂回收率测定结果
Tab.2 Recovery test results of 5 kinds of solvents (n=9)

表3样品测定结果
Tab.3 Results of content determination of samples (n=3)
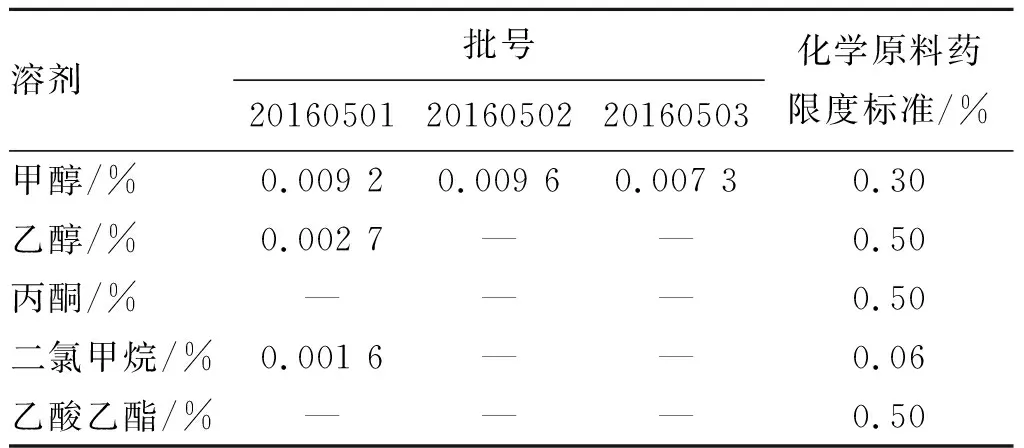
注: —表示未检出。
3 讨论
3.1溶解介质的选择 对于顶空进样,一般都选用水作为溶剂,水的溶解性较好,在氢火焰离子化检测器上无响应,对分析系统无污染;对不溶或微溶于水的溶剂,一般选择二甲基亚砜或N,N-二甲基甲酰胺(DMF)。经过溶解性实验表明,头孢唑兰难溶于水,且DMSO的沸点较高,在被测组分之后出峰,不干扰残留溶剂的测定,故选择DMSO作为溶剂。
3.2色谱柱的选择 选择色谱柱时,需考虑固定相、柱内径、膜厚和长度等因素。固定相的选择可遵循相似相溶基本原理;柱内径、膜厚和长度的选择依据样品质量浓度和仪器而定;对于本实验的头孢唑兰组分简单,使用30 m、内径小、薄液膜的色谱柱,可缩短分析时间。本实验分别考察了DB-624和HP-5毛细管色谱柱,其中DB-624为中等极性色谱柱,适用于碳氢化合物、烯烃、醇类、酯类、醚类、含氮溶剂和残留溶剂等的测定,HP-5为非极性毛细管色谱柱,适用于半挥发性化合物、生物碱、卤代化合物和脂肪酸甲酯等。实验结果显示,对比HP-5非极性色谱柱,DB-624中等极性色谱柱测定时,各有机溶剂均能达到有效分离,且峰形较好,因此本实验最终选用DB-624毛细管色谱柱。
3.3顶空平衡温度的选择 待测残留溶剂甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯的沸点分别为64.7,78.3,56.5,39.75和77 ℃,所测溶剂的沸点均不高于80 ℃。本实验选择了顶空平衡温度80与90 ℃考察,平衡时间均为30 min。在平衡温度为90 ℃时,各溶剂均达到最高响应值,且色谱图各峰峰形、分离度均能达到要求。因此本实验最终选择顶空平衡温度为90 ℃。
3.4测定结果 根据《中国药典》2015年版四部残留溶剂及限度的有关规定[10],本实验中残留溶剂的限度甲醇、乙醇、丙酮、二氯甲烷和乙酸乙酯分别不得超过0.3%,0.5%,0.5%,0.06%和0.5%,根据样品测定结果,本实验测定的样品中残留溶剂的含量均在限度范围内,检验结果均符合有关规定。
综上所述,本方法简便、灵敏,结果准确、可靠,适用于生产企业及其有关检验机构对头孢唑兰原料药进行质量控制。
