塞来昔布凝胶透皮促渗剂的配方研究
2018-11-24曾明辉熊静悦邱建平谭正怀
曾明辉,李 旭,熊静悦,邱建平,谭正怀*
(1.邛崃市医疗中心医院,成都 611530;2.四川省中医药科学院,成都 610041)
塞来昔布为非甾体抗炎药,通过抑制环氧化酶-2阻断花生四烯酸合成前列腺素而发挥抗炎镇痛作用,适用于急慢性骨关节炎、类风湿性关节炎和急性疼痛等疾病的治疗[1-2]。药物能否经皮给药,其前提是药物能渗透皮肤到达作用部位[3-4]。笔者利用2×2析因设计原则,采用改良Franz扩散池,以塞来昔布的累积释放量和稳态流量等参数为指标,用离体鼠皮筛选塞来昔布凝胶剂中透皮促渗剂薄荷醇和氮酮的配方,为塞来昔布凝胶剂的研究提供实验依据。
1 仪器与材料
1.1仪器 2690高效液相色谱系统 (美国Waters公司,包括自动进样器、996二极管阵列检测器和Empower3色谱工作站);BP211型电子天平(美国Sartorius公司);JD-4B型离体器官恒温装置(上海继德教学实验器械厂);78-1型磁力搅拌器(杭州仪表厂);320R型低温离心机(德国Hettich公司);Integral5型纯水仪(美国Millipore公司)。
1.2试药 塞来昔布对照品(印度Pharma Links制药公司,批号CX/0904,质量分数99.76%);塞来昔布原料药(萨斯化学技术有限公司,批号BL230166,质量分数98.03%);甲醇(TEDIA公司,HPLC/Spectro,批号15025012);卡波姆(AR,湖北兴银河化工有限公司,批号20151102);氢氧化钠(成都长联化工试剂有限公司);磷酸二氢钾(AR),氮酮(批号2014061601),薄荷醇(批号2014063001),均为成都市科龙化工试剂厂生产;脱毛膏(利洁时家化中国有限公司)。
1.3实验动物 SPF级昆明种小鼠,体质量20±2 g,雄性,由成都中医药大学动物实验中心提供(川实动管质7号)。
2 方法与结果
2.1塞来昔布凝胶剂的制备 处方为塞来昔布0.5 g、卡波姆1.0 g、丙二醇15 g、薄荷醇0.5~1 g和氮酮1~2 g,加纯化水至100 g,将上述处方按照凝胶剂的制备方法配制[5]。实验样品由四川邛崃市医疗中心医院提供。实验样品分为样品1,2,3和4共4组。样品1和2中氮酮含量为10 g·kg-1,薄荷醇含量分别为5和10 g·kg-1;样品3和4中氮酮含量为20 g·kg-1,薄荷醇含量分别为5和10 g·kg-1。
2.2工作曲线的制备
2.2.1色谱条件 Diamonsil C18(200 mm×4.6 mm,5 μm)色谱柱;以甲醇-水(85∶15)为流动相;检测波长:254 nm;流速:0.8 mL·min-1;进样量:10 μL;柱温:30 ℃[6-7]。
2.2.2工作曲线的绘制 精密称取塞来昔布对照品,加适量甲醇溶解,分别配制成含塞来昔布质量浓度为2.50,5.00,10.00,20.00,30.00和40.00 μg·mL-1的对照品溶液,分别按照2.2.1项下色谱条件测定塞来昔布峰面积,结果塞来昔布质量浓度在2.50~40.00 μg·mL-1范围内,峰面积(y)与质量浓度(x)线性关系良好,其回归方程为y=35 646.2x-40 216.8,r=0.996 9。塞来昔布供试品色谱峰峰形良好,与其他成分之间具有良好的分离度,对塞来昔布的测定无干扰。
2.2.3回收率和精密度测定 按照2.1项下方法配制塞来昔布空白凝胶剂。精密称取对照品适量,加入空白凝胶剂,混匀;精密称取凝胶剂适量,用甲醇溶解、定容,配制成3种不同质量浓度的塞来昔布对照品凝胶剂样品溶液;分别按照2.2.2项下方法进样3次,代入回归方程,计算得回收率分别为101.2%±0.71%,99.8%±0.83%和98.82%±0.91%。另取3种不同质量浓度的塞来昔布对照品凝胶剂样品溶液,同法测定,结果日内RSD值分别为1.26%,1.07%和1.31%;日间RSD值分别为1.67%,1.52%和1.94%。
2.3塞来昔布凝胶剂经皮渗透特性实验
2.3.1实验用鼠皮的制备 取小鼠,断颈处死,用脱毛膏脱去腹部被毛,剔除皮下组织,剥取皮肤;将无破损皮肤浸于质量浓度为9 g·L-1的氯化钠注射液中,置于4 ℃冰箱中保存。实验前用质量浓度为9 g·L-1的氯化钠注射液反复冲洗直至无浑浊,滤纸吸干备用。实验用鼠皮保存时间不得超过24 h。
2.3.2经皮渗透实验 采用改良Franz扩散池[8-9],将实验用鼠皮置于给药池与接受池之间,固定,使真皮层面向接受池,角质层面向供给室,鼠皮有效扩散面积为5.0 cm2。分别称取供试样品0.5 g,加入给药池中,并均匀涂布于鼠皮上。将含体积分数为30%甲醇的PBS缓冲液(pH值为6.8)注入接受池中,驱除气泡,保证缓冲液与鼠皮完全吻合。在32 ℃恒温下持续搅拌(400 r·min-1),分别于给药后1.0,3.0,6.0,9.0和12.0 h抽取接受液20 mL,立即补充相同体积的、32 ℃的接受液。用真空冷冻干燥法去除样品中的溶剂,残留物用甲醇溶解并定容,将样品溶液用0.45 μm微孔滤膜过滤,取滤液,按照2.2.2项下方法,测定样品中塞来昔布的质量浓度。用以下公式计算塞来昔布凝胶剂中塞来昔布的累积渗透量Q、稳态流量J及渗透系数Kp[10-11]:
(1)
J=V/A×dQ/dt
(2)
Kp=J/A×Co
(3)
其中,A为鼠皮有效渗透面积(5.0 cm2);V为每次取样体积(20 mL);Pn为第n个取样点的塞来昔布质量浓度(μg·mL-1);Co为塞来昔布在制剂中的初始质量浓度;dQ/dt为塞来昔布渗透达稳态时的斜率。

2.4实验结果
2.4.1凝胶剂中塞来昔布的累积渗透量测定结果 实验结果表明,凝胶剂中塞来昔布的累积渗透量,随着实验时间的延长而增大,见表1,其中以实验样品3的累积渗透量最大,在实验时间(12 h)内的累积渗透量为14.13 μg·cm-2。
2.4.2凝胶剂中塞来昔布透皮渗透参数的计算 将各实验样品组塞来昔布的累积渗透量Q对时间t的平方根进行线性回归,即得各实验样品组的回归方程,见表2。结果表明,各实验样品的塞来昔布的透皮渗透过程均符合Higuchi方程,样品3的Kp值和J值最大,分别为1.03 μL·cm-4和20.18 mL·cm-2。
表1凝胶剂中塞来昔布的累积渗透量测定结果

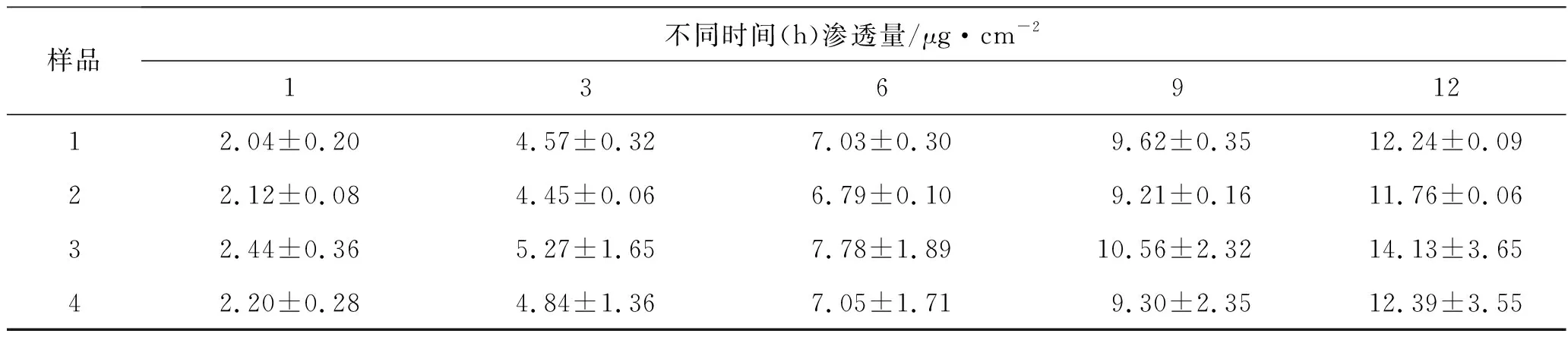
样品不同时间(h)渗透量/μg·cm-213691212.04±0.204.57±0.327.03±0.309.62±0.35 12.24±0.0922.12±0.084.45±0.066.79±0.109.21±0.16 11.76±0.0632.44±0.365.27±1.657.78±1.8910.56±2.32 14.13±3.6542.20±0.284.84±1.367.05±1.719.30±2.35 12.39±3.55
表2凝胶剂中塞来昔布的透皮渗透参数


样品方程rJ/mL·cm-2Kp/μL·cm-41Q=4.403t1/2-3.3540.99617.970.922Q=4.159t1/2-3.0090.99116.980.873Q=4.944t1/2-3.7010.99720.181.034Q=4.283t1/2-3.0120.99617.480.89
2.4.3凝胶剂透皮渗透K值的计算 对凝胶中塞来昔布的累积渗透量进行极差分析,分别计算凝胶中塞来昔布在12 h内的累积渗透量的K1和K2值,以K值最大的样品处方为最佳配方。见表3。由表3可知,样品3中的K1和K2最大,分别为24.63和26.52,即最佳配方为含薄荷醇和氮酮分别为5和20 g·kg-1。
2.4.4凝胶中经皮促渗剂交互作用分析结果 对凝胶中塞来昔布在12 h内的累积渗透量进行2×2析因设计的方差分析表明,凝胶中氮酮的F值为11.826(P<0.01),薄荷醇的F值为0.008(P>0.5)。
结果显示,塞来昔布凝胶中氮酮在促进塞来昔布的经皮渗透过程中发挥主要作用,而薄荷醇则对塞来昔布的经皮渗透作用无明显影响。但在实验质量浓度范围内,薄荷醇与氮酮联用时,其F值为2 017.13(P<0.001),说明两药联用对凝胶中塞来昔布的经皮渗透具有显著的协同增效作用,结果见表4。
表3凝胶剂中塞来昔布的累积渗透量极差分析结果
Tab.3 Results of range analysis of cumulative penetration quantity of celecoxib in Celecoxib Gels
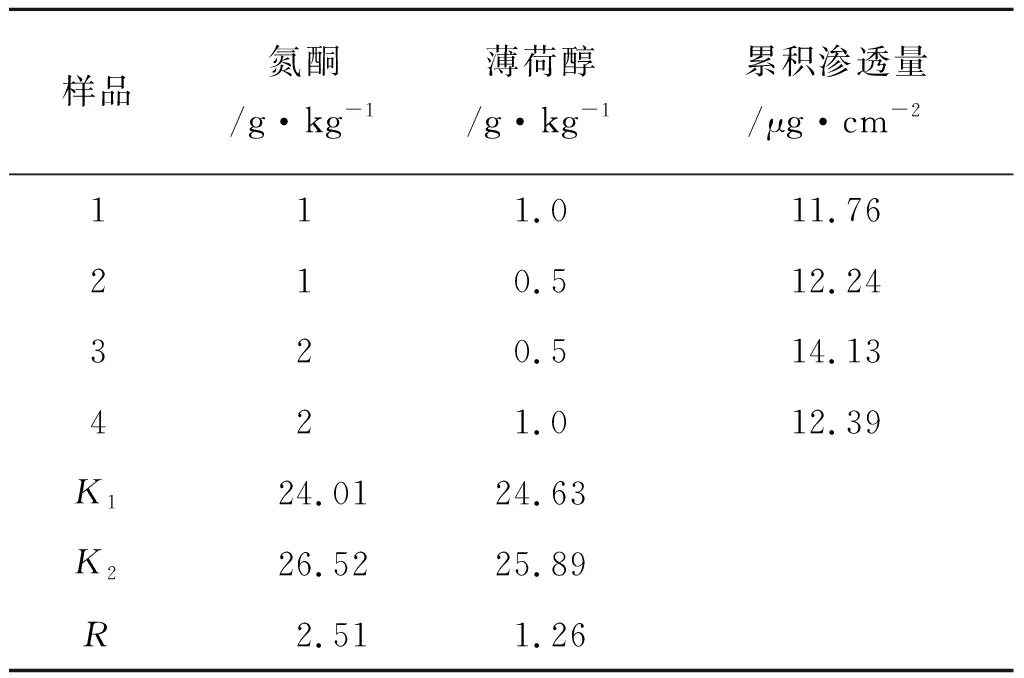
样品氮酮/g·kg-1薄荷醇/g·kg-1累积渗透量/μg·cm-2111.011.76210.512.24320.514.13421.012.39K124.0124.63K226.5225.89R2.511.26
表4凝胶剂中塞来昔布的累积渗透量方差分析结果
Tab.4 Results of variance analysis of cumulative penetration quantity of celecoxib in Celecoxib Gels
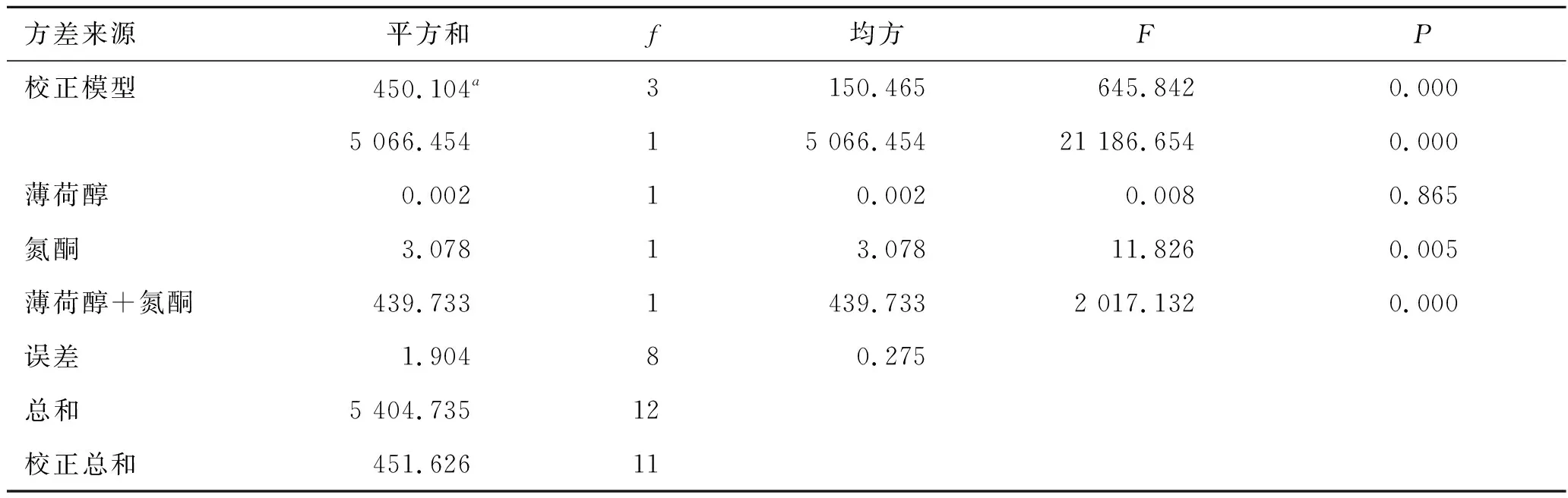
方差来源平方和f均方FP校正模型450.104a3150.465645.8420.0005 066.45415 066.45421 186.6540.000薄荷醇0.00210.0020.0080.865氮酮3.07813.07811.8260.005薄荷醇+氮酮 439.7331439.7332 017.1320.000误差1.90480.275总和5 404.73512校正总和451.62611
注:确定系数a=0.996(校正确定系数=0.995)。
3 讨论
目前塞来昔布临床使用的制剂主要为塞来昔布胶囊(商品名西乐葆),但使用后易发生胃肠道不良反应,存在导致心血管疾病的风险[12]。
经皮给药要求药物有一定的透皮速率,大部分药物的透皮速率都不能满足治疗要求。在提高药物透皮速率的药剂学方法中,除改变药物剂型、改进制剂工艺外,研究最多的方法是在处方中使用适宜的经皮促渗剂。目前常用的经皮促渗剂主要有氮酮、薄荷醇和二甲亚砜等[13-14]。文献报道,薄荷醇的用量超过20 g·kg-1时,可导致明显不良反应[15]。目前对氮酮作为经皮渗透剂的相关研究较多,其常用量为10~20 g·kg-1[16-17]。
本实验采用2×2析因设计原则,设定薄荷醇为5和10 g·kg-1、氮酮为10和20 g·kg-1。实验结果表明,氮酮对塞来昔布具有促渗作用,但氮酮含量为10和20 g·kg-1时,对塞来昔布的促渗作用无明显差异;而薄荷醇对塞来昔布则无明显促渗作用。将薄荷醇与氮酮联用时,对塞来昔布的透皮渗透表现出显著的协同增效作用,该结果与查振中等[18]报道的薄荷醇和氮酮对吲哚美辛体外促渗透作用的结果相同,薄荷醇和氮酮以一定比例联合使用时,对主药经皮渗透可产生协同增效作用,其机制目前尚不明确,可能与两者的促渗作用机制不同相关[14,19]。薄荷醇属于萜(烯)类化合物,促渗作用可能与其能优先地分配进入细胞间隙的角质层、增加脂质双分子层的流动性和可逆地裂解细胞间脂质等作用有关。氮酮是非离子表面活性剂,其促渗作用与角质中类脂质产生不规则排列和溶解皮肤的类脂有关。
实验结果表明,在实验设定的范围内,以卡波姆为凝胶基质时薄荷醇与氮酮联用的最佳配方比例为薄荷醇和氮酮分别为5和20 g·kg-1,以该比例配方组成的塞来昔布凝胶剂,在12 h内塞来昔布的累积渗透量的值最大,为14.13 μg·cm-2。笔者前期曾报道[20],以海藻酸钠为凝胶基质时薄荷醇与氮酮联用的最佳配方比例是薄荷醇和氮酮均为10 g·kg-1,以此比例配方组成的塞来昔布凝胶剂,在12 h内塞来昔布累积渗透量的最大值为27.39 μg·cm-2。2次实验证明,对于同一药物,当选用不同的凝胶基质时,在同一时间内,药物的经皮渗透量有明显差异。笔者认为,对塞来昔布而言,选用海藻酸钠作凝胶剂基质明显优于卡波姆。
