钢渣中游离氧化钙和氧化镁碳酸化反应
2018-11-22张妍,常钧*,何萍
张 妍, 常 钧*, 何 萍
( 1.大连理工大学 土木工程学院, 辽宁 大连 116024;2.营口理工学院 化学与环境工程系, 辽宁 营口 115014 )
0 引 言
我国的钢渣排放量巨大,但利用率很低,钢渣的堆积占用了大量土地,环境污染和资源浪费问题严重[1].将钢渣用于建筑材料中是目前钢渣的一种有效的利用形式.但是,钢渣中含有的较多游离CaO和游离MgO导致钢渣体积安定性不良.用钢渣做骨料的路面和建筑结构,几年后均出现了一定程度的膨裂,存在安全隐患[2-4].
CO2捕集与封存(CCS)技术是为了应对全球气候变化,减少化石能源使用产生的CO2而出现的,被视为近期最具潜力的减排技术之一[5].矿物存储是已知的唯一一种可以永久固定CO2的技术,反应生成的碳酸盐对环境没有负面影响[6].研究表明,一些富含钙镁的固体废弃物可以代替天然矿石作为矿物碳酸化的原料[7].固体废弃物的碳酸化反应可以固定CO2并消除其中的游离CaO和游离MgO,生成稳定的不溶性碳酸盐[8-10].可以用于碳酸化的固体废弃物主要包括钢渣、电石渣、废弃混凝土、水泥窑灰、垃圾焚化炉灰、某些金属冶炼过程中产生的尾渣等[8,11-12].综上,用碳酸化方法处理钢渣,既能解决钢渣利用中的体积安定性问题,又能够吸收CO2.本文对钢渣粉进行不同时间的碳酸化处理,并将处理前后的钢渣粉作为水泥混合材料,测定其压蒸安定性,以探究碳酸化处理对钢渣体积安定性的影响.
1 实 验
1.1 原材料
实验所用钢渣为本溪钢铁集团的BOF钢渣,水泥为大连小野田水泥有限公司P·O 42.5R水泥.钢渣和水泥的化学成分由X射线荧光光谱仪(XRF-1800,Shimadzu,Japan)测得,如表1所示.钢渣的XRD图谱由X射线衍射仪(Bruker D8 Advance Davinci Design)测得,如图1所示.
1.2 样品制备
1.2.1 碳酸化钢渣制备 将钢渣用球磨机粉磨后制得钢渣粉,激光粒度分析仪(NKT6200)分析表明其D10、D50、D90分别为3.28、10.44、123.88 μm.水泥比表面积自动测定仪(FBT-9)测得其比表面积为483.58 m2/kg.将钢渣粉与水按0.1水固比均匀混合[13],放入反应釜内,在CO2含量99.9%,压力0.2 MPa条件下进行碳酸化处理,碳酸化时间为0、10、20、30和60 min.随后,将试样取出并干燥,制得碳酸化钢渣粉,分别记作C0、C1、C2、C3和C4.

表1 水泥和钢渣的化学组成
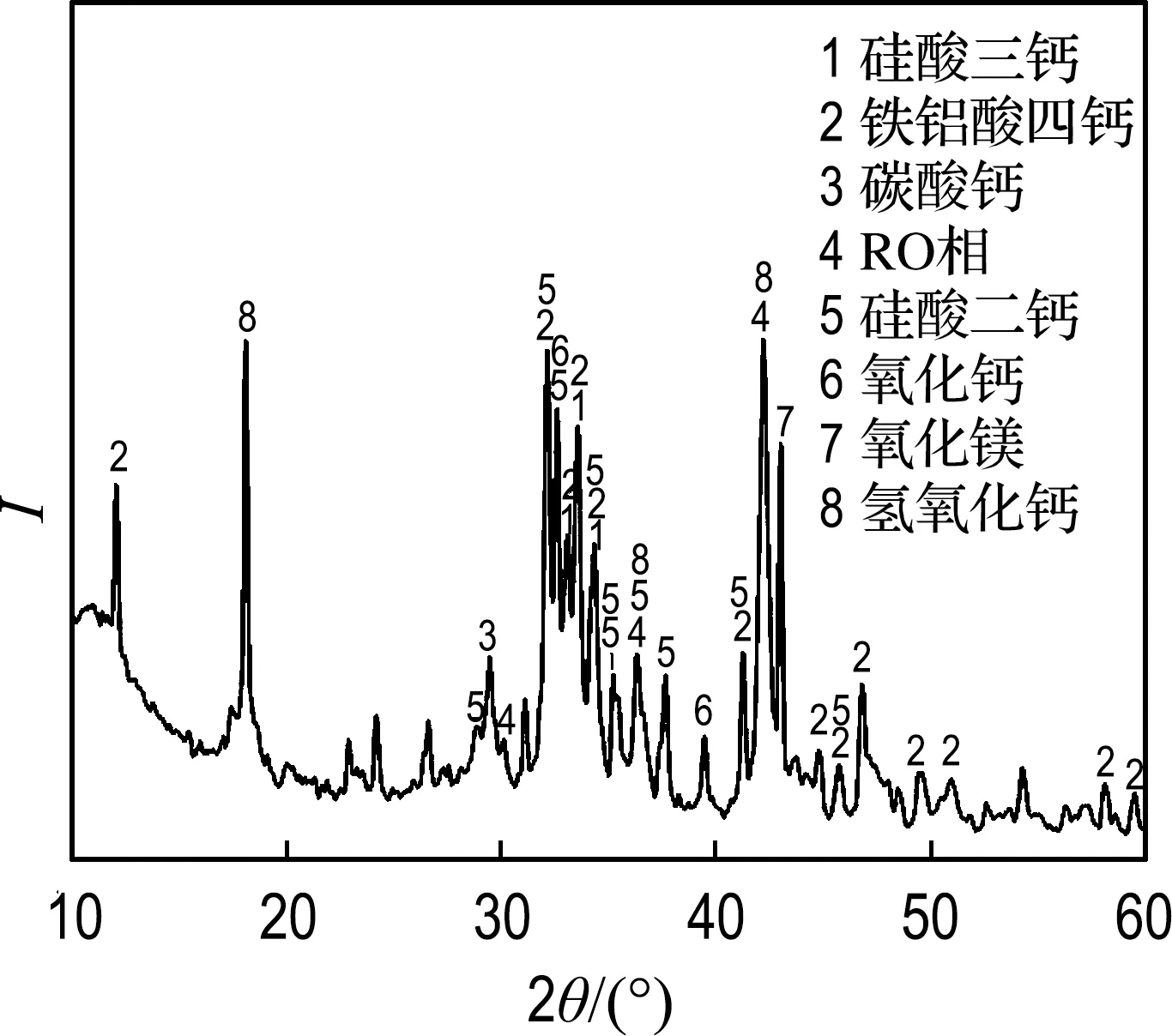
图1 钢渣的XRD图谱
1.2.2 钢渣/水泥试件制备 以钢渣粉和水泥为胶凝材料,按《水泥压蒸安定性试验方法》(GB/T 750—1992)制备25 mm×25 mm×280 mm净浆试件.其中,钢渣粉与水泥质量比为1∶1,参考GB/T 750—1992通过优化得到水胶比为0.3.将掺加C0、C1、C2、C3和C4钢渣粉的试件依次记为S0、S1、S2、S3和S4.
1.3 表 征
1.3.1 碳酸化增重率 称量碳酸化反应前干燥的钢渣质量,记为m0;碳酸化后将钢渣取出,立即放入烘箱内,在105 ℃条件下烘干24 h,称量碳酸化后钢渣质量,记为m1.钢渣增重率按下式计算:
(1)
1.3.2 压蒸安定性 将水泥净浆试件初始长度记为L0,压蒸后试件长度记为L1.每组测试3个试件,取平均值作为该组的压蒸膨胀率,试件的压蒸膨胀率按下式计算:
(2)
其中L为试件有效长度,250 mm.
1.3.3 化学滴定 参照《钢渣化学分析方法》(YB/T 140—2009)中游离CaO的测定方法,将碳酸化处理前后钢渣中游离CaO溶出,离心后取上层清液,依次加入去离子水、盐酸、三乙醇胺、氢氧化钠溶液和适量钙指示剂,用EDTA溶液滴定使溶液由红色变为蓝色,记录消耗的EDTA溶液体积,并计算出钢渣中的游离CaO含量.
1.3.4 综合热分析(TG/DTG) 将钢渣粉和压蒸后的试块研磨过45 μm筛,105 ℃烘干至恒重.采用METTLER TOLEDO TG/DSC1综合热分析仪对样品进行分析,测试气氛为N2,温度范围50~1 000 ℃,升温速率10 ℃/min.
1.3.5 X-射线衍射分析(XRD) 将碳酸化处理前后的钢渣粉及压蒸前后试件进行粉磨、过45 μm筛,采用X射线衍射仪(Cu靶,管电压40 kV,管电流40 mA)对样品进行XRD测试,测试单步长0.02°,单步时间1 s,2θ角范围5°~80°.
XRD定性分析采用Bruker DIFFRAC.EVA软件,检索数据库为Crystallography Open Database 2013,确定钢渣中各物相组成COD码见表2[14-24].

表2 物相与COD码
根据定性分析结果,进行XRD定量分析.利用Rietveld定量分析方法确定各物相在钢渣中的质量分数.
1.3.6 扫描电子显微镜(SEM) 采用美国FEI公司Quanta 450扫描电子显微镜对压蒸后的试块进行分析,观察其微观形貌.
2 结果与讨论
2.1 钢渣的压蒸安定性
将碳酸化反应前后钢渣质量按照式(1)进行计算,得到碳酸化试件的增重率(ω),如表3所示.

表3 碳酸化反应不同时间钢渣的增重率
由表3可知,随着碳酸化时间的延长,增重率增加.碳酸化反应10 min时,增重率仅为5.36%;反应20 min后,增重率明显提高,达到8.63%.碳酸化时间继续延长,增重率趋于平稳.研究表明,碳酸化反应在20 min以内增重速率较快,在20 min 后仍在继续增加,但增重速率减缓.
将钢渣/水泥试件进行压蒸处理,研究试件的体积安定性,用比长仪测定试件压蒸前后的长度,由式(2)计算出不同碳酸化反应时间试件的压蒸膨胀率,结果如表4所示.
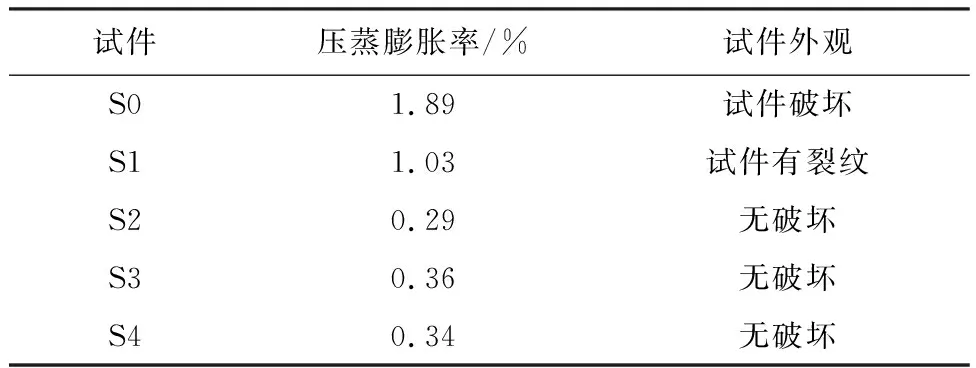
表4 试件的压蒸膨胀率及外观
由表4可知,S0膨胀率为1.89%,钢渣试件压蒸后严重破坏;S1试件压蒸后膨胀率为1.03%,表面有明显的裂纹;S2、S3和S4膨胀率分别为0.29%、0.36%、0.34%,试件压蒸后外观均无破坏.《水泥压蒸安定性试验方法》(GB/T 750—1992)规定:试件膨胀率小于0.5%,安定性合格.研究表明,碳酸化反应时间在20 min以上,试件膨胀率均小于0.5%,安定性合格.
2.2 游离CaO消解分析
2.2.1 TG分析 钢渣碳酸化反应不同时间后的TG/DTG曲线如图2所示.
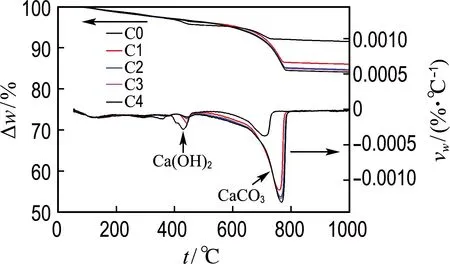
图2 碳酸化反应不同时间钢渣的TG/DTG曲线
从DTG曲线可以看出,400~500 ℃和500~800 ℃有两段明显的失重,分别是由Ca(OH)2和CaCO3分解引起的.在TG曲线中计算出相应的失重百分率,进而根据Ca(OH)2失去的H2O和CaCO3失去的CO2质量分数,计算出Ca(OH)2和CaCO3的含量,结果见表5.
表5 碳酸化反应不同时间钢渣中Ca(OH)2和CaCO3的含量
Tab.5 Content of Ca(OH)2and CaCO3in steel slag after different carbonation time
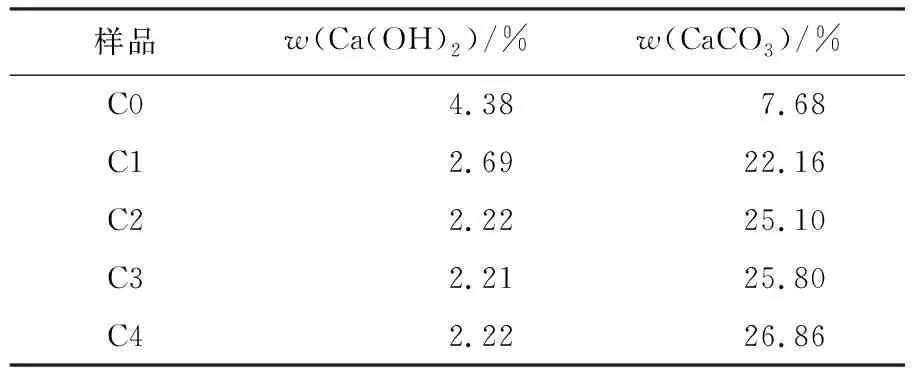
样品w(Ca(OH)2)/%w(CaCO3)/%C04.387.68C12.6922.16C22.2225.10C32.2125.80C42.2226.86
由表5可知,随着碳酸化反应时间的延长,Ca(OH)2的质量分数明显下降,未碳酸化的钢渣中Ca(OH)2含量为4.38%,反应10 min时,Ca(OH)2含量降至2.69%,反应进行到20 min时,Ca(OH)2含量为2.22%,且随着反应时间的继续延长基本保持恒定.未碳酸化的钢渣中CaCO3含量为7.68%,而反应10 min后钢渣中的CaCO3含量增加至22.16%,反应20 min时为25.10%,而后增加较少.综上可知,碳酸化反应在20 min时基本完成.
2.2.2 化学滴定 图3为经过化学滴定测出的游离CaO含量图.
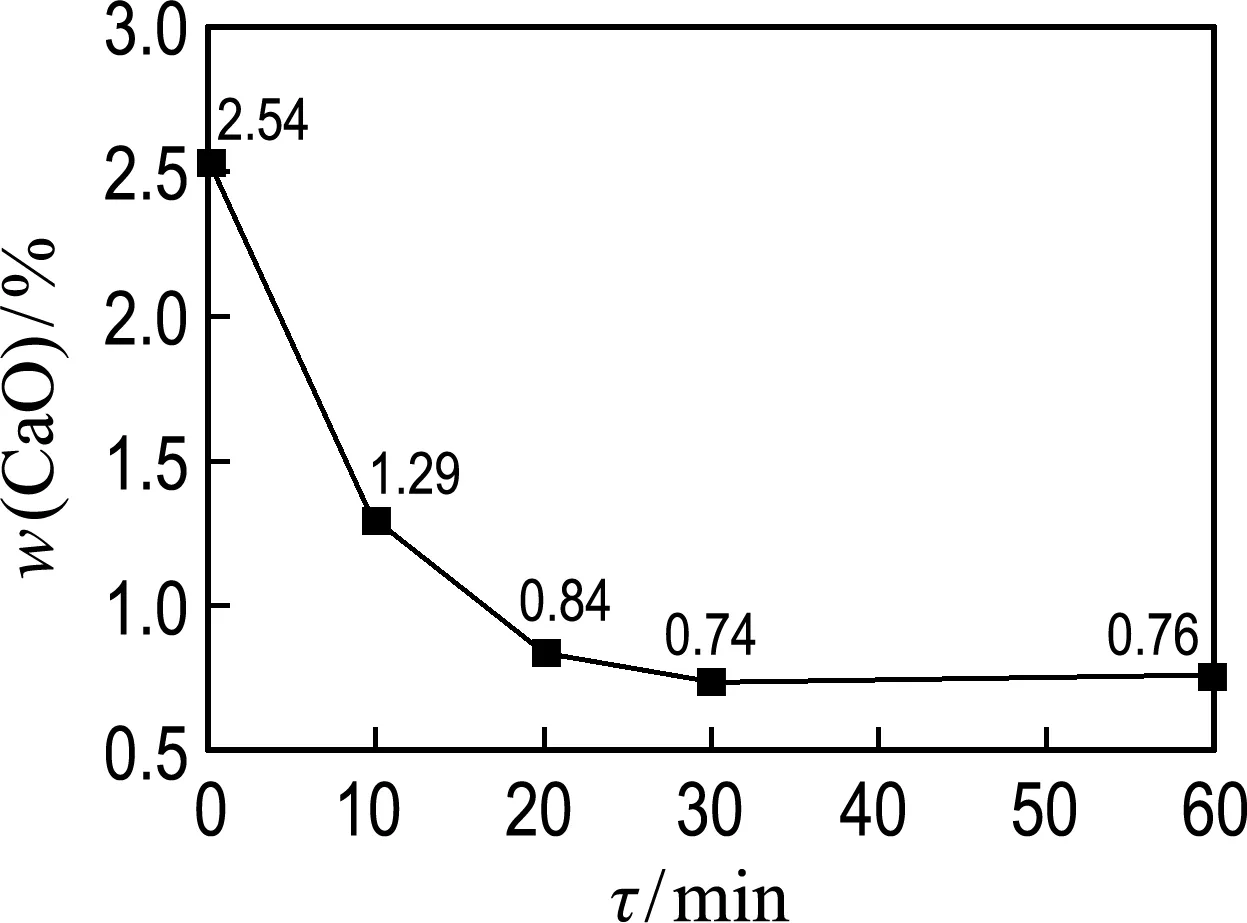
图3 碳酸化反应不同时间钢渣内游离CaO含量
结合表3和图3可知,游离CaO消解速度很快,碳酸化反应10 min后,钢渣增重率为5.36%,此时游离CaO含量从2.54%降至1.29%;反应20 min,钢渣增重率达到8.63%,游离CaO含量降至0.84%;而后钢渣增重率缓慢上升,而游离CaO含量缓慢下降并稳定至0.76%左右.可见,钢渣中游离CaO碳酸化反应活性很高,反应20 min 基本消解完全.
2.3 碳酸化对钢渣中镁离子的影响
图4给出了碳酸化反应不同时间钢渣的XRD图谱,由图可知碳酸化反应消耗了游离MgO,生成含镁方解石(CaxMg1-xCO3),是沉淀过程中Mg2+进入CaCO3中形成的,其衍射峰与方解石的衍射峰重叠[25].
对不同碳酸化反应时间的钢渣进行Rietveld物相定量分析.以碳酸化反应60 min的钢渣粉为例,拟合效果及各物相含量结果如图5所示.
不同碳酸化反应时间的钢渣各物相含量计算结果如表6所示.其中RO相化学式为0.593MgO·0.407FeO.

图4 钢渣碳酸化前后XRD图谱
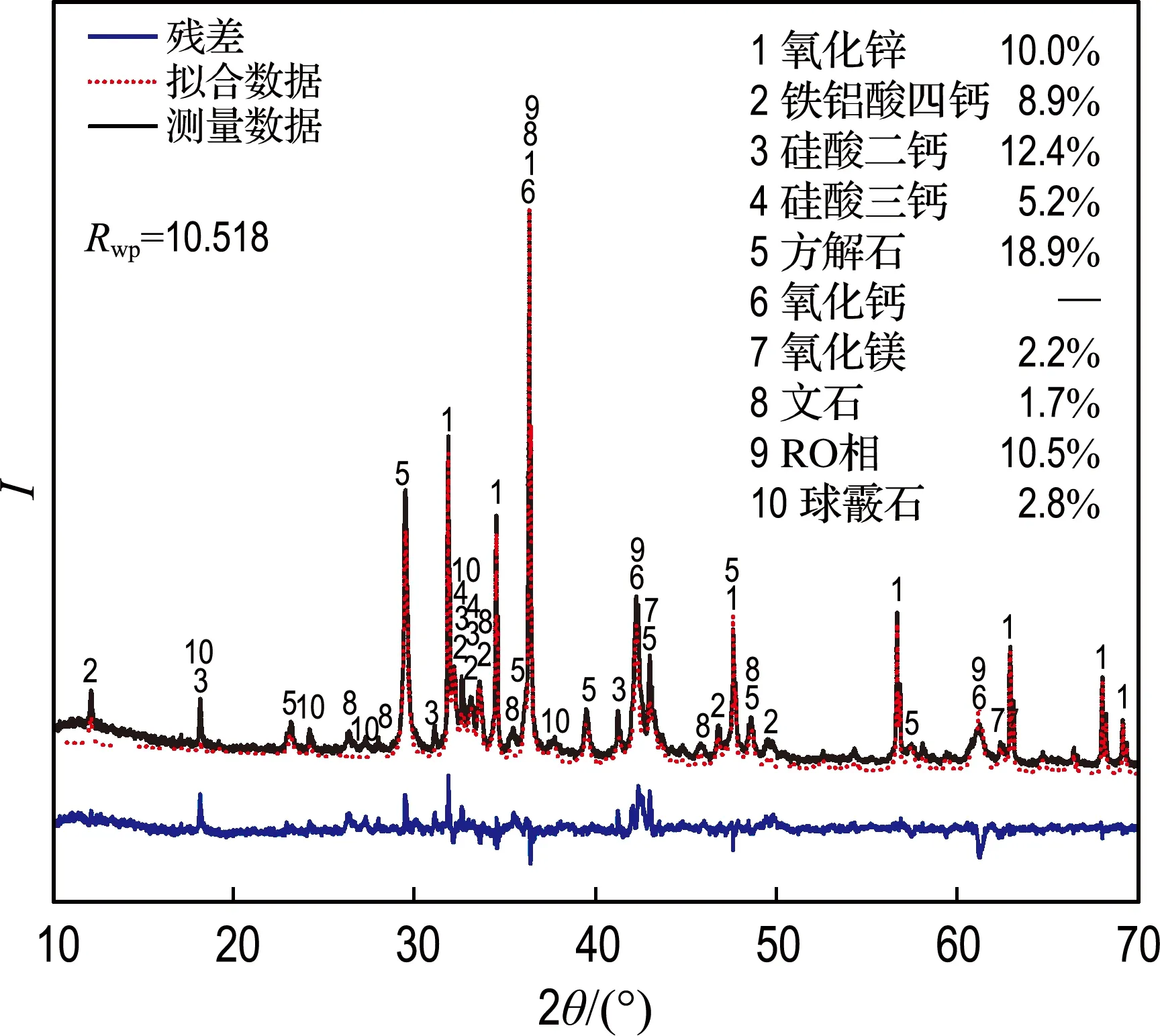
图5 Rietveld物相定量分析拟合效果
由计算结果可知,钢渣中镁离子主要有RO相和游离MgO两种存在形式,其中RO相对体积安定性无不良影响.当碳酸化反应进行到20 min 时,游离MgO含量由3.8%降至2.4%,同时钢渣中的硅酸盐相、游离CaO、Ca(OH)2也参与反应,生成含镁方解石(CaxMg1-xCO3),含量为20.3%,并伴有少量文石和球霰石生成.
图6为S0压蒸后的XRD图谱,图中MgO衍射峰(2θ=37.1°,43.1°,62.5°)消失,并未出现Mg(OH)2特征峰(2θ=18.6°,38.0°,51.0°),表明钢渣中游离MgO在压蒸后并未形成Mg(OH)2.

表6 碳酸化反应后钢渣中各物相含量
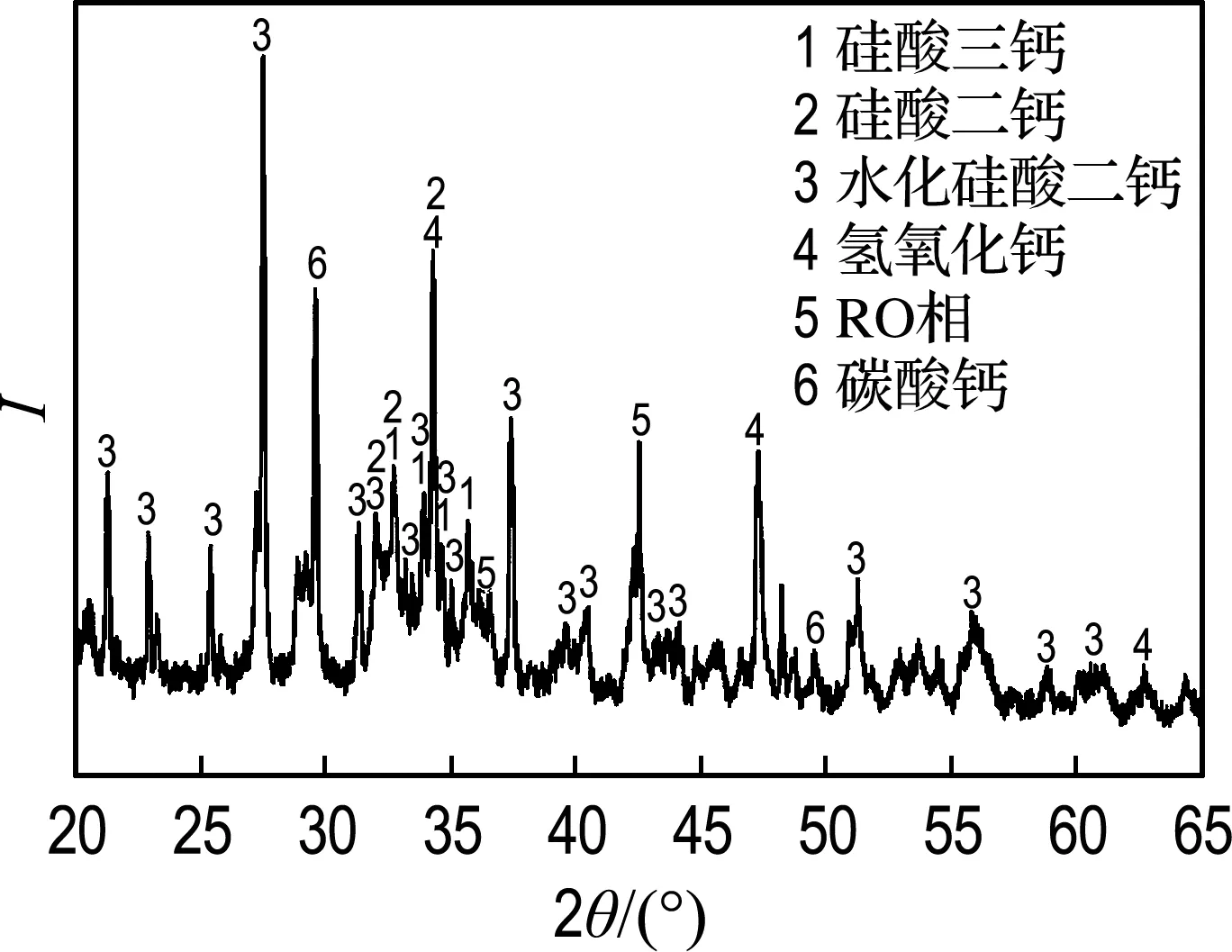
图6 S0压蒸后XRD图谱
图7(a)为S0扫描电子显微镜(SEM)照片,而图7(b)、(c)分别为图7(a)中1、2点的能谱(EDS).
由图7(a)可知,压蒸后试块中存在大量晶体,且在晶体表面附着有絮状物,结合图7(b)1点的EDS谱可知,该晶体为氢氧化钙,大量晶粒粗大的氢氧化钙堆积,体积膨胀,造成了试件的体积安定性不良;而2点的EDS谱显示,絮状物中含有较多的镁离子,说明方镁石水化后生成了无定形的水化硅酸镁,不影响试件的体积安定性.

(a) SEM照片
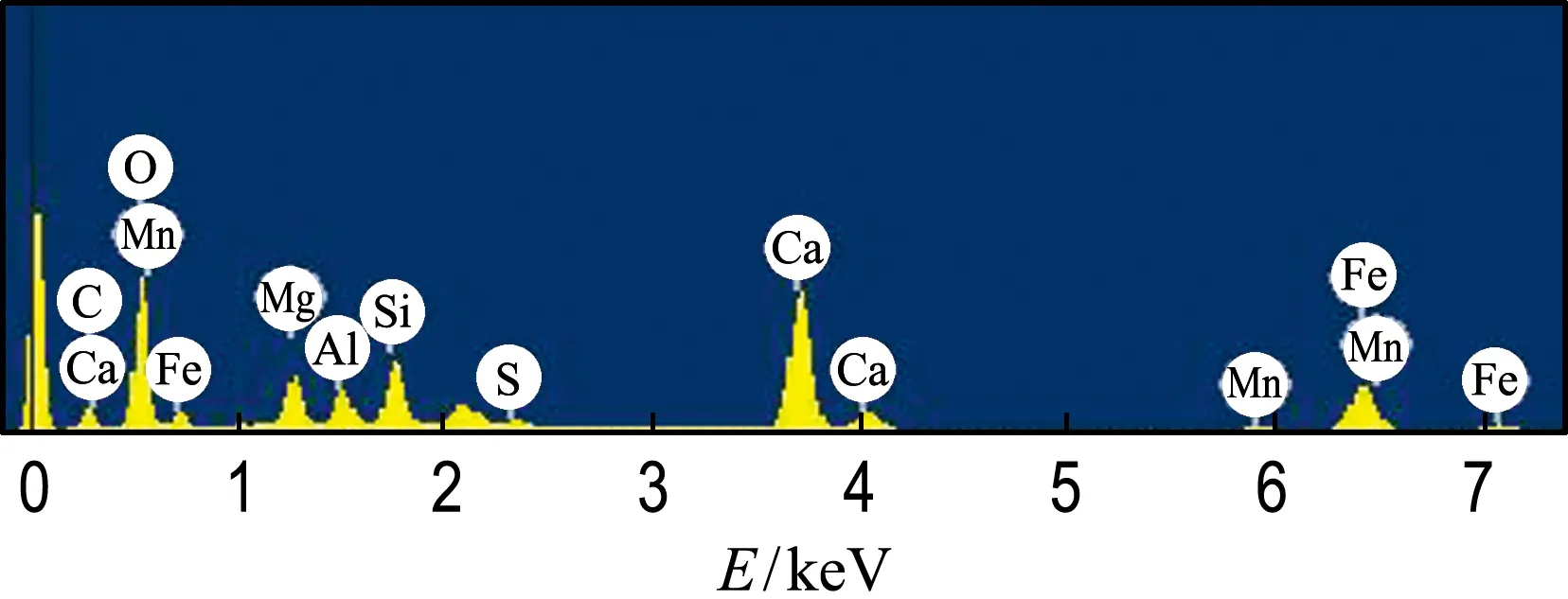
(c) EDS谱(2点)
图7 S0压蒸后的SEM照片及EDS谱
Fig.7 SEM photographs and EDS patterns of autoclaved S0
3 结 论
(1)在CO2含量为99.9%,压力为0.2 MPa,水固比为0.1条件下,对D10、D50、D90分别为3.28、10.44、123.88 μm,比表面积为483.58 m2/kg 的钢渣粉进行碳酸化处理;随着碳酸化反应时间的延长,试件的压蒸膨胀率持续减小.掺加未碳酸化钢渣的试件压蒸膨胀率为1.89%,碳酸化反应20 min后,压蒸膨胀率降至0.29%,小于0.5%,符合国家标准,体积安定性合格.
(2)碳酸化反应20 min时,钢渣增重8.63%,此时游离CaO含量由2.54%降至0.84%,游离MgO含量由3.8%降至2.4%.钢渣中的游离MgO压蒸后并未形成Mg(OH)2,而是以水化硅酸镁的形式存在于无定形物中,对试块的体积安定性无不良影响.
(3)钢渣中的硅酸盐、Ca(OH)2、游离CaO和游离MgO等物质持续与CO2进行反应,生成大量含镁方解石(CaxMg1-xCO3),同时生成少量文石和球霰石.
